Bikarbonat - Bicarbonate
|
|

|
|
| Navn | |
|---|---|
|
Systematisk IUPAC -navn
Hydroksidoksidkarbonat (1−) |
|
| Andre navn
Hydrogenkarbonat
|
|
| Identifikatorer | |
|
3D -modell ( JSmol )
|
|
| 3DMet | |
| 3903504 | |
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| 49249 | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
|
HCO- 3 |
|
| Molar masse | 61,0168 g mol −1 |
| logg P | −0,82 |
| Surhet (p K a ) | 10.3 |
| Grunnleggende (p K b ) | 7.7 |
| Konjugat syre | Kolsyre |
| Konjugert base | Karbonat |
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
| Infobox -referanser | |
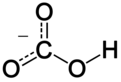
I uorganisk kjemi er bikarbonat ( IUPAC -anbefalt nomenklatur: hydrogenkarbonat ) en mellomform ved deprotonering av karbonsyre . Det er en polyatomisk anion med den kjemiske formelen H C O-
3.
Bikarbonat har en avgjørende biokjemisk rolle i det fysiologiske pH -buffersystemet .
Begrepet "bikarbonat" ble laget i 1814 av den engelske kjemikeren William Hyde Wollaston . Prefikset "bi" i "bikarbonat" kommer fra et utdatert navnesystem og er basert på observasjonen at det er dobbelt så mye karbonat ( CO2−
3) per natriumion i natriumbikarbonat (NaHCO 3 ) og andre bikarbonater enn i natriumkarbonat (Na 2 CO 3 ) og andre karbonater. Navnet lever videre som et trivielt navn .
Kjemiske egenskaper
Bikarbonationen (hydrogenkarbonationen) er en anion med den empiriske formelen HCO-
3og en molekylmasse på 61,01 dalton ; den består av ett sentralt karbonatom omgitt av tre oksygenatomer i et trigonal plant arrangement, med et hydrogenatom festet til en av oksygenene. Det er isoelektronisk med salpetersyre HNO
3. Bikarbonationen bærer en negativ formell ladning og er en amfiprotisk art som har både sure og basiske egenskaper. Det er både den konjugerte basen av karbonsyre H
2CO
3; og konjugerte syre av CO2−
3, karbonationen , som vist ved disse likevektsreaksjonene :
-
CO2−
3+ 2 H20, HCO-
3+ H 2 O + OH - ⇌ H 2 CO 3 + 2 OH -
- H 2 CO 3 + 2 H 2 O ⇌ HCO-
3+ H 3 O + + H 2 O ⇌ CO2−
3+ 2 H 3 O + .
Et bikarbonatsalt dannes når et positivt ladet ion fester seg til de negativt ladede oksygenatomene til ionet og danner en ionisk forbindelse . Mange bikarbonater er oppløselige i vann ved standard temperatur og trykk ; spesielt bidrar natriumbikarbonat til totalt oppløste faste stoffer , en vanlig parameter for vurdering av vannkvalitet .
Fysiologisk rolle
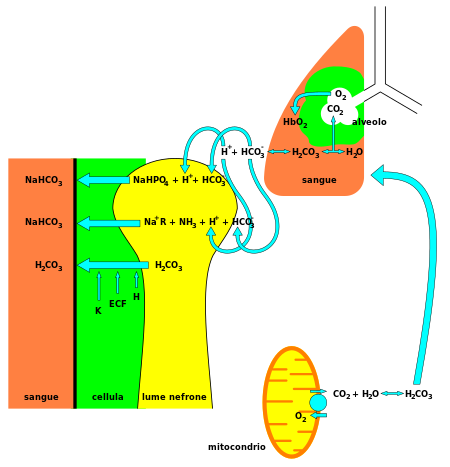
Bikarbonat ( HCO-
3) er en viktig komponent i pH -buffersystemet i menneskekroppen (opprettholder syre -base -homeostase ). 70% –75% av CO 2 i kroppen omdannes til karbonsyre (H 2 CO 3 ), som er konjugatsyren til HCO-
3 og kan fort bli til det.
Med karbonsyre som den sentrale mellomliggende art , bikarbonat - i forbindelse med vann, hydrogenioner , og karbondioksyd - danner dette buffersystem, som opprettholdes ved den flyktige likevekt som kreves for å tilveiebringe rask motstand mot pH-endringer i både de sure og basiske retninger . Dette er spesielt viktig for å beskytte vev i sentralnervesystemet , der pH -endringer for langt utenfor normalområdet i begge retninger kan vise seg å være katastrofale (se acidose eller alkalose ).
I tillegg spiller bikarbonat en nøkkelrolle i fordøyelsessystemet. Det øker den indre pH i magen, etter at svært sure fordøyelsessafter er ferdige med fordøyelsen av mat. Bikarbonat virker også for å regulere pH i tynntarmen. Det frigjøres fra bukspyttkjertelen som svar på hormonet sekretin for å nøytralisere det sure kimet som kommer inn i tolvfingertarmen fra magen.
Bikarbonat i miljøet
Bikarbonat er den dominerende formen for oppløst uorganisk karbon i sjøvann og i de fleste ferskvann. Som sådan er det en viktig synke i karbonsyklusen .
I ferskvannsøkologi frigjør sterk fotosyntetisk aktivitet av ferskvannsplanter i dagslys gassformig oksygen i vannet og produserer samtidig bikarbonationer. Disse forskyver pH -verdien oppover til graden av alkalinitet under visse omstendigheter kan bli giftig for noen organismer eller kan gjøre andre kjemiske bestanddeler som ammoniakk toksiske. I mørket, når ingen fotosyntese forekommer, frigjør respirasjonsprosesser karbondioksid, og det produseres ingen nye bikarbonationer, noe som resulterer i et raskt fall i pH.
Andre bruksområder
Det vanligste saltet av bikarbonationen er natriumbikarbonat , NaHCO 3 , som er kjent som natron . Ved oppvarming eller eksponering for en syre som eddiksyre ( eddik ) frigjør natriumbikarbonat karbondioksid . Dette brukes som et hevemiddel i baking .
Strømmen av bikarbonationer fra bergarter som forvitres av kolsyren i regnvann er en viktig del av karbonsyklusen .
Ammoniumbikarbonat brukes i produksjonen av fordøyelseskjeks .
Diagnostikk
I diagnostisk medisin er blodverdien av bikarbonat en av flere indikatorer på tilstanden til syrefasefysiologi i kroppen. Det måles sammen med karbondioksid , klorid , kalium og natrium for å vurdere elektrolyttnivået i en elektrolyttpaneltest (som har Current Procedural Terminology , CPT, kode 80051).
Parameteren standard bikarbonatkonsentrasjon (SBC e ) er bikarbonatkonsentrasjonen i blodet ved en P a CO 2 på 40 mmHg (5,33 kPa), full oksygenmetning og 36 ° C.
Bikarbonatforbindelser
- Natrium bikarbonat
- Kaliumbikarbonat
- Cesiumbikarbonat
- Magnesiumbikarbonat
- Kalsiumbikarbonat
- Ammoniumbikarbonat
- Kolsyre
Se også
Referanser
Eksterne linker
- Bikarbonater ved US National Library of Medicine Medical Subject Headings (MeSH)
