Blod -hjerne -barriere - Blood–brain barrier
| Blod-hjerne-barriere | |
|---|---|
 Oppløst permeabilitet ved BBB
vs. choroid plexus | |
| Detaljer | |
| System | Nevroimmunsystem |
| Identifikatorer | |
| Akronym (er) | BBB |
| MeSH | D001812 |
| Anatomisk terminologi | |
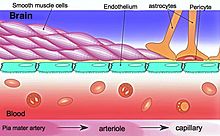
Den blod-hjerne-barrieren ( BBB ) er en meget selektiv semipermeabel grensen av endotelceller som hindrer oppløste stoffer i det sirkulerende blod fra ikke-selektivt krysset i den ekstracellulære væske fra det sentrale nervesystemet hvor nerveceller bor. Blod- hjerne barrieren er dannet av endotelceller i kapillære vegg , astrocyttkulturer slutt fot ensheathing den kapillære og pericytter innleiret i det kapillære basalmembran . Dette systemet tillater passage av noen små molekyler ved passiv diffusjon , samt selektiv og aktiv transport av ulike næringsstoffer, ioner, organiske anioner og makromolekyler som glukose og aminosyrer som er avgjørende for nevral funksjon.
Blod-hjerne-barrieren begrenser passasjen av patogener , diffusjon av oppløste stoffer i blodet og store eller hydrofile molekyler inn i cerebrospinalvæsken , samtidig som den tillater diffusjon av hydrofobe molekyler (O 2 , CO 2 , hormoner) og små ikke-polare molekyler. Barrierens celler transporterer aktivt metabolske produkter som glukose over barrieren ved hjelp av spesifikke transportproteiner . Barrieren begrenser også passasjen av perifere immunfaktorer, som signalmolekyler, antistoffer og immunceller, til CNS, og isolerer dermed hjernen fra skade på grunn av perifere immunhendelser.
Spesialiserte hjernestrukturer som deltar i sensorisk og sekretorisk integrasjon i hjernens nevrale kretsløp - de circumventrikulære organene og choroid plexus - har derimot svært gjennomtrengelige kapillærer.
Struktur

BBB kommer fra selektiviteten til de tette kryssene mellom endotelcellene i hjernekapillærene, og begrenser passering av oppløste stoffer. I grensesnittet mellom blod og hjerne er endotelceller tilstøtende kontinuerlig av disse tette veikryssene, som består av mindre underenheter av transmembrane proteiner , for eksempel occludin , claudiner (som Claudin-5 ), junctional adhesion molecule (for eksempel JAM- EN). Hvert av disse tette kryssproteinene er stabilisert til endotelcellemembranen av et annet proteinkompleks som inkluderer stillasproteiner som tett kryssprotein 1 (ZO1) og tilhørende proteiner.
BBB består av endotelceller som begrenser passering av stoffer fra blodet mer selektivt enn endotelceller fra kapillærer andre steder i kroppen. Astrocyttcelleprojeksjoner kalt astrocytiske føtter (også kjent som " glia limitans ") omgir endotelcellene til BBB, og gir biokjemisk støtte til disse cellene. BBB er forskjellig fra den ganske like blod-cerebrospinalvæskebarrieren , som er en funksjon av choroidale celler i choroid plexus , og fra blod-netthinnebarrieren , som kan betraktes som en del av hele området av slike barrierer.
Ikke alle kar i den menneskelige hjerne viser BBB -egenskaper. Noen eksempler på dette inkluderer de circumventrikulære organene , taket på den tredje og fjerde ventrikkel , kapillærer i pinealkjertelen på taket til diencephalon og pinealkjertelen . Pinealkjertelen utskiller hormonet melatonin "direkte inn i systemisk sirkulasjon", og derfor påvirkes ikke melatonin av blod -hjerne -barrieren.
Utvikling
BBB ser ut til å være funksjonell på fødselstidspunktet. P-glykoprotein , en transportør , eksisterer allerede i det embryonale endotelet.
Måling av hjerneopptak av forskjellige blodbårne oppløste stoffer viste at nyfødte endotelceller var funksjonelt lik de hos voksne, noe som indikerer at en selektiv BBB er aktiv ved fødselen.
Hos mus er Claudin-5-tapet under utvikling dødelig og resulterer i størrelsesselektiv løsning av BBB.
Funksjon
Blod -hjerne -barrieren virker effektivt for å beskytte hjernen mot sirkulerende patogener . Følgelig er blodbårne infeksjoner i hjernen sjeldne. Infeksjoner i hjernen som oppstår er ofte vanskelige å behandle. Antistoffer er for store til å krysse blod -hjerne -barrieren, og bare visse antibiotika kan passere. I noen tilfeller må et legemiddel administreres direkte i cerebrospinalvæsken hvor det kan komme inn i hjernen ved å krysse blod-cerebrospinalvæskebarrieren .
Blod -hjerne -barrieren kan bli lekker ved utvalgte nevrologiske sykdommer , for eksempel amyotrofisk lateral sklerose , epilepsi , hjernetraume og ødem, og ved systemiske sykdommer , som leversvikt . Blod -hjerne -barrieren blir mer gjennomtrengelig under betennelse , noe som muligens lar antibiotika og fagocytter bevege seg over BBB.
Sirkumventrikulære organer
Sirkumventrikulære organer (CVOer) er individuelle strukturer som ligger ved siden av den fjerde ventrikkel eller tredje ventrikkel i hjernen, og er preget av tette kapillarsenger med permeable endotelceller i motsetning til blod -hjernebarrieren. Inkludert blant CVOer som har svært gjennomtrengelige kapillærer er området postrema , subfornisk organ , vaskulært organ i lamina terminalis , median eminens , pinealkjertel og tre lapper i hypofysen .
Permeable kapillærer av de sensoriske CVOene (område postrema, subfornisk organ, vaskulært organ i lamina terminalis) muliggjør rask deteksjon av sirkulerende signaler i systemisk blod, mens de i de sekretoriske CVOene (median eminens, pinealkjertel, hypofyse -lapper) letter transport av hjernen -avledet signaler til sirkulerende blod. Følgelig er de CVO -permeable kapillærene poenget med toveis kommunikasjon mellom blod og hjerne for nevroendokrin funksjon.
Spesialiserte permeable soner
Randsonene mellom hjernevev "bak" blod -hjerne -barrieren og soner "åpne" for blodsignaler i visse CVO -er inneholder spesialiserte hybridkapillærer som er lekkere enn typiske hjernekapillærer, men ikke så gjennomtrengelige som CVO -kapillærer. Slike soner eksisterer på grensen til området postrema - nucleus tractus solitarii (NTS), og median eminence - hypotalamisk buet kjerne . Disse sonene ser ut til å fungere som hurtige transittområder for hjernestrukturer som er involvert i forskjellige nevrale kretser - som NTS og bueformet kjerne - for å motta blodsignaler som deretter overføres til nevral utgang. Den permeable kapillærsonen som deles mellom medianeminensen og den hypotalamiske bueformede kjernen forsterkes av brede perikapillære mellomrom, noe som letter toveis flyt av oppløste stoffer mellom de to strukturene, og indikerer at medianeminensen ikke bare er et sekretorisk organ, men også kan være et sanseorgan .
Terapeutisk forskning
Som et narkotikamål
Blod-hjerne-barrieren dannes av hjernens kapillære endotel og utelukker fra hjernen 100% av nevroterapi med store molekyler og mer enn 98% av alle småmolekylære legemidler. Å overvinne vanskeligheten med å levere terapeutiske midler til bestemte områder av hjernen er en stor utfordring for behandling av de fleste hjernesykdommer. I sin nevrobeskyttende rolle fungerer blod -hjerne -barrieren for å hindre levering av mange potensielt viktige diagnostiske og terapeutiske midler til hjernen. Terapeutiske molekyler og antistoffer som ellers kan være effektive i diagnostikk og terapi, krysser ikke BBB i tilstrekkelige mengder for å være klinisk effektive.
Mekanismer for narkotikamålretting i hjernen innebærer å gå enten "gjennom" eller "bak" BBB. Modaliteter for legemiddeltilførsel til hjernen i enhetsdoser gjennom BBB medfører at den forstyrres med osmotiske midler, eller biokjemisk ved bruk av vasoaktive stoffer, for eksempel bradykinin , eller til og med ved lokal eksponering for høyintensivt fokusert ultralyd (HIFU) .
Andre metoder som brukes for å komme gjennom BBB kan innebære bruk av endogene transportsystemer, inkludert bærermedierte transportører, for eksempel glukose- og aminosyrebærere, reseptormediert transcytose for insulin eller transferrin , og blokkering av aktive efflux-transportører som p -glykoprotein . Noen studier har vist at vektorer som er rettet mot BBB -transportører, for eksempel transferrinreseptoren , har vist seg å være fanget i endotelceller i hjernen i kapillærer, i stedet for å bli ferret over BBB inn i målområdet.
Nanopartikler
Nanoteknologi er under foreløpig forskning for potensialet for å lette overføring av legemidler over BBB. Kapillære endotelceller og tilhørende pericytter kan være unormale i svulster, og blod -hjerne -barrieren er ikke alltid intakt i hjernesvulster. Andre faktorer, for eksempel astrocytter , kan bidra til motstanden fra hjernesvulster mot terapi ved hjelp av nanopartikler. Fettløselige molekyler mindre enn 400 Dalton i vekt kan fritt diffundere forbi BBB gjennom lipid- mediert passiv diffusjon.
Historie
Paul Ehrlich var en bakteriolog som studerte farging , en prosedyre som brukes i mange mikroskopistudier for å gjøre fine biologiske strukturer synlige ved bruk av kjemiske fargestoffer. Da Ehrlich injiserte noen av disse fargestoffene (spesielt anilinfargestoffene som da ble mye brukt), farget fargestoffet alle organene til noen dyr, bortsett fra hjernen deres . På den tiden tilskrev Ehrlich denne mangelen på flekker til at hjernen ganske enkelt ikke tok opp så mye av fargestoffet.
Imidlertid, i et senere eksperiment i 1913, injiserte Edwin Goldmann (en av Ehrlichs studenter) fargestoffet direkte i cerebrospinalvæskene i dyrehjerner. Han fant ut at hjernen ble farget, men det gjorde ikke resten av kroppen, noe som demonstrerte eksistensen av en deling mellom de to. På den tiden ble det antatt at blodårene selv var ansvarlige for barrieren, siden det ikke ble funnet noen åpenbar membran. Konseptet med blod -hjerne -barrieren (den gang kalt hematoencephalic barriere ) ble foreslått av en Berlin -lege , Lewandowsky, i 1900.
Se også
- Blod -luftbarriere - Membran som skiller alveolær luft fra blod i lungekapillærer
- Blod -okulær barriere - Fysisk barriere mellom de lokale blodårene og de fleste deler av øyet selv
- Blod -netthinnebarriere - En del av blod -okulær barriere som forhindrer visse stoffer i å komme inn i netthinnen
- Blod -testis -barriere - En fysisk barriere mellom blodårene og seminiferous tubules av dyrestestene
- Blood – thymus barriere - Barriere dannet av de kontinuerlige blodkapillærene i thymic cortex