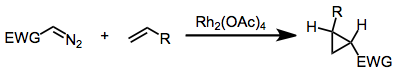Syklopropanering - Cyclopropanation
Syklopropanering refererer til enhver kjemisk prosess som genererer cyklopropanringer . Det er en viktig prosess i moderne kjemi da mange nyttige forbindelser bærer dette motivet; for eksempel pyretroider og et antall kinolonantibiotika ( ciprofloxacin , sparfloxacin , etc.). Imidlertid gjør den høye ringstammen som er tilstede i cyklopropaner dem utfordrende å produsere og krever generelt bruk av svært reaktive arter, slik som karbener , ylider og karbanioner . Mange av reaksjonene foregår på en cheletropisk måte.
Tilnærminger
Fra alkener som bruker karbenoidreagenser
Det finnes flere metoder for å konvertere alkener til cyklopropanringer ved hjelp av reagenser av karbentypen . Ettersom karbener i seg selv er svært reaktive, er det vanlig at de brukes i stabilisert form, referert til som karbenoid .
Simmons – Smith-reaksjon
I Simmons-Smith reaksjon av det reaktive carbenoid er iodomethylzinc jodid , som vanligvis er dannet ved en reaksjon mellom dijodmetan og en sink-kobber-par . Det er utviklet modifikasjoner som involverer billigere alternativer, slik som dibrometan eller diazometan og sinkjodid . Reaktiviteten til systemet kan også økes ved å bytte sink-kobberparet mot dietylsink . Asymmetriske versjoner er kjent.
Bruke diazoforbindelser
Visse diazo-forbindelser , slik som diazometan , kan reagere med olefiner for å produsere cyklopropaner på en 2-trinns måte. Det første trinnet involverer en 1,3-dipolær cykloaddisjon for å danne et pyrazolin som deretter gjennomgår denitrogenering, enten fotokjemisk eller ved termisk nedbrytning , for å gi cyklopropan. Den termiske ruten, som ofte bruker KOH og platina som katalysatorer, er også kjent som Kishner cyklopropansyntese etter den russiske kjemikeren Nikolai Kischner og kan også utføres ved bruk av hydrazin og α, β-umettede karbonylforbindelser . Nedbrytningsmekanismen har vært gjenstand for flere studier og er fortsatt noe kontroversiell, selv om det generelt er tenkt å gå via en diradisk art. Når det gjelder grønn kjemi, er denne metoden bedre enn andre karbenbaserte cyklopropanasjoner; ettersom det ikke involverer metaller eller halogenerte reagenser, og produserer bare N 2 som et biprodukt. Imidlertid kan reaksjonen være farlig da spormengder av ureagerte diazoforbindelser kan eksplodere under den termiske omorganiseringen av pyrazolinen.
Bruke diazoforbindelser med metallkatalyse
Metylfenyldiazoacetat og mange relaterte diazoderivater er forløpere for donor-akseptor-karbener , som kan brukes til cyklopropanering eller for å sette inn i CH-bindinger av organiske substrater. Disse reaksjonene katalyseres av dirhodium tetraacetat eller, mer spektakulært, relaterte chirale derivater.
Bruke gratis karbener
Gratis karbener kan brukes for cyklopropaneringsreaksjoner, men det er begrenset rom for dette, da få kan produseres beleilig og nesten alle er ustabile (se: karbendimerisering ). Et unntak er dihalocarbenes som dichlorocarbene eller difluorocarbene , som er rimelig stabile og vil reagere under dannelse av geminale dihalo-cyklopropaner. Disse forbindelsene kan deretter brukes til å danne allener via Skattebøl-omorganiseringen .
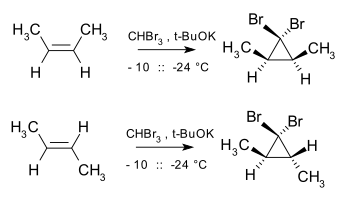
Den Buchner ringutvidelse reaksjon omfatter også dannelse av et stabilisert karben. Syklopropanering er også stereospesifikk da tilsetning av karben og karbenoider til alkener er en form for en cheletropisk reaksjon , med tilsetningen på en syn måte. For eksempel gir dibromokarben og cis -2-buten cis -2,3-dimetyl-1,1-dibromcyklopropan, mens trans- isomeren utelukkende gir trans- cyklopropan.
Fra alkener som bruker ylider
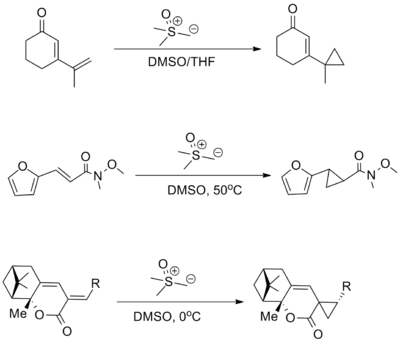
Syklopropaner kan genereres ved bruk av et svovelylid i Johnson – Corey – Chaykovsky-reaksjonen , men denne prosessen er i stor grad begrenset til bruk på elektronfattige olefiner, spesielt α, β-umettede karbonylforbindelser .
Intramolekylær syklisering
Syklopropaner kan oppnås ved en rekke intramolekylære sykliseringsreaksjoner . En enkel metode er å bruke primære haloalkaner som bærer passende plasserte elektronuttrekkende grupper. Behandling med en sterk base vil generere et karbanion som vil sykle på en 3-exo-trig måte, med fortrengning av halogenidet. Eksempler inkluderer dannelse av cyklopropylcyanid og cyklopropylacetylen. Denne mekanismen danner også grunnlaget for Favorskii-omorganiseringen .
En relatert prosess er sykliseringen av 1,3-dibromopropan via en Wurtz-kobling . Dette ble brukt til den første syntesen av cyklopropan av August Freund i 1881. Opprinnelig ble denne reaksjonen utført ved bruk av natrium, men utbyttet kan forbedres ved å bytte dette mot sink .
- BrCH'er 2- CH 2- CH 2- Br + 2 Na → (CH 2 ) 3 + 2 NaBr
Andre tilnærminger
- De Kulinkovich reaksjon danner cyclopropanols via en reaksjon mellom estere og Grignard-reagenser i nærvær av et titanalkoksyd.
- Den Bingel reaksjon er en spesialisert cyklopropanering reaksjon brukt til functionalise en Fulle .
- I di-pi-metan-omorganiseringen får fotokjemisk stimulering 1,4-diener til å omorganisere for å danne vinylsyklopropaner. Disse kan deretter gjennomgå omorganiseringer av vinylcyklopropan
- Syklopropan-fett-acyl-fosfolipidsyntase utfører cyklopropanering er biologiske systemer
Biosyntese

Selv om cyklopropaner er relativt sjeldne i biokjemi, har mange cyklopropaneringsveier blitt identifisert i naturen. De vanligste banene involverer ringlukkingsreaksjoner av karbokasjoner i terpenoider . Syklopropanfettsyrer er avledet fra angrepet av S-adenosylmetionin (SAM) på umettede fettsyrer. Forløperen til hormonet etylen , 1-aminocyklopropan-1-karboksylsyre er avledet direkte fra SMM via intramolekylær nukleofil fortrengning av SMe 2- gruppen etter kondensering med pyridoksalfosfat . Direkte karbenoverføring fra diazoestere til olefiner har også blitt oppnådd gjennom in vitro biokatalyse ved hjelp av konstruerte varianter av cytokrom P450- enzymet fra Bacillus megaterium som ble optimalisert av direkte utvikling .