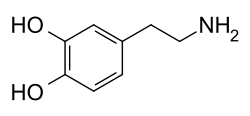
Dopamin - Dopamine

Skjelettformel av dopamin
| |

| |
| Kliniske data | |
|---|---|
| Andre navn | |
| Fysiologiske data | |
| Kilde vev | Substantia nigra ; ventralt tegmentalt område ; mange andre |
| Målvev | Systemomfattende |
| Reseptorer | D 1 , D 2 , D 3 , D 4 , D 5 , TAAR1 |
| Agonister | Direkte: apomorfin , bromokriptin Indirekte : kokain , amfetamin |
| Antagonister | Nevroleptika , metoklopramid , domperidon |
| Forløper | Fenylalanin , tyrosin og L-DOPA |
| Biosyntese | DOPA dekarboksylase |
| Metabolisme | MAO , KOMT |
| Identifikatorer | |
| |
| CAS -nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.000.101 |
| Kjemiske og fysiske data | |
| Formel | C 8 H 11 N O 2 |
| Molar masse | 153,181 g · mol −1 |
| 3D -modell ( JSmol ) | |
| |
| |
Dopamin ( DA , en sammentrekning av 3,4- d ihydr o xy p henethyl amin ) er en neurotransmitter som spiller flere viktige roller i hjerne og kropp. Det er en organisk kjemikalie fra katekolamin- og fenetylaminfamiliene . Dopamin utgjør omtrent 80% av katekolamininnholdet i hjernen. Det er et amin syntetisert ved å fjerne en karboksylgruppe fra et molekyl av dets forløperkjemikalie , L-DOPA , som syntetiseres i hjernen og nyrene. Dopamin syntetiseres også i planter og de fleste dyr. I hjernen fungerer dopamin som en nevrotransmitter - et kjemikalie som frigjøres av nevroner (nerveceller) for å sende signaler til andre nerveceller. Neurotransmittere syntetiseres i bestemte områder av hjernen, men påvirker mange regioner systemisk. Hjernen inkluderer flere forskjellige dopaminveier , hvorav den ene spiller en stor rolle i den motiverende komponenten i belønningsmotivert oppførsel . Forventningen til de fleste typer belønninger øker nivået av dopamin i hjernen, og mange vanedannende legemidler øker frigivelsen av dopamin eller blokkerer gjenopptaket til nevroner etter frigjøring. Andre hjernedopaminveier er involvert i motorisk kontroll og kontroll av frigjøring av forskjellige hormoner. Disse veiene og cellegruppene danner et dopaminsystem som er nevromodulerende .
I populærkultur og medier blir dopamin ofte fremstilt som hovedkjemikalien for nytelse, men den nåværende oppfatningen i farmakologi er at dopamin i stedet gir motivasjonskraft ; Med andre ord signalerer dopamin den oppfattede motiverende fremtredelsen (dvs. ønsket eller avsky) til et resultat, som igjen driver organismenes oppførsel mot eller bort fra å oppnå det resultatet.
Utenfor sentralnervesystemet fungerer dopamin først og fremst som en lokal parakrin messenger. I blodårene hemmer det frigjøring av noradrenalin og fungerer som en vasodilatator (ved normale konsentrasjoner); i nyrene øker det natriumutskillelsen og urinproduksjonen; i bukspyttkjertelen reduserer det insulinproduksjonen; i fordøyelsessystemet reduserer det gastrointestinal motilitet og beskytter tarmslimhinnen ; og i immunsystemet reduserer det aktiviteten til lymfocytter . Med unntak av blodårene syntetiseres dopamin i hvert av disse perifere systemene lokalt og utøver virkningen nær cellene som frigjør det.
Flere viktige sykdommer i nervesystemet er forbundet med dysfunksjoner i dopaminsystemet, og noen av de viktigste medisinene som brukes for å behandle dem, virker ved å endre effekten av dopamin. Parkinsons sykdom , en degenerativ tilstand som forårsaker skjelving og motorisk svekkelse, er forårsaket av tap av dopamin-utskillende nevroner i et område i mellomhjernen som kalles substantia nigra . Dens metabolske forløper L-DOPA kan produseres; Levodopa , en ren form for L-DOPA, er den mest brukte behandlingen for Parkinson. Det er bevis på at schizofreni innebærer endrede nivåer av dopaminaktivitet, og de fleste antipsykotiske legemidler som brukes for å behandle dette er dopaminantagonister som reduserer dopaminaktiviteten. Lignende dopaminantagonistmedisiner er også noen av de mest effektive anti-kvalme-midlene . Restless legs syndrom og oppmerksomhetsunderskudd hyperaktivitetsforstyrrelse (ADHD) er forbundet med redusert dopaminaktivitet. Dopaminerge sentralstimulerende midler kan være vanedannende i høye doser, men noen brukes ved lavere doser for å behandle ADHD. Dopamin i seg selv er tilgjengelig som en produsert medisin for intravenøs injeksjon : selv om det ikke kan nå hjernen fra blodet , gjør dets perifere effekter det nyttig i behandlingen av hjertesvikt eller sjokk , spesielt hos nyfødte babyer.
Struktur
Et dopaminmolekyl består av en katekolstruktur (en benzenring med to hydroksylsidegrupper ) med en amingruppe festet via en etylkjede . Som sådan er dopamin den enkleste mulige katekolaminen , en familie som også inkluderer nevrotransmittere noradrenalin og adrenalin . Tilstedeværelsen av en benzenring med dette aminvedlegget gjør det til et substituert fenetylamin , en familie som inneholder mange psykoaktive legemidler .
Som de fleste aminer er dopamin en organisk base . Som en base er den vanligvis protonert i sure omgivelser (i en syre-base-reaksjon ). Den protonerte formen er svært vannløselig og relativt stabil, men kan bli oksidert hvis den utsettes for oksygen eller andre oksidanter . I grunnleggende miljøer protoneres ikke dopamin. I denne frie baseformen er den mindre vannløselig og også mer reaktiv. På grunn av den økte stabilitet og vannoppløselighet av den protonerte form, er dopamin leveres for kjemiske eller farmasøytiske anvendelse som dopamin -hydroklorid -at er, jo hydroklorid salt som opprettes når dopamin er kombinert med saltsyre . I tørr form er dopaminhydroklorid et fint pulver som er hvitt til gult.
Biokjemi
|
|
Syntese
Dopamin er syntetisert i et begrenset sett av celletyper, hovedsakelig nevroner og celler i margen av binyrene . De primære og mindre metabolske veiene er henholdsvis:
- Primær: L -Penylalanin → L -Tyrosin → L -DOPA → Dopamin
- Mindre: L -Penylalanin → L -Tyrosin → p -Tyramin → Dopamin
- Mindre: L -Penylalanin → m -Tyrosin → m -Tyramin → Dopamin
Den direkte forløperen til dopamin, L -DOPA , kan syntetiseres indirekte fra den essensielle aminosyren fenylalanin eller direkte fra den ikke -essensielle aminosyren tyrosin . Disse aminosyrene finnes i nesten alle proteiner og er derfor lett tilgjengelige i matvarer, og tyrosin er den vanligste. Selv om dopamin også finnes i mange typer mat, er den ikke i stand til å krysse blod -hjernebarrieren som omgir og beskytter hjernen. Det må derfor syntetiseres inne i hjernen for å utføre sin neuronale aktivitet .
L -Fenylalanin omdannes til L -tyrosin av enzymet fenylalaninhydroksylase , med molekylært oksygen (O 2 ) og tetrahydrobiopterin som kofaktorer . L -tyrosin omdannes til L -DOPA av enzymet tyrosin hydroksylase , med tetrahydrobiopterin, O 2 , og jern (Fe 2+ ) som kofaktorer. L -DOPA omdannes til dopamin ved hjelp av enzymet aromatisk L -aminosyre-decarboxylase (også kjent som DOPA decarboxylase), med pyridoxalfosfat som kofaktor.
Selve dopamin brukes som forløper i syntesen av nevrotransmitterne noradrenalin og adrenalin. Dopamin omdannes til noradrenalin av enzymet dopamin β -hydroksylase , med O 2 og L -askorbinsyre som kofaktorer. Norepinefrin omdannes til epinefrin av enzymet fenyletanolamin N -metyltransferase med S -adenosyl -L -metionin som kofaktor.
Noen av kofaktorene krever også sin egen syntese. Mangel på nødvendig aminosyre eller kofaktor kan svekke syntesen av dopamin, noradrenalin og adrenalin.
Nedbrytning
Dopamin brytes ned til inaktive metabolitter av et sett med enzymer - monoaminoxidase (MAO), katekol -O -metyltransferase (COMT) og aldehyddehydrogenase (ALDH), som virker i rekkefølge. Begge isoformer av monoaminoxidase, MAO-A og MAO-B , metaboliserer effektivt dopamin. Det finnes forskjellige nedbrytningsveier, men hovedproduktet er homovanillinsyre (HVA), som ikke har noen kjent biologisk aktivitet. Fra blodet filtreres homovanillinsyre ut av nyrene og skilles deretter ut i urinen. De to primære metabolske rutene som omdanner dopamin til HVA er:
- Dopamin → DOPAL → DOPAC → HVA - katalysert av henholdsvis MAO, ALDH og COMT
- Dopamin → 3-Methoxytyramine → HVA-katalysert av henholdsvis COMT og MAO+ALDH
I klinisk forskning på schizofreni har målinger av homovanillinsyre i plasma blitt brukt til å estimere nivåer av dopaminaktivitet i hjernen. En vanskelighet i denne tilnærmingen er imidlertid å skille det høye nivået av homovanillinsyre i plasma som metaboliseres av noradrenalin.
Selv om dopamin normalt brytes ned av et oksidoreduktase -enzym, er det også utsatt for oksidasjon ved direkte reaksjon med oksygen, noe som gir kinoner pluss forskjellige frie radikaler som produkter. Oksidasjonshastigheten kan økes ved tilstedeværelse av jern ( jern) eller andre faktorer. Kinoner og frie radikaler produsert ved autoksydasjon av dopamin kan forgifte celler , og det er bevis på at denne mekanismen kan bidra til celletapet som oppstår ved Parkinsons sykdom og andre tilstander.
Funksjoner
Mobileffekter
| Familie | Reseptor | Gene | Type | Mekanisme |
|---|---|---|---|---|
| D1-aktig | D 1 | DRD1 | G s -koblet. | Øk intracellulære nivåer av cAMP ved å aktivere adenylatsyklase . |
| D 5 | DRD5 | |||
| D2-aktig | D 2 | DRD2 | G i -koblet. | Reduser intracellulære nivåer av cAMP ved å hemme adenylatsyklase . |
| D 3 | DRD3 | |||
| D 4 | DRD4 | |||
| TAAR | TAAR1 | TAAR1 |
G s -koblet. G q -koblet. |
Øk intracellulære nivåer av cAMP og intracellulær kalsiumkonsentrasjon. |
Dopamin utøver virkningen ved å binde seg til og aktivere celleoverflatereseptorer . Hos mennesker har dopamin en høy bindingsaffinitet for dopaminreseptorer og humant sporamin -assosiert reseptor 1 (hTAAR1). Hos pattedyr er det identifisert fem undertyper av dopaminreseptorer , merket fra D1 til D5. Alle fungerer som metabotrope , G-proteinkoblede reseptorer , noe som betyr at de utøver virkningen via et komplekst andre messenger-system . Disse reseptorene kan deles inn i to familier, kjent som D1-lignende og D2-lignende . For reseptorer lokalisert på nevroner i nervesystemet, kan den endelige effekten av D1-lignende aktivering (D1 og D5) være eksitasjon (via åpning av natriumkanaler ) eller inhibering (via åpning av kaliumkanaler ); den endelige effekten av D2-lignende aktivering (D2, D3 og D4) er vanligvis inhibering av målneuronet. Følgelig er det feil å beskrive dopamin i seg selv som enten eksitatorisk eller hemmende: dets effekt på et målneuron avhenger av hvilke typer reseptorer som er tilstede på membranen til nevronet og de interne responsene til nevronet til det andre budbringer -cAMP . D1 -reseptorer er de mest tallrike dopaminreseptorene i det menneskelige nervesystemet; D2 -reseptorer er neste; D3-, D4- og D5 -reseptorer er tilstede på betydelig lavere nivåer.
Lagring, frigjøring og gjenopptak
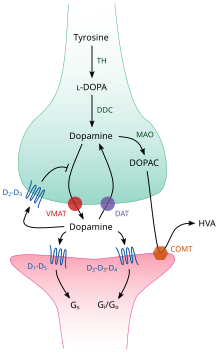
TH: tyrosinhydroksylase
DOPA: L-DOPA
DAT: dopamintransportør
DDC: DOPA dekarboksylase
VMAT: vesikulær monoamintransportør 2
MAO: Monoaminoxidase
COMT: Catechol-O- metyltransferase
HVA: Homovanillinsyre
Inne i hjernen fungerer dopamin som en nevrotransmitter og nevromodulator , og styres av et sett med mekanismer som er felles for alle monoamint neurotransmittere . Etter syntese transporteres dopamin fra cytosolen til synaptiske vesikler av en oppløst bærer - en vesikulær monoamintransportør , VMAT2 . Dopamin lagres i disse vesiklene til det blir kastet ut i den synaptiske kløften . I de fleste tilfeller skjer frigivelsen av dopamin gjennom en prosess som kalles eksocytose som er forårsaket av handlingspotensialer , men det kan også skyldes aktiviteten til en intracellulær sporamin-assosiert reseptor , TAAR1 . TAAR1 er en reseptor med høy affinitet for dopamin, sporaminer og visse substituerte amfetaminer som ligger langs membraner i det intracellulære miljøet i den presynaptiske cellen; aktivering av reseptoren kan regulere dopaminsignalering ved å indusere dopamin gjenopptakshemming og efflux , samt ved å hemme neuronal avfyring gjennom et mangfoldig sett med mekanismer.
Når den er i synapsen, binder dopamin seg til og aktiverer dopaminreseptorer. Dette kan være postsynaptiske dopaminreseptorer, som er lokalisert på dendritter (det postsynaptiske nevronet), eller presynaptiske autoreceptorer (f.eks. D 2 sh- og presynaptiske D 3 -reseptorer), som er lokalisert på membranen i en aksonterminal (det presynaptiske nevronet) . Etter at det postsynaptiske nevronet fremkaller et handlingspotensial, blir dopaminmolekyler raskt ubundne fra reseptorene. De absorberes deretter tilbake til den presynaptiske cellen, via gjenopptak formidlet enten av dopamintransportøren eller av plasmamembranen monoamintransportør . Når den er tilbake i cytosolen, kan dopamin enten brytes ned av en monoaminoxidase eller pakkes om til vesikler av VMAT2, noe som gjør den tilgjengelig for fremtidig frigjøring.
I hjernen moduleres nivået av ekstracellulær dopamin av to mekanismer: fasisk og tonisk overføring . Fasisk frigjøring av dopamin, som de fleste frigjøringer av nevrotransmitter i nervesystemet, drives direkte av handlingspotensialer i de dopaminholdige cellene. Tonisk dopamintransmisjon oppstår når små mengder dopamin frigjøres uten at presynaptiske handlingspotensialer går foran. Tonisk overføring reguleres av en rekke faktorer, inkludert aktiviteten til andre nevroner og gjenopptak av nevrotransmitter.
Nervesystemet

Inne i hjernen spiller dopamin viktige roller i utøvende funksjoner , motorisk kontroll , motivasjon , opphisselse , forsterkning og belønning , samt funksjoner på lavere nivå, inkludert amming , seksuell tilfredsstillelse og kvalme . De dopaminerge cellegruppene og veiene utgjør dopaminsystemet som er nevromodulerende .
Dopaminerge nevroner (dopaminproduserende nerveceller) er relativt få i antall-totalt rundt 400 000 i den menneskelige hjerne-og cellelegemene er begrenset i grupper til noen få relativt små hjerneområder. Men deres aksoner prosjektet til mange andre områder av hjernen, og de utøver kraftige effekter på sine mål. Disse dopaminerge cellegruppene ble først kartlagt i 1964 av Annica Dahlström og Kjell Fuxe, som tildelte dem etiketter som begynte med bokstaven "A" (for "aminergisk"). I deres opplegg inneholder områdene A1 til A7 nevrotransmitteren noradrenalin, mens A8 til A14 inneholder dopamin. De dopaminerge områdene de identifiserte er substantia nigra (gruppe 8 og 9); det ventrale tegmentale området (gruppe 10); posterior hypothalamus (gruppe 11); den bueformede kjernen (gruppe 12); den zona incerta (gruppe 13) og den periventrikulær kjernen (gruppe 14).
Substantia nigra er et lite mellomhjerneområde som danner en komponent i basalganglier . Dette har to deler - et inngangsområde kalt pars compacta og et utgangsområde pars reticulata . De dopaminerge nevronene finnes hovedsakelig i pars compacta (cellegruppe A8) og i nærheten (gruppe A9). Hos mennesker spiller projeksjonen av dopaminerge nevroner fra substantia nigra pars compacta til dorsal striatum, kalt nigrostriatal -banen , en betydelig rolle i kontrollen av motorisk funksjon og for å lære nye motoriske ferdigheter . Disse nevronene er spesielt sårbare for skader, og når et stort antall av dem dør, er resultatet et parkinsonistisk syndrom .
Det ventrale tegmentale området (VTA) er et annet mellomhjerneområde. Den mest fremtredende gruppen av VTA dopaminerge nevroner prosjekterer til prefrontal cortex via den mesokortiske banen og en annen mindre gruppe prosjekterer til nucleus accumbens via mesolimbic pathway . Til sammen betegnes disse to veiene samlet som mesokortikolimbisk projeksjon . VTA sender også dopaminerge projeksjoner til amygdala , cingulate gyrus , hippocampus og olfaktorisk pære . Mesokortikolimbiske nevroner spiller en sentral rolle i belønning og andre aspekter av motivasjon. Akkumulerende litteratur viser at dopamin også spiller en avgjørende rolle i aversiv læring gjennom dens effekter på en rekke hjerneområder.
Den bakre hypothalamus har dopamin -nevroner som projiserer til ryggmargen, men deres funksjon er ikke godt etablert. Det er noen bevis på at patologi i dette området spiller en rolle ved restless legs syndrom, en tilstand der folk har problemer med å sove på grunn av en overveldende tvang til å konstant bevege deler av kroppen, spesielt bena.
Den bueformede kjernen og den periventrikulære kjernen i hypothalamus har dopamin -nevroner som danner en viktig projeksjon - tuberoinfundibular -banen som går til hypofysen , hvor den påvirker utskillelsen av hormonet prolaktin . Dopamin er den primære nevroendokrine hemmeren for utskillelse av prolaktin fra den fremre hypofysen . Dopamin produsert av nevroner i den bueformede kjernen skilles ut i det hypofysiske portalsystemet til medianeminensen , som forsyner hypofysen . De prolaktin celler som produserer prolaktin, i fravær av dopamin utskiller prolaktin kontinuerlig; dopamin hemmer denne sekresjonen. I sammenheng med regulering av prolaktinsekresjon kalles dopamin tidvis prolaktinhemmende faktor, prolaktinhemmende hormon eller prolaktostatin.
Zona incerta, gruppert mellom de buede og periventrikulære kjernene, projiserer til flere områder av hypothalamus og deltar i kontrollen av gonadotropinfrigivende hormon , som er nødvendig for å aktivere utviklingen av mannlige og kvinnelige reproduktive systemer etter puberteten.
En ekstra gruppe dopamin-utskillende nevroner finnes i øyets netthinne . Disse nevronene er amakrinceller , noe som betyr at de ikke har noen axoner. De frigjør dopamin til det ekstracellulære mediet, og er spesielt aktive i dagslys, og blir stille om natten. Dette netthinnedopaminet øker aktiviteten til kjegleceller i netthinnen mens det undertrykker stavceller - resultatet er å øke følsomheten for farge og kontrast under sterke lysforhold, på bekostning av redusert følsomhet når lyset er svakt.
Basal ganglia

De største og viktigste kildene til dopamin i virveldyrhjernen er substantia nigra og ventralt tegmentalt område. Disse strukturene er nært beslektet med hverandre og funksjonelt like på mange måter. Begge er komponenter i midten av hjernen. Den største komponenten i basalganglier er striatum. Substantia nigra sender en dopaminerg projeksjon til dorsal striatum , mens det ventrale tegmentale området sender en lignende type dopaminerg projeksjon til det ventrale striatum .
Fremskritt i forståelsen av funksjonene til basalganglier har vært treg. De mest populære hypotesene, bredt sagt, foreslår at basalganglier spiller en sentral rolle i handlingsvalg . Handlingsvalgteorien i sin enkleste form foreslår at når en person eller et dyr er i en situasjon der flere atferd er mulige, avgjør aktivitet i basalgangliene hvilken av dem som utføres, ved å frigjøre responsen fra inhibering mens den fortsetter å hemme andre motoriske systemer at hvis den aktiveres vil det generere konkurrerende atferd. Derfor er basalganglier i dette konseptet ansvarlig for å starte atferd, men ikke for å bestemme detaljene for hvordan de utføres. Med andre ord danner de i hovedsak et beslutningssystem.
Basalganglier kan deles inn i flere sektorer, og hver er involvert i å kontrollere bestemte typer handlinger. Den ventrale sektoren i basalganglier (som inneholder det ventrale striatum og det ventrale tegmentale området) opererer på det høyeste nivået i hierarkiet, og velger handlinger på hele organismenivå. Dorsalsektorene (som inneholder dorsal striatum og substantia nigra) opererer på lavere nivåer, og velger de spesifikke musklene og bevegelsene som brukes for å implementere et gitt atferdsmønster.
Dopamin bidrar til handlingsvalgprosessen på minst to viktige måter. Først setter den "terskelen" for å sette i gang handlinger. Jo høyere nivå av dopaminaktivitet, jo lavere drivkraft kreves for å fremkalle en gitt oppførsel. Som en konsekvens fører høye nivåer av dopamin til høye nivåer av motorisk aktivitet og impulsiv oppførsel ; lave nivåer av dopamin fører til torpor og reduserte reaksjoner. Parkinsons sykdom, der dopaminnivået i substantia nigra -kretsen er sterkt redusert, er preget av stivhet og vanskeligheter med å starte bevegelse - men når mennesker med sykdommen blir konfrontert med sterke stimuli som en alvorlig trussel, kan reaksjonene deres være like kraftige som de til en frisk person. I motsatt retning kan medisiner som øker frigivelsen av dopamin, for eksempel kokain eller amfetamin, gi økt aktivitet, inkludert ekstrem psykomotorisk agitasjon og stereotype bevegelser .
Den andre viktige effekten av dopamin er som et "undervisnings" signal. Når en handling etterfølges av en økning i dopaminaktivitet, endres basalganglierkretsen på en måte som gjør det samme svar lettere å fremkalle når lignende situasjoner oppstår i fremtiden. Dette er en form for operasjonell kondisjonering , der dopamin spiller rollen som et belønningssignal.
Belønning
På språket som brukes til å diskutere belønningssystemet, er belønning den attraktive og motiverende egenskapen til en stimulans som induserer appetittfull atferd (også kjent som tilnærmingsatferd) og fullstendig atferd . En givende stimulans er en som kan få organismen til å nærme seg den og velge å konsumere den. Nytelse , læring (f.eks. Klassisk og operant kondisjonering ) og tilnærmingsatferd er de tre hovedfunksjonene til belønning. Som et aspekt av belønning gir nytelse en definisjon av belønning; mens alle lystbetont stimuli er givende, er imidlertid ikke alle givende stimuli behagelige (f.eks. ekstrinsiske belønninger som penger). Det motiverende eller ønskelige aspektet ved givende stimuli gjenspeiles av tilnærmingsatferden de induserer, mens gleden av inneboende belønninger skyldes å konsumere dem etter å ha skaffet dem. En nevropsykologisk modell som skiller disse to komponentene i en iboende givende stimulans, er incentivmotstandsmodellen , der "ønsker" eller begjær (mindre vanlig, "søker") tilsvarer appetitt- eller tilnærmingsatferd, mens "liker" eller nytelse tilsvarer fullført atferd. Hos mennesker som er rusmisbrukere , blir "det å savne" dissosiert med "å like" ettersom ønsket om å bruke et avhengighetsskapende stoff øker, mens gleden man får ved å konsumere det, reduseres på grunn av stofftoleranse .
I hjernen fungerer dopamin delvis som et globalt belønningssignal. En innledende dopamin respons på en stimulus givende koder for informasjon om den salience , verdi, og sammenheng av en belønning. I forbindelse med belønningsrelatert læring fungerer dopamin også som et belønningsprediksjonssignal , det vil si i hvilken grad verdien av en belønning er uventet. I følge denne hypotesen foreslått av Montague, Dayan og Sejnowski, gir belønninger som forventes ikke en annen fasisk dopaminrespons i visse dopaminerge celler, men belønninger som er uventede eller større enn forventet, gir en kortvarig økning i synaptisk dopamin , mens utelatelse av en forventet belønning faktisk fører til at dopaminfrigivelsen faller under bakgrunnsnivået. "Forutsigelsesfeil" -hypotesen har trukket særlig interesse fra beregningsnevrovitenskapsmenn, fordi en innflytelsesrik beregningsmessig læringsmetode kjent som tidsmessig forskjellslæring gjør stor bruk av et signal som koder for prediksjonsfeil. Denne sammensmeltningen av teori og data har ført til et fruktbart samspill mellom nevrovitere og datavitenskapere som er interessert i maskinlæring .
Bevis fra mikroelektrodeopptak fra hjernen til dyr viser at dopamin -nevroner i det ventrale tegmentale området (VTA) og substantia nigra er sterkt aktivert av et stort antall givende hendelser. Disse belønningsresponsive dopamin-nevronene i VTA og substantia nigra er avgjørende for belønningsrelatert kognisjon og fungerer som den sentrale komponenten i belønningssystemet. Funksjonen til dopamin varierer i hver aksonal projeksjon fra VTA og substantia nigra; for eksempel tildeler VTA– nucleus accumbens skallprojeksjon incentiv salience ("want") til givende stimuli og tilhørende signaler , oppdaterer VTA– prefrontal cortex -projeksjon verdien av forskjellige mål i samsvar med deres insentivmotstand, VTA - amygdala og VTA-hippocampus-projeksjoner formidler konsolidering av belønningsrelaterte minner, og både VTA– nucleus accumbens core og substantia nigra-dorsal striatumveier er involvert i læring av motoriske responser som letter tilegnelse av givende stimuli. Noe aktivitet i VTA dopaminerge anslag ser ut til å være assosiert med belønningsprediksjon også.
Glede
Mens dopamin har en sentral rolle i å forårsake "lyst", assosiert med de appetittfulle eller tilnærmede atferdsresponsene til givende stimuli, har detaljerte studier vist at dopamin ikke bare kan likestilles med hedonisk "liking" eller nytelse, som gjenspeiles i den fullstendige atferdsresponsen. Dopamin-nevrotransmisjon er involvert i noen, men ikke alle aspekter av fornøyelsesrelatert kognisjon, siden nytelsessentre har blitt identifisert både i dopaminsystemet (dvs. nucleus accumbens shell) og utenfor dopaminsystemet (dvs. ventral pallidum og parabrachial kjerne ). For eksempel oppleves direkte elektrisk stimulering av dopaminveier, ved bruk av elektroder implantert i hjernen, og mange typer dyr er villige til å arbeide for å få det. Antipsykotiske legemidler reduserer dopaminnivået og har en tendens til å forårsake anhedoni , en redusert evne til å oppleve nytelse. Mange typer gledelige opplevelser - som sex, spising og spill av videospill - øker frigivelsen av dopamin. Alle vanedannende legemidler påvirker direkte eller indirekte dopamin -nevrotransmisjon i nucleus accumbens; disse stoffene øker stoffets "mangel", noe som fører til tvangsmessig bruk av narkotika, når de gjentas flere ganger i høye doser, antagelig gjennom sensibilisering av insentiv-salience . Legemidler som øker synaptiske dopaminkonsentrasjoner inkluderer psykostimulerende midler som metamfetamin og kokain. Disse gir økt "ønsket" atferd, men endrer ikke uttrykk for glede eller endring av metning. Imidlertid gir opiatmedisiner som heroin og morfin økning i uttrykk for "liking" og "lyst" atferd. Dessuten søker dyr der det ventrale tegmentale dopaminsystemet har blitt gjort inaktive, ikke mat, og vil sulte ihjel hvis de blir overlatt til seg selv, men hvis mat legges i munnen, vil de konsumere det og vise uttrykk som tyder på nytelse.
En klinisk studie fra januar 2019 som vurderte effekten av en dopaminforløper ( levodopa ), dopaminantagonist ( risperidon ) og en placebo på belønningssvar på musikk - inkludert graden av glede som oppleves under musikalske frysninger , målt ved endringer i elektrodermal aktivitet så vel som subjektive vurderinger - fant ut at manipulering av dopamin -nevrotransmisjon toveis regulerer nytelseskognisjon (spesielt den hedoniske virkningen av musikk ) hos mennesker. Denne forskningen viser at økt dopamin neurotransmission fungerer som en ufravikelig forutsetning for behage hedonic reaksjoner på musikk hos mennesker.
Utenfor nervesystemet
Dopamin krysser ikke blod -hjerne -barrieren, så syntesen og funksjonene i perifere områder er i stor grad uavhengige av syntesen og funksjonene i hjernen. En betydelig mengde dopamin sirkulerer i blodet, men funksjonene der er ikke helt klare. Dopamin er funnet i blodplasma på nivåer sammenlignbare med de av epinefrin, men i mennesker, over 95% av dopamin i plasma er i form av dopamin sulfat , et konjugat produsert av enzymet sulfotransferase 1A3 / 1A4 virker på fri dopamin. Hoveddelen av dette dopaminsulfatet produseres i mesenteriet som omgir deler av fordøyelsessystemet. Produksjonen av dopaminsulfat antas å være en mekanisme for avgiftning av dopamin som inntas som mat eller produseres av fordøyelsesprosessen-nivåene i plasma stiger vanligvis mer enn femti ganger etter et måltid. Dopaminsulfat har ingen kjente biologiske funksjoner og skilles ut i urinen.
Den relativt lille mengden ukonjugert dopamin i blodet kan produseres av det sympatiske nervesystemet , fordøyelsessystemet eller muligens andre organer. Det kan virke på dopaminreseptorer i perifert vev, eller metaboliseres, eller konverteres til noradrenalin av enzymet dopamin beta -hydroksylase , som frigjøres til blodet av binyrebarken. Noen dopaminreseptorer er plassert i veggene i arteriene, hvor de fungerer som en vasodilatator og en hemmer av frigjøring av noradrenalin. Disse svarene kan bli aktivert av dopamin som frigjøres fra halspulsdelen under forhold med lite oksygen, men om arterielle dopaminreseptorer utfører andre biologisk nyttige funksjoner er ikke kjent.
Utover sin rolle i modulering av blodstrømmen, er det flere perifere systemer der dopamin sirkulerer innenfor et begrenset område og utfører en eksokrin eller parakrin funksjon. De perifere systemene der dopamin spiller en viktig rolle inkluderer immunsystemet , nyrene og bukspyttkjertelen .
Immunforsvar
I immunsystemet virker dopamin på reseptorer som er tilstede på immunceller, spesielt lymfocytter . Dopamin kan også påvirke immunceller i milten , benmargen og sirkulasjonssystemet . I tillegg kan dopamin syntetiseres og frigjøres av immunceller selv. Hovedvirkningen av dopamin på lymfocytter er å redusere aktiveringsnivået. Den funksjonelle betydningen av dette systemet er uklar, men det gir en mulig rute for interaksjoner mellom nervesystemet og immunsystemet, og kan være relevant for noen autoimmune lidelser.
Nyrer
Det renale dopaminerge systemet er lokalisert i cellene til nefronet i nyrene, hvor alle subtyper av dopaminreseptorer er tilstede. Dopamin syntetiseres også der, av tubulære celler, og slippes ut i rørformet væske . Dets handlinger inkluderer å øke blodtilførselen til nyrene, øke den glomerulære filtreringshastigheten og øke utskillelsen av natrium i urinen. Derfor kan defekter i nyre dopaminfunksjon føre til redusert utskillelse av natrium og følgelig resultere i utvikling av høyt blodtrykk . Det er sterke bevis på at feil i produksjonen av dopamin eller i reseptorene kan resultere i en rekke patologier, inkludert oksidativt stress , ødem og enten genetisk eller essensiell hypertensjon. Oksidativt stress kan i seg selv forårsake hypertensjon. Defekter i systemet kan også skyldes genetiske faktorer eller høyt blodtrykk.
Bukspyttkjertelen
I bukspyttkjertelen er dopamins rolle noe kompleks. Bukspyttkjertelen består av to deler, en eksokrin og en endokrin komponent. Den eksokrine delen syntetiserer og utskiller fordøyelsesenzymer og andre stoffer, inkludert dopamin, i tynntarmen. Funksjonen til dette utskilte dopaminet etter at det kommer inn i tynntarmen er ikke klart fastslått - mulighetene inkluderer å beskytte tarmslimhinnen mot skade og redusere gastrointestinal motilitet (hastigheten som innholdet beveger seg gjennom fordøyelsessystemet).
Bukspyttkjerteløyene utgjør den endokrine delen av bukspyttkjertelen, og syntetiserer og utskiller hormoner inkludert insulin i blodet. Det er bevis på at betacellene i holmene som syntetiserer insulin inneholder dopaminreseptorer, og at dopamin virker for å redusere mengden insulin de frigjør. Kilden til deres dopamininngang er ikke klart fastslått - den kan komme fra dopamin som sirkulerer i blodet og kommer fra det sympatiske nervesystemet, eller den kan syntetiseres lokalt av andre typer bukspyttkjertelceller.
Medisinsk bruk
Dopamin som produsert medisin selges blant annet under handelsnavnene Intropin, Dopastat og Revimine. Det er på Verdens helseorganisasjons liste over essensielle medisiner . Det er mest brukt som et stimulerende legemiddel i behandlingen av alvorlig lavt blodtrykk , langsom hjertefrekvens og hjertestans . Det er spesielt viktig for behandling av disse hos nyfødte spedbarn . Det gis intravenøst. Siden halveringstiden for dopamin i plasma er veldig kort-omtrent ett minutt hos voksne, to minutter hos nyfødte spedbarn og opptil fem minutter hos premature spedbarn-gis det vanligvis i et kontinuerlig intravenøst drypp i stedet for en enkelt injeksjon.
Virkningene, avhengig av dosering, inkluderer en økning i natriumutskillelsen i nyrene, en økning i urinproduksjonen, en økning i hjertefrekvensen og en økning i blodtrykket . Ved lave doser virker det gjennom det sympatiske nervesystemet for å øke hjertemuskulaturens sammentrekningskraft og puls, og derved øke hjerteeffekten og blodtrykket. Høyere doser forårsaker også vasokonstriksjon som ytterligere øker blodtrykket. Eldre litteratur beskriver også svært lave doser som antas å forbedre nyrefunksjonen uten andre konsekvenser, men ferske anmeldelser har konkludert med at doser på så lave nivåer ikke er effektive og noen ganger kan være skadelige. Noen effekter skyldes stimulering av dopaminreseptorer, men de fremtredende kardiovaskulære effektene skyldes dopamin som virker på α 1 , β 1 og β 2 adrenerge reseptorer .
Bivirkninger av dopamin inkluderer negative effekter på nyrefunksjonen og uregelmessige hjerteslag . Den LD 50 , eller dødelig dose som er ventet å være dødelig i 50% av befolkningen, er blitt funnet å være: 59 mg / kg (mus, administrert intravenøst ); 95 mg/kg (mus; administrert intraperitonealt ); 163 mg/kg (rotte; administrert intraperitonealt); 79 mg/kg (hund; administrert intravenøst).
En fluorert form av L-DOPA kjent som fluorodopa er tilgjengelig for bruk i positronemisjonstomografi for å vurdere funksjonen til nigrostriatalveien.
Sykdom, lidelser og farmakologi
Dopaminsystemet spiller en sentral rolle i flere viktige medisinske tilstander, inkludert Parkinsons sykdom, hyperaktivitetsforstyrrelse, Tourettes syndrom , schizofreni , bipolar lidelse og avhengighet . Bortsett fra dopamin i seg selv, er det mange andre viktige legemidler som virker på dopaminsystemer i forskjellige deler av hjernen eller kroppen. Noen brukes til medisinske eller rekreasjonsformål, men nevrokjemister har også utviklet en rekke forskningsmedisiner, hvorav noen binder seg med høy affinitet til spesifikke typer dopaminreseptorer og enten agoniserer eller motvirker effekten, og mange som påvirker andre aspekter ved dopaminfysiologi , inkludert dopamintransportørhemmere , VMAT -hemmere og enzymhemmere .
Eldre hjerne
En rekke studier har rapportert en aldersrelatert nedgang i dopaminsyntese og dopaminreseptortetthet (dvs. antall reseptorer) i hjernen. Denne nedgangen har vist seg å forekomme i striatum og ekstratriatale områder. Nedgang i D 1 , D 2 og D 3 reseptorene er godt dokumentert. Reduksjonen av dopamin med aldring antas å være ansvarlig for mange nevrologiske symptomer som øker i frekvens med alderen, for eksempel redusert armsving og økt stivhet . Endringer i dopaminnivåer kan også forårsake aldersrelaterte endringer i kognitiv fleksibilitet.
Andre nevrotransmittere, som serotonin og glutamat , viser også en nedgang i produksjonen med aldring.
Multippel sklerose
Studier rapporterte at ubalanse av dopamin påvirker tretthet ved multippel sklerose. Hos pasienter med multippel sklerose hemmer dopamin produksjonen av IL-17 og IFN-y av mononukleære celler i perifert blod.
Parkinsons sykdom
Parkinsons sykdom er en aldersrelatert lidelse preget av bevegelsesforstyrrelser som stivhet i kroppen, tregere bevegelser og skjelving av lemmer når de ikke er i bruk. I avanserte stadier utvikler det seg til demens og til slutt død. Hovedsymptomene er forårsaket av tap av dopaminutskillende celler i substantia nigra. Disse dopamincellene er spesielt sårbare for skader, og en rekke fornærmelser, inkludert encefalitt (som avbildet i boken og filmen " Awakenings "), gjentatte sportsrelaterte hjernerystelser og noen former for kjemisk forgiftning som MPTP , kan føre til betydelig celletap, som produserer et parkinsonistisk syndrom som i hovedtrekkene ligner Parkinsons sykdom. De fleste tilfellene av Parkinsons sykdom er imidlertid idiopatiske , noe som betyr at årsaken til celledød ikke kan identifiseres.
Den mest brukte behandlingen for parkinsonisme er administrering av L-DOPA, metabolsk forløper for dopamin. L-DOPA omdannes til dopamin i hjernen og forskjellige deler av kroppen av enzymet DOPA decarboxylase. L-DOPA brukes i stedet for dopamin i seg selv fordi det, i motsetning til dopamin, er i stand til å krysse blod-hjerne-barrieren . Det administreres ofte sammen med en enzymhemmer for perifer dekarboksylering som karbidopa eller benserazid , for å redusere mengden som omdannes til dopamin i periferien og derved øke mengden L-DOPA som kommer inn i hjernen. Når L-DOPA administreres regelmessig over en lengre periode, begynner en rekke ubehagelige bivirkninger som dyskinesi ofte å dukke opp; Likevel regnes det som det beste tilgjengelige langsiktige behandlingsalternativet for de fleste tilfeller av Parkinsons sykdom.
L-DOPA-behandling kan ikke gjenopprette de tapte dopamincellene, men det får de resterende cellene til å produsere mer dopamin, og kompenserer derved for tapet i minst en viss grad. I avanserte stadier begynner behandlingen å mislykkes fordi celletapet er så alvorlig at de resterende ikke kan produsere nok dopamin uavhengig av L-DOPA-nivåer. Andre legemidler som forbedrer dopaminfunksjonen, for eksempel bromokriptin og pergolid , brukes også noen ganger til å behandle Parkinsonisme, men i de fleste tilfeller ser L-DOPA ut til å gi den beste avveiingen mellom positive effekter og negative bivirkninger.
Dopaminerge medisiner som brukes til å behandle Parkinsons sykdom er noen ganger forbundet med utviklingen av et dopamindysreguleringssyndrom , som innebærer overforbruk av dopaminerg medisinering og medisinindusert tvangsmessig engasjement i naturlige belønninger som gambling og seksuell aktivitet. Sistnevnte atferd er lik den som observeres hos personer med atferdsavhengighet .
Narkotikaavhengighet og psykostimulerende midler

Kokain , substituerte amfetaminer (inkludert metamfetamin ), Adderall , metylfenidat (markedsført som Ritalin eller Concerta ) og andre psykostimulanter utøver sin effekt hovedsakelig eller delvis ved å øke dopaminnivået i hjernen med en rekke mekanismer. Kokain og metylfenidat er dopamintransportblokkere eller gjenopptakshemmere ; de hemmer ikke-konkurransedyktig gjenopptak av dopamin, noe som resulterer i økte dopaminkonsentrasjoner i den synaptiske kløften. Som kokain øker også substituerte amfetamin og amfetamin konsentrasjonen av dopamin i den synaptiske kløften , men med forskjellige mekanismer.
Effektene av psykostimulerende midler inkluderer økning i hjertefrekvens, kroppstemperatur og svette; forbedringer i årvåkenhet, oppmerksomhet og utholdenhet; økning i glede produsert av givende hendelser; men ved høyere doser uro, angst eller til og med tap av kontakt med virkeligheten . Legemidler i denne gruppen kan ha et høyt avhengighetspotensial på grunn av deres aktiverende effekter på det dopamin-medierte belønningssystemet i hjernen. Noen kan imidlertid også være nyttige ved lavere doser for behandling av oppmerksomhetsunderskudd hyperaktivitetsforstyrrelse (ADHD) og narkolepsi . En viktig differensierende faktor er begynnelsen og varigheten av virkningen. Kokain kan tre i kraft på sekunder hvis den injiseres eller inhaleres i fri baseform; effektene varer fra 5 til 90 minutter. Denne raske og korte handlingen gjør effekten lett oppfattet og gir den følgelig et stort avhengighetspotensial. Metylfenidat tatt i pilleform, derimot, kan ta to timer å nå toppnivåer i blodet, og avhengig av formulering kan effektene vare i opptil 12 timer. Disse lengre virkende formuleringene har fordelen av å redusere potensialet for misbruk og forbedre vedheft ved behandling ved å bruke mer praktiske doseringsregimer.

En rekke vanedannende medisiner gir en økning i belønningsrelatert dopaminaktivitet. Stimulerende midler som nikotin , kokain og metamfetamin fremmer økte nivåer av dopamin som ser ut til å være hovedfaktoren for å forårsake avhengighet. For andre vanedannende medikamenter så som den opioid heroin, kan den økte nivåer av dopamin i belønningssystemet bare spiller en mindre rolle i avhengighet. Når mennesker som er avhengige av sentralstimulerende midler går gjennom tilbaketrekning, opplever de ikke den fysiske lidelsen forbundet med alkoholuttak eller tilbaketrekning fra opiater; i stedet opplever de craving, et intenst ønske om stoffet preget av irritabilitet, rastløshet og andre opphisselsessymptomer, forårsaket av psykologisk avhengighet .
Dopaminsystemet spiller en avgjørende rolle i flere aspekter av avhengighet. På det tidligste stadiet kan genetiske forskjeller som endrer uttrykket av dopaminreseptorer i hjernen forutsi om en person vil finne stimulanser tiltalende eller aversiv. Forbruk av sentralstimulerende midler gir økninger i dopaminnivået i hjernen som varer fra minutter til timer. Til slutt utløser den kroniske økningen i dopamin som kommer med gjentatt høydosestimulerende forbruk et omfattende sett med strukturelle endringer i hjernen som er ansvarlige for atferdsavvikene som kjennetegner en avhengighet. Behandling av sentralstimulerende avhengighet er veldig vanskelig, for selv om forbruket opphører, gjør ikke det suget som følger med psykologisk tilbaketrekning. Selv når trangen ser ut til å være utdødd, kan den dukke opp igjen når den står overfor stimuli som er forbundet med stoffet, for eksempel venner, steder og situasjoner. Foreningsnettverk i hjernen henger sterkt sammen.
Psykose og antipsykotiske legemidler
Psykiatere på begynnelsen av 1950 -tallet oppdaget at en klasse med legemidler kjent som typiske antipsykotika (også kjent som store beroligende midler ) ofte var effektive for å redusere de psykotiske symptomene på schizofreni. Innføringen av det første mye brukte antipsykotiske, klorpromazin (Thorazine), på 1950 -tallet, førte til at mange pasienter med schizofreni ble frigitt fra institusjoner i årene som fulgte. På 1970 -tallet forsto forskerne at disse typiske antipsykotika fungerte som antagonister på D2 -reseptorene. Denne erkjennelsen førte til den såkalte dopaminhypotesen om schizofreni , som postulerer at schizofreni i stor grad skyldes hyperaktivitet i hjernedopaminsystemer. Dopaminhypotesen trakk ytterligere støtte fra observasjonen om at psykotiske symptomer ofte ble forsterket av dopaminforbedrende sentralstimulerende midler som metamfetamin, og at disse stoffene også kan produsere psykose hos friske mennesker hvis de tas i store nok doser. I de følgende tiårene ble det utviklet andre atypiske antipsykotika som hadde færre alvorlige bivirkninger. Mange av disse nyere stoffene virker ikke direkte på dopaminreseptorer, men gir i stedet endringer i dopaminaktiviteten indirekte. Disse stoffene ble også brukt til å behandle andre psykoser. Antipsykotiske legemidler har en stort undertrykkende effekt på de fleste typer aktiv oppførsel, og reduserer spesielt vrangforestillingen og opphisset atferd som er karakteristisk for åpen psykose.
Senere observasjoner har imidlertid fått dopaminhypotesen til å miste popularitet, i det minste i sin enkle originale form. For det første viser pasienter med schizofreni vanligvis ikke målbart økte nivåer av hjernedopaminaktivitet. Likevel fortsetter mange psykiatere og nevrovitere å tro at schizofreni innebærer en slags dysfunksjon av dopaminsystemet. Etter hvert som "dopaminhypotesen" har utviklet seg over tid, har imidlertid den type dysfunksjoner den postulerer en tendens til å bli stadig mer subtil og kompleks.
Psykofarmakolog Stephen M. Stahl foreslo i en gjennomgang av 2018 at i mange tilfeller av psykose, inkludert schizofreni, bidro tre sammenkoblede nettverk basert på dopamin, serotonin og glutamat - hver for seg eller i forskjellige kombinasjoner - til overeksitasjon av dopamin D2 -reseptorer. i det ventrale striatum .
Hyperaktivitetsforstyrrelse med oppmerksomhetsunderskudd
Endret dopamin -nevrotransmisjon er implisert i oppmerksomhetsunderskudds hyperaktivitetsforstyrrelse (ADHD), en tilstand assosiert med nedsatt kognitiv kontroll , noe som igjen fører til problemer med å regulere oppmerksomhet ( oppmerksomhetskontroll ), hemme atferd ( hemmende kontroll ) og glemme ting eller mangle detaljer ( arbeide minne ), blant andre problemer. Det er genetiske koblinger mellom dopaminreseptorer, dopamintransportøren og ADHD, i tillegg til koblinger til andre nevrotransmitterreseptorer og transportører. Det viktigste forholdet mellom dopamin og ADHD involverer stoffene som brukes til å behandle ADHD. Noen av de mest effektive terapeutiske midlene for ADHD er psykostimulerende midler som metylfenidat (Ritalin, Concerta) og amfetamin (Evekeo, Adderall, Dexedrine), legemidler som øker både dopamin og noradrenalin i hjernen. De kliniske effektene av disse psykostimulantene ved behandling av ADHD formidles gjennom indirekte aktivering av dopamin- og noradrenalinreseptorer, spesielt dopaminreseptor D 1 og adrenoceptor α 2 , i prefrontal cortex.
Smerte
Dopamin spiller en rolle i smertebehandling i flere nivåer av sentralnervesystemet, inkludert ryggmargen, periaqueductal grey , thalamus , basal ganglia og cingulate cortex . Reduserte nivåer av dopamin har vært assosiert med smertefulle symptomer som ofte oppstår ved Parkinsons sykdom. Unormaliteter ved dopaminerg nevrotransmisjon forekommer også ved flere smertefulle kliniske tilstander, inkludert brennende munnsyndrom , fibromyalgi og rastløse bensyndrom.
Kvalme
Kvalme og oppkast er i stor grad bestemt av aktivitet i området postrema i medulla av hjernestammen , i et område kjent som chemoreceptor trigger sonen . Dette området inneholder en stor populasjon av type D2 dopaminreseptorer. Følgelig har medisiner som aktiverer D2 -reseptorer et stort potensial for å forårsake kvalme. Denne gruppen inkluderer noen medisiner som gis mot Parkinsons sykdom, samt andre dopaminagonister som apomorfin . I noen tilfeller er D2-reseptorantagonister som metoklopramid nyttige som kvalmehemmende midler .
Sammenlignende biologi og evolusjon
Mikroorganismer
Det er ingen rapporter om dopamin i archaea , men det er påvist i noen typer bakterier og i protozoen kalt Tetrahymena . Kanskje enda viktigere, det er typer bakterier som inneholder homologer av alle enzymene som dyr bruker for å syntetisere dopamin. Det har blitt foreslått at dyr avledet sitt dopaminsyntetiserende maskineri fra bakterier, via horisontal genoverføring som kan ha skjedd relativt sent i evolusjonstiden, kanskje som et resultat av den symbiotiske innlemmelsen av bakterier i eukaryote celler som ga opphav til mitokondrier .
Dyr
Dopamin brukes som en nevrotransmitter hos de fleste flercellede dyr. I svamper er det bare en enkelt rapport om tilstedeværelsen av dopamin, uten indikasjon på dets funksjon; Imidlertid har dopamin blitt rapportert i nervesystemet til mange andre radielt symmetriske arter, inkludert maneter av cnidarianer , hydra og noen koraller . Dette daterer fremveksten av dopamin som en nevrotransmitter tilbake til nervesystemets tidligste utseende, for over 500 millioner år siden i den kambriumske perioden. Dopamin fungerer som en nevrotransmitter hos virveldyr , pighuder , leddyr , bløtdyr og flere typer ormer .
I alle typer dyr som har blitt undersøkt, har dopamin vist seg å endre motorisk oppførsel. I modellorganismen , nematoden Caenorhabditis elegans , reduserer den bevegelse og øker matforskende bevegelser; i flatorm produserer den "skruelignende" bevegelser; hos igler hemmer det svømming og fremmer kryp. På tvers av et stort utvalg av virveldyr har dopamin en "aktiverende" effekt på atferdsbytte og responsvalg, sammenlignbar med effekten hos pattedyr.
Dopamin har også konsekvent vist seg å spille en rolle i belønningslæring i alle dyregrupper. Som med alle virveldyr - virvelløse dyr som rundorm , flatorm , bløtdyr og vanlige fruktfluer kan alle trenes til å gjenta en handling hvis den konsekvent etterfølges av en økning i dopaminnivået. I fruktfluer antyder forskjellige elementer for belønningslæring en modulær struktur for insektbelønningssystemet som stort sett er parallelt med det pattedyret. For eksempel regulerer dopamin kort- og langsiktig læring hos aper; i fruktfluer, medierer forskjellige grupper av dopamin-nevroner belønningssignaler for kortsiktige og langsiktige minner.
Det hadde lenge vært antatt at leddyr var et unntak fra dette med dopamin som ble sett på å ha en negativ effekt. Belønning ble sett på å bli formidlet i stedet av octopamine , en nevrotransmitter nært knyttet til noradrenalin. Nyere studier har imidlertid vist at dopamin spiller en rolle i belønningslæring hos fruktfluer. Det har også blitt funnet at den givende effekten av oktopamin skyldes at den aktiverer et sett dopaminerge nevroner som man ikke tidligere har fått tilgang til i forskningen.
Planter
Mange planter, inkludert en rekke næringsplanter, syntetiserer dopamin i ulik grad. De høyeste konsentrasjonene er observert i bananer - fruktkjøttet av røde og gule bananer inneholder dopamin i nivåer på 40 til 50 vektdeler per million. Poteter, avokado, brokkoli og rosenkål kan også inneholde dopamin i nivåer på 1 del per million eller mer; appelsiner, tomater, spinat, bønner og andre planter inneholder målbare konsentrasjoner mindre enn 1 del per million. Dopaminen i planter syntetiseres fra aminosyren tyrosin, ved biokjemiske mekanismer som ligner de som dyr bruker. Det kan metaboliseres på en rekke måter, og produserer melanin og en rekke alkaloider som biprodukter. Funksjonene til plantekatekolaminer er ikke klart fastslått, men det er bevis på at de spiller en rolle i responsen på stressfaktorer som bakteriell infeksjon, fungerer som vekstfremmende faktorer i noen situasjoner og endrer måten sukker metaboliseres på. Reseptorene som formidler disse handlingene er ennå ikke identifisert, og heller ikke de intracellulære mekanismene de aktiverer.
Dopamin som forbrukes i mat kan ikke virke på hjernen, fordi den ikke kan krysse blod -hjerne -barrieren. Imidlertid er det også en rekke planter som inneholder L-DOPA, metabolsk forløper for dopamin. De høyeste konsentrasjonene finnes i bladene og bønnebøttene til plantene av slekten Mucuna , spesielt i Mucuna pruriens (fløyelsbønner), som har blitt brukt som kilde til L-DOPA som et stoff. Et annet anlegg som inneholder betydelige mengder L-DOPA er Vicia faba , anlegget som produserer fava-bønner (også kjent som "bredbønner"). Nivået av L-DOPA i bønnene er imidlertid mye lavere enn i belgskallene og andre deler av planten. Frøene til Cassia- og Bauhinia- trærne inneholder også betydelige mengder L-DOPA.
I en art av marine grønne alger Ulvaria obscura , en hovedkomponent i noen algeblomster , er dopamin tilstede i svært høye konsentrasjoner, anslått til 4,4% av tørrvekten. Det er tegn på at dette dopaminet fungerer som et forsvar mot planteetere , og reduserer forbruket av snegler og isopoder .
Som en forløper for melanin
Melaniner er en familie av mørkpigmenterte stoffer som finnes i et bredt spekter av organismer. Kjemisk er de nært beslektet med dopamin, og det er en type melanin, kjent som dopamin-melanin , som kan syntetiseres ved oksidasjon av dopamin via enzymet tyrosinase . Melaninet som mørkner menneskelig hud er ikke av denne typen: det syntetiseres av en bane som bruker L-DOPA som en forløper, men ikke dopamin. Imidlertid er det betydelige bevis på at neuromelanin som gir en mørk farge til hjernens substantia nigra i det minste delvis er dopamin-melanin.
Dopamin-avledet melanin vises sannsynligvis også i minst noen andre biologiske systemer. Noe av dopaminet i planter vil sannsynligvis bli brukt som en forløper for dopamin-melanin. De komplekse mønstrene som vises på sommerfuglvinger, samt svart-hvite striper på kroppene til insektlarver, antas også å være forårsaket av romlig strukturerte opphopninger av dopamin-melanin.
Historie og utvikling
Dopamin ble først syntetisert i 1910 av George Barger og James Ewens ved Wellcome Laboratories i London, England og ble først identifisert i den menneskelige hjerne av Katharine Montagu i 1957. Det ble kalt dopamin fordi det er et monoamin hvis forløper i Barger-Ewens-syntesen er 3,4- d ihyd o xy p henyl a lanine (levodopa eller L-DOPA). Dopamins funksjon som nevrotransmitter ble først anerkjent i 1958 av Arvid Carlsson og Nils-Åke Hillarp ved Laboratory for Chemical Pharmacology ved National Heart Institute of Sweden . Carlsson ble tildelt Nobelprisen i fysiologi eller medisin 2000 for å ha vist at dopamin ikke bare er en forløper for noradrenalin (noradrenalin) og adrenalin (adrenalin), men også selv er en nevrotransmitter.
Polydopamin
Forskning motivert av klebende polyfenoliske proteiner i blåskjell førte til oppdagelsen i 2007 at et stort utvalg materialer, hvis de plasseres i en løsning av dopamin ved litt grunnleggende pH , vil bli belagt med et lag av polymerisert dopamin, ofte referert til som polydopamin . Denne polymeriserte dopaminen dannes ved en spontan oksidasjonsreaksjon, og er formelt en type melanin. Syntese innebærer vanligvis reaksjon av dopaminhydroklorid med Tris som base i vann. Strukturen til polydopamin er ukjent.
Polydopaminbelegg kan dannes på objekter som varierer i størrelse fra nanopartikler til store overflater. Polydopaminsjikt har kjemiske egenskaper som har potensial til å være ekstremt nyttige, og mange studier har undersøkt mulige bruksområder. På det enkleste nivået kan de brukes til beskyttelse mot lysskader, eller for å danne kapsler for levering av legemidler. På et mer sofistikert nivå kan deres klebeegenskaper gjøre dem nyttige som substrater for biosensorer eller andre biologisk aktive makromolekyler.