Medfødt hjertefeil - Congenital heart defect
| Medfødt hjertefeil | |
|---|---|
| Andre navn | Medfødt hjerteanomali, medfødt hjertesykdom |
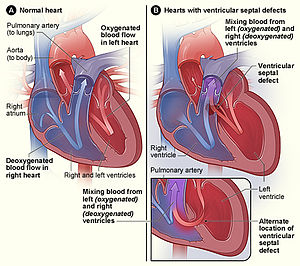 | |
| Den normale strukturen i hjertet (venstre) i forhold til to vanlige steder for en ventrikelseptumdefekt (høyre), den vanligste formen for medfødt hjertefeil. | |
| Spesialitet | Kardiologi |
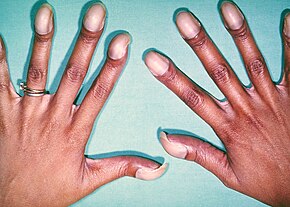
| Symptomer | Rask pust, blåaktig hud , dårlig vektøkning, trøtthet |
| Komplikasjoner | Hjertefeil |
| Typer | Cyanotiske hjertefeil , ikke-cyanotiske hjertefeil |
| Årsaker | Ofte ukjent |
| Risikofaktorer | Rubella -infeksjon under graviditet , alkohol eller tobakk , foreldre som er nært beslektet, dårlig ernæringsstatus, tar antidepressiva under graviditet eller fedme hos mor |
| Behandling | Ingen, kateterbaserte prosedyrer , hjertekirurgi , hjertetransplantasjon |
| Prognose | Generelt bra (med behandling) |
| Frekvens | 48,9 millioner (2015) |
| Dødsfall | 303 300 (2015) |
En medfødt hjertefeil ( CHD ), også kjent som en medfødt hjerteanomali og medfødt hjertesykdom , er en defekt i hjertets struktur eller store kar som er tilstede ved fødselen . Tegn og symptomer avhenger av den spesifikke typen defekt. Symptomene kan variere fra ingen til livstruende. Når det er tilstede, kan symptomene omfatte rask pust, blåaktig hud ( cyanose ), dårlig vektøkning og trøtthet. CHD forårsaker ikke brystsmerter. De fleste medfødte hjertefeil er ikke forbundet med andre sykdommer. En komplikasjon av CHD er hjertesvikt .
Årsaken til en medfødt hjertefeil er ofte ukjent. Risikofaktorer inkluderer visse infeksjoner under graviditet som rubella , bruk av visse medisiner eller medisiner som alkohol eller tobakk , foreldre som er nært beslektet, eller dårlig ernæringsstatus eller fedme hos moren. Å ha en forelder med medfødt hjertefeil er også en risikofaktor. En rekke genetiske tilstander er forbundet med hjertefeil, inkludert Downs syndrom , Turners syndrom og Marfan syndrom . Medfødte hjertefeil er delt inn i to hovedgrupper: cyanotiske hjertefeil og ikke-cyanotiske hjertefeil , avhengig av om barnet har potensial til å bli blåaktig i fargen. Defektene kan involvere hjerteets indre vegger, hjerteklaffene eller de store blodårene som fører til og fra hjertet.
Medfødte hjertefeil kan delvis forebygges gjennom rubella -vaksinasjon , tilsetning av jod til salt og tilsetning av folsyre til visse matvarer. Noen feil trenger ikke behandling. Andre kan effektivt behandles med kateterbaserte prosedyrer eller hjertekirurgi . Noen ganger kan det være nødvendig med en rekke operasjoner, eller det kan være nødvendig med en hjertetransplantasjon . Med passende behandling er resultatene generelt gode, selv med komplekse problemer.
Medfødte hjertefeil er den vanligste fødselsdefekten . I 2015 var de til stede hos 48,9 millioner mennesker globalt. De påvirker mellom 4 og 75 per 1000 levendefødte, avhengig av hvordan de blir diagnostisert. I omtrent 6 til 19 av 1000 forårsaker de en moderat til alvorlig grad av problemer. Medfødte hjertefeil er den viktigste årsaken til fødselsskaderelaterte dødsfall: i 2015 resulterte de i 303 300 dødsfall, ned fra 366 000 dødsfall i 1990.
Tegn og symptomer
Tegn og symptomer er relatert til type og alvorlighetsgrad av hjertefeilen. Symptomer oppstår ofte tidlig i livet, men det er mulig for noen CHDs å bli uoppdaget gjennom livet. Noen barn har ingen tegn, mens andre kan vise kortpustethet, cyanose , besvimelse , hjerteklump, underutvikling av lemmer og muskler, dårlig fôring eller vekst eller luftveisinfeksjoner. Medfødte hjertefeil forårsaker unormal hjertestruktur som resulterer i produksjon av visse lyder som kalles hjerteklump . Disse kan noen ganger oppdages ved auskultasjon ; Imidlertid er ikke alle hjertemumlinger forårsaket av medfødte hjertefeil.
Tilhørende forhold
Medfødte hjertefeil er forbundet med en økt forekomst av syv andre spesifikke medisinske tilstander, sammen kalt VACTERL -foreningen :
- V - Vertebrale anomalier
- A - Anal atresia
- C - Kardiovaskulære anomalier
- T - Trakeoesofageal fistel
- E - esophageal atresi
- R - Nyre (nyre) og/eller radiale anomalier
- L - Limb defekter
Ventrikelseptumdefekt (VSD), atrialseptumfeil og tetralogi av Fallot er de vanligste medfødte hjertefeilene som er sett i VACTERL -foreningen. Mindre vanlige defekter i foreningen er truncus arteriosus og transponering av de store arteriene.
Årsaker
Årsaken til medfødt hjertesykdom kan være genetisk, miljømessig eller en kombinasjon av begge.
Genetisk
Genetiske mutasjoner , ofte sporadiske, representerer den største kjente årsaken til medfødte hjertefeil. De er beskrevet i tabellen nedenfor.
| Genetiske lesjoner | Tilskrivbare prosent | Eksempler | Primær genetisk testing metode |
|---|---|---|---|
| Aneuploidier | 5-8% | Overlevende autosomale trisomier (kromosomer 13 , 18 , 21 ), kromosom X -monosomi (Turners syndrom) | Karyotyping |
| Kopier tallvarianter | 10-12% | 22q11.2 sletting/duplisering (velocardiofacial/DiGeorge syndrom) , 1 q21.1 sletting/duplisering , 8p23.1 sletting/duplisering , 15q11.2 sletting (Burnside-Butlers syndrom) | Array -komparativ genomisk hybridisering (også kjent som kromosomal mikroarrayanalyse) |
| Arvet proteinkodende enkeltnukleotidvariant (SNV) eller liten innsetting/sletting (indel) | 3-5% | Holt-Oram syndrom , Noonan syndrom , Alagille syndrom | Genpanel |
| De novo proteinkodende SNV eller indel | ~ 10% | Mutasjoner i gener uttrykt sterkt under hjerteutvikling | Hele exome sekvensering |
Molekylære veier
Genene som regulerer den komplekse utviklingssekvensen er bare delvis belyst. Noen gener er assosiert med spesifikke defekter. En rekke gener har vært assosiert med hjerte -manifestasjoner. Mutasjoner av et hjertemuskelprotein, α-myosin heavy chain ( MYH6 ) er assosiert med atriale septumdefekter. Flere proteiner som interagerer med MYH6 er også forbundet med hjertefeil. Transkripsjonsfaktoren GATA4 danner et kompleks med TBX5 som samhandler med MYH6. En annen faktor, homeobox (utviklings) genet, NKX2-5 , samhandler også med MYH6. Mutasjoner av alle disse proteinene er assosiert med både atriale og ventrikulære septaldefekter; I tillegg er NKX2-5 assosiert med defekter i den elektriske ledningen i hjertet og TBX5 er relatert til Holt-Oram syndrom som inkluderer elektriske ledningsdefekter og abnormiteter i øvre lem. Den Wnt signale co-faktorer BCL9 , BCL9L og PYGO kan være en del av denne molekylære reaksjonsveier, som når deres gener er mutert, dette fører til fenotyper som ligner på funksjonene som finnes i Holt-Oram syndrom . Et annet T-box-gen, TBX1 , er involvert i velo-cardio-facial syndrom DiGeorge syndrom , den vanligste slettingen som har omfattende symptomer, inkludert defekter i hjerteutløpet, inkludert tetralogi av Fallot .
| MYH6 | GATA4 | NKX2-5 | TBX5 | TBX1 | |
|---|---|---|---|---|---|
| Lokus | 14q11.2-q13 | 8p23.1-p22 | 5q34 | 12q24.1 | 22q11.2 |
| Syndrom | Holt-Oram | DiGeorge | |||
| Atrial septal defekter | ✔ | ✔ | ✔ | ✔ | |
| Ventrikelseptumdefekter | ✔ | ✔ | ✔ | ||
| Elektriske ledningsforstyrrelser | ✔ | ✔ | |||
| Avvik i avløpskanalen | ✔ | ||||
| Ikke-kardiale manifestasjoner | Avvik i øvre lemmer | Liten eller fraværende tymus Små eller fraværende parathyroider Ansiktsavvik |
Den hakk signalveien , en reguleringsmekanisme for cellevekst og differensiering, spiller brede roller i flere aspekter av hjerte utvikling. Hakkelementer er involvert i bestemmelsen av høyre og venstre side av kroppsplanen, slik at den retningsvise foldingen av hjerterøret kan påvirkes. Hakksignalering er involvert tidlig i dannelsen av endokardputer og fortsetter å være aktiv etter hvert som utviklingen til septa og ventiler. Det er også involvert i utviklingen av ventrikkelveggen og tilkoblingen av utstrømningskanalen til de store karene. Mutasjoner i genet for en av de hakkede ligandene, Jagged1 , er identifisert i de fleste undersøkte tilfeller av arteriohepatisk dysplasi ( Alagille syndrom ), preget av defekter i de store karene (lungearteriestenose), hjerte ( tetralogi av Fallot hos 13% tilfeller), lever, øyne, ansikt og bein. Selv om mindre enn 1% av alle tilfeller, der det ikke finnes noen feil i Jagged1 -genet, finnes feil i Notch2 -genet. I 10% av tilfellene finnes ingen mutasjon i begge genene. For et annet medlem av genfamilien er mutasjoner i Notch1 -genet assosiert med bicuspid aortaklaff , en ventil med to brosjyrer i stedet for tre. Notch1 er også forbundet med forkalkning av aortaklaffen, den tredje vanligste årsaken til hjertesykdom hos voksne.
Mutasjoner av en celle -reguleringsmekanisme, Ras / MAPK -banen er ansvarlig for en rekke syndromer, inkludert Noonan syndrom , LEOPARD syndrom , Costello syndrom og kardiofaciokutant syndrom der det er hjerteinvolvering. Selv om de listede forholdene er kjente genetiske årsaker, er det sannsynligvis mange andre gener som er mer subtile. Det er kjent at risikoen for medfødte hjertefeil er høyere når det er en nær slektning med en.
Miljø
Kjente miljøfaktorer inkluderer visse infeksjoner under graviditet som rubella , medisiner ( alkohol , hydantoin , litium og talidomid ) og mors sykdom ( diabetes mellitus , fenylketonuri og systemisk lupus erythematosus ). Alkoholeksponering hos far ser også ut til å øke risikoen for medfødte hjertefeil.
Å være overvekt eller fedme øker risikoen for medfødt hjertesykdom. I tillegg, etter hvert som fedme hos mor øker, øker også risikoen for hjertefeil. En distinkt fysiologiske mekanisme er ikke blitt identifisert til å forklare sammenhengen mellom mors fedme og CHD, men både før graviditet folatmangel og diabetes har vært innblandet i noen studier.
Mekanisme
Det er en kompleks hendelsesrekkefølge som resulterer i et godt dannet hjerte ved fødselen og forstyrrelse av en hvilken som helst del kan resultere i en defekt. Den ordnede timingen for cellevekst, cellemigrasjon og programmert celledød (" apoptose ") har blitt studert grundig, og genene som styrer prosessen blir belyst. Rundt utviklingsdag 15 eksisterer cellene som skal bli hjertet i to hesteskoformede bånd i det midterste vevslaget ( mesoderm ), og noen celler vandrer fra en del av det ytre laget ( ektoderm ), nevrale kam , som er kilde til en rekke celler som finnes i hele kroppen. På utviklingsdag 19 dannes et par vaskulære elementer, "endokardialrørene". Rørene smelter sammen når celler mellom da gjennomgår programmert død og celler fra det første hjertefeltet migrerer til røret, og danner en ring av hjerteceller ( myocytter ) rundt det om dagen 21. På dag 22 begynner hjertet å slå og etter dag 24, sirkulerer blod.
På dag 22 er sirkulasjonssystemet bilateralt symmetrisk med sammenkoblede kar på hver side og hjertet består av et enkelt rør plassert i midtlinjen av kroppsoppsettet. Delene som vil bli atria og vil ligge nærmest hodet er de mest fjerne fra hodet. Fra dag 23 til og med 28 bretter og vrir hjerterøret seg, med de fremtidige ventriklene som beveger seg til venstre for midten (hjertets ultimate plassering) og atria beveger seg mot hodet.
På dag 28 begynner områder av vev i hjerterøret å ekspandere innover; etter omtrent to uker smelter disse utvidelsene, det membranøse " septum primum " og de muskulære " endokardputer " til å danne hjertets fire kamre. Hvis du ikke smelter ordentlig, vil det føre til en feil som kan føre til at blod lekker mellom kamre. Etter at dette har skjedd, begynner celler som har migrert fra nevrale kammen å dele bulbus cordis , hovedutstrømningskanalen deles i to av veksten en spiralformet septum og blir de store karene - det stigende segmentet av aorta og lungestammen. Hvis separasjonen er ufullstendig, er resultatet en "vedvarende truncus arteriose". Fartøyene kan reverseres (" transponering av de store fartøyene "). De to halvdelene av den splittede kanalen må vandre til de riktige posisjonene over de riktige ventriklene. En svikt kan føre til at noe blod strømmer inn i feil kar ( f.eks. Overstyrende aorta ). Det firkammerede hjertet og de store karene har funksjoner som kreves for fosterets vekst . Lungene er ikke ekspandert og har ikke plass til hele sirkulasjonsvolumet. Det finnes to strukturer for å skyte blodstrømmen vekk fra lungene. Celler i en del av septum primum dør og skaper et hull mens muskelceller, " septum secundum ", vokser langs høyre atrialside septum primum, bortsett fra ett område, og etterlater et gap der blod kan passere fra høyre artium til venstre atrium, foramen ovale . Et lite fartøy, ductus arteriosus, lar blod fra lungearterien passere til aorta.
Endringer ved fødselen
Ductus arteriosus holder seg åpen på grunn av sirkulerende faktorer, inkludert prostaglandiner . Foramen ovale forblir åpen på grunn av blodstrømmen fra høyre atrium til venstre atrium. Etter hvert som lungene ekspanderer, flyter blod lett gjennom lungene og den membranøse delen av foramen ovale (septum primum) flopper over den muskulære delen (septum secundum). Hvis nedleggelsen er ufullstendig, er resultatet et patent foramen ovale . De to klaffene kan smelte sammen, men mange voksne har en foramen ovale som forblir stengt bare på grunn av trykkforskjellen mellom atria.
Teorier
Rokitansky (1875) forklarte medfødte hjertefeil som brudd i hjerteutviklingen på forskjellige ontogenesetrinn . Spitzer (1923) behandler dem som tilbake til et av fylogenesetrinnene . Krimski (1963), som syntetiserte to tidligere synspunkter, betraktet medfødte hjertesykdommer som et stopp for utvikling på et bestemt stadium av ontogenese, som tilsvarer dette eller det stadiet av fylogenesen. Derfor kan disse teoriene bare forklare feminine og nøytrale typer defekter.
Diagnose
Mange medfødte hjertefeil kan diagnostiseres prenatalt ved foster ekkokardiografi . Dette er en test som kan utføres i andre trimester av svangerskapet, når kvinnen er omtrent 18–24 uker gravid. Det kan være abdominal ultralyd eller transvaginal ultralyd .
Hvis en baby blir født med cyanotisk hjertesykdom, stilles diagnosen vanligvis kort tid etter fødselen på grunn av den blå fargen på huden (kalt cyanose).
Hvis en baby blir født med septaldefekt eller obstruksjonsdefekt, er symptomene ofte bare merkbare etter flere måneder eller noen ganger til og med etter mange år.
Klassifisering
Det finnes en rekke klassifiseringssystemer for medfødte hjertefeil. I 2000 ble International Congenital Heart Surgery Nomenclature utviklet for å gi et generisk klassifiseringssystem.
Hypoplasi
Hypoplasi kan påvirke hjertet, noe som vanligvis resulterer i underutvikling av høyre ventrikkel eller venstre ventrikkel . Dette fører til at bare den ene siden av hjertet er i stand til å pumpe blod til kroppen og lungene effektivt. Hypoplasi i hjertet er sjelden, men er den mest alvorlige formen for CHD. Det kalles hypoplastisk venstre hjertesyndrom når det påvirker venstre side av hjertet og hypoplastisk høyre hjertesyndrom når det påvirker høyre side av hjertet. Under begge forhold er tilstedeværelsen av et patent ductus arteriosus (og når hypoplasia påvirker høyre side av hjertet, et patent foramen ovale ) avgjørende for spedbarnets evne til å overleve til akutt hjerteoperasjon kan utføres, siden uten disse veiene blod kan ikke sirkulere til kroppen (eller lungene, avhengig av hvilken side av hjertet som er defekt). Hypoplasi i hjertet er vanligvis en cyanotisk hjertefeil .
Obstruktive defekter
Obstruktive defekter oppstår når hjerteventiler, arterier eller vener er unormalt smale eller blokkerte . Vanlige defekter inkluderer pulmonal stenose , aortastenose og koarktasjon av aorta , med andre typer som bicuspid aortaklaffstenose og subaortisk stenose som er relativt sjeldne. Enhver innsnevring eller blokkering kan forårsake hjerteforstørrelse eller hypertensjon .
Septal defekter
Skilleveggen er en vevvegg som skiller venstre hjerte fra høyre hjerte . Defekter i interatrial septum eller interventrikulær septum lar blod strømme fra venstre side av hjertet til høyre, noe som reduserer hjertets effektivitet. Ventrikelseptumdefekter er kollektivt den vanligste typen CHD, selv om omtrent 30% av voksne har en type atrialseptumfeil som kalles probe patent foramen ovale .
Cyanotiske defekter
Cyanotiske hjertefeil kalles slike fordi de resulterer i cyanose , en blågrå misfarging av huden på grunn av oksygenmangel i kroppen. Slike defekter inkluderer vedvarende truncus arteriosus , total unormal lungeventilkobling , tetralogi av Fallot , transponering av de store karene og tricuspid atresi .
Defekter
- Aortastenose
- Atrial septal defekt (ASD)
- Atrioventrikulær septaldefekt (AVSD)
- Bicuspid aortaklaff
- Kardiomyopati
- Komplett hjerteblokk (CHB)
- Dextrocardia
- Dobbelt innløp venstre ventrikkel (DILV)
- Dobbelt utløp høyre ventrikkel (DORV)
- Ebsteins anomali
- Hypoplastisk venstre hjerte syndrom (HLHS)
- Hypoplastisk høyre hjertesyndrom (HRHS)
- Mitral stenose
- Vedvarende truncus arteriosus
- Lungeatresi
- Lungestenose
- Rhabdomyomas (Tumors of the Heart)
- Transponering av de store fartøyene
- Tricuspid atresia
- Ventrikelseptumdefekt (VSD)
- Wolff-Parkinson-White syndrom (WPW)
Noen forhold påvirker de store karene eller andre karene i nærheten av hjertet, men ikke hjertet selv, men klassifiseres ofte som medfødte hjertefeil.
- Coarctation of aorta (CoA)
- Dobbel aortabue , avvikende subklavisk arterie og andre misdannelser av de store arteriene
- Avbrutt aortabue (IAA)
- Patent ductus arteriosus (PDA)
- Scimitar syndrom (SS)
Noen konstellasjoner av flere defekter finnes ofte sammen.
- Tetralogy of Fallot (ToF)
- Pentalogien til Cantrell
- Shones syndrom / Shones kompleks / Shones anomali
Behandling
CHD kan kreve kirurgi og medisiner. Medisiner inkluderer diuretika, som hjelper kroppen med å eliminere vann, salter og digoksin for å styrke hjertesammentrekningen. Dette reduserer hjerterytmen og fjerner litt væske fra vev. Noen feil krever kirurgiske inngrep for å gjenopprette sirkulasjonen tilbake til normal, og i noen tilfeller er det nødvendig med flere operasjoner.
Intervensjonell kardiologi tilbyr nå pasienter minimalt invasive alternativer til kirurgi for noen pasienter. Melody Transcatheter Pulmonary Valve (TPV), godkjent i Europa i 2006 og i USA i 2010 under et humanitært utstyrsfritak (HDE), er designet for å behandle medfødte hjertesykdomspasienter med dysfunksjonell kanal i sitt høyre ventrikkelutløp (RVOT) . RVOT er forbindelsen mellom hjertet og lungene; når blod når lungene, blir det beriket med oksygen før det pumpes til resten av kroppen. Transkateter-lungeventilteknologi gir et mindre invasivt middel for å forlenge levetiden til en mislykket RVOT-kanal og er designet for å la leger levere en ny lungeventil via et kateter gjennom pasientens blodårer.
Mange mennesker krever livslang spesialisert hjertebehandling, først hos en barnekardiolog og senere hos en voksen medfødt kardiolog. Det er mer enn 1,8 millioner voksne som lever med medfødte hjertefeil.
Epidemiologi
Hjertefeil er blant de vanligste fødselsdefektene , som forekommer hos 1% av levendefødte (2-3% inkludert bicuspid aortaklaff). I 2013 hadde 34,3 millioner mennesker CHD. I 2010 resulterte de i 223 000 dødsfall, ned fra 278 000 dødsfall i 1990.
For medfødte hjertefeil som oppstår uten familiehistorie ( de novo ), er tilbakefallsrisikoen hos avkom 3-5%. Denne risikoen er høyere ved hindringer i utstrømning av venstre ventrikkel, heterotaksi og atrioventrikulære septumdefekter.
Terminologi
Medfødte hjertefeil er kjent av en rekke navn, inkludert medfødt hjerteanomali, medfødt hjertesykdom, hjertefeil og medfødte kardiovaskulære misdannelser.
Se også
Referanser
Eksterne linker
| Klassifisering | |
|---|---|
| Eksterne ressurser |
- Medfødt hjertefeil på Curlie
- Informasjon om medfødt hjertesykdom for foreldre.