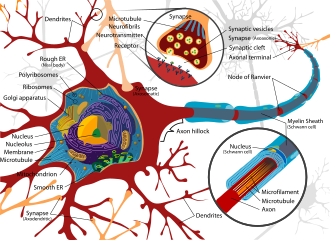
Nevrotoksin -Neurotoxin

Nevrotoksiner er giftstoffer som er ødeleggende for nervevev (forårsaker nevrotoksisitet ). Nevrotoksiner er en omfattende klasse av eksogene kjemiske nevrologiske fornærmelser som kan påvirke funksjonen i både utviklende og modent nervevev negativt. Begrepet kan også brukes til å klassifisere endogene forbindelser, som ved unormal kontakt kan vise seg nevrologisk toksiske. Selv om nevrotoksiner ofte er nevrologisk destruktive, er deres evne til å spesifikt målrette mot nevrale komponenter viktig i studiet av nervesystemer. Vanlige eksempler på nevrotoksiner inkluderer bly , etanol (drikker alkohol), glutamat , nitrogenoksid , botulinumtoksin (f.eks. Botox), tetanustoksin og tetrodotoksin . Noen stoffer som nitrogenoksid og glutamat er faktisk essensielle for riktig funksjon av kroppen og har kun nevrotoksiske effekter ved for høye konsentrasjoner.
Nevrotoksiner hemmer nevronkontroll over ionekonsentrasjoner over cellemembranen , eller kommunikasjon mellom nevroner over en synapse . Lokal patologi for nevrotoksineksponering inkluderer ofte nevroneksitotoksisitet eller apoptose , men kan også inkludere gliacelleskade . Makroskopiske manifestasjoner av nevrotoksineksponering kan inkludere omfattende skader på sentralnervesystemet som intellektuell funksjonshemming , vedvarende hukommelsessvikt , epilepsi og demens . I tillegg er nevrotoksin-mediert skade på perifert nervesystem som nevropati eller myopati vanlig. Det er vist støtte for en rekke behandlinger rettet mot å dempe nevrotoksin-mediert skade, som antioksidant- og antitoksinadministrasjon .
Bakgrunn
Eksponering for nevrotoksiner i samfunnet er ikke nytt, siden sivilisasjoner har vært utsatt for nevrologisk destruktive forbindelser i tusenvis av år. Et bemerkelsesverdig eksempel er den mulige betydelige blyeksponeringen under Romerriket som følge av utviklingen av omfattende rørleggernettverk og vanen med å koke vin med vin i blypanner for å søte den, prosessen som genererer blyacetat, kjent som "blysukker". Delvis har nevrotoksiner vært en del av menneskets historie på grunn av nervesystemets skjøre og følsomme natur, noe som gjør det svært utsatt for forstyrrelser.
Nervevevet som finnes i hjernen , ryggmargen og periferien omfatter et ekstraordinært komplekst biologisk system som i stor grad definerer mange av de unike egenskapene til individer. Som med ethvert svært komplekst system, kan imidlertid selv små forstyrrelser i omgivelsene føre til betydelige funksjonelle forstyrrelser. Egenskaper som fører til mottakelighet av nervevev inkluderer et høyt overflateareal av nevroner, et høyt lipidinnhold som holder på lipofile toksiner, høy blodstrøm til hjernen som induserer økt effektiv eksponering av toksiner, og vedvarende nevroner gjennom et individs levetid, noe som fører til sammensetning. av skader. Som et resultat har nervesystemet en rekke mekanismer designet for å beskytte det mot indre og ytre angrep, inkludert blod-hjernebarrieren.
Blod -hjerne-barrieren (BBB) er et kritisk eksempel på beskyttelse som hindrer giftstoffer og andre skadelige forbindelser fra å nå hjernen. Siden hjernen krever næringsinngang og fjerning av avfall, blir den perfundert av blodstrømmen. Blod kan imidlertid bære en rekke inntatte giftstoffer, noe som vil indusere betydelig nevrondød hvis de når nervevev. Således omgir beskyttende celler kalt astrocytter kapillærene i hjernen og absorberer næringsstoffer fra blodet og transporterer dem deretter til nevronene, og isolerer effektivt hjernen fra en rekke potensielle kjemiske fornærmelser.
Denne barrieren skaper et tett hydrofobt lag rundt kapillærene i hjernen, og hemmer transporten av store eller hydrofile forbindelser. I tillegg til BBB gir choroid plexus et lag med beskyttelse mot toksinabsorpsjon i hjernen. Årehinneplexusene er vaskulariserte lag av vev som finnes i hjernens tredje, fjerde og laterale ventrikler , som gjennom funksjonen til deres ependymale celler er ansvarlige for syntesen av cerebrospinalvæske (CSF). Viktigere, gjennom selektiv passasje av ioner og næringsstoffer og innfanging av tungmetaller som bly, opprettholder choroid plexusene et strengt regulert miljø som inneholder hjernen og ryggmargen.
Ved å være hydrofobe og små, eller hemme astrocyttfunksjonen, er noen forbindelser inkludert visse nevrotoksiner i stand til å trenge inn i hjernen og indusere betydelig skade. I moderne tid har forskere og leger blitt stilt overfor utfordringen med å identifisere og behandle nevrotoksiner, noe som har resultert i en økende interesse for både nevrotoksikologisk forskning og kliniske studier. Selv om klinisk nevrotoksikologi stort sett er et spirende felt, har det blitt gjort omfattende inngrep i identifiseringen av mange miljømessige nevrotoksiner som fører til klassifiseringen av 750 til 1000 kjente potensielt nevrotoksiske forbindelser. På grunn av den kritiske betydningen av å finne nevrotoksiner i vanlige miljøer, er det utviklet spesifikke protokoller av United States Environmental Protection Agency (EPA) for testing og bestemmelse av nevrotoksiske effekter av forbindelser (USEPA 1998). I tillegg har in vitro- systemer økt i bruk ettersom de gir betydelige forbedringer i forhold til de mer vanlige in vivo- systemene fra fortiden. Eksempler på forbedringer inkluderer håndterbare, ensartede miljøer og eliminering av kontaminerende effekter av systemisk metabolisme. In vitro-systemer har imidlertid gitt problemer ettersom det har vært vanskelig å replikere kompleksiteten i nervesystemet på riktig måte, for eksempel interaksjonene mellom støttende astrocytter og nevroner i å lage BBB. For ytterligere å komplisere prosessen med å bestemme nevrotoksiner ved testing in vitro, kan nevrotoksisitet og cytotoksisitet være vanskelig å skille ettersom å eksponere nevroner direkte for forbindelser kanskje ikke er mulig in vivo, da det er in vitro. I tillegg kan det hende at celleresponsen på kjemikalier ikke nøyaktig formidler et skille mellom nevrotoksiner og cytotoksiner, ettersom symptomer som oksidativt stress eller skjelettmodifikasjoner kan oppstå som svar på begge .
I et forsøk på å adressere denne komplikasjonen har nevrittutvekster (enten aksonale eller dendritiske) som svar på påførte forbindelser nylig blitt foreslått som et mer nøyaktig skille mellom ekte nevrotoksiner og cytotoksiner i et in vitro testmiljø. På grunn av de betydelige unøyaktighetene knyttet til denne prosessen, har det imidlertid gått tregt med å få bred støtte. I tillegg har biokjemiske mekanismer blitt mer utbredt i neurotoksintesting, slik at forbindelser kan screenes for tilstrekkelighet til å indusere cellemekanismeinterferens, som hemming av acetylkolinesterasekapasiteten til organofosfater (inkluderer DDT og saringass ). Selv om metoder for å bestemme nevrotoksisitet fortsatt krever betydelig utvikling, har identifiseringen av skadelige forbindelser og toksineksponeringssymptomer gjennomgått betydelig forbedring.
Applikasjoner innen nevrovitenskap
Selv om de er forskjellige i kjemiske egenskaper og funksjoner, deler nevrotoksiner den felles egenskapen at de virker av en eller annen mekanisme som fører til enten forstyrrelse eller ødeleggelse av nødvendige komponenter i nervesystemet . Nevrotoksiner kan imidlertid på grunn av deres design være svært nyttige innen nevrovitenskap . Ettersom nervesystemet i de fleste organismer er både svært komplekst og nødvendig for å overleve, har det naturlig nok blitt et mål for angrep fra både rovdyr og byttedyr. Siden giftige organismer ofte bruker nevrotoksinene sine for å dempe et rovdyr eller bytte veldig raskt, har giftstoffer utviklet seg til å bli svært spesifikke for målkanalene deres, slik at giftstoffet ikke lett binder andre mål (se Ion Channel-toksiner ). Som sådan gir nevrotoksiner en effektiv måte som visse elementer i nervesystemet kan målrettes nøyaktig og effektivt med. Et tidlig eksempel på nevrotoksinbasert målretting brukte radiomerket tetrodotoksin for å analysere natriumkanaler og oppnå nøyaktige målinger om deres konsentrasjon langs nervemembraner . På samme måte gjennom isolering av visse kanalaktiviteter, har nevrotoksiner gitt muligheten til å forbedre den originale Hodgkin-Huxley-modellen av nevronen der det ble teoretisert at enkelt generiske natrium- og kaliumkanaler kunne stå for de fleste nervevevsfunksjoner. Fra denne grunnleggende forståelsen har bruken av vanlige forbindelser som tetrodotoksin, tetraetylammonium og bungarotoksiner ført til en mye dypere forståelse av de distinkte måtene individuelle nevroner kan oppføre seg på.
Mekanismer for aktivitet
Siden nevrotoksiner er forbindelser som påvirker nervesystemet negativt, er en rekke mekanismer som de fungerer gjennom, gjennom hemming av nevroncellulære prosesser. Disse inhiberte prosessene kan variere fra membrandepolarisasjonsmekanismer til inter-nevronkommunikasjon . Ved å hemme evnen for nevroner til å utføre sine forventede intracellulære funksjoner, eller sende et signal til en nabocelle, kan nevrotoksiner indusere systemisk nervesystemstopp som i tilfelle av botulinumtoksin , eller til og med nervevevsdød. Tiden som kreves for utbruddet av symptomer ved nevrotoksineksponering kan variere mellom ulike toksiner, og være i størrelsesorden timer for botulinumtoksin og år for bly.
| Nevrotoksin klassifisering | Nevrotoksiner |
|---|---|
| Na-kanalhemmere | Tetrodotoksin |
| K-kanalhemmere | Tetraetylammonium |
| Cl-kanalhemmere | Klorotoksin , |
| Ca-kanalhemmere | Konotoksin |
| Hemmere av synaptisk vesikkelfrigjøring | Botulinumtoksin , |
| Blod-hjerne-barriere-hemmere | aluminium , |
| Reseptorhemmere/antagonister | Bungarotoksin , |
| Reseptoragonister |
anatoksin-a ,
JWH-018 , |
| Cytoskjelett interferens | Ammoniakk , |
| Ca-mediert cytotoksisitet | Lede |
| Flere effekter |
Etanol ,
N-heksan , |
| Reseptorselektive nevrotoksiner | MPP + |
| Endogene nevrotoksinkilder |
Nitrogenoksid ,
Glutamat , |
Inhibitorer
Natriumkanal
Tetrodotoksin

Tetrodotoxin (TTX) er en gift produsert av organismer som tilhører Tetraodontiformes-ordenen , som inkluderer pufferfisk , havsolfisk og piggsvinfisk . I pufferfisken finnes TTX i leveren , gonadene , tarmene og huden . TTX kan være dødelig hvis det konsumeres, og har blitt en vanlig form for forgiftning i mange land. Vanlige symptomer på TTX-forbruk inkluderer parestesi (ofte begrenset til munn og lemmer ), muskelsvakhet, kvalme og oppkast og manifesterer seg ofte innen 30 minutter etter inntak . Den primære mekanismen som TTX er giftig med, er gjennom hemming av natriumkanalfunksjon, som reduserer den funksjonelle kapasiteten til nevronkommunikasjon. Denne hemmingen påvirker i stor grad en følsom undergruppe av natriumkanaler kjent som TTX-sensitive (TTX-s), som også tilfeldigvis er i stor grad ansvarlig for natriumstrømmen som driver depolariseringsfasen til nevronaksjonspotensialer .
TTX-resistent (TTX-r) er en annen form for natriumkanal som har begrenset følsomhet for TTX, og som stort sett finnes i aksoner med liten diameter, slik som de som finnes i nocisepsjonsnevroner . Når et betydelig nivå av TTX inntas, vil det binde natriumkanaler på nevroner og redusere deres membranpermeabilitet for natrium. Dette resulterer i en økt effektiv terskel for nødvendige eksitatoriske signaler for å indusere et aksjonspotensial i en postsynaptisk nevron. Effekten av denne økte signalgrensen er en redusert eksitabilitet av postsynaptiske nevroner , og påfølgende tap av motorisk og sensorisk funksjon som kan resultere i lammelse og død. Selv om assistert ventilasjon kan øke sjansen for overlevelse etter TTX-eksponering, er det foreløpig ingen antitoksin. Bruk av acetylkolinesterasehemmeren Neostigmin eller den muskarine acetylkolinantagonisten atropin (som vil hemme parasympatisk aktivitet), kan imidlertid øke sympatisk nerveaktivitet nok til å forbedre sjansen for overlevelse etter TTX-eksponering.
Kaliumkanal
Tetraetylammonium
Tetraetylammonium (TEA) er en forbindelse som, i likhet med en rekke nevrotoksiner, først ble identifisert gjennom sine skadelige effekter på nervesystemet og vist å ha evnen til å hemme funksjonen til motoriske nerver og dermed sammentrekningen av muskulaturen på en lignende måte . til curare. I tillegg, gjennom kronisk TEA-administrasjon, vil muskelatrofi bli indusert. Det ble senere bestemt at TEA fungerer in vivo primært gjennom sin evne til å hemme både kaliumkanalene som er ansvarlige for den forsinkede likeretteren sett i et aksjonspotensial og en viss populasjon av kalsiumavhengige kaliumkanaler. Det er denne evnen til å hemme kaliumfluks i nevroner som har gjort TEA til et av de viktigste verktøyene innen nevrovitenskap. Det har blitt antatt at evnen for TEA til å hemme kaliumkanaler er avledet fra dens lignende romfyllende struktur som kaliumioner. Det som gjør TEA veldig nyttig for nevrovitenskapsmenn er dens spesifikke evne til å eliminere kaliumkanalaktivitet, og dermed tillate studiet av nevronresponsbidrag fra andre ionekanaler, for eksempel spenningsstyrte natriumkanaler. I tillegg til sine mange bruksområder i nevrovitenskapelig forskning, har TEA vist seg å fungere som en effektiv behandling av Parkinsons sykdom gjennom sin evne til å begrense utviklingen av sykdommen.
Kloridkanal
Klorotoksin
Klorotoksin (Cltx) er den aktive forbindelsen som finnes i skorpiongift , og er først og fremst giftig på grunn av dens evne til å hemme ledningsevnen til kloridkanaler . Svelging av dødelige volumer av Cltx resulterer i lammelse gjennom denne ionekanalforstyrrelsen. I likhet med botulinumtoksin har Cltx vist seg å ha betydelig terapeutisk verdi. Bevis har vist at Cltx kan hemme evnen for gliomer til å infiltrere sunt nervevev i hjernen, og redusere potensiell invasiv skade forårsaket av svulster betydelig.
Kalsiumkanal
Konotoksin
Konotoksiner representerer en kategori av giftstoffer produsert av den marine kjeglesneglen, og er i stand til å hemme aktiviteten til en rekke ionekanaler som kalsium-, natrium- eller kaliumkanaler. I mange tilfeller inkluderer giftstoffene som frigjøres av de forskjellige typene kjeglesnegler en rekke forskjellige typer konotoksiner, som kan være spesifikke for forskjellige ionekanaler, og dermed skape en gift som er i stand til utbredt nervefunksjonsavbrudd. En av de unike formene for konotoksiner, ω-konotoksin ( ω-CgTx ) er svært spesifikk for Ca-kanaler og har vist nytte ved å isolere dem fra et system. Siden kalsiumfluks er nødvendig for riktig eksitabilitet av en celle, kan enhver betydelig hemming forhindre en stor mengde funksjonalitet. Det er betydelig at ω-CgTx er i stand til langsiktig binding til og inhibering av spenningsavhengige kalsiumkanaler lokalisert i membranene til nevronene, men ikke muskelcellene.
Synaptisk vesikkelfrigjøring
Botulinumtoksin
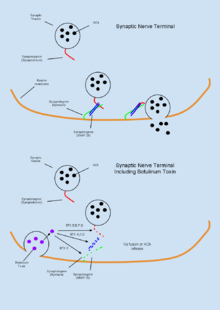
Botulinumtoksin (BTX) er en gruppe nevrotoksiner som består av åtte distinkte forbindelser, referert til som BTX-A,B,C,D,E,F,G,H, som produseres av bakterien Clostridium botulinum og fører til muskellammelse . Et spesielt unikt trekk ved BTX er dets relativt vanlige terapeutiske bruk ved behandling av dystoni og spastisitetsforstyrrelser , samt for å indusere muskelatrofi til tross for at det er det mest giftige stoffet som er kjent. BTX fungerer perifert for å hemme frigjøring av acetylkolin (ACh) ved det nevromuskulære krysset gjennom degradering av SNARE-proteinene som kreves for ACh- vesikkel-membranfusjon . Siden toksinet er svært biologisk aktivt, er en estimert dose på 1μg/kg kroppsvekt tilstrekkelig til å indusere et utilstrekkelig tidalvolum og resulterende død ved kvelning . På grunn av sin høye toksisitet har BTX-antitoksiner vært et aktivt forskningsområde. Det har blitt vist at capsaicin (aktiv forbindelse som er ansvarlig for varme i chilipepper ) kan binde TRPV1-reseptoren uttrykt på kolinerge nevroner og hemme de toksiske effektene av BTX.
Tetanustoksin
Tetanus neurotoxin (TeNT) er en forbindelse som funksjonelt reduserer hemmende overføringer i nervesystemet, noe som resulterer i muskelstivkrampe. TeNT ligner på BTX, og er faktisk svært lik i struktur og opprinnelse; begge tilhører samme kategori av clostridiale nevrotoksiner . I likhet med BTX, hemmer TeNT kommunikasjon mellom nevroner ved hjelp av vesikulær nevrotransmitter (NT) frigjøring. En bemerkelsesverdig forskjell mellom de to forbindelsene er at mens BTX hemmer muskelsammentrekninger , induserer TeNT dem. Selv om begge toksiner hemmer vesikkelfrigjøring ved nevronsynapser, er årsaken til denne forskjellige manifestasjonen at BTX hovedsakelig fungerer i det perifere nervesystemet (PNS) mens TeNT stort sett er aktivt i sentralnervesystemet (CNS ) . Dette er et resultat av TeNT-migrering gjennom motoriske nevroner til de hemmende nevronene i ryggmargen etter å ha kommet inn gjennom endocytose . Dette resulterer i tap av funksjon i hemmende nevroner i CNS som resulterer i systemiske muskelsammentrekninger . I likhet med prognosen for en dødelig dose BTX, fører TeNT til lammelse og påfølgende kvelning .
Blod-hjernebarriere
Aluminium
Nevrotoksisk oppførsel av aluminium er kjent for å oppstå ved inntreden i sirkulasjonssystemet , hvor det kan migrere til hjernen og hemme noen av de avgjørende funksjonene til blod-hjernebarrieren (BBB). Et tap av funksjon i BBB kan gi betydelig skade på nevronene i CNS, da barrieren som beskytter hjernen mot andre giftstoffer som finnes i blodet, ikke lenger vil være i stand til slik handling. Selv om metallet er kjent for å være nevrotoksisk, er effektene vanligvis begrenset til pasienter som ikke er i stand til å fjerne overflødige ioner fra blodet, for eksempel de som opplever nyresvikt . Pasienter som opplever aluminiumstoksisitet kan vise symptomer som nedsatt læring og redusert motorisk koordinasjon . I tillegg er systemiske aluminiumnivåer kjent for å øke med alderen, og har vist seg å korrelere med Alzheimers sykdom , noe som impliserer det som en nevrotoksisk forårsakende forbindelse av sykdommen. Til tross for sin kjente toksisitet i sin ioniske form, er studier delt på potensiell toksisitet ved bruk av aluminium i emballasje og kokeapparater.
Merkur
Kvikksølv er i stand til å indusere CNS-skade ved å migrere inn i hjernen ved å krysse BBB. Kvikksølv finnes i en rekke forskjellige forbindelser, selv om metylkvikksølv (MeHg + ), dimetylkvikksølv og dietylkvikksølv er de eneste signifikant nevrotoksiske formene. Dietylkvikksølv og dimetylkvikksølv regnes som noen av de mest potente nervegiftene som noen gang er oppdaget. MeHg + oppnås vanligvis gjennom inntak av sjømat , da det har en tendens til å konsentrere seg i organismer høyt oppe i næringskjeden. Det er kjent at kvikksølvionet hemmer transport av aminosyrer (AA) og glutamat (Glu), noe som potensielt kan føre til eksitotoksiske effekter.
Reseptoragonister og -antagonister
Anatoksin-a
| Ekstern video | |
|---|---|
|
University of Nottingham |
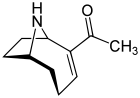
Undersøkelser av anatoksin- a , også kjent som "Very Fast Death Factor", begynte i 1961 etter døden til kuer som drakk fra en innsjø som inneholdt en algeoppblomstring i Saskatchewan, Canada. Det er et cyanotoksin produsert av minst fire forskjellige slekter av cyanobakterier , og har blitt rapportert i Nord-Amerika, Europa, Afrika, Asia og New Zealand.
Giftige effekter fra anatoksin - en fremgang veldig raskt fordi det virker direkte på nervecellene ( nevronene ). De progressive symptomene på anatoksineksponering er tap av koordinasjon, rykninger , kramper og rask død ved luftveislammelse . Nervevevet som kommuniserer med muskler inneholder en reseptor som kalles den nikotiniske acetylkolinreseptoren . Stimulering av disse reseptorene forårsaker en muskelkontraksjon . Anatoksinet - et molekyl er formet slik at det passer til denne reseptoren, og på denne måten etterligner det den naturlige nevrotransmitteren som normalt brukes av reseptoren, acetylkolin . Når det først har utløst en sammentrekning, lar ikke anatoksin nevronene gå tilbake til hviletilstanden, fordi det ikke brytes ned av kolinesterase som normalt utfører denne funksjonen. Som et resultat trekker muskelcellene seg permanent sammen, kommunikasjonen mellom hjernen og musklene blir forstyrret og pusten stopper.
Da det først ble oppdaget, ble giftstoffet kalt Very Fast Death Factor (VFDF) fordi når det ble injisert inn i kroppshulen til mus, induserte det skjelvinger, lammelser og død i løpet av få minutter. I 1977 ble strukturen til VFDF bestemt som et sekundært, bicyklisk aminalkaloid , og det ble omdøpt til anatoksin- a . Strukturelt ligner det kokain. Det er fortsatt interesse for anatoksin på grunn av farene det utgjør for rekreasjons- og drikkevann, og fordi det er et spesielt nyttig molekyl for å undersøke acetylkolinreseptorer i nervesystemet. Giftighetens deadliness gjør at den har et høyt militært potensial som giftvåpen.
Bungarotoksin
Bungarotoxin er en forbindelse med kjent interaksjon med nikotinacetylkolinreseptorer (nAChRs), som utgjør en familie av ionekanaler hvis aktivitet utløses av nevrotransmitterbinding. Bungarotoxin produseres i en rekke forskjellige former, selv om en av de ofte brukte formene er den langkjedede alfaformen, α-bungarotoxin , som er isolert fra den båndede kraitslangen . Selv om det er ekstremt giftig ved inntak, har α-bungarotoksin vist omfattende nytte i nevrovitenskap, da det er spesielt dyktig til å isolere nAChRs på grunn av dets høye affinitet til reseptorene. Siden det finnes flere former for bungarotoksin, er det forskjellige former for nAChR som de vil binde seg til, og α-bungarotoksin er spesielt spesifikt for α7-nAChR . Denne α7-nAChR fungerer for å tillate kalsiumiontilstrømning inn i celler, og vil derfor, når den blokkeres av inntatt bungarotoksin, produsere skadelige effekter, ettersom ACh-signalering vil bli hemmet. På samme måte kan bruken av α-bungarotoksin være svært nyttig i nevrovitenskap hvis det er ønskelig å blokkere kalsiumfluks for å isolere effekter av andre kanaler. I tillegg kan forskjellige former for bungarotoksin være nyttige for å studere hemmet nAChR og deres resulterende kalsiumionstrøm i forskjellige systemer i kroppen. For eksempel er α-bungarotoksin spesifikt for nAChR som finnes i muskulaturen og κ-bungarotoksin er spesifikt for nAChR som finnes i nevroner.
Caramboxin
Caramboxin (CBX) er et giftstoff som finnes i stjernefrukt ( Averrhoa carambola) . Personer med noen typer nyresykdom er utsatt for uønskede nevrologiske effekter, inkludert rus, anfall og til og med død etter å ha spist stjernefrukt eller drukket juice laget av denne frukten. Caramboxin er et nytt ikke-peptid aminosyretoksin som stimulerer glutamatreseptorene i nevroner. Caramboxin er en agonist av både NMDA- og AMPA- glutamaterge ionotropiske reseptorer med potente eksitatoriske, krampaktige og nevrodegenerative egenskaper.
Curare
Begrepet " curare " er tvetydig fordi det har blitt brukt til å beskrive en rekke giftstoffer som på tidspunktet for navngivningen ble forstått annerledes enn dagens forståelser. Tidligere har karakteriseringen betydd giftstoffer brukt av søramerikanske stammer på piler eller piler , selv om den har modnet til å spesifisere en spesifikk kategorisering av giftstoffer som virker på det nevromuskulære krysset for å hemme signalering og dermed indusere muskelavslapping. Nevrotoksinkategorien inneholder en rekke forskjellige giftstoffer, selv om alle opprinnelig ble renset fra planter med opprinnelse i Sør-Amerika. Effekten som injisert curare-gift vanligvis er forbundet med er muskellammelse og påfølgende død. Curare fungerer spesielt for å hemme nikotiniske acetylkolinreseptorer ved det nevromuskulære krysset . Normalt lar disse reseptorkanalene natriumioner inn i muskelceller for å sette i gang et aksjonspotensial som fører til muskelkontraksjon. Ved å blokkere reseptorene, er nevrotoksinet i stand til å redusere signalering av nevromuskulære overganger betydelig, en effekt som har resultert i at det brukes av anestesiologer for å gi muskelavslapning.
Cytoskjelett interferens
Ammoniakk
Ammoniakktoksisitet ses ofte gjennom to administreringsveier, enten gjennom inntak eller gjennom endogene plager som leversvikt . Et bemerkelsesverdig tilfelle der ammoniakktoksisitet er vanlig, er som respons på levercirrhose som resulterer i hepatisk encefalopati , og kan resultere i cerebralt ødem (Haussinger 2006). Dette hjerneødemet kan være et resultat av ombygging av nerveceller. Som en konsekvens av økte konsentrasjoner har ammoniakkaktivitet in vivo vist seg å indusere hevelse av astrocytter i hjernen gjennom økt produksjon av cGMP (Cyclic Guanosine Monophosphate) i cellene som fører til proteinkinase G-mediert (PKG) cytoskjelettmodifikasjoner. Den resulterende effekten av denne toksisiteten kan være redusert hjernens energimetabolisme og funksjon. Det er viktig at de toksiske effektene av ammoniakk på ombygging av astrocytter kan reduseres gjennom administrering av L-karnitin . Denne ombyggingen av astrocytter ser ut til å være mediert gjennom ammoniakk-indusert mitokondriell permeabilitetsovergang. Denne mitokondrielle overgangen er et direkte resultat av glutaminaktivitet , en forbindelse som dannes fra ammoniakk in vivo. Administrering av antioksidanter eller glutaminasehemmer kan redusere denne mitokondrieovergangen, og potensielt også ombygging av astrocytter.
Arsenikk
Arsen er et nevrotoksin som ofte finnes konsentrert i områder utsatt for landbruksavrenning , gruvedrift og smeltesteder (Martinez-Finley 2011). En av effektene av arseninntak under utviklingen av nervesystemet er hemming av neurittvekst som kan forekomme både i PNS og CNS. Denne nevrittveksthemmingen kan ofte føre til defekter i nevral migrasjon , og betydelige morfologiske endringer av nevroner under utvikling ), ofte fører til nevralrørsdefekter hos nyfødte . Som en metabolitt av arsen dannes arsenitt etter inntak av arsen og har vist betydelig toksisitet for nevroner innen ca. 24 timer etter eksponering. Mekanismen for denne cytotoksisiteten fungerer gjennom arsenittinduserte økninger i intracellulære kalsiumionnivåer i nevroner, som senere kan redusere mitokondrielt transmembranpotensial som aktiverer kaspaser , og utløser celledød. En annen kjent funksjon av arsenitt er dens destruktive natur mot cytoskjelettet gjennom hemming av nevrotrådtransport . Dette er spesielt ødeleggende siden nevrotrådene brukes i grunnleggende cellestruktur og støtte. Litiumadministrasjon har imidlertid vist lovende å gjenopprette noe av den tapte nevrofilamentmotiliteten. I tillegg, i likhet med andre nevrotoksinbehandlinger, har administrering av visse antioksidanter vist noe løfte når det gjelder å redusere nevrotoksisiteten til inntatt arsen.
Kalsiummediert cytotoksisitet
Lede
Bly er et kraftig nevrotoksin hvis toksisitet har vært anerkjent i minst tusenvis av år. Selv om nevrotoksiske effekter for bly finnes hos både voksne og små barn , er den utviklende hjernen spesielt utsatt for blyindusert skade, effekter som kan inkludere apoptose og eksitotoksisitet. En underliggende mekanisme som bly er i stand til å forårsake skade på, er dens evne til å bli transportert av kalsium ATPase-pumper over BBB, noe som muliggjør direkte kontakt med de skjøre cellene i sentralnervesystemet. Nevrotoksisitet skyldes blyets evne til å virke på samme måte som kalsiumioner, da konsentrert bly vil føre til cellulært opptak av kalsium som forstyrrer cellulær homeostase og induserer apoptose. Det er denne intracellulære kalsiumøkningen som aktiverer proteinkinase C (PKC), som viser seg som læringssvikt hos barn som følge av tidlig blyeksponering. I tillegg til å indusere apoptose, hemmer bly interneuronsignalering gjennom forstyrrelse av kalsiummediert nevrotransmitterfrigjøring.
Nevrotoksiner med flere effekter
Etanol

Som et nevrotoksin har etanol vist seg å forårsake skade på nervesystemet og påvirke kroppen på en rekke måter. Blant de kjente effektene av etanoleksponering er både forbigående og varige konsekvenser. Noen av de varige effektene inkluderer langsiktig redusert nevrogenese i hippocampus , utbredt hjerneatrofi og indusert betennelse i hjernen. Det er verdt å merke seg at kronisk etanolinntak i tillegg har vist seg å indusere reorganisering av cellulære membranbestanddeler, noe som fører til et lipid-dobbeltlag preget av økte membrankonsentrasjoner av kolesterol og mettet fett . Dette er viktig ettersom nevrotransmittertransport kan svekkes gjennom hemming av vesikulær transport, noe som resulterer i redusert nevrale nettverksfunksjon. Et betydelig eksempel på redusert inter-nevronkommunikasjon er evnen for etanol til å hemme NMDA-reseptorer i hippocampus, noe som resulterer i redusert langsiktig potensering (LTP) og minneinnhenting. NMDA har vist seg å spille en viktig rolle i LTP og følgelig minnedannelse. Med kronisk etanolinntak øker imidlertid følsomheten til disse NMDA-reseptorene for å indusere LTP i de mesolimbiske dopaminneuronene på en inositol 1,4,5-trifosfat (IP3) avhengig måte. Denne omorganiseringen kan føre til nevronal cytotoksisitet både gjennom hyperaktivering av postsynaptiske nevroner og gjennom indusert avhengighet til kontinuerlig etanolforbruk. Det har i tillegg blitt vist at etanol direkte reduserer intracellulær kalsiumionakkumulering gjennom hemmet NMDA-reseptoraktivitet, og dermed reduserer kapasiteten for forekomsten av LTP.
I tillegg til de nevrotoksiske effektene av etanol i modne organismer, er kronisk inntak i stand til å indusere alvorlige utviklingsdefekter. Det ble først vist bevis i 1973 på en sammenheng mellom kronisk etanolinntak hos mødre og defekter hos deres avkom. Dette arbeidet var ansvarlig for å lage klassifiseringen av føtalt alkoholsyndrom , en sykdom preget av vanlige morfogenese- avvik som defekter i kraniofacial dannelse, utvikling av lemmer og kardiovaskulær dannelse. Størrelsen på etanolnevrotoksisitet hos fostre som fører til føtalt alkoholsyndrom har vist seg å være avhengig av antioksidantnivåer i hjernen som vitamin E. Siden fosterhjernen er relativt skjør og utsatt for indusert stress, kan alvorlige skadelige effekter av alkoholeksponering sees i viktige områder som hippocampus og lillehjernen . Alvorlighetsgraden av disse effektene er direkte avhengig av mengden og hyppigheten av etanolforbruket til moren, og utviklingsstadiet til fosteret. Det er kjent at etanoleksponering resulterer i reduserte antioksidantnivåer, mitokondriell dysfunksjon (Chu 2007) og påfølgende nevronal død, tilsynelatende som et resultat av økt generasjon av reaktive oksidative arter (ROS). Dette er en plausibel mekanisme, siden det er redusert tilstedeværelse i fosterhjernen av antioksidantenzymer som katalase og peroksidase . Til støtte for denne mekanismen resulterer administrering av høye nivåer av vitamin E i kosten i reduserte eller eliminerte etanolinduserte nevrotoksiske effekter hos fostre.
n-heksan
n- Heksan er et nervegift som har vært ansvarlig for forgiftningen av flere arbeidere i kinesiske elektronikkfabrikker de siste årene.
Reseptorselektive nevrotoksiner
MPP +
MPP + , den toksiske metabolitten til MPTP , er et selektivt nevrotoksin som interfererer med oksidativ fosforylering i mitokondrier ved å hemme kompleks I , noe som fører til utarming av ATP og påfølgende celledød. Dette skjer nesten utelukkende i dopaminerge nevroner av substantia nigra , noe som resulterer i presentasjonen av permanent parkinsonisme hos utsatte personer 2–3 dager etter administrering.
Endogene nevrotoksinkilder
I motsetning til de fleste vanlige kildene til nevrotoksiner som er ervervet av kroppen gjennom inntak, stammer endogene nevrotoksiner både fra og utøver sine effekter in vivo . I tillegg, selv om de fleste giftstoffer og eksogene nevrotoksiner sjelden vil ha nyttige in vivo-evner, brukes endogene nevrotoksiner ofte av kroppen på nyttige og sunne måter, for eksempel nitrogenoksid som brukes i cellekommunikasjon. Det er ofte først når disse endogene forbindelsene blir svært konsentrerte at de fører til farlige effekter.
Nitrogenoksid
Selv om nitrogenoksid (NO) ofte brukes av nervesystemet i inter-nevronkommunikasjon og signalering, kan det være aktivt i mekanismer som fører til iskemi i storhjernen (Iadecola 1998). Nevrotoksisiteten til NO er basert på dens betydning for glutamateksitotoksisitet, da NO genereres på en kalsiumavhengig måte som respons på glutamatmediert NMDA-aktivering, som skjer med en forhøyet hastighet i glutamateksitotoksisitet. Selv om NO letter økt blodstrøm til potensielt iskemiske områder av hjernen, er det også i stand til å øke oksidativt stress , indusere DNA-skade og apoptose. En økt tilstedeværelse av NO i et iskemisk område av CNS kan således gi betydelig toksiske effekter.
Glutamat
Glutamat , som nitrogenoksid, er en endogent produsert forbindelse som brukes av nevroner for å fungere normalt, og er tilstede i små konsentrasjoner i hele den grå substansen i CNS. En av de mest bemerkelsesverdige bruksområdene for endogent glutamat er dets funksjon som en eksitatorisk nevrotransmitter. Når det er konsentrert, blir glutamat giftig for omkringliggende nevroner. Denne toksisiteten kan både være et resultat av direkte dødelighet av glutamat på nevroner og et resultat av indusert kalsiumfluks inn i nevroner som fører til hevelse og nekrose. Det er vist støtte for at disse mekanismene spiller en betydelig rolle i sykdommer og komplikasjoner som Huntingtons sykdom , epilepsi og hjerneslag .
Se også
Notater
Referanser
- Adams, Michael E.; Olivera, Baldomero M. (1994). "Neurotoksiner: Oversikt over en ny forskningsteknologi". Trender i nevrovitenskap . 17 (4): 151–55. doi : 10.1016/0166-2236(94)90092-2 . PMID 7517594 . S2CID 3984106 .
- Arnon, Stephen S.; Schechter, Robert; Inglesby, Thomas V.; Henderson, Donald A.; Bartlett, John G.; Ascher, Michael S.; Eitzen, Edward; Fint, Anne D.; Hauer, Jerome; Layton, Marcelle; Lillibridge, Scott; Osterholm, Michael T.; O'Toole, Tara; Parker, Gerald; Perl, Trish M.; Russell, Philip K.; Swerdlow, David L.; Tonat, Kevin (2001). "Botulinumtoksin som et biologisk våpen". Journal of the American Medical Association . 285 (8): 1059–069. doi : 10.1001/jama.285.8.1059 . PMID 11209178 .
- Aschner, M.; Aschner, J. (1990). "kvikksølv-nevrotoksisitet: mekanismer for transport av blod-hjernebarriere". Nevrovitenskap og bioatferdsanmeldelser . 14 (2): 169–76. doi : 10.1016/s0149-7634(05)80217-9 . PMID 2190116 . S2CID 8777931 .
- Banks, William A.; Kastin, Abba J. (1989). "Aluminiumindusert nevrotoksisitet: endringer i membranfunksjonen ved blod-hjerne-barrieren". Nevrovitenskap og bioatferdsanmeldelser . 13 (1): 47–53. doi : 10.1016/s0149-7634(89)80051-x . PMID 2671833 . S2CID 46507895 .
- Baum-Baicker, Cynthia (1985). "Helsefordelene ved moderat alkoholforbruk: En gjennomgang av litteraturen". Narkotika- og alkoholavhengighet . 15 (3): 207–27. doi : 10.1016/0376-8716(85)90001-8 . PMID 4028954 .
- Beckman, JS (1990). "Tilsynelatende hydroksylradikalproduksjon av peroksynitritt: implikasjoner for endotelskade fra nitrogenoksid og superoksid" . Proceedings of the National Academy of Sciences . 87 (4): 1620–624. Bibcode : 1990PNAS...87.1620B . doi : 10.1073/pnas.87.4.1620 . PMC 53527 . PMID 2154753 .
- Bergamini, Carlo M.; Gambetti, Stefani; Dondi, Alessia; Cervellati, Carlo (2004). "Oksygen, reaktive oksygenarter og vevsskade". Gjeldende farmasøytisk design . 10 (14): 1611–626. doi : 10.2174/1381612043384664 . PMID 15134560 .
-
Bernier Brian E., Whitaker Leslie R., Morikawa Hitoshi (2011). "Tidligere etanolopplevelse forbedrer synaptisk plastisitet til NMDA-reseptorer i det ventrale tegmentale området" . Journal of Neuroscience . 31 (14): 5305–212. doi : 10.1523/JNEUROSCI.5282-10.2011 . PMC 3086894 . PMID 21471355 .
{{cite journal}}: CS1 vedlikehold: flere navn: forfatterliste ( lenke ) - Bisset, Norman G (1992). "Krig og jaktgifter i den nye verden. Del 1. Merknader om Curares tidlige historie". Journal of Ethnopharmacology . 36 (1): 1–26. doi : 10.1016/0378-8741(92)90056-w . PMID 1501489 .
- Blanco, Ana M.; Valles, Soraya L.; Pascual, Maria; Guerri, Consuelo (2005). "Involvering av TLR4/Type I IL-1-reseptorsignalering i induksjon av inflammatoriske mediatorer og celledød indusert av etanol i dyrkede astrocytter" . Journal of Immunology . 175 (10): 6893–899. doi : 10.4049/jimmunol.175.10.6893 . PMID 16272348 .
- Bleich, S (2003). "Hyperhomocysteinemi som en ny risikofaktor for hjernekrymping hos pasienter med alkoholisme". Nevrovitenskapsbrev . 335 (3): 179–82. doi : 10.1016/s0304-3940(02)01194-1 . PMID 12531462 . S2CID 33032529 .
- Bonfoco E (1995). "Apoptose og nekrose: to distinkte hendelser indusert, henholdsvis av milde og intense fornærmelser med N-metyl-D-aspartat eller nitrogenoksid / superoksid i kortikale cellekulturer" . Proceedings of the National Academy of Sciences . 92 (16): 7162–166. Bibcode : 1995PNAS...92.7162B . doi : 10.1073/pnas.92.16.7162 . PMC 41299 . PMID 7638161 .
- Bradbury, MW; Deane, R (1993). "Permeabilitet av blod±hjernebarrieren til bly. [Anmeldelse]". Nevrotoksikologi . 14 (2–3): 131–6. PMID 8247388 .
- Brender, J.; Suarez, L.; Felkner, M.; Gilani, Z.; Stinchcomb, D.; Moody, K.; Henry, J.; Hendricks, K. (2006). "Modereksponering for arsenikk, kadmium, bly og kvikksølv og nevralrørsdefekter hos avkom". Miljøforskning . 101 (1): 132–39. Bibcode : 2006ER....101..132B . doi : 10.1016/j.envres.2005.08.003 . PMID 16171797 .
- Bressler, J; Kim, KA; Chakraborti, T; Goldstein, G (1999). "Molekylære mekanismer for blynevrotoksisitet. [Anmeldelse]". Neurochem Res . 24 (4): 595–600. doi : 10.1023/A:1022596115897 . PMID 10227691 . S2CID 3017703 .
- Brocardo, Patricia S.; Gil-Mohapel, Joana; Christie, Brian R. (2011). "Rollen til oksidativt stress i fosteralkoholspektrumforstyrrelser". Hjerneforskningsanmeldelser . 67 (1–2): 209–25. doi : 10.1016/j.brainresrev.2011.02.001 . PMID 21315761 . S2CID 1213492 .
- Brookes, N (1988). "Spesifisitet og reversibilitet av inhibering av HgCl av glutamattransport i astrocytkulturer". Journal of Neurochemistry . 50 (4): 1117–122. doi : 10.1111/j.1471-4159.1988.tb10581.x . PMID 2894409 . S2CID 27522735 .
- Buzanska, L.; Zablocka, B.; Dybel, A.; Domanska-Janik, K.; Albrecht, J. (2000). "Forsinket induksjon av apoptose av ammoniakk i C6 gliomceller". Neurochemistry International . 37 (2–3): 287–97. doi : 10.1016/s0197-0186(00)00030-9 . PMID 10812214 . S2CID 33351533 .
- Carmichael WW, Biggs DF, Gorham PR (1975). "Toksikologi og farmakologisk virkning av Anabaena flos-aquae-toksin". Vitenskap . 187 (4176): 542–544. Bibcode : 1975Sci...187..542C . doi : 10.1126/science.803708 . PMID 803708 .
- Carmichael WW, Gorham PR (1978). "Anatoksiner fra kloner av Anabaena flos-aquae isolert fra innsjøer i det vestlige Canada". Mitt. Infernalsk. Verein. Limnol . 21 : 285–295.
- Chan, HM (2011) "Mercury in Fish: Human Health Risks." Encyclopedia of Environmental Health : 697–704.
- Choi, D (1988). "Kalsiummediert nevrotoksisitet: forhold til spesifikke kanaltyper og rolle i iskemisk skade". Trender i nevrovitenskap . 11 (10): 465–69. doi : 10.1016/0166-2236(88)90200-7 . PMID 2469166 . S2CID 36909560 .
- Choi, DW; Rothman, SM (1990). "Rollen til glutamatnevrotoksisitet i hypoksisk-iskemisk nevronal død". Årlig gjennomgang av nevrovitenskap . 13 (1): 171–82. doi : 10.1146/annurev.neuro.13.1.171 . PMID 1970230 .
- Choi, Dennis W (1987). "Ionisk avhengighet av glutamatnevrotoksisitet" . Journal of Neuroscience . 7 (2): 369–79. doi : 10.1523/JNEUROSCI.07-02-00369.1987 . PMC 6568907 . PMID 2880938 .
- Choi, Dennis W.; Maulucci-Gedde, Margaret; Kriegstein, Arnold R. (1987). "Glutamatnevrotoksisitet i kortikal cellekultur" . Journal of Neuroscience . 7 (2): 357–68. doi : 10.1523/JNEUROSCI.07-02-00357.1987 . PMC 6568898 . PMID 2880937 .
- Chu, Jennifer; Tong, Ming; Monte, Suzanne M. (2007). "Kronisk etanoleksponering forårsaker mitokondriell dysfunksjon og oksidativt stress i umodne nevroner i sentralnervesystemet". Acta Neuropathologica . 113 (6): 659–73. doi : 10.1007/s00401-007-0199-4 . PMID 17431646 . S2CID 25418731 .
- Clancy, Barbara; Finlay, Barbara L.; Darlington, Richard B.; Anand, KJS (2007). "Ekstrapolere hjerneutvikling fra eksperimentelle arter til mennesker" . Nevrotoksikologi . 28 (5): 931–37. doi : 10.1016/j.neuro.2007.01.014 . PMC 2077812 . PMID 17368774 .
- Costa, Lucio G., Gennaro Giordano og Marina Guizzetti (2011) In vitro nevrotoksikologi: metoder og protokoller. New York: Humana.
- Coyle, Joseph T.; Schwarcz, Robert (1976). "Lesjon av striatale nevroner med Kainic Acid gir en modell for Huntingtons Chorea". Natur . 246 (5574): 244–46. Bibcode : 1976Natur.263..244C . doi : 10.1038/263244a0 . PMID 8731 . S2CID 4271762 .
- Cruz, Lourdes J.; Olivera, Baldomero M. (1987). "Kalsiumkanalantagonister ω-konotoksin definerer et nytt nettsted med høy affinitet". Journal of Biological Chemistry . 14 (261): 6230–233.
- Davis, S.; Slakter, SP; Morris, R. (1992). "NMDA-reseptorantagonisten D-2-amino-5fosfonpentanoat (D-AP5) svekker romlig læring og LTP in vivo ved intracerebrale konsentrasjoner som kan sammenlignes med de som blokkerer LTP in vitro" . Journal of Neuroscience . 12 (1): 21–34. doi : 10.1523/JNEUROSCI.12-01-00021.1992 . PMC 6575679 . PMID 1345945 .
- Dawson, VL (1991). "Nitric Oxide medierer glutamat-nevrotoksisitet i primære kortikale kulturer" . Proceedings of the National Academy of Sciences . 88 (14): 6368–371. Bibcode : 1991PNAS...88.6368D . doi : 10.1073/pnas.88.14.6368 . PMC 52084 . PMID 1648740 .
- Debin, John A., John E. Maggio og Gary R. Strichartz (1993) "Purification and Characterization of Chlorotoxin, a Chloride Channel Ligand from the Venom of the Scorpion." The American Physiological Society , s. 361–69.
- DeFuria, Jason; Shea, Thomas B. (2007). "Arsen hemmer nevrofilamenttransport og induserer perikaryal akkumulering av fosforylerte nevrofilamenter: Roller til JNK og GSK-3β". Hjerneforskning . 1181 : 74–82. doi : 10.1016/j.brainres.2007.04.019 . PMID 17961518 . S2CID 37068398 .
- Defuria, Jason (2006) "The Environmental Neurotoxin Arsenic impairs Neurofilament Dynamics by Overactivation of C-JUN Terminal Kinase: Potential Role for Amyotrophic Lateral Sclerosis." UMI , s. 1–16.
- Deng Wenbin, Poretz Ronald D (2003). "Oligodendroglia i utviklingsnevrotoksisitet". Nevrotoksikologi . 24 (2): 161–78. doi : 10.1016/s0161-813x(02)00196-1 . PMID 12606289 .
- Deshane, Jessy; Garner, Craig C.; Sontheimer, Harald (2003). "Klortoksin hemmer gliomcelleinvasjon via matrisemetalloproteinase-2" . Journal of Biological Chemistry . 278 (6): 4135–144. doi : 10.1074/jbc.m205662200 . PMID 12454020 .
- Devlin JP, Edwards OE, Gorham PR, Hunter NR, Pike RK, Stavric B (1977). "Anatoxin-a, et giftig alkaloid fra Anabaena flos-aquae NRC-44h" . Kan. J. Chem . 55 (8): 1367–1371. doi : 10.1139/v77-189 . Arkivert fra originalen 2012-07-09.
- Dikranian, K (2001). "Apoptose i in vivo pattedyrforhjernen" . Nevrobiologi av sykdom . 8 (3): 359–79. doi : 10.1006/nbdi.2001.0411 . PMID 11447994 . S2CID 21965033 .
- Dixit A, Dhaked RK, Alam SI, Singh L (2005). "Militært potensial for biologiske nevrotoksiner". Toxin anmeldelser . 24 (2): 175–207. doi : 10.1081/TXR-200057850 . S2CID 85651107 .
- Dobbs, Michael R (2009) Klinisk nevrotoksikologi. Philadelphia: Saunders-Elsevier.
- Dutertre, S.; Lewis, R. (2006). "Toksininnsikt i nikotiniske acetylkolinreseptorer". Biokjemisk farmakologi . 72 (6): 661–70. doi : 10.1016/j.bcp.2006.03.027 . PMID 16716265 .
- Garcia-Rodriguez, C.; Geren, IN; Lou, J.; Conrad, F.; Forsyth, C.; Wen, W.; Chakraborti, S.; Zao, H.; Manzanarez, G.; Smith, TJ; Brown, J.; Tepp, WH; Liu, N.; Wijesuriya, S.; Tomic, MT; Johnson, EA; Smith, LA; Marks, JD (2011). "Svar vedr.: 'Nøytralisering av humane monoklonale antistoffer som binder flere serotyper av botulinumnevrotoksin' av Garcia-Rodriguez et al., PEDS, 2011; 24:321–331" . Protein Engineering Design og utvalg . 24 (9): 633–34. doi : 10.1093/protein/gzr012 .
- Garthwaite, John; Charles, Sarah L.; Chess-Williams, Russel (1988). "Endotel-avledet avslappende faktorfrigivelse ved aktivering av NMDA-reseptorer foreslår rolle som intercellulær messenger i hjernen". Natur . 336 (24): 385–88. Bibcode : 1988Natur.336..385G . doi : 10.1038/336385a0 . PMID 2904125 . S2CID 4361381 .
- Gartlon, J.; Kinsner, A.; Balprice, A.; Coecke, S.; Clothier, R. (2006). "Evaluering av en foreslått in vitro-teststrategi ved bruk av nevronale og ikke-nevronale cellesystemer for å oppdage nevrotoksisitet". Toksikologi in vitro . 20 (8): 1569–581. doi : 10.1016/j.tiv.2006.07.009 . PMID 16959468 .
- Gil-Mohapel, Joana; Boehme, Fanny; Kainer, Leah; Christie, Brian R. (2010). "Hippocampal celletap og nevrogenese etter føtal alkoholeksponering: innsikt fra forskjellige gnagermodeller". Hjerneforskningsanmeldelser . 64 (2): 283–303. doi : 10.1016/j.brainresrev.2010.04.011 . PMID 20471420 . S2CID 10159395 .
- Haghdoost-Yazdi, Hashem; Faraji, Ayda; Fraidouni, Negin; Movahedi, Mohadeseh; Hadibeygi, Elham; Vaezi, Fatemeh (2011). "Betydende effekter av 4-aminopyridin og tetraetylammonium i behandlingen av 6-hydroksydopamin-indusert Parkinsons sykdom". Atferdsmessig hjerneforskning . 223 (1): 70–74. doi : 10.1016/j.bbr.2011.04.021 . PMID 21540059 . S2CID 7100177 .
- Harry, GJ; Billingsley, Melvin; Bruinink, Arendd; Campbell, Iain L.; Classen, Werner; Dorman, David C.; Galli, Corrado; Ray, David; Smith, Robert A.; Tilson, Hugh A. (1998). "In vitro-teknikker for vurdering av nevrotoksisitet" . Miljøhelseperspektiver . 106 (Suppl 1): 131–58. doi : 10.2307/3433917 . JSTOR 3433917 . PMC 1533280 . PMID 9539010 .
- Häussinger, Dieter (2006). "Lavgradig cerebralt ødem og patogenesen av hepatisk encefalopati ved cirrhosis" . Hepatologi . 43 (6): 1187–190. doi : 10.1002/hep.21235 . PMID 16729329 .
- Hensley, K (1994). "En modell for β-amyloidaggregasjon og nevrotoksisitet basert på frie radikalgenerering av peptidet: relevans for Alzheimers sykdom" . Proceedings of the National Academy of Sciences . 91 (8): 3270–274. Bibcode : 1994PNAS...91.3270H . doi : 10.1073/pnas.91.8.3270 . PMC 43558 . PMID 8159737 .
- Herbert, MR (2006) "Autisme og miljøgenomikk." NeuroToxicology , s. 671–84. Web.
- Hodge, A. Trevor (2002) Romerske akvedukter og vannforsyning . London: Duckworth.
- How, C (2003). "Tetrodotoxin-forgiftning". American Journal of Emergency Medicine . 21 (1): 51–54. doi : 10.1053/ajem.2003.50008 . PMID 12563582 .
- Hue, Bernard; Buckingham, Steven D.; Buckingham, David; Sattelle, David B. (2007). "Handlinger av slangenevrotoksiner på en insekt nikotinisk kolinerg synapse". Virvelløse nevrovitenskap . 7 (3): 173–78. doi : 10.1007/s10158-007-0053-3 . PMID 17710455 . S2CID 31599093 .
- Iadecola Constantino (1997). "Lyse og mørke sider av nitrogenoksid ved iskemisk hjerneskade". Trender i nevrovitenskap . 20 (3): 132–39. doi : 10.1016/s0166-2236(96)10074-6 . PMID 9061868 . S2CID 45011034 .
- Jacob, Reed B.; McDougal, Owen M. (2010). "M-superfamilien til konotoksiner: en anmeldelse" . Cellulær og molekylær livsvitenskap . 67 (1): 17–27. doi : 10.1007/s00018-009-0125-0 . PMC 3741454 . PMID 19705062 .
- Jevtovic-Todorovic, Vesna; Hartman, Richard E.; Izumi, Yukitoshi; Benshoff, Nicholas D.; Dikranian, Krikor; Zorumski, Charles F.; Olney, John W.; Wozniak, David F. (2003). "Tidlig eksponering for vanlige anestesimidler forårsaker utbredt nevrodegenerasjon i den utviklende rottehjernen og vedvarende læringssvikt" . Journal of Neuroscience . 23 (3): 876–82. doi : 10.1523/JNEUROSCI.23-03-00876.2003 . PMC 6741934 . PMID 12574416 .
- Jones, K (1973). "Mønster av misdannelse hos avkom av kroniske alkoholiske mødre". The Lancet . 301 (7815): 1267–271. doi : 10.1016/s0140-6736(73)91291-9 . PMID 4126070 .
- Kiernan, Matthew C.; Isbister, Geoffrey K.; Cindy; Lin, S.-Y.; Burke, David; Bostock, Hugh (2005). "Akutt tetrodotoksinindusert nevrotoksisitet etter inntak av pufferfisk". Annals of Neurology . 57 (3): 339–48. doi : 10.1002/ana.20395 . PMID 15732107 . S2CID 40455149 .
- King, Steven W.; Velsmakende, John; Wills, Michael R.; Gitelman, HJ (1981). "Den kliniske biokjemien til aluminium". Kritiske anmeldelser i kliniske laboratorievitenskaper . 14 (1): 1–20. doi : 10.3109/10408368109105861 . PMID 7016437 .
- Konopacka, Agnieszka; Konopacki, Filip A.; Albrecht, Jan (2009). "Protein Kinase G er involvert i ammoniakk-indusert hevelse av astrocytter". Journal of Neurochemistry . 109 : 246–51. doi : 10.1111/j.1471-4159.2009.05802.x . PMID 19393034 . S2CID 42719321 .
- Lafon-Cazal, Mireille; Pietri, Sylvia; Culcasi, Marcel; Bockaert, Joel (1993). "NMDA-avhengig superoksidproduksjon og nevrotoksisitet". Natur . 364 (6437): 535–37. Bibcode : 1993Natur.364..535L . doi : 10.1038/364535a0 . PMID 7687749 . S2CID 4246917 .
- Lasley, SM; Green, MC; Gilbert, ME (1999). "Påvirkning av eksponeringsperiode på in vivo hippocampal glutamat og GABA-frigjøring hos rotter som er kronisk utsatt for bly". Nevrotoksikologi . 20 (4): 619–29. PMID 10499360 .
- Lau, FL; Wong, CK; Jepp, SH (1995). "Puffer Fish Forgiftning" . Emergency Medicine Journal . 12 (3): 214–15. doi : 10.1136/emj.12.3.214 . PMC 1342486 . PMID 8581253 .
- Lewendon, G.; Kinra, S.; Nelder, R.; Cronin, T. (2001). "Bør barn med utviklings- og atferdsproblemer rutinemessig screenes for bly?" . Arkiv for sykdom i barndommen . 85 (4): 286–88. doi : 10.1136/adc.85.4.286 . PMC 1718950 . PMID 11567935 .
- Lidsky Theodore I (2003). "Blynevrotoksisitet hos barn: grunnleggende mekanismer og kliniske korrelater" . Hjerne . 126 (1): 5–19. doi : 10.1093/brain/awg014 . PMID 12477693 .
- Liu, Kuang-Kai; Chen, Mei-Fang; Chen, Po-Yi; Lee, Tony J F.; Cheng, Chia-Liang; Chang, Chia-Ching; Ho, Yen-Peng; Jui-I, Chao (2008). "Alfa-bungarotoksin binder til målcelle i et visuelt system i utvikling av karboksylert nanodiamant" . Nanoteknologi . 19 (20): 205102. Bibcode : 2008Nanot..19t5102L . doi : 10.1088/0957-4484/19/20/205102 . PMID 21825732 . S2CID 1260143 .
- Liu, Yuan; McDermott, Suzanne; Lawson, Andrew; Aelion, C. Marjorie (2010). "Forholdet mellom mental retardasjon og utviklingsforsinkelser hos barn og nivåene av arsenikk, kvikksølv og bly i jordprøver tatt i nærheten av deres mors bolig under svangerskapet" . International Journal of Hygiene and Environmental Health . 213 (2): 116–23. doi : 10.1016/j.ijheh.2009.12.004 . PMC 2836425 . PMID 20045663 .
- Lorenzo, A (1994). "β-Amyloid nevrotoksisitet krever fibrildannelse og hemmes av kongorødt" . Proceedings of the National Academy of Sciences . 91 (25): 12243–2247. Bibcode : 1994PNAS...9112243L . doi : 10.1073/pnas.91.25.12243 . PMC 45413 . PMID 7991613 .
- Lotti, Marcello og Angelo Moretto (1989) "Organofosfat-indusert forsinket polynevropati." Toxicological Reviews, 24 (1) (2005): 37–49.
- Martinez-Finley, Ebany J.; Goggin, Samantha L.; Labrecque, Matthew T.; Allan, Andrea M. (2011). "Redusert uttrykk for MAPK/ERK-gener i perinatalt arseneksponert avkom indusert av glukokortikoidreseptormangel" . Nevrotoksikologi og teratologi . 33 (5): 530–37. doi : 10.1016/j.ntt.2011.07.003 . PMC 3183307 . PMID 21784148 .
- Martini, Frederic, Michael J. Timmons og Robert B. Tallitsch (2009) Human Anatomy. San Francisco: Pearson/Benjamin Cummings.
- Matsuoka, Masato; Igisu, Hideki; Kohriyama, Kazuaki; Inoue, Naohide (1991). "Undertrykkelse av nevrotoksisitet av ammoniakk av L-karnitin". Hjerneforskning . 567 (2): 328–31. doi : 10.1016/0006-8993(91)90814-c . PMID 1817738 . S2CID 10250413 .
- McCleskey, EW (1987). "Omega-konotoksin: Direkte og vedvarende blokade av spesifikke typer kalsiumkanaler i nevroner, men ikke muskler" . Proceedings of the National Academy of Sciences . 84 (12): 4327–331. Bibcode : 1987PNAS...84.4327M . doi : 10.1073/pnas.84.12.4327 . PMC 305078 . PMID 2438698 .
- Meldrum, B.; Garthwaite, J. (1990). "Eksitatorisk aminosyrenevrotoksisitet og nevrodegenerativ sykdom". Trender i farmakologiske vitenskaper . 11 (9): 379–87. doi : 10.1016/0165-6147(90)90184-a . PMID 2238094 .
- Metcalf, James S.; Codd, Geoffrey A. (2009). "Cyanobakterier, nevrotoksiner og vannressurser: Er det implikasjoner for menneskelig nevrodegenerativ sykdom?". Amyotrofisk lateral sklerose . 10 : 74–78. doi : 10.3109/17482960903272942 . PMID 19929737 . S2CID 41880444 .
- Mitchell, J. Jean; Paiva, Michael; Barrow Heaton, Marieta (1999). "Antioksidantene vitamin E og β-karoten beskytter mot etanolindusert nevrotoksisitet i embryonale rottehippocampale kulturer". Alkohol . 17 (2): 163–68. doi : 10.1016/s0741-8329(98)00051-2 . PMID 10064385 .
- Moore RE (1977). "Giftstoffer fra blågrønne alger". Biovitenskap . 27 (12): 797–802. doi : 10.2307/1297756 . JSTOR 1297756 .
- Montecucco C (1986). "Hvordan binder stivkrampe og botulinumtoksiner til nevronale membraner?". Trender i biokjemiske vitenskaper . 11 (8): 314–17. doi : 10.1016/0968-0004(86)90282-3 .
- Morris, Stephanie A., David W. Eaves, Aleksander R. Smith og Kimberly Nixon (2009) "Alcohol Inhibition of Neurogenesis: A Mechanism of Hippocampal Neurodegeneration in an Adolescent Alcohol Abuse Model." Hippocampus: NA.
- Nadler; Victor, J.; Perry, Bruce W.; Cotman, Carl W. (1978). "Intraventrikulær Kainic Acid ødelegger fortrinnsvis hippocampale pyramideceller". Natur . 271 (5646): 676–77. Bibcode : 1978Natur.271..676N . doi : 10.1038/271676a0 . PMID 625338 . S2CID 4267990 .
- Nasjonalt senter for miljøvurdering (2006) "Toksikologiske vurderinger av cyanobakterielle toksiner: anatoksin-a" NCEA-C-1743
- Norenberg, MD; Rao, KV Rama; Jayakumar, AR (2004). "Ammoniakknevrotoksisitet og mitokondriell permeabilitetsovergang". Journal of Bioenergetics and Biomembranes . 36 (4): 303–07. doi : 10.1023/b:jobb.0000041758.20071.19 . PMID 15377862 . S2CID 39221153 .
- Olivera, Baldomero M.; Cruz, Lourdes J.; De Santos, Victoria; LeCheminant, Garth; Griffin, David; Zeikus, Regina; McIntosh, J. Michael; Galyan, Robert; Varga, Janos (1987). "Neuronale kalsiumkanalantagonister. Diskriminering mellom kalsiumkanalundertyper ved bruk av .omega.-konotoksin fra Conus Magus Venom". Biokjemi . 26 (8): 2086–090. doi : 10.1021/bi00382a004 . PMID 2441741 .
- Olney, John W (2002). "Ny innsikt og nye problemer i utviklingsnevrotoksikologi". Nevrotoksikologi . 23 (6): 659–68. doi : 10.1016/s0161-813x(01)00092-4 . PMID 12520755 .
- Pirazzini, Marco, Ornella Rossetto, Paolo Bolognese, Clifford C. Shone og Cesare Montecucco (2011) "Dobbelt forankring til membranen og intakt inter-kjede disulfidbinding er nødvendig for lav PH-indusert inntreden av stivkrampe og botulinumnevrotoksiner i nevroner. " Cellulær mikrobiologi: nr. Trykk.
- Rabe, Ausma; He Lee, Moon; Shek, Judy; Wisniewski, Henryk M. (1982). "Læringsunderskudd hos umodne kaniner med aluminiuminduserte nevrofibrillære endringer". Eksperimentell nevrologi . 76 (2): 441–46. doi : 10.1016/0014-4886(82)90220-5 . PMID 6896495 . S2CID 7495252 .
- Rocha, RA; Gimeno-Alcaniz, JV; Martín-Ibanez, Raymond; Canals, JM; Vélez, D.; Devesa, V. (2011). "Arsen og fluor induserer nevral stamcelleapoptose". Toksikologibrev . 203 (3): 237–44. doi : 10.1016/j.toxlet.2011.03.023 . PMID 21439358 .
- Roed, A (1989). "Effektene av tetraetylammonium under rykninger og tetanisk stimulering av forberedelse av frenisk nervemembran i rotten". Nevrofarmakologi . 28 (6): 585–92. doi : 10.1016/0028-3908(89)90137-8 . PMID 2547180 . S2CID 1916154 .
- Rothman, S.; Thurston, J.; Hauhart, R. (1987). "Forsinket nevrotoksisitet av eksitatoriske aminosyrer in vitro". Nevrovitenskap . 22 (2): 471–80. doi : 10.1016/0306-4522(87)90347-2 . PMID 3670595 . S2CID 6038419 .
- Schlesinger, Edward B (1946). "Curare en gjennomgang av dens terapeutiske effekter og deres fysiologiske grunnlag". American Journal of Medicine . 1 (5): 518–30. doi : 10.1016/0002-9343(46)90073-3 . PMID 21001466 .
- Siebler, M.; Koller, H.; Schmalenbach, C.; Muller, H. (1988). "GABA-aktiverte kloridstrømmer i nevroner i dyrkede rottehippocampale og septalregioner kan hemmes av Curare og Atropin". Nevrovitenskapsbrev . 93 (2–3): 220–24. doi : 10.1016/0304-3940(88)90085-7 . PMID 2468110 . S2CID 10645685 .
- Simpson, LL (1986). "Molekylær farmakologi av botulinumtoksin og tetanustoksin". Årlig gjennomgang av farmakologi og toksikologi . 26 (1): 427–53. doi : 10.1146/annurev.pharmtox.26.1.427 . PMID 3521461 .
- Soroceanu, Liliana; Gillespie, Yancey; Khazaeli, MB; Sontheimer, Harold (1998). "Bruk av klorotoksin for målretting av primære hjernesvulster". Kreftforskning . 58 (21): 4871–879. PMID 9809993 .
- Spencer PS, Schaumburg HH, Ludolph AC (Eds) (2000) Eksperimentell og klinisk nevrotoksikologi. Oxford University Press, Oxford, s. 1310.
- Stanfield, Peter R (1983). "Tetraetylammoniumioner og kaliumpermeabiliteten til eksitable celler". Anmeldelser av fysiologi, biokjemi og farmakologi . 97 : 1–49. doi : 10.1007/bfb0035345 . ISBN 978-3-540-11701-8. PMID 6306751 .
- Stewart I, Seawright AA, Shaw GR (2008). "Cyanobakteriell forgiftning hos husdyr, ville pattedyr og fugler - en oversikt" (PDF) . Cyanobakteriell skadelig algeoppblomstring: vitenskapens tilstand og forskningsbehov . Fremskritt innen eksperimentell medisin og biologi. 619 : 613–637. doi : 10.1007/978-0-387-75865-7_28 . ISBN 978-0-387-75864-0. PMID 18461786 .
- Taffe, MA; Kotzebue, RW; Crean, RD; Crawford, EF; Edwards, S.; Mandyam, CD (2010). "Fra omslaget: Langvarig reduksjon i hippocampus nevrogenese ved alkoholforbruk hos unge ikke-menneskelige primater" . Proceedings of the National Academy of Sciences . 107 (24): 11104–1109. Bibcode : 2010PNAS..10711104T . doi : 10.1073/pnas.0912810107 . PMC 2890755 . PMID 20534463 .
- Takadera, Tsuneo; Suzuki, Risa; Mohri, Tetsuro (1990). "Beskyttelse av etanol av kortikale nevroner fra N-metyl-d-aspartat-indusert nevrotoksisitet er assosiert med blokkering av kalsiumtilstrømning". Hjerneforskning . 537 (1–2): 109–14. doi : 10.1016/0006-8993(90)90346-d . PMID 1982237 . S2CID 22160700 .
- Thyagarajan, B.; Krivitskaya, N.; Potian, JG; Hognason, K.; Garcia, CC; McArdle, JJ (2009). "Capsaicin beskytter muse-nevromuskulære koblinger fra de nevropalytiske effektene av botulinumnevrotoksin A." Journal of Pharmacology and Experimental Therapeutics . 331 (2): 361–71. doi : 10.1124/jpet.109.156901 . PMC 2775269 . PMID 19654265 .
- Tymianski, Michael; Charlton, Milton P.; Carlen, Peter L.; Tator, Charles H. (2003). "Kildespesifisitet av tidlig kalsiumnevrotoksisitet i dyrkede embryonale spinalnevroner" . Journal of Neuroscience . 13 (5): 2095–104. doi : 10.1523/JNEUROSCI.13-05-02085.1993 . PMC 6576557 . PMID 8097530 .
- Tsetlin, VI; Hucho, F. (2004). "Slange- og snegletoksiner som virker på nikotiniske acetylkolinreseptorer: grunnleggende aspekter og medisinske anvendelser" . FEBS brev . 557 (1–3): 9–13. doi : 10.1016/s0014-5793(03)01454-6 . PMID 14741333 .
- USEPA (United States Environmental Protection Agency) (1998) Testretningslinjer for helseeffekter. OPPTS 870.6200. Nevrotoksisitetsscreeningsbatteri. Washington DC, USEPA.
- Vahidnia, A., GB Van Der Voet og FA De Wolff (2007) "Arsenic Neurotoxicity A Review." Human & Experimental Toxicology, 26 (10): 823–32.
- Walton, J (2006). "Aluminium i hippocampale nevroner fra mennesker med Alzheimers sykdom". Nevrotoksikologi . 27 (3): 385–94. doi : 10.1016/j.neuro.2005.11.007 . PMID 16458972 .
- Widmaier, Eric P., Hershel Raff, Kevin T. Strang og Arthur J. Vander (2008) Vanders Human Physiology: The Mechanisms of Body Function. Boston: McGraw-Hill høyere utdanning.
- Williamson, Lura C.; Halpern, Jane L.; Montecucco, Cesare; Brown, JE; Neale, Elaine A. (1996). "Clostridiale nevrotoksiner og substratproteolyse i intakte nevroner" . Journal of Biological Chemistry . 271 (13): 7694–699. doi : 10.1074/jbc.271.13.7694 . PMID 8631808 .
- Wood SA; Rasmussen JP; Holland PT; Campbell R.; Crowe ALM (2007). "Første rapport om Cyanotoxin Anatoxin-A fra Aphanizomenon issatschenkoi (cyanobakterier)". Journal of Physology . 43 (2): 356–365. doi : 10.1111/j.1529-8817.2007.00318.x . S2CID 84284928 .
- Yamada, Kiyofumi; Tanaka, Tomoko; Han, Daiken; Senzaki, Kouji; Kameyama, Tsutomu; Nabeshima, Toshitaka (1999). "Beskyttende effekter av Idebenone og α-tokoferol på β-amyloid-(1–42)-indusert lærings- og hukommelsesmangel hos rotter: Implikasjon av oksidativt stress i β-amyloid-indusert nevrotoksisitet in vivo". European Journal of Neuroscience . 11 (1): 83–90. doi : 10.1046/j.1460-9568.1999.00408.x . PMID 9987013 . S2CID 84408095 .
- Yan; Du, Shi; Chen, Xi; Fu, Jin; Chen, Ming; Zhu, Huaijie; Roher, Alex; Slattery, Timothy; Zhao, Lei; Nagashima, Mariko; Morser, John; Migheli, Antonio; Nawroth, Peter; Stern, David; Marie Schmidt, Ann (1996). "RAGE og amyloid-β-peptidnevrotoksisitet ved Alzheimers sykdom". Natur . 382 (6593): 685–91. Bibcode : 1996Natur.382..685Y . doi : 10.1038/382685a0 . PMID 8751438 . S2CID 4372023 .
- Yang, X (2007) Forekomst av det cyanobakterielle nevrotoksinet, anatoxin-a, i New York State farvann ProQuest. ISBN 978-0-549-35451-2 .
- Zhang, J.; Dawson, V.; Dawson, T.; Snyder, S. (1994). "Nitrogenoksidaktivering av poly(ADP-ribose) syntetase i nevrotoksisitet". Vitenskap . 263 (5147): 687–89. Bibcode : 1994Sci...263..687Z . doi : 10.1126/science.8080500 . PMID 8080500 .
Videre lesning
- Brain Facts Book hos The Society for Neuroscience
- Nevrovitenskapstekster ved University of Texas Medical School
- In Vitro Neurotoxicology: An Introduction at Springerlink
- Biologi av NMDA-reseptoren ved NCBI
- Advances in the Neuroscience of Addiction, 2. utgave ved NCBI
Eksterne linker
- Environmental Protection Agency ved United States Environmental Protection Agency
- Alkohol og alkoholisme ved Oxford Medical Journals
- Nevrotoksikologi ved Elsevier Journals
- Neurotoxin Institute ved Neurotoxin Institute
- [1] Nevrotoksiner] hos Toxipedia