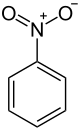
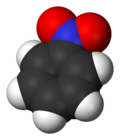
Nitrobenzen - Nitrobenzene
|
|
|||

|
|||
| Navn | |||
|---|---|---|---|
|
Foretrukket IUPAC-navn
Nitrobenzen |
|||
| Andre navn
Nitrobenzol
Olje av mirbane |
|||
| Identifikatorer | |||
|
3D-modell ( JSmol )
|
|||
| ChEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,002,469 |
||
| KEGG | |||
|
PubChem CID
|
|||
| RTECS-nummer | |||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eiendommer | |||
| C 6 H 5 NO 2 | |||
| Molarmasse | 123,11 g / mol | ||
| Utseende | gulaktig, oljeaktig væske | ||
| Lukt | skarp, som lim skopuss | ||
| Tetthet | 1.199 g / cm 3 | ||
| Smeltepunkt | 5,7 ° C (42,3 ° F; 278,8 K) | ||
| Kokepunkt | 210,9 ° C (411,6 ° F; 484,0 K) | ||
| 0,19 g / 100 ml ved 20 ° C | |||
| Damptrykk | 0,3 mmHg (25 ° C) | ||
| -61,80 · 10 −6 cm 3 / mol | |||
| Viskositet | 1,8112 mPa · s | ||
| Farer | |||
|
EU-klassifisering (DSD) (utdatert)
|
|
||
| R-setninger (utdaterte) |
R10 , R23 / 24/25 , R40 , R48 / 23/24 , R51 / 53 , R62 |
||
| S-setninger (utdaterte) |
(S1 / 2) , S28 , S36 / 37 , S45 , S61 |
||
| NFPA 704 (branndiamant) | |||
| Flammepunkt | 88 ° C (190 ° F; 361 K) | ||
| 480 ° C (896 ° F; 753 K) | |||
| Eksplosive grenser | 1,8% -? | ||
| Dødelig dose eller konsentrasjon (LD, LC): | |||
|
LD 50 ( median dose )
|
780 mg / kg (rotte, oral) 600 mg / kg (rotte, oral) 590 mg / kg (mus, oral) |
||
|
LD Lo ( lavest publisert )
|
750 mg / kg (hund, oral) | ||
| NIOSH (amerikanske helseeksponeringsgrenser): | |||
|
PEL (tillatt)
|
TWA 1 ppm (5 mg / m 3 ) [hud] | ||
|
REL (anbefalt)
|
TWA 1 ppm (5 mg / m 3 ) [hud] | ||
|
IDLH (umiddelbar fare)
|
200 spm | ||
| Beslektede forbindelser | |||
|
Beslektede forbindelser
|
Aniline Benzenediazonium klorid Nitrosobensen |
||
|
Med mindre annet er angitt, blir data gitt for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infoboksreferanser | |||
Nitrobenzen er en organisk forbindelse med den kjemiske formelen C 6 H 5 NO 2 . Det er et vann-uløselig blek gul olje med en mandel -lignende lukt. Det fryser for å gi grønn-gule krystaller. Den produseres i stor skala fra benzen som forløper til anilin . I laboratoriet brukes det av og til som løsemiddel , spesielt for elektrofile reagenser .
Produksjon
Nitrobenzen fremstilles ved nitrering av benzen med en blanding av konsentrert svovelsyre , vann og salpetersyre . Denne blandingen kalles noen ganger "blandet syre." Produksjonen av nitrobenzen er en av de mest farlige prosesser som utføres i den kjemiske industri på grunn av den eksoterme karakter av reaksjonen (Δ H = -117 kJ / mol).
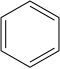 +
+ 
Verdens kapasitet for nitrobenzen i 1985 var omtrent 1,7 × 10 6 tonn .
Den Nitreringen prosessen involverer dannelsen av nitronium- ion (NO 2 + ), etterfulgt av en elektrofil aromatisk substitusjon omsetning av det med benzen. Nitroniumionet genereres ved omsetning av salpetersyre og et surt dehydratiseringsmiddel, typisk svovelsyre:
- HNO 3 + H + ⇌ NO 2 + + H 2 O
Bruker
Omtrent 95% av den produserte nitrobenzenen er hydrogenert til anilin :
- C 6 H 5 NO 2 + 3 H 2 → C 6 H 5 NH 2 + 2 H 2 O
Anilin er en forløper for uretanpolymerer , gummikjemikalier , plantevernmidler , fargestoffer (spesielt azofargestoffer ), eksplosiver og legemidler .
 Mest anilin forbrukes i produksjonen av metylendianilin , en forløper for polyuretaner.
Mest anilin forbrukes i produksjonen av metylendianilin , en forløper for polyuretaner.
Spesialiserte applikasjoner
Nitrobenzen blir også brukt for å maskere ubehagelig lukt i skoen og gulvpoleringsmidler, lær dressinger, malingsoppløsningsmidler , og andre materialer. Omdestillert, som olje av mirbane, hadde nitrobenzen blitt brukt som en billig parfyme for såper . Det har blitt erstattet av mindre giftige kjemikalier for dette formålet. Et betydelig handelsmarked for nitrobenzen er dets bruk i produksjonen av smertestillende paracetamol (også kjent som acetaminophen) (Mannsville 1991). Nitrobenzen brukes også i Kerr-celler , siden den har en uvanlig stor Kerr-konstant . Bevis antyder at det brukes i landbruket som plantevekst / blomstrende stimulant.
Organiske reaksjoner
Bortsett fra omdannelsen til anilin, kan nitrobenzen selektivt reduseres til azoksybenzen , azobenzen , nitrosobenzen , hydrazobenzen og fenylhydroksylamin . Det har blitt brukt som en mild oksidant i reaksjoner som Skraup kinolinsyntese .
Sikkerhet
Nitrobenzen er svært giftig ( terskelgrenseverdi 5 mg / m 3 ) og absorberes lett gjennom huden.
Langvarig eksponering kan forårsake alvorlig skade på sentralnervesystemet , svekke synet, forårsake lever- eller nyreskade, anemi og lungeirritasjon. Innånding av damp kan forårsake hodepine, kvalme, tretthet, svimmelhet, cyanose , svakhet i armer og ben, og kan i sjeldne tilfeller være dødelig. Oljen absorberes lett gjennom huden og kan øke hjertefrekvensen, forårsake kramper eller sjelden død. Svelging kan på samme måte forårsake hodepine, svimmelhet, kvalme, oppkast og irritasjon i mage-tarmkanalen, tap av følelse / bruk i lemmer og forårsaker også indre blødninger.
Nitrobenzen er ansett som et sannsynlig humant kreftfremkallende middel av United States Environmental Protection Agency, og er av IARC klassifisert som kreftfremkallende som er gruppe 2B som er "muligens kreftfremkallende for mennesker". Det har vist seg å forårsake lever-, nyre- og skjoldbruskkjertelen og karcinomer hos rotter.
Det er klassifisert som et ekstremt farlig stoff i USA som definert i seksjon 302 i US Emergency Planning and Community Right-to-Know Act (42 USC 11002), og er underlagt strenge rapporteringskrav fra anlegg som produserer, lagrer, eller bruk den i betydelige mengder.
Populær kultur
- Novellen 1927 The Avenging Chance av Anthony Berkeley diskuterer moderne bruk av nitrobenzen. Det er også i sentrum av tomten i Berkeleys The Poisoned Chocolates Case av 1929.
- I Nero Wolfe- detektivromanen The Red Box fra 1937 av Rex Stout , blir en person myrdet ved å ha "olje av mirbane" sølt på seg i bilen sin.