P -type kalsiumkanal - P-type calcium channel
Den P-type kalsiumkanal er en type av spenningsavhengige kalsiumkanal . I likhet med mange andre høyspent-gatede kalsiumkanaler, bestemmer α1-underenheten de fleste av kanalens egenskaper. 'P' betyr cerebellare Purkinje -celler , og refererer til kanalens første oppdagelsessted. Kalsiumkanaler av P-type spiller en lignende rolle som kalsiumkanalen av N-typen i frigjøring av nevrotransmitter ved den presynaptiske terminalen og i nevronell integrasjon i mange nevronale typer.
Historie
Kalsiumkanalforsøkene som førte til oppdagelsen av kalsiumkanaler av P-typen ble opprinnelig fullført av Llinás og Sugimori i 1980. Kalsiumkanaler av P-typen ble navngitt i 1989 fordi de ble oppdaget i purkinje-nevroner hos pattedyr . De var i stand til å bruke et in vitro -preparat for å undersøke ionestrømmene som står for Purkinje -cellers elektrofysiologiske egenskaper . De fant at det er kalsiumavhengige handlingspotensialer som stiger sakte og faller raskt og deretter gjennomgår hyperpolarisering . Handlingspotensialene var spenningsavhengige og etterhyperpolariserende potensialer ble koblet til piggbruddene, som befinner seg innenfor dendritene til Purkinje -cellene. Uten kalsiumfluks i Purkinje -cellene, brenner handlingspotensialer sporadisk med høy frekvens.
Grunnleggende funksjoner og struktur
| kalsiumkanal, spenningsavhengig, P/Q-type, alfa 1A-underenhet | |||||||
|---|---|---|---|---|---|---|---|
| Identifikatorer | |||||||
| Symbol | CACNA1A | ||||||
| Alt. symboler | Cav2.1 , CACNL1A4, SCA6, MHP1, MHP | ||||||
| IUPHAR | 532 | ||||||
| NCBI -gen | 773 | ||||||
| HGNC | 1388 | ||||||
| OMIM | 601011 | ||||||
| RefSeq | NM_000068 | ||||||
| UniProt | O00555 | ||||||
| Andre data | |||||||
| Lokus | Chr. 19 s13 | ||||||
| |||||||
P-type kalsiumkanaler er spenningsavhengige kalsiumkanaler som er klassifisert under høyspenningsaktiverte klasse-kanalen, sammen med L-, N-, Q- og R-type kanaler. Disse kanalene krever en sterk depolarisering for å bli aktivert. De finnes på aksonterminaler, så vel som i somatodendritiske områder av nevroner i sentral- og perifert nervesystem. Kalsiumkanaler av P-type er også kritiske for vesikelfrigivelse , spesielt nevrotransmittere og hormoner ved synaptiske terminaler av eksitatoriske og hemmende synapser.
Spenningsstyrte kalsiumkanaler av P-type består av en hovedporedannende α1-underenhet (som mer spesifikt refereres til som CaV2.1 ), en α2-underenhet og en β-underenhet. Det kan være γ -underenheter i kalsiumkanaler i skjelettmuskulaturen. Α1-underenheten er spesifikt kodet av CACNA1A- genet og består av fire domener, som hver inneholder seks transmembrane (S1-S6) som spenner over α-helixer. S1-S2-sløyfen og S6- regionen antas å være ansvarlig for kanalens inaktivering, S4-regionen fungerer som spenningssensor og S5-S6-sløyfe danner porene. Det er syv underenheter innenfor α1 -underenheten. A-underenheten, kalt α1ACa2+, tilsvarer det som er funksjonelt definert som P-type og Q-type isoformer. P-type og Q-type kalsiumkanaler er nært beslektet ettersom de er produsert fra det samme genet via alternativ spleising. Som en komplikasjon av den alternative spleising kan kanaler av P-type og Q-type ha forskjellige underenhetssammensetninger. Β -underenheten regulerer kinetikken og uttrykket for kanalen, sammen med α2δ -underenheten.
Kanaldistribusjon
De fleste kalsiumkanaler av P-type er lokalisert i nervesystemet og hjertet. Antistoffmerking er den primære metoden som brukes for å identifisere kanalplassering.
Områder med høyt uttrykk i pattedyrsystemer inkluderer:
- Purkinje celledendritter
- Glatt endoplasmatisk retikulum
- Plasmamembranen til den soma (cellelegemet)
- Periglomerulære celler i olfaktoripæren
- Cerebellar cortex
- Nevroner i hjernestammen , entorhinal og pyriform cortices og habenula .
Kanalblokkere
Kalsiumkanalblokkere av P-type virker hindre strømmen av kalsium. Blokkering av kalsiumstrømmer kan føre til at organismen opplever nedsatt funksjon og levedyktighet. Disse effektene kan føre til ulike sykdommer som er beskrevet mer detaljert i delen nedenfor.
Den pore av P-typen av kalsiumkanaler er følsomme for forbindelser som kan deles inn i tre grupper:
- Peptid- ionekanalblokkere
- Lavmolekylære forbindelser
- Terapeutikk
Det er bare to peptid giftstoffer som selektivt å blokkere P-type kanaler: ω- agatoxin IVA og IVB ω-agatoxin. De andre nevnte blokkere, som lav molekylvekt og terapeutiske blokkere, er ikke -selektive. Dette betyr at de kan handle både på P-kanaler og andre kanaler.
Selektivt peptidtoksin ω-agatoksin
De to kjente blokkerne som er spesifikke for P-type kalsiumkanaler, er peptider avledet fra edderkoppgiften til Agelenopsis aperta . Giftstoffene fra dette giftet som viser selektivitet for P-type kanaler er ω-agatoksin IVA og ω-agatoksin IVB. Hver av disse peptidtoksinene er laget av 48 aminosyrer som er bundet av fire disulfidbindinger . Selv om ω-agatoksin IVA og ω-agatoksin IVB har samme affinitet og selektivitet for P-type kanaler, er kinetikken deres forskjellig. Ω-agatoksin IVA påvirker portmekanismen til P-typen kanal. Når det er en sterk depolarisering for å aktivere kanalen, kan ω-agatoksin IVA ikke lenger blokkere kanalen. Derfor har ω-agatoksin IVA en veldig lav affinitet for kanalen når den er åpen. Den binder seg til α 1A -underenheten på utsiden av poren. Ω-agatoksin IVA- reseptoren på P-typen kanal er lokalisert ved S3-S4-linkeren. På den annen side skjer kanalblokkering med ω-agatoksin IVB mye saktere. Likevel, to-agatoksin IVA, kan ω-agatoksin IVB ikke binde seg til kanalen ved sterk depolarisering.
Ikke-selektive peptidtoksiner
- ω-Grammotoxin SIA er et peptidtoksin avledet fra giften til edderkoppen Grammostola spatulata . Det virker til å modifisere P-type kanal gating .
- ω-PnTx3-3, PnTx3-3 og fonetoksin IIA er alle toksiner fra edderkoppen Phonoetrica nigriventer som virker for å blokkere strømmen gjennom P-type kalsiumkanaler.
- DW13.3 er et peptidtoksin fra edderkoppen Filistata hibernalis og består av 74 aminosyrer. Det fungerer også for å blokkere strømmen gjennom P-type kalsiumkanaler.
- w- Conotoxins er avledet fra giften av kjegle snegler . ω-Conotoxin MVIIC virker i de hippocampale CA1 pyramidale nevronene for å blokkere kanalene av P-typen. Innenfor hippocampus CA3 -nevroner blokkerer dette toksinet synaptisk overføring . Effekten er treg.
- Calcicludine er fra gift fra Dendroaspis angusticeps , som er en grønn mamba . Den har muligheten til å spenningsavhengig blokkere kanaler av P-type.
- Kurotoksin er fra gift fra skorpionen Parabuthus . I nevroner i thalamus reduserer kurtoxin kalsiumstrømmer med høy terskel , men i Purkinje -cellene øker det kalsiumstrømmene.
Lavmolekylær kanalblokkere av P-type
Lavmolekylære kanalblokkere har fordeler i forhold til peptidblokkere i utvikling av medikamenter. En fordel med lavmolekylære kanalblokkere er at de kan trenge gjennom vev , noe som er viktig for å krysse blod-hjerne-barrieren . Det er ingen spesifikk kanalblokker med lav molekylvekt for kanaler av P-type. Imidlertid er det en rekke av disse blokkeringsforbindelsene som kan påvirke aktiviteten til kanalene av P-typen. Disse inkluderer:
- Roscovitine er en hemmer av syklinavhengig kinase . Det øker strømmen av kalsium i neostriatale interneuroner ved å bremse deaktiveringen av kanalen. Roscovitin kan også enten fungere som en agonist eller antagonist for P-type kalsiumkanaler i den presynaptiske membranen.
- Isoprenalin er en β-adrenoceptoragonist og forårsaker en økning i P-type kalsiumkanalstrøm. Isoprenalin virker gjennom en cAMP -signalvei .
- Eliprodil og antazolin er NMDA-reseptorantagonister og virker for å blokkere P-type kanaler. Eliprodil kan redusere kanalstrømmer av P-type i Purkinje-nevronene i lillehjernen .
- Dodecylamin kan bare blokkere kanaler av P-type når de er i åpen tilstand.
- Etanol kan blokkere kanaler av P-type når den er i høy nok konsentrasjon. Blokkering av kanalene av P-typen kan være årsaken til ataksi når man drikker alkohol .
Terapeutikk
Det er terapeutiske midler som brukes klinisk som kan påvirke aktiviteten til kalsiumkanaler av P-type. Imidlertid antas det primære målet for disse terapeutikkene ikke å være kanaler av P-type. For eksempel virker kalsiumantagonister , som brukes til å behandle koronar hjertesykdom , hypertensjon og hjertearytmi , ved å hemme kalsiumkanaler av L-type eller T-type . Noen av disse kalsiumantagonistene inkluderer verapamil , diltiazem , amlodipin , benidipin , cilnidipin , nikardipin og barnidipin . Selv om hovedmålet ikke er kanaler av P-type, virker disse kalsiumantagonistene også for å blokkere funksjonen til kanaler av P-type. Videre er flunarizin en annen kalsiumantagonist som brukes til å behandle migrene . Hovedmålene er spenningsgatede kalsiumkanaler og natriumkanaler . Flunarizine hemmer kanalene av P-typen som er plassert i de neokortikale skivene . Det virker for å hemme den innadgående strømmen av kalsium. Migrene som den hjelper til med å forhindre skyldes mutasjoner i "cacna1a" -genet til P-typen kanalunderenhet. Også forbindelser som blokkerer kanaler av P-type er vist å hjelpe mot anfall . Epileptiske anfall er forårsaket av økt nevrotransmisjon , som delvis er et resultat av kanaler av P-type. Forbindelser som levetiracetam , lamotrigin og karbamazepin er kjent for å blokkere kanalene av P-typen, noe som har bidratt til å redusere forekomsten av anfall. Totalt sett er det forskjellige ikke-selektive kalsiumkanalblokkere som hjelper til med å lindre symptomer på hypertensjon , schizofreni , hjertearytmi , epilepsi , smerte , astma , bradykardi , angina pectoris og Alzheimers sykdom . Selv om mange av de terapeutiske forbindelsenes hovedmål ikke er kanaler av P-type, må videre forskning avgjøre om de kliniske effektene av disse forbindelsene også påvirkes av P-type kanalblokkering.
Relaterte sykdommer
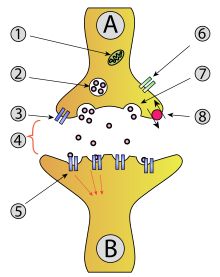
Det er en rekke nevrologiske sykdommer som har blitt tilskrevet feilfunksjonelle eller muterte P/Q -kanaler.
Alzheimers sykdom
Ved Alzheimers sykdom er det en progressiv opphopning av β-amyloidprotein (Aβ) i hjernen. Amyloidplakk utvikler seg som resulterer i de viktigste symptomene på Alzheimers sykdom. Aβ globulomer protein er et kunstig stoff som brukes i forskningseksperimenter som har lignende egenskaper som Aβ oligomer som er tilstede i kroppen. Aβ -oligomer regulerer direkte kalsiumkanaler av P/Q -typen. Α1A -underenheten er ansvarlig for ledningen av kalsiumstrøm. Når bare kalsiumkanaler av P/Q -type er tilstede med Aβ -globulomerprotein, er det en direkte effekt på α1A -underenheten og resulterer i en økt kalsiumstrøm gjennom kalsiumkanalen av P/Q -typen. Responsen er doseavhengig, ettersom konsentrasjoner på 20nM og 200nM Aβ -globulomer er nødvendige for betydelig økning av kalsiumstrøm gjennom kanalen i Xenopus -oocytter, noe som viser at en viss oppbygging av Aβ -globulomer er nødvendig før effektene blir sett. Når kalsiumstrømmen økes, stiger også frigivelsen av nevrotransmitter , noe som gir en mulig årsak til toksisiteten hos pasienter med Alzheimers sykdom.
Migrene hodepine
De CACNA1A genet koder for alfa-underenheten av P / Q-typen kalsiumkanal. Den R192Q mutasjon i genet CACNA1A er en forsterkning av funksjon mutasjon for P2X3-reseptorer. P2X3 -reseptorer er tilstede i trigeminusganglionneuroner og antas å være en hovedbidragsyter til familiær hemiplegisk migrene . Ved å bruke et knockin -eksperiment kan denne mutasjonen uttrykkes i mus slik at forskning kan utføres. Mutantmusen har en betydelig høyere P2X3 -reseptoraktivitet enn villtypemusen på grunn av økt sannsynlighet for kanalåpning og kanalaktivering ved lavere spenninger. Denne økte reseptoraktiviteten resulterer i en høyere strøm av kalsium gjennom P/Q -typen kalsiumkanal. Den økte intracellulære kalsiumkonsentrasjonen kan bidra til akutte trigeminusmerter som vanligvis resulterer i hodepine. Bevis støtter at migrene er en lidelse i hjernens eksitabilitet preget av mangelfull regulering av den kortikale eksitatorisk -hemmende balansen.
Beslag
Levetiracetam er et antiepileptisk legemiddel enn det som kan brukes til å behandle delvise og generaliserte anfall . Levetiracetam hemmer frigjøring av P/Q-kanal-mediert glutamat og reduserer eksitatoriske postsynaptiske strømmer for både AMPA- og NMDA-reseptorer i hippocampus , spesielt dentate gyrus , som er kjent for å spre beslagsaktiviteter. Inhiberingen av glutamatfrigivelse resulterer i en antiepileptisk respons hos pasienter fordi den reduserer den eksitatoriske postsynaptiske strømmen. Det er mange forskjellige typer kalsiumkanaler, så for å bevise at P/Q-typen kalsiumkanaler er direkte involvert, ble en P/Q-type spenningsgated kalsiumkanalhemmer, omega-agatoksin TK , brukt til å blokkere kanalen. Når de ble blokkert, hadde pasientene ikke lenger nytte av de antiepileptiske effektene av legemidlene. Når blokkere for L -type og N -type kalsiumkanaler ble brukt, ble effekten av Levetiracetam fortsatt sett. Dette er et sterkt bevis på at kalsiumkanaler av P/Q -type er involvert i Levetiracetam -behandlingen som muliggjør lindring av anfall.
Mutasjonsstudier
Mange kalsiumkanalmutasjoner av P-typen resulterer i et redusert nivå av intracellulært fritt kalsium. Opprettholde kalsiumhomeostase er avgjørende for normalt fungerende nevroner. Endring av den cellulære kalsiumionkonsentrasjonen fungerer som en utløser for flere sykdommer, i alvorlige tilfeller kan disse sykdommene resultere i masse neuronal død.
Mutasjonsstudier lar eksperimenter studere genetisk arvelige kanalopatier . En kanalopati er enhver sykdom som skyldes en ionekanal med funksjonsfulle underenheter eller regulatoriske proteiner. Ett eksempel på en P-type kalsiumkanalkanopati er vist hos homozygote ataksiske mus, som er recessive for både svingende og slankere gener. Disse musene har mutasjoner i alfa1A -underenheten til kanalene deres av P/Q -type. Mutasjoner i disse kanalene resulterer i mangler i cerebellare Purkinje -celler som dramatisk reduserer kanalens strømtetthet.
De mutrende mutasjonene i mus skyldes en missense-mutasjon og forårsaker forsinket anfall og ataksi. Den vaklende mutasjonen erstatter et enkelt prolin i stedet for et leucin i P-regionen av kanalen. P-regionen er ansvarlig for dannelsen av ionekanalporen . Den slankere mutasjonen, som resulterer i mer alvorlige symptomer enn den mutrende mutasjonen, har vist seg å skyldes en enkelt nukleotidsubstitusjon som forårsaker spleisefeil i de kanalene som er åpne leseramme. Mutasjoner i den poredannende underenheten av kalsiumkanaler av typen P forårsaker ataksi, sterkt endret åndedrett, ved å redusere minuttventilasjon og gi symptomer forbundet med atelektase . Mutasjoner til Ca V 2.1 har også vist seg å påvirke overføringen i pre-Bötzinger-komplekset , en klynge av interneuroner i hjernestammen som bidrar til å regulere pusten.


