pH -indikator - pH indicator
| Syrer og baser |
|---|
 |
| Acid typer |
| Base typer |
En pH -indikator er en halokrom kjemisk forbindelse tilsatt i små mengder til en løsning, slik at løsningens pH ( surhet eller basalitet ) kan bestemmes visuelt. Derfor er en pH -indikator en kjemisk detektor for hydroniumioner (H 3 O + ) eller hydrogenioner (H + ) i Arrhenius -modellen . Normalt får indikatoren fargen på løsningen til å endre seg avhengig av pH. Indikatorer kan også vise endring i andre fysiske egenskaper; for eksempel viser luktindikatorer endring i lukten . PH -verdien til en nøytral løsning er 7,0 ved 25 ° C ( standard laboratorieforhold ). Løsninger med en pH -verdi under 7,0 regnes som sure og løsninger med pH -verdi over 7,0 er basiske (alkaliske). Siden de fleste naturlig forekommende organiske forbindelser er svake protolytter, karboksylsyrer og aminer , finner pH -indikatorer mange anvendelser innen biologi og analytisk kjemi. Videre danner pH -indikatorer en av de tre hovedtypene indikatorforbindelser som brukes i kjemisk analyse. For kvantitativ analyse av metallkationer foretrekkes bruk av kompleksometriske indikatorer , mens den tredje sammensatte klassen, redoksindikatorene , brukes i titreringer som involverer en redoksreaksjon som grunnlag for analysen.
Teori
I seg selv er pH -indikatorer ofte svake syrer eller svake baser. Det generelle reaksjonsskjemaet til en pH -indikator kan formuleres som:
- HInd + H
2O , H
3O+
+ Ind-
Her står HInd for syreformen og Ind - for den konjugerte basen til indikatoren. Forholdet mellom disse bestemmer fargen på løsningen og kobler fargen til pH -verdien. pH -indikatorer som er svake protolytter, Henderson - Hasselbalch -ligningen for dem kan skrives som:
- pH = p K a + log 10
[ Ind-
] / [Bakre]
Ligningen, avledet fra surhet konstant , fastslår at når pH-verdien er lik p K en verdi av indikatoren, begge arter er til stede i et 1: 1 forhold. Hvis pH er over p K a -verdien, er konsentrasjonen av konjugatbasen større enn konsentrasjonen av syren, og fargen assosiert med konjugatbasen dominerer. Hvis pH er under p K a -verdien, er det motsatte sant.
Vanligvis er fargeendringen ikke øyeblikkelig ved p K a -verdien, men det finnes et pH -område der en blanding av farger er tilstede. Dette pH -området varierer mellom indikatorene, men som en tommelfingerregel faller det mellom p K a verdi pluss eller minus en. Dette forutsetter at løsninger beholder fargen så lenge minst 10% av de andre artene vedvarer. For eksempel, hvis konsentrasjonen av konjugatbasen er 10 ganger større enn konsentrasjonen av syren, er forholdet deres 10: 1, og følgelig er pH p K a + 1. Omvendt, hvis et 10 ganger overskudd av syren forekommer med hensyn til basen, er forholdet 1:10 og pH er p K a - 1.
For optimal nøyaktighet bør fargeforskjellen mellom de to artene være så tydelig som mulig, og jo smalere pH -området til fargen endres jo bedre. I noen indikatorer, for eksempel fenolftalein , er en av artene fargeløs, mens i andre indikatorer, for eksempel metylrød , gir begge artene en farge. Selv om pH -indikatorene fungerer effektivt ved sitt angitte pH -område, blir de vanligvis ødelagt i de ekstreme ender av pH -skalaen på grunn av uønskede side -reaksjoner.
applikasjon
pH -indikatorer brukes ofte i titreringer i analytisk kjemi og biologi for å bestemme omfanget av en kjemisk reaksjon . På grunn av det subjektive valget (bestemmelse) av farge, er pH -indikatorer utsatt for upresise avlesninger. For applikasjoner som krever presis måling av pH, brukes ofte en pH -måler . Noen ganger brukes en blanding av forskjellige indikatorer for å oppnå flere jevne fargeendringer over et bredt spekter av pH -verdier. Disse kommersielle indikatorene (f.eks. Universalindikator og Hydrion -papirer ) brukes når bare grov kunnskap om pH er nødvendig.
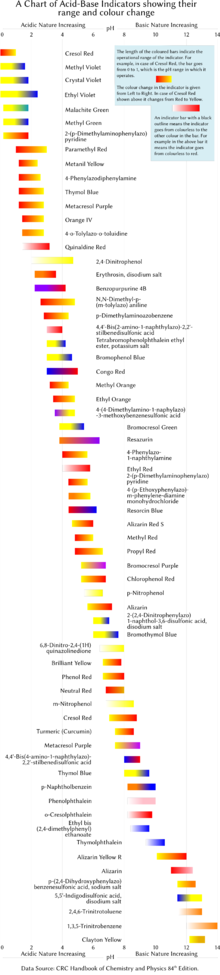
Tabellen nedenfor er flere vanlige pH -indikatorer i laboratoriet. Indikatorer viser vanligvis mellomfarger ved pH -verdier innenfor det angitte overgangsområdet. For eksempel viser fenolrød en oransje farge mellom pH 6,8 og pH 8,4. Overgangsområdet kan skifte litt avhengig av konsentrasjonen av indikatoren i løsningen og temperaturen den brukes til. Figuren til høyre viser indikatorer med driftsområde og fargeendringer.
| Indikator | Lav pH -farge | Overgang lav ende |
Overgang high end |
Høy pH -farge |
|---|---|---|---|---|
| Gentian fiolett ( metyl fiolett 10B ) | gul | 0,0 | 2.0 | blå fiolett |
| Malakittgrønn (første overgang) | gul | 0,0 | 2.0 | grønn |
| Malakittgrønn (andre overgang) | grønn | 11.6 | 14.0 | fargeløs |
| Thymol blå (første overgang) | rød | 1.2 | 2.8 | gul |
| Tymolblå (andre overgang) | gul | 8.0 | 9.6 | blå |
| Metylgult | rød | 2.9 | 4.0 | gul |
| Bromfenolblått | gul | 3.0 | 4.6 | blå |
| Kongo rød | blå fiolett | 3.0 | 5.0 | rød |
| Metylorange | rød | 3.1 | 4.4 | gul |
| Skjermet metylorange (første overgang) | rød | 0,0 | 3.2 | lilla-grå |
| Skjermet metylorange (andre overgang) | lilla-grå | 3.2 | 4.2 | grønn |
| Bromokresol grønn | gul | 3.8 | 5.4 | blå |
| Metylrød | rød | 4.4 | 6.2 | gul |
| Metyl lilla | lilla | 4.8 | 5.4 | grønn |
| Azolitmin (lakmus) | rød | 4.5 | 8.3 | blå |
| Bromokresol lilla | gul | 5.2 | 6.8 | lilla |
| Bromothymol blå (første overgang) | magenta | <0 | 6.0 | gul |
| Bromothymol blå (andre overgang) | gul | 6.0 | 7.6 | blå |
| Fenol rød | gul | 6.4 | 8.0 | rød |
| Nøytral rød | rød | 6.8 | 8.0 | gul |
| Naphtholphthalein | blek rød | 7.3 | 8.7 | grønnblå |
| Cresol rød | gul | 7.2 | 8.8 | rødlig-lilla |
| Cresolphthalein | fargeløs | 8.2 | 9.8 | lilla |
| Fenolftalein (første overgang) | oransje rød | <0 | 8.3 | fargeløs |
| Fenolftalein (andre overgang) | fargeløs | 8.3 | 10,0 | lilla-rosa |
| Fenolftalein (tredje overgang) | lilla-rosa | 12.0 | 13,0 | fargeløs |
| Thymolphthalein (første overgang) | rød | <0 | 9.3 | fargeløs |
| Thymolphthalein (andre overgang) | fargeløs | 9.3 | 10.5 | blå |
| Alizarine Yellow R | gul | 10.2 | 12.0 | rød |
| Indigo karmin | blå | 11.4 | 13,0 | gul |
Universell indikator
| pH -område | Beskrivelse | Farge |
|---|---|---|
| 1-3 | Sterk syre | rød |
| 3-6 | Svak syre | Oransje/gul |
| 7 | Nøytral | Grønn |
| 8 - 11 | Svak base | Blå |
| 11-14 | Sterk base | Fiolett/Indigo |
Presis pH -måling

En indikator kan brukes for å oppnå ganske presise målinger av pH ved å måle absorbans kvantitativt ved to eller flere bølgelengder. Prinsippet kan illustreres ved å ta indikatoren som en enkel syre, HA, som dissosierer til H + og A - .
- HA ⇌ H + + A -
Verdien av syredissosiasjonskonstanten , p K a , må være kjent. De molare Absorbansene , c HA og c A - av de to artene HA og A - ved bølgelengder λ x og λ y må også ha blitt bestemt ved foregående forsøk. Forutsatt at ølens lov blir overholdt, er de målte absorbansene A x og A y ved de to bølgelengdene ganske enkelt summen av absorbansene som skyldes hver art.
Dette er to ligninger i de to konsentrasjonene [HA] og [A - ]. Når den er løst, oppnås pH som
Hvis det måles på mer enn to bølgelengder, kan konsentrasjonene [HA] og [A - ] beregnes med lineære minste kvadrater . Faktisk kan et helt spekter brukes til dette formålet. Prosessen er illustrert for indikatoren bromokresol grønn . Det observerte spekteret (grønt) er summen av spektrene til HA (gull) og til A - (blå), vektet for konsentrasjonen av de to artene.
Når en enkelt indikator brukes, er denne metoden begrenset til målinger i pH -området p K a ± 1, men dette området kan utvides ved å bruke blandinger av to eller flere indikatorer. Fordi indikatorer har intense absorpsjonsspektra, er indikatorkonsentrasjonen relativt lav, og indikatoren i seg selv antas å ha en ubetydelig effekt på pH.
Ekvivalenspunkt
Ved syrebasetitreringer kan en uegnet pH-indikator indusere en fargeendring i den indikatorholdige løsningen før eller etter det faktiske ekvivalenspunktet. Som et resultat kan forskjellige ekvivalenspunkter for en løsning konkluderes basert på pH -indikatoren som brukes. Dette er fordi den minste fargeendringen av den indikatorholdige løsningen antyder at ekvivalenspunktet er nådd. Derfor har den mest egnede pH -indikatoren et effektivt pH -område, der endringen i farge er tydelig, som omfatter pH til ekvivalenspunktet til løsningen som titreres.
Naturlig forekommende pH -indikatorer
Mange planter eller plantedeler inneholder kjemikalier fra den naturlig fargede anthocyaninfamilien . De er røde i sure løsninger og blå i grunnleggende. Antocyaniner kan ekstraheres med vann eller andre løsningsmidler fra et mangfold av fargede planter er plantedeler, inkludert fra blader ( rødkål ); blomster ( geranium , valmue , eller roseblader); bær ( blåbær , solbær ); og stilker ( rabarbra ). Å trekke ut anthocyaniner fra husholdningsplanter, spesielt rødkål , for å danne en rå pH -indikator er en populær innledende kjemidemonstrasjon.
Lakmus , brukt av alkymister i middelalderen og fremdeles lett tilgjengelig, er en naturlig pH -indikator laget av en blanding av lavarter , spesielt Roccella tinctoria . Ordet lakmus er bokstavelig talt fra 'farget mose' på gammelnorsk (se Litr ). Fargen endres mellom rødt i syreoppløsninger og blått i alkalier. Begrepet 'lakmus test' har blitt en mye brukt metafor for enhver test som påstår å skille autoritativt mellom alternativer.
Hortensia macrophylla blomster kan endre farge avhengig av jordens surhet. I sur jord oppstår kjemiske reaksjoner i jorda som gjør aluminium tilgjengelig for disse plantene, og gjør blomstene blå. I alkaliske jordarter kan disse reaksjonene ikke forekomme, og derfor tas ikke aluminium opp av anlegget. Som et resultat forblir blomstene rosa.
En annen nyttig naturlig pH -indikator er krydderiet Gurkemeie . Den er gul når den utsettes for syrer og rødbrun når den er i nærheten av en alkali .
| Indikator | Lav pH -farge | Høy pH -farge |
|---|---|---|
| Hortensia blomster | blå | rosa til lilla |
| Antocyaniner | rød | blå |
| Litmus | rød | blå |
| Gurkemeie | gul | rødbrun |
Lilla blomkål dynket i natron (til venstre) og eddik (til høyre). Anthocyanin fungerer som en pH -indikator.
Se også
Referanser
- Lang indikatorliste
- "Komplett indikatorliste" (PDF) (på fransk). (57,3 KiB )


![{\ displaystyle {\ begin {align} A_ {x} & = [{\ ce {HA}}] \ varepsilon _ {{\ ce {HA}}}^{x}+[{\ ce {A-}} ] \ varepsilon _ {{\ ce {A-}}}^{x} \\ A_ {y} & = [{\ ce {HA}}] \ varepsilon _ {{\ ce {HA}}}^{y }+[{\ ce {A-}}] \ varepsilon _ {{\ ce {A-}}}^{y} \ end {justert}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/407bba3b954782cbec25c32d99393bf282c2c36d)
![{\ displaystyle \ mathrm {pH} = \ mathrm {p} K _ {\ mathrm {a}}+\ log {\ frac {[{\ ce {A-}}]} {[{\ ce {HA}}] }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2ed476e8f78a1980748a81ec195978b60032411f)




