Omvendt zoonose - Reverse zoonosis
Omvendt zoonosis , også kjent som zooanthroponosis, og noen ganger anthroponosis (gresk Zoon "dyr", Anthropos "man", nous " sykdom"), refererer til patogener reservoired i mennesker som er i stand til å bli overført til ikke-menneskelige dyr .
Terminologi
Antroponose refererer til patogener som kommer fra mennesker og kan inkludere overføring fra menneske til ikke-menneske, men også overføring fra menneske til menneske. Begrepet zoonose refererer teknisk til sykdom overført mellom ethvert dyr og et annet dyr, menneske eller ikke-menneske, uten skjønn, og har også blitt definert som sykdom som overføres fra dyr til mennesker og omvendt . På grunn av menneskesentrerte medisinske forstyrrelser har zoonose imidlertid en tendens til å bli brukt på samme måte som antropozoonose, som spesifikt refererer til patogener reservert hos ikke-menneskelige dyr som er overførbare til mennesker.
Ytterligere forvirring på grunn av hyppigheten av forskere som bruker "anthropozoonosis" og "zooanthroponosis" om hverandre ble løst under et komitémøte i Joint Food and Agriculture and World Health Organization i 1967 som anbefalte bruk av "zoonosis" for å beskrive toveis utveksling av smittsomme patogener mellom dyr og mennesker.
Fordi mennesker sjelden er i direkte kontakt med ville dyr og introduserer patogener gjennom "myk kontakt", må begrepet "sapronotiske midler" introduseres. Sapronoser (gresk sapros "henfallende") refererer til menneskelige sykdommer som har evnen til å vokse og replikere (ikke bare overleve eller forurense) i abiotiske miljøer som jord, vann, forfallne planter, dyrekropper, utskillelse og andre underlag. I tillegg kan sapro-zoonoser karakteriseres som å ha både en levende vert og et ikke-dyrt utviklingssted for organisk materiale, jord eller planter. Det må bemerkes at obligatoriske intracellulære parasitter som ikke kan replikere utenfor cellene og er helt reproduktivt avhengige av å komme inn i cellen for å bruke intracellulære ressurser som virus, rickettsiae, chlamydiae og Cryptosporidium parvum, ikke kan være sapronotiske midler.
Etymologiske fallgruver
Kategorisering av sykdom i epidemiologiske klasser etter infeksjonens antatte kilde eller overføringsretning reiser en rekke motsetninger som kan løses ved bruk av sykliske modeller som demonstrert av følgende scenarier:
Zoonose vs omvendt zoonose vs antroponose
I tilfelle av sykdommer som overføres fra leddyr- vektorer så som urban gul feber , denguefeber , epidemisk tyfus , tickborne feber med tilbakefall , Zika feber , og malaria , blir differensiering mellom begrepene stadig mer uklar. For eksempel blir et menneske smittet med malaria bitt av en mygg som også senere blir smittet. Dette er et tilfelle av omvendt zoonose (menneske til dyr). Imidlertid infiserer den nylig infiserte myggen et annet menneske. Dette kan være et tilfelle av zoonose (dyr til menneske) hvis myggen regnes som den opprinnelige kilden, eller antroponose (fra menneske til menneske) hvis mennesket regnes som den opprinnelige kilden. Hvis denne infiserte myggen i stedet infiserte en ikke-menneskelig primat, kan det betraktes som et tilfelle av omvendt zoonose/zooantroponose (fra menneske til dyr) hvis mennesket regnes som den primære kilden, eller ganske enkelt zoonose (dyr til dyr) hvis myggen blir vurdert hovedkilden.
Zoonose vs antroponose
På samme måte kunne HIV med opprinnelse i simianer (crossover på grunn av at mennesker spiste vill sjimpanse bushmeat ) og influensa A -virus med avianer (crossover på grunn av et antigent skifte) i utgangspunktet ha blitt ansett som en zoonotisk overføring ettersom infeksjonene først kom fra virveldyr, men kunne for tiden å bli sett på som en antroponose på grunn av dets potensial til å overføre mellom mennesker til mennesker.
Sapronose vs sapro-zoonose
Typiske eksempler på sapronotiske midler er sopp som coccidioidomycosis , histoplasmose , aspergillose , cryptococcosis , Microsporum gips . Noen kan være bakterielle fra sporulerende clostridium og bacillus til Rhodococcus equi, Burkholderia pseudomallei, Listeria , Erysipelothrix , Yersinia pseudotuberculosis, legionellosis, Pontiac feber og ikke -tuberkuløse mykobakterier. Andre sapronotiske midler er amebiske som ved primær amebisk meningoencephalitt . Nok en gang oppstår klassifiseringsvansker når det gjelder sporulerende bakterier hvis smittsomme sporer bare produseres etter en betydelig periode med inaktiv vegetativ vekst i et abiotisk miljø, men dette anses fortsatt som et tilfelle av sapronoser. Imidlertid kan tilfeller av zoo-sapronoser som involverer Listeria , Erysipelothrix , Yersinia pseudotuberculosis , Burkholderia pseudomallei og Rhodococcus equi overføres av et dyr eller et abiotisk substrat, men skjer vanligvis via fekal-oral rute mellom mennesker og andre dyr.
Etuier med overføringsmåter
Leddyrvektorer
Malaria
Malaria involverer syklisk infeksjon av dyr (mennesker og ikke-mennesker) og mygg fra slekten Anopheles med en rekke Plasmodium- arter. Plasmodium -parasitten overføres til myggen mens den lever av blodet til det infiserte dyret, hvorpå den starter en sporogen syklus i myggens tarm som vil infisere et annet dyr ved neste blodmåltid. Det ser ikke ut til å ha noen skadelige effekter på myggen som følge av parasittinfeksjonen. Den Plasmodium brasilianum parasitt som normalt finnes i primater er morfologisk like malaria induserende Plasmodium malariae som er mer vanlig hos mennesker, og det er omstridt hvorvidt de to er faktisk forskjellige arter. Likevel oppsto 12 rapporter om malaria i de eksternt lokaliserte Yanomami -samfunnene i den venezuelanske Amazonas, der det overraskende ble funnet å være forårsaket av en stamme av P. brasilianum med 100% identiske med sekvenser som ble funnet i Alouatta seniculus aper. Dette antyder en bestemt zoonose og stor mulighet for tilbakeslag i ikke-menneskelige primatbånd som omvendte zoonoser.
Afrikansk sovesyke
Trypanosoma brucei gambiense (T. b. Gambiense) er en art af afrikanske trypanosomer som er protozoan hemoflagellater som eransvarlige for trypanosomiasis (mer kjent som afrikansk sovesyke ) hos mennesker og andre dyr. Protozoa overføres via Tsetse -fluer der de formerer seg og kan overføres til enda en dyrevert under fluens blodmåltidsmating . Utbrudd av sovesyke i visse menneskelige samfunn har blitt eliminert, men bare midlertidig ettersom konstant gjeninnføring fra ukjente kilder statistisk tyder på tilstedeværelsen av et ikke-menneskelig reservoar der tilbakeslag av patogenet opprettholdes i en sylvatisk syklus og gjeninnføres i byene syklus. Tilstedeværelsen av T. b. gambiense er funnet separat hos mennesker og husdyr. Dette ansporet til en molekylær studie som sammenlignet serumreaktivitet hos griser , geiter og kyr med humant serum der det var bemerkelsesverdige likheter i alle prøver, men spesielt i griseprøver. Kombinert impliserer disse funnene en omvendt zoonotisk overføring fra menneske til dyr.
Arbovirus
Gul feber -virus, Dengue -febervirus og Zika -virus er av slekten Flavivirus, og Chikungunya -viruset er av slekten Alphavirus . Alle regnes som arbovirus som angir deres evne til å overføres gjennom leddyrvektorer. Sylvatiske overføringssykluser for arbovirus i ikke-menneskelige primatsamfunn har potensial til å strømme over i en bysyklus hos mennesker der mennesker kan være blindvei i scenarier der ytterligere blanding elimineres, men mye mer sannsynlig er at disse virusene kommer tilbake til begge sykluser på grunn av utslipp. Tilsynelatende krever vedlikehold av en arboviral bysyklus mellom mennesker en sjelden eller undersøkt sammenheng av faktorer. En av følgende situasjoner oppstår:
- Et infisert menneske i urbane omgivelser mater en sylvatisk (vanligvis eksternt plassert) mygg som Haemogogus (som har en relativt lang levetid sammenlignet med andre mygg og kan overføre viruset over lengre perioder) som infiserer et annet menneske eller ikke-menneskelig dyr som vil fungere som et reservoar.
- En urban Aedes (mer vanlig funnet i urbane områder mater og overfører viruset til et annet menneske eller ikke-menneskelig dyr som vil tjene som et reservoar.
- Tilstrekkelig antall sylvatiske vektormygg og dyrereservoaret bor i den samme økologiske nisjen i nær kontakt for å fremme og opprettholde den zoonotiske syklusen til viruset.
- Dyrreservoaret til viruset opprettholder et passende virusnivå i blodet for å tillate infeksjon av en vektormygg.
- En brovektormygg som Aedes albopictus , som kan overleve i et urbant område og spre seg til landlige, semi-landlige og skogsområder, kan føre viruset til et sylvatisk miljø.
- Zikafeber: Zika -viruset er forårsaket av det enkeltstrengede RNA -flaviviruset som bruker Aedes -mygg som en vektor for å infisere andre mennesker og dyr. En zika -virusstamme fra 2015 isolert fra et menneske i Brasil ble brukt til å infisere gravide rhesus -makaker intravenøst og intra fostervann . Både demningene og morkakene ble infisert med Zika -positive vevsprøver som ble registrert i opptil 105 dager. Dette bekrefter et omvendt zoonotisk overføringspotensial mellom mennesker og ikke-menneskelige primater.
- Gul feber: Gul feber -virus overføres også av bitt av en infisert Aedes- eller Haemagogus -myggart som lever av et infisert dyr. Det historiske forløpet for den amerikanske slavehandelen er et godt eksempel på introduksjon av et patogen for å skape en helt ny sylvatisk syklus. Tidligere hypoteser om en " New World YFV" ble lagt til hvile i en studie fra 2007 som undersøkte hastigheter på nukleotidsubstitusjon og divergens for å fastslå at gul feber ble introdusert i Amerika for omtrent 400 år siden fra Vest -Afrika . Det var også rundt 1600 -tallet at gul feber ble dokumentert av europeere som var medskyldige i slavehandel. Den faktiske introduksjonsmåten kunne ha spilt ut i en rekke scenarier om et viremisk menneske fra den gamle verden, infisert mygg fra den gamle verden, egg lagt av en infisert mygg fra den gamle verden, eller alle tre ble transportert til Amerika, da overføring av gul feber ikke var uvanlig på seilskip. Midt i nyere utbrudd av gul feber i det sørøstlige Brasil var potensialet for tilbakeslag sterkt indikert. Molekylære sammenligninger av ikke-humane primatutbruddsstammer viste seg å være nærmere beslektet med menneskelige stammer enn stammer avledet fra andre ikke-menneskelige primater, noe som tyder på en fortsatt omvendt zoonose.
- Chikungunya: Chikungunya -viruset er et enkeltstrenget RNA -alfavirus som vanligvis overføres av Aedes -myggen til en annen dyrevert. Det er ingen bevis som tyder på en barriere for at Chikungunya bytter vertskap mellom mennesker og ikke-menneskelige primater fordi den ikke har noen preferanser hos en gitt primatart. Den har et stort potensial for å spyle over eller spyle tilbake til sylvatiske sykluser, slik tilfellet var med lignende arbovirus som ble importert til Amerika under slavehandelen. Studier har bevist chikungunyas potensial for å oralt infisere sylvatiske myggtyper, inkludert Haemagogus leucocelaenus og Aedes terrens . Videre, i en serologisk undersøkelse utført i ikke-menneskelige primater i urbane og bynære områder i Bahia-staten , viste 11 dyr chikungunya nøytraliserende antistoffer .
- Dengue -feber: Dengue -viruset er et flavivirus som også kan overføres av Aedes -myggvektorer til andre dyreverter. Dengue ble også introdusert for Amerika av slavehandelen sammen med Aedes aegypti. En studie fra 2009 i Fransk Guyana funnet at infeksjoner av dengue virus type 1 til 4 var til stede i ulike typer Neotropical skog pattedyr enn primater som gnagere , pungdyr , og flaggermus . Etter sekvensanalyser ble det avslørt at de 4 ikke-humane pattedyrstammene hadde en 89% til 99% likhetsindeks til menneskelige stammer som sirkulerte samtidig. Dette bekrefter at andre pattedyr i nærheten har potensial til å bli smittet av menneskelige kilder og indikerer tilstedeværelse av en bysyklus. En sak for å bevise at leddyrvektorene er i stand til å bli smittet, kommer fra Brasil hvor Aedes albopictus (som frekventerer bakgårdene til menneskelige hus, men lett sprer seg til landlige, semi-landlige og ville miljøer) ble funnet infisert med dengue-virus 3 i São Paulo Stat. I mellomtiden, i delstaten Bahia, ble den sylvatiske vektoren Haemogogus leucocelaenus funnet å være infisert med denguevirus 1. I en annen studie utført i Atlanterhavskogen i Bahia ble primater ( Leontopithecus chrysomelas og Sapajus xanthosternos ) funnet med antistoff dengue -virus 1 og 2 mens dovendyr ( Bradypus torquatus ) hadde antistoffer mot denguevirus 3, noe som tyder på mulig tilstedeværelse av en etablert sylvatisk syklus.
Villdyr
Et stort antall ville dyr med habitater som ennå ikke må inngripe av mennesker, påvirkes fortsatt av sapronotiske midler gjennom forurenset vann.
Giardia
- Beavers : Giardia ble introdusert for bever gjennom avrenning av menneskelig kloakk oppstrøms en beverkoloni.
Influensa A -virus undertype H1N1
- Sel : I 1999 ble villsel innlagt i et nederlandsk selrehabiliteringssenter med influensalignende symptomer, og det ble funnet at de faktisk var infisert med en menneskelig influensa B- lignende virus som hadde sirkulert hos mennesker i 1995 og hadde gjennomgått et antigent skifte siden tilpasning til den nye selverten.
Tuberkulose
- Kronhjort , villsvin : I områder med intensiv viltforvaltning som inkluderte storviltgjerde, tilleggsfôringssteder og beitende husdyr,dukket det opptilfeller av tuberkuloseskader hos villhjort og villsvin. Noen villsvin og hjort delte de samme tuberkulosestammene som lignet dem som finnes hos husdyr og mennesker, noe som tyder på en mulig sapronotisk eller sapro-zoonotisk forurensning av delte vannkilder, tilleggsfôr, direkte kontakt med mennesker eller husdyr, eller deres utskillelse.
Husdyrfellesskapsdyr
E coli
- Hunder , hester : Bevis for infeksjon av humane E. coli- stammer hos flere hunder og hester over hele Europa ble funnet, noe som impliserte muligheten for zoonotisk inter-spesiell overføring av multiresistente stammer fra mennesker til selskapsdyr og omvendt.
Tuberkulose
- Hund: En Yorkshire terrier ble innlagt på en veterinærklinikk med kronisk hoste, dårlig vektoppbevaring og oppkast rapportert i flere måneder hvor det ble avslørt at eieren hadde kommet seg etter tuberkulose, men hunden testet først negativt for tuberkulose i 2 forskjellige molekylære analyser og ble skrevet ut. 8 dager senere ble hunden avlivet på grunn av en urinrørsobstruksjon . En nekroskopi ble utført der lever- og trakeobronchial lymfeknute -prøver faktisk testet positivt for nøyaktig samme tuberkulosestamme som eieren hadde tidligere. Dette er et veldig klart tilfelle av omvendt zoonose.
Influensa A -virus undertype H1N1
- Ildere : Ildere brukes ofte i kliniske studier hos mennesker , og potensialet for menneskelig influensa for å infisere dem ble tidligere bekreftet. Bekreftelse på naturlig overføring av en menneskelig H1N1 -stamme fra utbruddet i 2009 i husdyr -ilder impliserer imidlertid videre overføring fra menneske til dyr.
covid-19
Midt i den globale pandemien av COVID-19 i 2020 ble mottakelighet for katter, ilder, hunder, kyllinger , griser og ender for SARS-CoV-2- koronaviruset undersøkt, og det ble funnet at det kan replikeres hos katter og ilder med dødelige resultater .
- Katter : Viruset kan overføres i luften mellom katter. Viralt RNA ble påvist i avføring innen 3-5 dager etter infeksjon, og patologiske studier påviste viralt RNA i den myke ganen , mandlene og luftrøret . Kattunger ervervet massive lesjoner i lungene, nasal og tracheal slimhinnen epitheliums . Overvåkning for SARS-CoV-2 hos katter bør betraktes som et supplement til eliminering av COVID-19 hos mennesker.
- Ildere: Ildere ble inokulert med virale stammer fra miljøet på Huanan sjømatmarkedet i Wuhan, Kina, samt menneskelige isolater fra Wuhan. Det ble funnet at med begge isolatene kan viruset replikere i ilder i øvre luftveier i opptil 8 dager uten å forårsake sykdom eller død, og viralt RNA ble påvist i rektale vattpinner. Patologiske studier utført etter 13 dager med infeksjon avslørte mild peribronchitt i lungene, alvorlig lymfoplasmacytisk perivaskulitt og vaskulitt blant andre plager med antistoffproduksjon mot SARS-CoV-2 påvist i alle ilder. Det faktum at SARS-CoV-2 replikerer effektivt i ilderens øvre luftveier, gjør dem til en kandidatmodell for å evaluere antivirale legemidler eller vaksinekandidater mot COVID-19.
- Hunder: Av de testede Beagle- hundene ble viralt RNA påvist i avføring og 50% av Beagles som ble inokulert serokonvertert etter 14 dager, mens de andre 50% forble seronegative som demonstrerte lav følsomhet for SARS-CoV-2 hos hunder.
- Kylling, and, gris: Det var ingen tegn på følsomhet hos kyllinger, ender eller griser med alle virale RNA -vattpinner som ga negative resultater og seronegative etter 14 dager etter vaksinering.
Husdyr husdyr
Influensa A -virus undertype H1N1
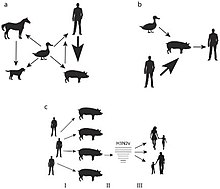
- Kalkuner : En norsk kalkunoppdretters flokk viste en nedgang i eggproduksjon uten andre kliniske tegn etter at en gårdshand rapporterte å ha H1N1 . En studie viste at kalkunene også hadde H1N1 og var seropositive overfor antigenene. Maternelt avledede H1N1 -antistoffer ble påvist i eggeplommer og ytterligere genetiske analyser avslørte en identisk H1N1 -stamme i kalkunene som gårdsarbeideren som sannsynligvis infiserte kalkunene under kunstig befruktning .
- Gris: H1N1 -overføring fra menneske til gris ble rapportert i Canada, Korea, og til slutt kom det til å omfatte alle kontinenter, unntatt Antarktis under utbruddet i 2009. Det har også vært kjent for å spre seg under sesongepidemier i Frankrike mellom mennesker og griser.
Meticillinresistent Staphylococcus aureus
- Hester: 11 pasienter av heste som ble innlagt på et veterinærsykehus av forskjellige årsaker fra forskjellige gårder i løpet av omtrent ett år, viste MRSA -infeksjoner senere. Med tanke på at MRSA -isolater er ekstremt sjeldne hos hester, ble det antydet at MRSA -utbruddet skyldtes nosokomial infeksjon fra et menneske under hestens opphold på sykehuset.
- Kuer, kalkuner, griser: Et tilfelle av omvendt zoonose ble foreslått for å forklare hvordan en bestemt menneskelig Methicillin Sensitive Streptococcus Aureus -stamme ble funnet hos husdyr (griser, kalkuner, kyr) med ikke bare tap av menneskelige virulensgener (som kan redusere zoonotisk potensial for menneskelig kolonisering), men også tilsetning av meticillinresistens og et tetracyklin (som vil øke forekomsten av MRSA -infeksjoner). Bekymringen her er at overdreven bruk av antibiotika i husdyrproduksjoner forverrer etableringen av nye antibiotikaresistente zoonotiske patogener .
Ville dyr i fangenskap
Tuberkulose
- Elefanter : I 1996rapporterteThe Hawthorne Circus Corporation 4 av elefantene og 11 av deres voktere som hadde M. tuberculosis -infeksjoner. Dessverre hadde disse elefantene blitt leid ut til forskjellige sirkushandlinger og zoologiske hager over hele Amerika. Dette ansporet til en landsomfattende epidemi , men fordi tuberkulose ikke er en sykdom som vanligvis overføres fra dyr til mennesker, ble det antydet at epidemien skyldtes overføring fra en menneskelig fører til en fanget elefant.
- Alpakkaer : Et utbrudd av alpakka -koronaviruset i 2007 pågrunn av blandingen som skjedde på en nasjonal alpakkautstilling, førte til en sammenligning mellom menneske- og alpakka -koronavirus i et forsøk på å utlede kilden til utbruddet. Det ble funnet at alpakka -koronaviruset mest evolusjonært ligner en menneskelig koronavirusstamme som ble isolert på 1960 -tallet, noe som tyder på at et alpakka -koronavirus veldig godt kunne ha sirkulert i flere tiår og forårsaket luftveissykdom i besetninger som ikke ble oppdaget på grunn av mangel på diagnostiske evner. Det foreslår også en overføringsform mellom mennesker og alpakka.
Helminter og protozoer
- Primater : Ved Universitetet i Ibadan zoologiske hage i Nigeria , fekale prøver av dyrepassere testet positivt for helminths ( Ancylostoma Duodenale , Ascaris lumbricoides og Trichuris trichiura ) og protozoer ( Giardia lamblia og Entamoeba histolytica ). Den nøyaktig samme stammen av helminter og protozoiske cyster ble funnet i dyrehagen ikke-menneskelige primater, noe som innebar en zoonose mellom de to.
Meslinger
- Ikke-menneskelige primater: I 1996, en meslinger skjedde utbrudd i en helligdom i 94 ikke-menneskelige primater. Selv om kilden til utbruddet aldri ble bestemt, viste serum- og urintesting at viruset definitivt var forbundet med nylige tilfeller av meslinger i USA
Helicobacter pylori
- Pungdyr : The stripe-face dunnart er en australsk pungdyr som har møtt flere utbrudd av Helicobacter pylori i fangenskap. Mageprøvetaking fra pungdyret avslørte at H. pylori -stammen som var ansvarlig for utbruddene, var 100% på linje med en stamme som stammer fra den menneskelige tarmkanalen. Dermed kan det antas at utbruddet var forårsaket av håndtererne.
Ville dyr i bevaringsområder
- Sjimpanser : Overføring av det menneskelige koronaviruset HCoV-OC43 til ville sjimpanser ( Pan troglodytes verus ) som bor i Taï nasjonalpark , Côte d'Ivoire ble rapportert i 2016 til 2017. Disse sjimpansene var vant til menneskelig tilstedeværelse som hadde studert disse spesielle lokalsamfunn siden 1980-tallet HCoV-OC43, som tilhører arten Betacoronavirus 1 (BetaCoV1), forårsaker vanligvis episoder med forkjølelse hos mennesker (dette utelukker SARS og MERS ), men har også blitt påvist hos hovdyr , rovdyr og lagomorfer . Derfor er det helt sannsynlig at forskere eller krypskyttere utilsiktet kunne ha spredt viruset til sjimpansene og dermed avslørt enda et grensesnitt for bytte av koronavirusvert.
Rhinovirus C
- Sjimpanser: Selv om det tidligere ble ansett som et unikt menneskelig patogen, var humant Rhinovirus C fast bestemt på å være årsaken til et utbrudd av luftveisinfeksjoner i 2013 i sjimpanser i Uganda . Undersøkelse av sjimpanser fra hele Afrika fant at de viser en universell homozygositet for 3 CDHR3-Y529- allelen ( cadherinrelatert familiemedlem) som er en reseptor som drastisk øker mottakeligheten for rhinovirus C-infeksjon og astma hos mennesker. Hvis respiratoriske virus av menneskelig opprinnelse er i stand til å opprettholde sirkulasjon i ikke-menneskelige primater, kan dette vise seg å være skadelig hvis infeksjonen smitter inn i menneskelige samfunn.
Tuberkulose
- Elefanter: En nekroskopi av en frittgående afrikansk elefant ( Loxodonta africana ) i Kruger nasjonalpark i Sør-Afrika fant betydelig lungeskade på grunn av en menneskelig stamme av M. tuberculosis. Elefanter utforsker miljøet med koffertene sine, derfor var det svært sannsynlig at aerosoliserte patogener fra husholdningsavfall, forurenset vann fra et menneskelig samfunn oppstrøms, menneskelig ekskrementer eller forurenset mat fra turister var kilden til infeksjonen.
Pneumovirus
- Sjimpanser: I Uganda infiserte rapporter om respiratoriske virus av menneskelig opprinnelse to sjimpanser (Pan troglodytes schweinfurthii) i samme skog. Det ble senere oppdaget å være forårsaket av et humant metapneumovirus (også kjent som MPV, Pneumoviridae , Metapneumovirus ) og et humant respirovirus 3 (også kjent som HRV3, Paramyxoviridae , Respirovirus , eller tidligere kjent som parainfluensavirus 3 ).
Omvendt zoonose hos gorillaer
- Gorillaer : Konserveringsområder som er utsatt for økoturisme i Uganda, Rwanda og Den demokratiske republikken Kongo , har frittgående gorillaer blitt stadig mer vant til menneskers tilstedeværelse, enten det er i form av rangerguider, turister, sporere, veterinærer, krypskyttere eller forskere. Iodamoeba buetschlii , Giardia lamblia , Chilomastix sp. , Endolimax nana , Entamoeba coli og Entamoeba histolytica har blitt funnet i avføringen til gorillaer og promiskuøse avføring etterlatt av mennesker som går inn i habitatet. I tillegg økte antallet Cryptosporidium sp. og kapillariainfeksjoner ble funnet i gorillaer som opprettholdt hyppigere kontakt med mennesker enn de som ikke gjorde det. Sammen antyder disse funnene forekomsten av omvendte zoonoser.