Sensorineural hørselstap - Sensorineural hearing loss
| Sensorineural hørselstap | |
|---|---|
 | |
| Tverrsnitt av sneglehuset. | |
| Spesialitet | Otorinolaryngology |
Sensorineural hørselstap ( SNHL ) er en type hørselstap der grunnårsaken ligger i det indre øret eller sanseorganet ( cochlea og tilhørende strukturer) eller vestibulokokleær nerve ( kranialnerv VIII). SNHL står for rundt 90% av rapportert hørselstap. SNHL er vanligvis permanent og kan være mild, moderat, alvorlig, dyp eller total. Ulike andre deskriptorer kan brukes avhengig av formen på audiogrammet , for eksempel høyfrekvent, lavfrekvent, U-formet, hakket, toppet eller flat.
Sensorisk hørselstap oppstår ofte som en konsekvens av skadede eller mangelfulle cochlea hårceller . Hårceller kan være unormale ved fødselen eller skadet i løpet av et individ. Det er både ytre årsaker til skade, inkludert infeksjon , og ototoksiske legemidler, så vel som iboende årsaker, inkludert genetiske mutasjoner . En vanlig årsak eller en forverrende faktor i SNHL er langvarig eksponering for miljøstøy eller støyindusert hørselstap . Eksponering for en enkelt veldig høy lyd, for eksempel et pistolskudd eller bombeeksplosjon, kan føre til støyindusert hørselstap. Å bruke hodetelefoner med høyt volum over tid, eller å være i høye omgivelser regelmessig, for eksempel på en høy arbeidsplass, sportsbegivenheter, konserter og bruk av støyende maskiner, kan også være en risiko for støyindusert hørselstap.
Nevralt , eller "retrokochlear", hørselstap oppstår på grunn av skade på cochlear nerve (CVIII). Denne skaden kan påvirke initieringen av nerveimpulsen i cochleausnerven eller overføringen av nerveimpulsen langs nerven inn i hjernestammen .
De fleste tilfeller av SNHL har en gradvis forverring av hørselsterskler som oppstår over år til tiår. I noen kan tapet til slutt påvirke store deler av frekvensområdet . Det kan være ledsaget av andre symptomer som øresus ( tinnitus ) og svimmelhet eller svimmelhet ( svimmelhet ). Den vanligste typen sensorineural hørselstap er aldersrelatert ( presbycusis ), etterfulgt av støyindusert hørselstap (NIHL).
Hyppige symptomer på SNHL er tap av skarphet ved å skille forgrunnsstemmer mot støyende bakgrunner, vanskeligheter med å forstå på telefonen, noen typer lyder som virker overdrevent høye eller skingrende, vanskeligheter med å forstå noen deler av talen ( frikativer og sibilanter ), tap av lydretning ( spesielt med høyfrekvente lyder), oppfatning om at folk mumler når de snakker, og vanskeligheter med å forstå tale. Lignende symptomer er også forbundet med andre typer hørselstap; audiometri eller andre diagnostiske tester er nødvendige for å skille mellom sensorineuralt hørselstap.
Identifikasjon av sensorineural hørselstap gjøres vanligvis ved å utføre en ren toneaudiometri (et audiogram) der beinledningsgrenser blir målt. Tympanometri og tale-audiometri kan være nyttig. Testing utføres av en audiolog .
Det er ingen påvist eller anbefalt behandling eller kur mot SNHL; behandling av hørselstap er vanligvis ved hjelp av hørselsstrategier og høreapparater. I tilfeller av dyp eller total døvhet er et cochleaimplantat et spesialisert høreapparat som kan gjenopprette et funksjonelt hørselsnivå. SNHL kan i det minste delvis forebygges ved å unngå miljøstøy, ototoksiske kjemikalier og medisiner, og hodetraumer, og behandle eller inokulere mot visse utløsende sykdommer og tilstander som hjernehinnebetennelse .
Tegn og symptomer
Siden det indre øret ikke er direkte tilgjengelig for instrumenter, identifiseres det ved pasientrapportering av symptomene og audiometrisk testing. Av de som presenterer for legen sin med sensorineural hørselstap, rapporterer 90% at de har redusert hørselen, 57% rapporterer at de har en propp i øret, og 49% rapporterer at de har ringet i øret ( tinnitus ). Omtrent halvparten rapporterer vestibulære (vertigo) problemer.
For en detaljert redegjørelse for symptomer som er nyttige for screening, ble det laget et egenvurderingsspørreskjema av American Academy of Otolaryngology , kalt Hearing Handicap Inventory for Adults (HHIA). Det er en undersøkelse av 25 spørsmål om subjektive symptomer.
Årsaker
Sensorineural hørselstap kan være genetisk eller ervervet (dvs. som en konsekvens av sykdom, støy, traumer, etc.). Folk kan ha hørselstap fra fødselen ( medfødt ), ellers kan hørselstapet komme senere. Mange saker er relatert til alderdom (aldersrelatert).
Genetisk
Hørselstap kan arves. Mer enn 40 gener har vært involvert i årsaken til døvhet. Det er 300 syndromer med tilhørende hørselstap, og hvert syndrom kan ha årsaksgener.
Recessive , dominerende , X-koblede eller mitokondrie genetiske mutasjoner kan påvirke strukturen eller metabolismen i det indre øret. Noen kan være enkeltpunktsmutasjoner , mens andre skyldes kromosomavvik . Noen genetiske årsaker gir hørselstap sent. Mitokondrielle mutasjoner kan forårsake SNHL iem1555A> G, noe som gjør individet følsomt for de ototoksiske effektene av aminoglykosidantibiotika .
- Den vanligste årsaken til resessiv genetisk medfødt hørselshemming i utviklede land er DFNB1 , også kjent som Connexin 26 døvhet eller GJB2- relatert døvhet.
- De vanligste syndromiske formene for nedsatt hørsel inkluderer (dominerende) Sticklers syndrom og Waardenburg syndrom , og (recessivt) Pendred syndrom og Usher syndrom .
- Mitokondrie-mutasjoner som forårsaker døvhet er sjeldne: MT-TL1- mutasjoner forårsaker MIDD (maternell arvelig døvhet og diabetes) og andre tilstander som kan inkludere døvhet som en del av bildet.
- TMPRSS3- genet ble identifisert av dets tilknytning til både medfødt og autosomal recessiv døvhet hos barn. Dette genet uttrykkes i føtale snegle og mange andre vev, og antas å være involvert i utvikling og vedlikehold av det indre øret eller innholdet av perilymfen og endolymfen . Det ble også identifisert som et tumorassosiert gen som er overuttrykt i eggstokktumorer .
- Charcot – Marie – Tannsykdom en arvelig nevrologisk lidelse med forsinket debut som kan påvirke ørene så vel som andre organer. Hørselstapet i denne tilstanden er ofte ANSD (auditory neuropathy spectrum disorder) en nevral årsak til hørselstap.
- Muckle – Wells syndrom , en sjelden arvelig autoinflammatorisk lidelse, kan føre til hørselstap.
- Autoimmun sykdom : selv om det sannsynligvis er sjeldent, er det mulig for autoimmune prosesser å målrette mot sneglehinnen spesielt, uten symptomer som påvirker andre organer. Granulomatose med polyangiitt , en autoimmun tilstand, kan utløse hørselstap.
Medfødt
- Infeksjoner:
- Medfødt rubellasyndrom , CRS, skyldes transplacental overføring av rubellavirus under graviditet. CRS har blitt kontrollert av universell vaksinasjon ( MMR eller MMRV-vaksine ).
- Cytomegalovirus (CMV) -infeksjon er den vanligste årsaken til progressivt sensorineural hørselstap hos barn. Det er en vanlig virusinfeksjon som er kontrahert ved kontakt med infiserte kroppsvæsker som spytt eller urin og lett overføres i barnehager og dermed fra småbarn til forventede mødre. CMV-infeksjon under graviditet kan påvirke fosteret som utvikler seg og føre til læringsvansker samt hørselstap.
- Toksoplasmose , en parasittisk sykdom som rammer 23% av befolkningen i USA, kan forårsake sensorineural døvhet til fosteret i livmoren.
- Hypoplastiske hørselsnerver eller abnormiteter i sneglehuset. Unormal utvikling av det indre øret kan forekomme i noen genetiske syndromer som LAMM syndrom (labyrintisk aplasi, mikrotia og mikrodonti), Pendred syndrom , branchio-oto- nyresyndrom , CHARGE syndrom
- GATA2-mangel , en gruppering av flere lidelser forårsaket av vanlig defekt, nemlig familiær eller sporadisk inaktiverende mutasjon i en av de to foreldrenes GATA2- gener . Disse autosomale dominerende mutasjonene forårsaker en reduksjon, dvs. en haploinsuffisiens , i mobilnivåene til genets produkt, GATA2 . GATA2- proteinet er en transkripsjonsfaktor som er avgjørende for den embryonale utviklingen , vedlikehold og funksjonalitet av bloddannende , lymfatisk dannende og andre vevdannende stamceller . Som en konsekvens av disse mutasjonene er cellulære nivåer av GATA2 mangelfulle, og individer utvikler seg over tid hematologiske, immunologiske, lymfatiske og / eller andre lidelser. GATA2-mangelinduserte abnormiteter i lymfesystemet foreslås å være ansvarlig for en svikt i å generere det perilymfatiske rommet rundt det indre øreens halvsirkulære kanaler , som igjen ligger til grunn for utviklingen av sensorineural hørselstap.
Presbycusis
Progressivt aldersrelatert hørselstap eller sensitivitet kan starte så tidlig som 18 år, og påvirker først de høye frekvensene, og menn mer enn kvinner. Slike tap blir kanskje ikke synlige før langt senere i livet. Presbycusis er den klart dominerende årsaken til sensorineural hørselstap i industrialiserte samfunn. En studie utført i Sudan, med en befolkning uten høy støyeksponering, fant betydelig færre tilfeller av hørselstap sammenlignet med aldersmatchede tilfeller fra et industriland. Lignende funn ble rapportert av en studie utført av en befolkning fra påskeøya, som rapporterte dårligere hørsel blant de som tilbrakte tid i industriland sammenlignet med de som aldri forlot øya. Forskere har hevdet at andre faktorer enn forskjeller i støyeksponering, som genetisk sminke, også kan ha bidratt til funnene. Hørselstap som forverres med alderen, men er forårsaket av andre faktorer enn normal aldring, for eksempel støyindusert hørselstap, er ikke presbycusis, selv om det kan være vanskelig å differensiere de individuelle effektene av flere årsaker til hørselstap. En av tre personer har betydelig hørselstap ved fylte 65 år; 75 år gammel, en av to. Aldersrelatert hørselstap er verken forebyggbart eller reversibelt.
Bråk
De fleste som lever i det moderne samfunnet lider av en viss grad av progressivt sensorineural (dvs. permanent) støyindusert hørselstap (NIHL) som følge av overbelastning og skade det sensoriske eller nevrale apparatet til hørsel i det indre øret. NIHL er vanligvis et frafall eller hakk sentrert ved 4000 Hz. Både intensitet (SPL) og varighet av eksponering, og repeterende eksponering for usikre nivåer av støy bidrar til cochlear skade som resulterer i hørselstap. Jo høyere støyen er, desto kortere er den sikre mengden eksponering. NIHL kan være enten permanent eller midlertidig, kalt en terskelforskyvning. Usikre støynivåer kan være så lite som 70 dB (omtrent dobbelt så høyt som vanlig samtale) hvis det er langvarig (24-timers) eller kontinuerlig eksponering. 125 dB (en høy rockekonsert er ~ 120 dB) er smertenivået; lyder over dette nivået forårsaker øyeblikkelig og permanent øreskade.
Støy og aldring er de viktigste årsakene til presbycusis , eller aldersrelatert hørselstap, den vanligste typen hørselstap i industrisamfunnet. Farene ved miljø- og yrkesstøyeksponering er allment anerkjent. Mange nasjonale og internasjonale organisasjoner har etablert standarder for sikre nivåer av eksponering for støy i industri, miljø, militær, transport, jordbruk, gruvedrift og andre områder. Lydintensitet eller lydtrykknivå (SPL) måles i desibel (dB). For referanse:
| db nivå | Eksempel |
|---|---|
| 45 dB | Omgivende støynivå rundt hjemmet |
| 60 dB | Stille kontor |
| 60–65 dB | Normal samtale |
| 70 dB | Bygatestøy på 25 'eller gjennomsnittlig TV-lyd |
| 80 dB | Støyende kontor |
| 95–104 dB | Nattklubb dansegulv |
| 120 dB | Torden i nærheten eller en høy rockekonsert |
| 150–160 dB | Skudd fra en håndholdt pistol |
En økning på 6 dB representerer en dobling av SPL, eller energien til lydbølgen, og derfor dens tilbøyelighet til å forårsake øreskader. Fordi menneskelige ører hører logaritmisk, ikke lineært, tar det en økning på 10 dB for å produsere en lyd som oppfattes å være dobbelt så høy. Ørebeskadigelse på grunn av støy er proporsjonal med lydintensitet, ikke opplevd lydstyrke, så det er misvisende å stole på subjektiv oppfatning av lydstyrke som en indikasjon på risikoen for hørsel, det vil si at det kan undervurdere faren betydelig.
Selv om standardene varierer moderat i intensitetsnivå og eksponeringsvarighet som ansett som trygge, kan noen retningslinjer utledes.
Den sikre mengden eksponering reduseres med en faktor på 2 for hver økning i SPL (3 dB for NIOSH-standard eller 5 dB for OSHA- standard). For eksempel er den sikre daglige eksponeringsmengden ved 85 dB (90 dB for OSHA) 8 timer, mens den sikre eksponeringen ved 94 dB (A) (nattklubbnivå) bare er 1 time. Støytraumer kan også forårsake et reversibelt hørselstap, kalt en midlertidig terskelforskyvning. Dette skjer vanligvis hos personer som blir utsatt for skuddveier eller fyrverkerier, og som hører ringe i ørene etter hendelsen ( tinnitus ).
- Omgivende miljøstøy : Befolkning som bor i nærheten av flyplasser, lokaltog og jernbanestasjoner, motorveier og industriområder er utsatt for støynivåer, vanligvis i området 65 til 75 dBA. Hvis livsstil inkluderer betydelige forhold utendørs eller åpent vindu, kan disse eksponeringene over tid forringe hørselen. US Dept. of Housing and Urban Development setter standarder for støypåvirkning i bolig- og kommersielle byggesoner. HUDs støystandarder finnes i 24 CFR Part 51, Subpart B. Miljøstøy over 65 dB definerer et støypåvirket område.
- Personlig lydelektronikk : Personlig lydutstyr som iPod (iPod når ofte 115 desibel eller høyere), kan produsere kraftig nok lyd til å forårsake betydelig NIHL.
- Akustisk traume: Eksponering for en enkelt hendelse med ekstremt høy lyd (for eksempel eksplosjoner) kan også forårsake midlertidig eller permanent hørselstap. En typisk kilde til akustisk traume er en for høy musikkonsert.
- Arbeidsplasserstøy: OSHA-standardene 1910.95 Generell industri yrkesstøyeksponering og 1926.52 Byggebransjen yrkesstøyeksponering identifiserer nivået på 90 dB (A) for 8 timers eksponering som det nivået som er nødvendig for å beskytte arbeidstakere mot hørselstap.
Sykdom eller lidelse
-
Inflammatorisk
- Suppurativ labyrintitt eller otitis interna (betennelse i det indre øret)
- Sukkersyke En nylig studie fant at hørselstap er dobbelt så vanlig hos personer med diabetes som det er hos de som ikke har sykdommen. Også av de 86 millioner voksne i USA som har prediabetes er frekvensen av hørselstap 30 prosent høyere enn hos de med normal blodsukker. Det er ikke fastslått hvordan diabetes er relatert til hørselstap. Det er mulig at de høye blodsukkernivåene forbundet med diabetes forårsaker skade på de små blodkarene i det indre øret, på samme måte som diabetes kan skade øynene og nyrene. Lignende studier har vist en mulig sammenheng mellom hørselstap og nevropati (nerveskade).
-
Svulst
- Cerebellopontine vinkel svulst (kryss av pons og cerebellum ) - Cerebellopontine vinkel er utgangsstedet for både ansiktsnerven (CN7) og den vestibulokokleære nerven (CN8). Pasienter med disse svulstene har ofte tegn og symptomer som tilsvarer kompresjon av begge nervene.
- Akustisk nevrom (vestibulært schwannom) - godartet svulst fra Schwann-celler som påvirker vestibulokokleær nerve
- Meningioma - godartet svulst i pia og arachnoid mater
- Cerebellopontine vinkel svulst (kryss av pons og cerebellum ) - Cerebellopontine vinkel er utgangsstedet for både ansiktsnerven (CN7) og den vestibulokokleære nerven (CN8). Pasienter med disse svulstene har ofte tegn og symptomer som tilsvarer kompresjon av begge nervene.
- Ménières sykdom - forårsaker sensorineural hørselstap i det lave frekvensområdet (125 Hz til 1000 Hz). Ménières sykdom er preget av plutselige svimmelhetsangrep, som varer minutter til timer før tinnitus , lydfullhet og svingende hørselstap. Det er relativt sjeldent og ofte overdiagnostisert.
- Bakteriell meningitt, f.eks. Pneumokokk, meningokokk, haemophilus influenzae, kan skade sneglehinnen - Hørselstap er en av de vanligste ettervirkningene av bakteriell hjernehinnebetennelse. Det er anslått at 30% av bakterielle hjernehinnebetennelsestilfeller resulterer i mild til dypt hørselstap. Barn er mest utsatt: sytti prosent av all bakteriell hjernehinnebetennelse forekommer hos små barn under fem år.
- Viral
- AIDS- og ARC- pasienter opplever ofte hørselsanomalier.
- Kusma (epidemisk parotitt) kan resultere i dypt sensorineural hørselstap (90 dB eller mer), ensidig (det ene øret) eller bilateralt (begge ørene).
- Meslinger kan resultere i hørselsnerveskade, men gir oftere et blandet (sensorineural pluss ledende) hørselstap, og kan være bilateralt.
- Ramsay Hunt syndrom type II (herpes zoster oticus)
- Bakteriell
- Syfilis overføres ofte fra gravide til fostrene, og om lag en tredjedel av de smittede barna vil til slutt bli døve.
Ototoksiske og nevrotoksiske legemidler og kjemikalier
Noen reseptfrie legemidler og reseptbelagte medisiner og visse industrielle kjemikalier er ototoksiske. Eksponering for disse kan føre til midlertidig eller permanent hørselstap.
Noen medisiner forårsaker irreversibel skade på øret, og er begrenset i bruken av denne grunn. Den viktigste gruppen er aminoglykosidene (hovedmedlem gentamicin ). En sjelden mitokondriell mutasjon, m.1555A> G, kan øke individets følsomhet for den ototoksiske effekten av aminoglykosider. Langvarig misbruk av hydrokodon (Vicodin) er kjent for å forårsake raskt sensorineuralt hørselstap, vanligvis uten vestibulære symptomer. Metotreksat , et cellegiftmiddel, er også kjent for å forårsake hørselstap. I de fleste tilfeller gjenoppretter ikke hørselstap når stoffet stoppes. Paradoksalt nok brukes metotreksat også til behandling av autoimmunindusert inflammatorisk hørselstap.
Ulike andre medisiner kan reversere hørselen. Dette inkluderer loop- diuretika , sildenafil (Viagra), høy eller vedvarende dosering av NSAIDs ( aspirin , ibuprofen , naproxen og forskjellige reseptbelagte legemidler: celecoxib , etc.), kinin og makrolidantibiotika ( erytromycin , etc.). Cytotoksiske midler slik som karboplatin, brukt til å behandle maligniteter, kan gi opphav til en doseavhengig SNHL, og det samme kan medikamenter som desferrioxamin, brukt til hematologiske lidelser som talassemi; pasienter som foreskriver disse legemidlene, må overvåkes av hørselen.
Langvarig eller gjentatt miljø- eller arbeidsrelatert eksponering for ototoksiske kjemikalier kan også føre til sensorineural hørselstap. Noen av disse kjemikaliene er:
- butylnitritt - kjemikalie brukt rekreasjonsmessig kjent som ' poppers '
- karbondisulfid - et løsningsmiddel som brukes som byggestein i mange organiske reaksjoner
- styren , en industriell kjemisk forløper for polystyren , en plast
- karbonmonoksid , en giftig gass som skyldes ufullstendig forbrenning
- tungmetaller: tinn , bly , mangan , kvikksølv
- heksan , et industrielt løsningsmiddel og en av de viktigste bestanddelene i bensin
- etylbenzen , et industrielt løsningsmiddel som brukes i produksjonen av styren
- toluen og xylen , svært giftige petrokjemiske løsningsmidler. Toluen er en komponent i bensin med høy oktan; xylen brukes til produksjon av polyesterfibre og harpikser.
- trikloretylen , et industrielt avfettingsmiddel
- Organofosfat plantevernmidler
Hodeskade
Det kan være skader på selve øret eller på de sentrale hørselsveiene som behandler informasjonen som ørene overfører. Mennesker som får hodeskade er utsatt for hørselstap eller tinnitus, enten midlertidig eller permanent. Kontaktidretter som fotball (US NFL), hockey og cricket har en betydelig forekomst av hodeskader (hjernerystelse). I en undersøkelse av pensjonerte NFL-spillere, som alle rapporterte om en eller flere hjernerystelser i løpet av spillkarrieren, hadde 25% hørselstap og 50% hadde tinnitus.
Perinatale forhold
Disse er mye mer vanlige hos premature babyer, spesielt de under 1500 g ved fødselen. For tidlig fødsel kan være assosiert med problemer som resulterer i sensorineural hørselstap som anoksi eller hypoksi (dårlig oksygennivå), gulsott, intrakraniell blødning, hjernehinnebetennelse. Fosteralkoholsyndrom er rapportert å forårsake hørselstap hos opptil 64% av spedbarn som er født til alkoholholdige mødre, fra den ototoksiske effekten på fosteret som utvikler seg, pluss underernæring under graviditet fra det overskytende alkoholinntaket .
Jodmangel / hypotyreose
Jodmangel og endemisk hypotyreose er assosiert med hørselstap. Hvis en gravid mor ikke har tilstrekkelig med jodinntak under graviditeten, påvirker det utviklingen av det indre øret i fosteret, noe som fører til sensorineural døvhet. Dette skjer i visse områder av verden, for eksempel Himalaya, hvor jod er mangelfull i jorden og dermed dietten. I disse områdene er det en høy forekomst av endemisk struma. Denne årsaken til døvhet forhindres ved å tilsette jod til salt.
Hjerneslag
Hjerneslag i en region som påvirker auditiv funksjon, for eksempel et bakre sirkulasjonsinfarkt, har vært assosiert med døvhet.
Patofysiologi
Sensorisk hørselstap er forårsaket av unormal struktur eller funksjon av hårcellene i organet til Corti i sneglehuset . Nevrale hørselshemminger er konsekvenser av skade på den åttende hjernenerven (den vestibulokokleære nerven ) eller hjernestammen . Hvis høyere nivåer av øregangen påvirkes, er dette kjent som sentral døvhet . Sentral døvhet kan presentere seg som sensorineural døvhet, men skal kunne skilles fra historie og audiologisk testing.
Cochlear døde regioner i sensorisk hørselstap
Hørselshemming kan være assosiert med skade på hårcellene i sneglehuset. Noen ganger kan det være fullstendig tap av funksjon av indre hårceller (IHC) over et bestemt område av sneglehinnen; dette kalles en "død region". Regionen kan defineres i form av rekkevidden av karakteristiske frekvenser (CFs) til IHCs og / eller nevroner umiddelbart ved siden av den døde regionen.
Cochlea hårceller
Ytre hårceller (OHC) bidrar til strukturen til Corti-organet , som ligger mellom basilærmembranen og tektormembranen i sneglehuset (se figur 3). Tunnelen til korti, som går gjennom Corti-organet, deler OHC-ene og de indre hårcellene (IHC-er). OHC er koblet til retikulær laminær og deiters celler. Det er omtrent tolv tusen OHC i hvert menneskelig øre, og disse er ordnet i opptil fem rader. Hver OHC har små "hår" eller flimmerhår, på sin øvre overflate kjent som stereocilia , og disse er også ordnet i rader som er gradert i høyden. Det er omtrent 140 stereocilia på hver OHC.
Den grunnleggende rollen til OHC og IHC er å fungere som sensoriske reseptorer . Hovedfunksjonen til IHCene er å overføre lydinformasjon via afferente nevroner . De gjør dette ved å overføre mekaniske bevegelser eller signaler til nevral aktivitet. Når stimulert, beveger stereocilia på IHCs seg, forårsaker en strøm av elektrisk strøm til å passere gjennom hårcellene. Denne elektriske strømmen skaper handlingspotensialer i de tilkoblede afferente nevronene.
OHC er forskjellige ved at de faktisk bidrar til den aktive mekanismen til sneglehuset. De gjør dette ved å motta mekaniske signaler eller vibrasjoner langs basilærmembranen, og overføre dem til elektrokjemiske signaler. Stereocilia funnet på OHC er i kontakt med tektormembranen. Derfor, når basilærmembranen beveger seg på grunn av vibrasjoner, bøyer stereocilia seg. Retningen de bøyer i, dikterer skytefrekvensen til hørselsneuronene som er koblet til OHC-ene.
Den bøyning av stereocilia mot basal legeme av OHC bevirker magnetisering av hår cellen. Dermed oppstår en økning i avfyringshastigheten til hørselsneuronene som er koblet til hårcellen. På den annen side forårsaker bøyningen av stereocilia vekk fra basallegemet til OHC hemming av hårcellen. Dermed oppstår en reduksjon i avfyringshastigheten til hørselsneuronene som er koblet til hårcellen. OHC er unike fordi de er i stand til å trekke seg sammen og utvide seg (elektromotilitet). Derfor, som svar på de elektriske stimuleringene som tilbys av den kraftige nervetilførselen, kan de endre seg i lengde, form og stivhet. Disse endringene påvirker responsen fra basilar membranen til lyd. Det er derfor tydelig at OHC-ene spiller en viktig rolle i de aktive prosessene i sneglehuset. Hovedfunksjonen til den aktive mekanismen er å finjustere basilar membranen, og gi den en høy følsomhet for stille lyder. Den aktive mekanismen er avhengig av at snegleorganet er i god fysiologisk tilstand. Imidlertid er cochlea veldig utsatt for skade.
Skader på hårceller
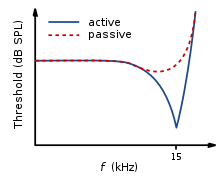
SNHL er oftest forårsaket av skade på OHC og IHC. Det er to metoder som de kan bli skadet på. For det første kan hele hårcellen dø. For det andre kan stereocilia bli forvrengt eller ødelagt. Skader på sneglehinnen kan forekomme på flere måter, for eksempel ved virusinfeksjon, eksponering for ototoksiske kjemikalier og intens støyeksponering. Skader på OHC-ene resulterer i enten en mindre effektiv aktiv mekanisme, eller det fungerer kanskje ikke i det hele tatt. OHC-er bidrar til å gi høy følsomhet for stille lyder i et bestemt frekvensområde (ca. 2–4 kHz). Dermed resulterer skade på OHC-ene i reduksjon av følsomheten til den basilære membranen for svake lyder. Det er derfor nødvendig med forsterkning av disse lydene, for at den basilære membranen skal kunne reagere effektivt. IHC er mindre utsatt for skade sammenlignet med OHC. Imidlertid, hvis de blir skadet, vil dette resultere i et generelt tap av følsomhet.
Nevrale tuningkurver
Frekvensselektivitet
Den vandrende bølgen langs basilærmembranen topper på forskjellige steder langs den, avhengig av om lyden er lav eller høy frekvens. På grunn av massen og stivheten til den basilære membranen toppes lavfrekvente bølger i toppunktet, mens høyfrekvente lyder topp i den basale enden av sneglehuset. Derfor er hver posisjon langs basilærmembranen finjustert til en bestemt frekvens. Disse spesifikt innstilte frekvensene blir referert til som karakteristiske frekvenser (CF).
Hvis en lyd som kommer inn i øret blir forskjøvet fra den karakteristiske frekvensen, vil responsstyrken fra basilærmembranen gradvis reduseres. Finjusteringen av basilærmembranen er opprettet ved å legge inn to separate mekanismer. Den første mekanismen er en lineær passiv mekanisme, som er avhengig av den mekaniske strukturen til den basilære membranen og dens omkringliggende strukturer. Den andre mekanismen er en ikke-lineær aktiv mekanisme, som først og fremst er avhengig av funksjonen til OHC, og også den generelle fysiologiske tilstanden til selve snegleorganet. Basaren og toppunktet på basilærmembranen er forskjellige i stivhet og bredde, noe som får basilimembranen til å svare på varierende frekvenser ulikt langs lengden. Basen på den basilære membranen er smal og stiv, noe som resulterer i at den reagerer best på høyfrekvente lyder. Toppunktet på basilærmembranen er bredere og mye mindre stiv i forhold til basen, noe som får den til å svare best på lave frekvenser.
Denne selektiviteten til visse frekvenser kan illustreres med nevrale innstillingskurver. Disse viser frekvensene en fiber reagerer på, ved å vise terskelnivåer (dB SPL) av hørselsnerven fibre som en funksjon av forskjellige frekvenser. Dette demonstrerer at hørselsnerven fibre reagerer best, og har dermed bedre terskler ved fiberens karakteristiske frekvens og frekvenser som omgir den umiddelbart. Basilimembranen sies å være "skarpt innstilt" på grunn av den skarpe "V" -formede kurven, med "spissen" sentrert på hørselsfiberens karakteristiske frekvens. Denne formen viser hvor få frekvenser en fiber reagerer på. Hvis det var en bredere V-form, ville den svare på flere frekvenser (se figur 4).
IHC vs OHC hørselstap
En normal nevral innstillingskurve er preget av en bredt innstilt lavfrekvens 'hale', med en fininnstilt midtfrekvens 'spiss'. Imidlertid, der det er delvis eller fullstendig skade på OHC-ene, men med uskadede IHC-er, vil den resulterende innstillingskurven vise eliminering av følsomhet ved stille lyder. Det vil si hvor den nevrale innstillingskurven normalt ville være mest følsom (på 'spissen') (se figur 5).
Der både OHC og IHC er skadet, vil den resulterende nevrale innstillingskurven vise eliminering av følsomhet ved 'spissen'. Imidlertid, på grunn av IHC-skade, blir hele innstillingskurven hevet, noe som gir tap av følsomhet over alle frekvenser (se figur 6). Det er bare nødvendig at den første raden av OHC-er blir skadet for at eliminering av det finjusterte 'spissen' skal skje. Dette støtter ideen om at forekomsten av OHC-skade og dermed tap av følsomhet for stille lyder, forekommer mer enn IHC-tap.
Når IHC-ene eller en del av basilærmembranen blir skadet eller ødelagt, slik at de ikke lenger fungerer som transdusere, er resultatet en 'død region'. Døde regioner kan defineres i form av de karakteristiske frekvensene til IHC, relatert til det spesifikke stedet langs den basilære membranen der den døde regionen forekommer. Forutsatt at det ikke har skjedd noen forskyvning i de karakteristiske frekvensene knyttet til visse regioner i basilærmembranen på grunn av skaden av OHC. Dette skjer ofte med IHC-skade. Døde regioner kan også defineres av det anatomiske stedet for den ikke-fungerende IHC (for eksempel en "apikal død region"), eller av de karakteristiske frekvensene til IHC ved siden av den døde regionen.
Død region audiometri
Ren tone audiometri (PTA)
Døde regioner påvirker audiometriske resultater, men kanskje ikke på den måten som forventet. For eksempel kan det forventes at terskler ikke ville oppnås ved frekvensene i det døde området, men ville bli oppnådd ved frekvenser ved siden av det døde området. Forutsatt at normal hørsel eksisterer rundt det døde området, vil det derfor produsere et audiogram som har en dramatisk bratt skråning mellom frekvensen der en terskel oppnås, og frekvensen der en terskel ikke kan oppnås på grunn av den døde regionen.
Det ser imidlertid ut til at dette ikke er tilfelle. Døde regioner kan ikke finnes tydelig via PTA- lydgrammer . Dette kan være fordi selv om nevronene som innerverer den døde regionen, ikke kan reagere på vibrasjoner ved deres karakteristiske frekvens. Hvis basilar membranvibrasjonen er stor nok, vil nevroner innstilt på forskjellige karakteristiske frekvenser som de som grenser til det døde området stimuleres på grunn av spredning av eksitasjon. Derfor vil man få svar fra pasienten ved testfrekvensen. Dette er referert til som "off-place-lytting", og er også kjent som "off-frequency listening". Dette vil føre til at en falsk terskel blir funnet. Dermed ser det ut til at en person har bedre hørsel enn de faktisk har, noe som resulterer i at en død region blir savnet. Derfor, ved bruk av PTA alene, er det umulig å identifisere omfanget av en død region (se figur 7 og 8).
Følgelig, hvor mye påvirkes en audiometrisk terskel av en tone med frekvensen i en død region? Dette avhenger av plasseringen av den døde regionen. Terskler ved døde regioner med lav frekvens er mer unøyaktige enn døde regioner med høyere frekvens. Dette har blitt tilskrevet det faktum at eksitasjon på grunn av vibrasjon av basilærmembranen sprer seg oppover fra de apikale områdene av basilimembranen, mer enn eksitasjon sprer seg nedover fra høyere frekvens basale regioner av cochlea. Dette mønsteret av spredning av eksitasjon ligner fenomenet "oppadgående spredning av maskering". Hvis tonen er tilstrekkelig høy til å produsere nok eksitasjon i det normalt fungerende området av sneglehinnen, slik at den er over denne områdets terskel. Tonen vil bli oppdaget på grunn av lytting utenfor frekvensen, noe som resulterer i en villedende terskel.
For å bidra til å overvinne problemet med PTA som produserer unøyaktige terskler i døde regioner, kan maskering av området utenfor den døde regionen som stimuleres brukes. Dette betyr at terskelen til det reagerende området er tilstrekkelig hevet, slik at den ikke kan oppdage spredning av eksitasjon fra tonen. Denne teknikken har ført til antydningen om at en lavfrekvent død region kan være relatert til et tap på 40-50 dB. Ettersom et av målene med PTA er å avgjøre om det er en død region eller ikke, kan det imidlertid være vanskelig å vurdere hvilke frekvenser som skal maskeres uten bruk av andre tester.
Basert på forskning har det blitt antydet at en lavfrekvent død region kan gi et relativt flatt tap, eller et veldig gradvis skrånende tap mot høyere frekvenser. Siden den døde regionen vil være mindre påviselig på grunn av den oppadgående spredningen av eksitasjon. Mens det kan være et mer åpenbart bratt skrånende tap ved høye frekvenser for en høyfrekvent død region. Selv om det er sannsynlig at skråningen representerer den mindre markerte nedadgående spredningen av eksitasjon, snarere enn nøyaktige terskler for de frekvensene med ikke-fungerende hårceller. Midtfrekvente døde regioner, med et lite område, ser ut til å ha mindre innvirkning på pasientens evne til å høre i hverdagen, og kan gi et hakk i PTA-terskelen. Selv om det er klart at PTA ikke er den beste testen for å identifisere en død region.
Psykoakustisk tuningkurver (PTC) og terskelutjevningstøy (TEN) tester
Selv om det fortsetter en viss debatt om påliteligheten av slike tester, har det blitt antydet at psykoakustiske tuningkurver (PTC) og terskelutjevningsstøy (TEN) -resultater kan være nyttige for å oppdage døde regioner, i stedet for PTA. PTC-er ligner nevrale innstillingskurver. De illustrerer nivået på en masker (dB SPL) tone ved terskelen, som en funksjon av avvik fra senterfrekvens (Hz). De måles ved å presentere en fast lavintensitet ren tone mens de også presenterer en smalbåndsmasker, med varierende senterfrekvens. Maskeringsnivået er variert, slik at nivået av masker som trengs for å bare maskere testsignalet, blir funnet for maskeren ved hver senterfrekvens. Spissen av PTC er der maskeringsnivået som trengs for å bare maskere testsignalet er det laveste. For vanlige hørselsfolk er dette når maskeringssenterfrekvensen er nærmest frekvensen til testsignalet (se figur 9).
Når det gjelder døde regioner, når testsignalet ligger innenfor grensene til et dødt område, blir spissen av PTC forskjøvet til kanten av det døde området, til området som fremdeles fungerer og oppdager spredning av eksitasjon fra signalet. Når det gjelder et lavfrekvent dødområde, forskyves spissen oppover, noe som indikerer et lavfrekvent dødområde som starter ved kurvetoppen. For en høyfrekvent død region forskyves spissen nedover fra signalfrekvensen til funksjonsområdet under den døde regionen. Den tradisjonelle metoden for å skaffe PTC er imidlertid ikke praktisk for klinisk bruk, og det er blitt hevdet at TEN ikke er nøyaktige nok. En rask metode for å finne PTC er utviklet, og den kan gi løsningen. Imidlertid er mer forskning for å validere denne metoden nødvendig før den kan aksepteres klinisk.
Perseptuelle konsekvenser av en død region
Audiogram- konfigurasjoner er ikke gode indikatorer på hvordan en død region vil påvirke en person funksjonelt, hovedsakelig på grunn av individuelle forskjeller. For eksempel er et skrånende audiogram ofte tilstede med en død region på grunn av spredning av eksitasjon. Imidlertid kan individet godt bli påvirket annerledes enn noen med et tilsvarende skrånende audiogram forårsaket av delvis skade på hårceller i stedet for en død region. De vil oppfatte lyder annerledes, men lydprogrammet antyder at de har samme grad av tap. Huss og Moore undersøkte hvordan hørselshemmede pasienter oppfatter rene toner, og fant at de oppfatter toner som støyende og forvrengt, mer (i gjennomsnitt) enn en person uten hørselsnedsettelse. Imidlertid fant de også at oppfatningen av toner som støy ikke var direkte relatert til frekvenser i de døde områdene, og derfor ikke var en indikator på en død region. Dette antyder derfor at audiogrammer, og deres dårlige representasjon av døde regioner, er unøyaktige prediktorer for pasientens oppfatning av ren tonekvalitet.
Forskning av Kluk og Moore har vist at døde regioner også kan påvirke pasientens oppfatning av frekvenser utover de døde regionene. Det er en forbedring i evnen til å skille mellom toner som avviker veldig lite i frekvens, i regioner like utenfor de døde regionene sammenlignet med toner lenger borte. En forklaring på dette kan være at kortikatskartlegging har skjedd. Nevroner som normalt vil bli stimulert av den døde regionen, har blitt tildelt til å svare på fungerende områder i nærheten. Dette fører til en overrepresentasjon av disse områdene, noe som resulterer i økt perseptuell følsomhet for små frekvensforskjeller i toner.
Vestibulokoklear nervepatologi
- medfødt misdannelse i den indre lydkanalen,
- neoplastiske og pseudo-neoplastiske lesjoner, med spesiell detaljert vekt på schwannoma av den åttende kranialnerven (akustisk neurom),
- ikke-neoplastisk indre auditiv kanal / Cerebello Pontinvinkelpatologi, inkludert vaskulære løkker,
Diagnose
Sakshistorie
Før undersøkelsen gir en sakshistorie veiledning om konteksten til hørselstap.
- stor bekymring
- informasjon om graviditet og fødsel
- medisinsk historie
- utviklingshistorie
- familie historie
Otoskopi
Direkte undersøkelse av den ytre kanalen og trommehinnen (trommehinnen) med et otoskop , et medisinsk utstyr satt inn i øregangen som bruker lys for å undersøke tilstanden til det ytre øre og trommehinnen, og mellomøret gjennom den halvgjennomsiktige membranen.
Differensial testing
Differensialtesting er mest nyttig når det er ensidig hørselstap, og skiller ledende fra sensorineural tap. Disse utføres med en lavfrekvent innstillingsgaffel, vanligvis 512 Hz, og kontrastmålinger av luft- og beinledet lydoverføring.
- Weber-test , der en stemmegaffel berøres til pannens midtlinje, lokaliseres til det normale øret hos personer med ensidig sensorineural hørselstap.
- Rinne-test , som tester luftledning vs benledning er positiv, fordi både bein og luftledning er redusert likt.
- mindre vanlige Bing- og Schwabach-varianter av Rinne-testen.
- absolutt beinledningstest (ABC).
Tabell 1 . En tabell som sammenligner sensorineural med ledende hørselstap
| Kriterier | Sensorineural hørselstap | Ledende hørselstap |
| Anatomisk sted | Det indre øre , hjernenerven VIII eller sentrale behandlingssentre | Mellomøret (ossikulær kjede), trommehinne eller ytre øre |
| Weber-test | Lyd lokaliseres til normalt øre i ensidig SNHL | Lyd lokaliseres til det berørte øret (øre med ledende tap) i ensidige tilfeller |
| Rinne-test | Positiv Rinne; luftledning> beinledning (både luft- og beinledning reduseres likt, men forskjellen mellom dem er uendret). | Negativ Rinne; beinledning> luftledning (bein / luftspalte) |
Andre, mer komplekse, tester av auditiv funksjon er nødvendige for å skille mellom de forskjellige typer hørselstap. Benledningsgrenser kan skille sensorineural hørselstap fra ledende hørselstap. Andre tester, som oto-akustiske utslipp, akustiske stapediale reflekser, tale-audiometri og fremkalt respons-audiometri er nødvendig for å skille mellom sensorisk, nevral og auditiv prosessering av hørselsnedsettelser.
Tympanometri
Et tympanogram er resultatet av en test med et tympanometer. Den tester funksjonen til mellomøret og mobiliteten til trommehinnen. Det kan bidra til å identifisere ledende hørselstap på grunn av sykdom i mellomøret eller trommehinnen fra andre typer hørselstap inkludert SNHL.
Audiometri
Et audiogram er resultatet av en hørselstest. Den vanligste typen hørselstest er ren tone-audiometri (PTA). Den kartlegger tersklene for hørselsfølsomhet ved et utvalg av standardfrekvenser mellom 250 og 8000 Hz. Det er også høyfrekvent ren tone-audiometri som tester frekvenser fra 8000-20.000 Hz. PTA kan brukes til å skille mellom ledende hørselstap, sensorineural hørselstap og blandet hørselstap. Et hørselstap kan beskrives etter sin grad, dvs. mild, moderat, alvorlig eller dyp, eller ved sin form, dvs. høy frekvens eller skrånende, lav frekvens eller stigende, hakk, U-formet eller 'cookie-bite', toppet eller flatt.
Det finnes også andre typer audiometri designet for å teste hørselskarphet i stedet for følsomhet (tale-audiometri), eller for å teste auditiv nevralveisending (fremkalt respons-audiometri).
Bildebehandling av magnetisk resonans
MR-skanning kan brukes til å identifisere grove strukturelle årsaker til hørselstap. De brukes til medfødt hørselstap når endringer i form av det indre øret eller hørselsnerven kan hjelpe til med å diagnostisere årsaken til hørselstapet. De er også nyttige i tilfeller der det er mistanke om en svulst eller for å bestemme graden av skade på hørselstap forårsaket av bakteriell infeksjon eller autoimmun sykdom. Skanning har ingen verdi i aldersrelatert døvhet.
Forebygging
Presbycusis er den viktigste årsaken til SNHL og er progressiv og ikke til å forebygge, og på dette tidspunktet har vi verken somatisk eller genterapi for å motvirke arvelighetsrelatert SNHL. Men andre årsaker til ervervet SNHL kan i stor grad forebygges, spesielt årsaker til nosocusis. Dette vil innebære å unngå miljøstøy og traumatisk støy som rockekonserter og nattklubber med høy musikk. Bruk av støydempende tiltak som ørepropper er et alternativ, i tillegg til å lære om støynivåene man blir utsatt for. For øyeblikket eksisterer det flere nøyaktige apper for måling av lydnivå . Å redusere eksponeringstiden kan også bidra til å håndtere risikoen fra høye eksponeringer.
Behandling
Behandlingsmodaliteter faller inn i tre kategorier: farmakologisk, kirurgisk og ledelse. Siden SNHL er en fysiologisk nedbrytning og anses som permanent, er det per denne tiden ingen godkjente eller anbefalte behandlinger.
Det har vært betydelige fremskritt innen identifisering av menneskelige døvhetsgener og klargjøring av deres cellulære mekanismer, så vel som deres fysiologiske funksjon hos mus. Likevel er farmakologiske behandlingsalternativer svært begrensede og klinisk uprøvde. Slike farmasøytiske behandlinger som anvendes, er lindrende snarere enn helbredende, og adressert til den underliggende årsaken hvis en kan identifiseres, for å unngå progressiv skade.
Dypt eller totalt hørselstap kan være mottakelig for behandling av cochleaimplantater , som stimulerer cochleaire nerveender direkte. Et cochleaimplantat er kirurgisk implantasjon av et batteridrevet elektronisk medisinsk utstyr i det indre øret. I motsetning til høreapparater , som gir lyder høyere, gjør cochleaimplantater arbeidet med skadede deler av det indre øret (cochlea) for å gi lydsignaler til hjernen. Disse består av både interne implanterte elektroder og magneter og eksterne komponenter. Kvaliteten på lyden er forskjellig fra naturlig hørsel, men kan gjøre det mulig for mottakeren å gjenkjenne tale- og miljølyder. På grunn av risiko og utgifter er en slik operasjon reservert for tilfeller av alvorlig og funksjonshemmende hørselshemming
Håndtering av sensorineural hørselstap innebærer å benytte strategier for å støtte eksisterende hørsel som leppelesing, forbedret kommunikasjon etc. og forsterkning ved hjelp av høreapparater . Høreapparater er spesielt innstilt på det enkelte hørselstap for å gi maksimal nytte.
Forskning
Legemidler
- Antioksidante vitaminer - Forskere ved University of Michigan rapporterer at en kombinasjon av høye doser vitamin A, C og E og magnesium, tatt en time før støyeksponering og fortsatte som en behandling daglig i fem dager, var veldig effektiv kl. forebygge permanent støyindusert hørselstap hos dyr.
- Tanakan - et merkenavn for et internasjonalt reseptbelagt ekstrakt av Ginkgo biloba. Det er klassifisert som en vasodilator. Blant forskningsanvendelsene er behandling av sensorineural døvhet og tinnitus antatt å være av vaskulær opprinnelse.
- Koenzym Q10 - et stoff som ligner på et vitamin, med antioksidantegenskaper. Den er laget i kroppen, men nivåene faller med alderen.
- ebselen , et syntetisk medikamentmolekyl som etterligner glutationperoksidase (GPx), et kritisk enzym i det indre øret som beskytter det mot skader forårsaket av høye lyder eller støy
Stamcelle- og genterapi
Regenerering av hårceller ved bruk av stamcelle- og genterapi er år eller tiår unna å være klinisk gjennomførbar. Imidlertid er det for tiden studier på gang med emnet, med den første FDA- godkjente studien som begynner i februar 2012.
Plutselig sensorineural hørselstap
Plutselig sensorineural hørselstap (SSHL eller SSNHL), ofte kjent som plutselig døvhet, oppstår som et uforklarlig, raskt hørselstap - vanligvis i det ene øret - enten på en gang eller over flere dager. Ni av ti personer med SSHL mister hørselen i bare ett øre. Det bør betraktes som en medisinsk nødsituasjon. Forsinket diagnose og behandling kan gjøre behandlingen mindre effektiv eller ineffektiv.
Eksperter anslår at SSHL slår en person per 100 hvert år, vanligvis voksne i 40- og 50-årene. Det faktiske antall nye tilfeller av SSHL hvert år kan være mye høyere fordi tilstanden ofte går udiagnostisert.
Presentasjon
Mange merker at de har SSHL når de våkner om morgenen. Andre merker det først når de prøver å bruke det øredøvede øret, for eksempel når de bruker en telefon. Atter andre merker en høy, alarmerende "pop" like før hørselen forsvinner. Personer med plutselig døvhet blir ofte svimmel, har ring i ørene (tinnitus), eller begge deler.
Diagnose
SSHL diagnostiseres via ren tone-audiometri. Hvis testen viser et tap på minst 30 dB i tre tilstøtende frekvenser, blir hørselstapet diagnostisert som SSHL. For eksempel vil et hørselstap på 30 dB få samtaletale til å høres mer ut som en hvisking.
Årsaker
Bare 10 til 15 prosent av tilfellene diagnostisert som SSHL har en identifiserbar årsak. De fleste tilfeller er klassifisert som idiopatisk , også kalt plutselig idiopatisk hørselstap (SIHL) og idiopatisk plutselig sensorineural hørselstap (ISSHL eller ISSNHL) De fleste bevis peker på en eller annen form for betennelse i det indre øret som den vanligste årsaken til SSNHL.
- Viral - Hevelsen kan skyldes et virus. Et herpes-virus antas å være den vanligste årsaken til plutselig sensorineural hørselstap. Herpesviruset ligger i hvilemodus i kroppene våre og aktiveres av ukjent grunn.
- Vaskulær iskemi i det indre øret eller hjernenerven VIII (CN8)
- Perilymph fistula , vanligvis på grunn av et brudd i de runde eller ovale vinduene og lekkasje av perilymph . Pasienten vil vanligvis også oppleve svimmelhet eller ubalanse . En historie med traumer er vanligvis til stede, og endringer i hørsel eller svimmelhet skjer med endring i intrakranielt trykk, for eksempel med anstrengelse; løfte, blåse etc.
- Autoimmun - kan skyldes en autoimmun sykdom som systemisk lupus erythematosus , granulomatose med polyangiitt
Behandling
Hørselstap gjenoppretter helt hos rundt 35-39% av pasientene med SSNHL, vanligvis innen en til to uker fra starten. Åttifem prosent av de som får behandling fra øre-halssykdommer (noen ganger kalt en ØNH-kirurg) vil gjenopprette noe av hørselen.
- vitaminer og antioksidanter
- vasodilatatorer
- betahistine (Betaserc), et middel mot svimmelhet
- hyperbar oksygen
- reologiske midler som reduserer viskositeten i blodet (slik som hydroksyetylstivelse , dekstran og pentoksifyllin )
- betennelsesdempende midler, primært orale kortikosteroider som prednison , metylprednison
- Intratympanisk administrasjon - Gelformuleringer er under etterforskning for å gi mer jevn medisintilførsel til det indre øret. Lokal medikamentavlevering kan oppnås gjennom intratympanisk administrering, en minimalt invasiv prosedyre hvor trommehinnen blir bedøvd og et medikament administreres i mellomøret. Fra mellomøret kan et medikament diffundere over det runde vindusmembranen inn i det indre øret. Intratympanisk administrering av steroider kan være effektiv for plutselig sensorineural hørselstap for noen pasienter, men kliniske data av høy kvalitet er ikke generert. Intratympanisk administrering av et anti-apoptotisk peptid (JNK-hemmer) blir for tiden evaluert i klinisk utvikling i sen fase.
Epidemiologi
Generelt hørselstap rammer nærmere 10% av den globale befolkningen. Bare i USA forventes det at 13,5 millioner amerikanere lider av sensorineural hørselstap. Av de som er rammet av sensorineural hørselstap, er omtrent 50% medfødt familie . De øvrige 50% skyldes infeksjoner fra mødre eller fostre, postnatale infeksjoner, virusinfeksjoner på grunn av røde hunder eller cytomegalovirus , ototoksiske legemidler, eksponering for høye lyder, alvorlig hodeskade og for tidlig fødsel
Av de genetisk relaterte sensorineurale hørselstapstilfellene er 75% autosomal recessiv , 15-20% autosomal dominant og 1-3% kjønnsbundet. Mens det spesifikke genet og proteinet fremdeles er ukjent, antas mutasjoner i connexin 26-genet nær DFNB1-stedet i kromosom 13 å utgjøre mesteparten av det autosomale recessive genetiske relaterte sensorineurale hørselstapet.
Minst 8,5 per 1000 barn yngre enn 18 år har sensorineural hørselstap. Generelt hørselstap er proporsjonalt relatert til alder. Minst 314 per 1000 personer eldre enn 65 år har nedsatt hørsel. Flere risikofaktorer for sensorineural hørselstap har blitt studert det siste tiåret. Osteoporose, stapedektomi-kirurgi , pneumokokkvaksinasjoner, mobiltelefonbrukere og hyperbilirubinemi ved fødselen er blant noen av de kjente risikofaktorene.
Se også
- Ledende hørselstap , hørselstap primært forårsaket av forhold i mellomøret
- Kortikal døvhet , en annen type nervedøvhet
- Hørselstap
- Det indre øret , den innerste delen av øret som inneholder det sensorineurale høreapparatet
- Otosklerose , en til tider assosiert eller forgjenger ledende hørselstap hos mellomøret
- Tinnitus , ringer i ørene, et vanlig akkompagnement av SNHL
Merknader
Referanser
38. Ghazavi H, Kargoshaei AA, Jamshidi-Koohsari M, "Undersøkelse av vitamin D-nivåer hos pasienter med plutselig sensorisk-nevralt hørselstap og dets effekt på behandlingen", American journal of otolaryngology and head and neck medicine and suegery, November 2019 https : //doi.org/10.1016/j.amjoto.2019.102327
Eksterne linker
| Klassifisering | |
|---|---|
| Eksterne ressurser |