Sjögrens syndrom - Sjögren syndrome
| Sjögrens syndrom | |
|---|---|
| Andre navn | Sjögrens syndrom, sicca syndrom |
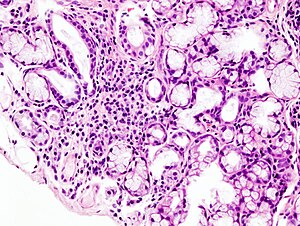 | |
| Bilde med et mikroskop av fokal lymfoid infiltrasjon i den mindre spyttkjertelen assosiert med Sjögren syndrom. | |
| Uttale | |
| Spesialitet |
Immunologi , revmatologi |
| Symptomer | Tørr munn , tørre øyne , andre områder med tørrhet |
| Komplikasjoner | Lymfom |
| Vanlig start | Middelalder |
| Varighet | Lang sikt |
| Årsaker | Autoimmun sykdom (ukjent årsak) |
| Diagnostisk metode | Vevsbiopsi , blodprøver |
| Differensialdiagnose | Medisinsk bivirkning, angst , sarkoidose , amyloidose |
| Behandling | Kunstige tårer , medisiner for å redusere betennelse, kirurgi |
| Prognose | Normal levetid |
| Frekvens | ~ 0,7% |
Sjögrens syndrom ( SjS , SS ) er en langsiktig autoimmun sykdom som påvirker kroppens fuktighetsproduserende (lacrimal og spytt) kjertler , og ofte alvorlig påvirker andre organsystemer, for eksempel lunger, nyrer og nervesystem. Primære symptomer er tørrhet ( munntørrhet og tørre øyne ), smerter og tretthet . Andre symptomer kan være tørr hud , tørrhet i skjeden, kronisk hoste, nummenhet i armer og ben, trøtthet , muskel- og leddsmerter og problemer med skjoldbruskkjertelen . De som er rammet har også en økt risiko (15%) for lymfom .
Selv om den eksakte årsaken er uklar, antas det å innebære en kombinasjon av genetikk og en miljøutløser som eksponering for et virus eller en bakterie . Det kan oppstå uavhengig av andre helseproblemer (primært Sjögrens syndrom) eller som et resultat av en annen bindevevsforstyrrelse (sekundært Sjögrens syndrom). Sjögrens syndrom kan være assosiert med andre autoimmune sykdommer, inkludert revmatoid artritt (RA), systemisk lupus erythematosus (SLE) eller systemisk sklerose. Den betennelse som resulterer gradvis skader kjertlene. Diagnosen er ved biopsi av fuktighetsproduserende kjertler og blodprøver for spesifikke antistoffer . På biopsi er det vanligvis lymfocytter i kjertlene.
Selv om Sjögrens syndrom er en av de vanligste autoimmun sykdommer, har den ingen spesifikke og ikke-invasive diagnostiske tester, og behandlingen er rettet mot å håndtere personens symptomer . For tørre øyne kan kunstige tårer , medisiner for å redusere betennelse, punkterte plugger eller kirurgi for å lukke tårekanalene bli prøvd. For tørr munn kan det brukes tyggegummi (helst sukkerfritt), sipping vann eller et spyttsubstitutt . Hos de med ledd- eller muskelsmerter kan ibuprofen brukes. Medisiner som kan forårsake tørrhet, for eksempel antihistaminer , kan også stoppes. Den mest spesifikke eksisterende diagnostiske testen krever leppebiopsi.
Sykdommen ble beskrevet i 1933 av Henrik Sjögren , som den er oppkalt etter; Imidlertid finnes det en rekke tidligere beskrivelser av personer med symptomene. Mellom 0,2 og 1,2% av befolkningen er berørt, hvor halvparten har hovedformen og halvparten sekundærformen. Hunnene påvirkes omtrent 10 ganger så ofte som menn. Selv om sykdommen vanligvis begynner i middelalderen , kan hvem som helst bli påvirket. Blant de uten andre autoimmune lidelser er forventet levealder uendret.
Tegn og symptomer
Kjennetegnet for Sjögrens syndrom er munntørrhet og keratokonjunktivitt sicca (tørre øyne). Vaginal tørrhet , tørr hud og tørr nese kan også forekomme. Andre organer i kroppen kan også påvirkes, inkludert nyrene, blodårene, lungene, leveren, bukspyttkjertelen og hjernen.
Hudtørrhet hos noen mennesker med SS kan være et resultat av lymfocytisk infiltrasjon i hudkjertlene . Symptomene kan utvikle seg lumsk, med diagnosen ofte ikke vurdert på flere år fordi sicca kan tilskrives medisiner, tørre omgivelser eller aldring, eller kan betraktes som ikke av en alvorlighetsgrad som begrenser nivået på undersøkelsen som er nødvendig for å fastslå tilstedeværelsen av den underliggende autoimmune lidelsen.
Sjögrens syndrom kan skade vitale organer , med symptomer som kan platåere eller forverres, eller gå i remisjon , som med andre autoimmune sykdommer. Noen mennesker kan bare oppleve de milde symptomene på tørre øyne og munn, mens andre har symptomer på alvorlig sykdom. Mange pasienter kan behandle problemer symptomatisk . Andre opplever tåkesyn , konstant ubehag i øyet, tilbakevendende munninfeksjoner , hovne parotidkjertler , dysfoni ( stemmeforstyrrelser inkludert heshet) og problemer med å svelge og spise. Sløvende tretthet og leddsmerter kan forringe livskvaliteten alvorlig. Noen pasienter kan utvikle nyreinvolvering (autoimmun tubulær nefritt ) som fører til proteinuri (overskudd av protein i urinen), urin konsentrering defekt , og distal renal tubulær acidose .
Komplikasjoner
Blant komplikasjonene som er diskutert ovenfor, har kvinner med anti-Ro/SS-A og anti-La/SS-B antistoffer som blir gravide en økt frekvens av nyfødt lupus erythematosus med medfødt hjerteblokk som krever pacemaker . Type I kryoglobulinemi er en kjent komplikasjon av Sjögrens syndrom.
Sjögrens syndrom kan påvirke organer som lever, bukspyttkjertel, nyrer, lunger og sentralnervesystemet.
Tilhørende forhold
Sjögrens syndrom er forbundet med en rekke andre medisinske tilstander, hvorav mange er autoimmune eller revmatiske lidelser, for eksempel cøliaki , fibromyalgi , SLE (lupus) , autoimmun thyroiditt , multippel sklerose og spondyloartropati , og flere maligniteter , hovedsakelig non-Hodgkin lymfom .
Årsaker
Årsaken til Sjögrens syndrom er ukjent, men det kan være påvirkning av en kombinasjon av genetiske, miljømessige og andre faktorer, slik tilfellet er med mange andre autoimmune lidelser. Rundt 20 autoantistoffer kan være involvert.
Genetikk
Observasjonen av høye frekvenser av autoimmune lidelser i familier med en historie med Sjögrens syndrom er knyttet til en genetisk disposisjon for syndromet. Studier av polymorfismer av human leukocytt-antigen (HLA) -Dr og HLA-DQ- gen regioner i Sjøgrens pasienter viser differensial mottagelighet for syndromet som et resultat av forskjellige typer av den resulterende autoantistoff -produksjon.
Hormoner
Siden Sjögrens syndrom er forbundet med høy forekomst hos kvinner, antas det at kjønnshormoner , spesielt østrogen , påvirker humorale og cellemedierte immunresponser som påvirker mottakeligheten for syndromet. Androgener anses generelt for å forhindre autoimmunitet. Studier på musemodeller antyder at østrogenmangel stimulerer presentasjonen av autoantigener , noe som fremkaller Sjögrens lignende symptomer.
Mikrokimerisme
Mikrokimerisme av fosterceller (avkom lymfoidceller i mors sirkulasjon ) kan generere autoimmunitet hos kvinner som tidligere har vært gravide . Generering av et autoimmun potensial via mikrokimerisme kan føre til en bytte fra en stille form for autoimmunitet med aldersavhengig reduksjon i selvtoleranse .
Miljø
Virale proteiner , oppslukte molekyler eller forringede selvstrukturer kan starte autoimmunitet ved molekylær etterligning og øke sjansene for utvikling av Sjögrens syndrom. Epstein-Barr-virus , hepatitt C og humant T-celle leukemivirus-1 er blant de mest undersøkte smittestoffene ved Sjögrens syndrom. Til dags dato har det ikke blitt identifisert noen direkte årsaker og virkningssammenheng mellom disse patogenene og utviklingen av Sjögrens syndrom. Skadede selvstrukturer rettet mot apoptose kan feilaktig utsettes for immunsystemet, noe som utløser autoimmunitet i eksokrine kjertler , som ofte er utsatt for autoimmune responser.
Patogenese
De patogenetiske mekanismene ved Sjögrens syndrom er ikke fullstendig belyst, noe som resulterer i mangel på patofysiologisk kunnskap om behandling av denne autoimmune eksokrinopati . Selv om de mange faktorene som bidrar til utviklingen av denne sykdommen har gjort det vanskelig å oppdage den eksakte opprinnelsen og årsaken, har store fremskritt det siste tiåret bidratt til et foreslått sett med patogene hendelser som oppstår før diagnosen Sjögrens syndrom.
Sjögrens syndrom ble opprinnelig foreslått som et spesifikt, selvopprettholdende , immunsystem-mediert tap av eksokrine kjertler, spesielt acinar og duktale celler . Selv om dette forklarer de mer åpenbare symptomene (for eksempel mangel på spytt og lakrimalvæske ), forklarer det ikke de mer utbredte systemiske effektene som er sett i sykdomsutviklingen.
I nærvær av en mottagelig genetisk bakgrunn antas både miljømessige og hormonelle faktorer i stand til å utløse infiltrering av lymfocytter, spesielt CD4+ T -celler , B -celler og plasmaceller , noe som forårsaker kjerteldysfunksjon i spytt- og tårekjertlene.
Sjögrens syndrom er assosiert med økte nivåer i cerebrospinalvæske (CSF) av IL-1RA , en interleukin 1- antagonist . Dette antyder at sykdommen begynner med økt aktivitet i interleukin 1-systemet, etterfulgt av en autoregulerende oppregulering av IL-1RA for å redusere den vellykkede bindingen av interleukin 1 til dets reseptorer. Interleukin 1 sannsynlig er det markør for tretthet, men økte IL-1RA er observert i CSF og er forbundet med økt tretthet gjennom cytokin -indusert sykdom oppførsel . Sjögrens syndrom er imidlertid preget av reduserte nivåer av IL-1ra i spytt, som kan være ansvarlig for betennelse i munnen og tørrhet. Pasienter med sekundært Sjögrens syndrom viser også ofte tegn og symptomer på sine primære revmatiske lidelser, for eksempel systemisk lupus erythematosus , revmatoid artritt eller systemisk sklerose .
Genetisk predisposisjon
Det genetiske stedet som er mest signifikant assosiert med primær SS er hovedhistokompatibilitetskomplekset / humant leukocyttantigen (MHC / HLA) -region, som demonstrert av de foreløpige resultatene av den første genomomfattende assosiasjonsstudien . Denne studien inkluderte data fra en funnkohort av 395 pasienter av europeisk herkomst med primært Sjögrens syndrom og 1 975 friske kontrollpersoner , og fra en replikasjonsstudie som omfattet 1 234 tilfeller og 4779 friske kontrollpersoner. Forbindelser med polymorfismer lokalisert på seks uavhengige steder ble også påvist; IRF5 , STAT4 , BLK , IL12A , TNIP1 , og CXCR5 . Dette antydet også aktivering av det medfødte immunsystemet , særlig gjennom IFN-systemet, B-celleaktivering gjennom CXCR5- rettet rekruttering til lymfoide follikler og B-celle reseptor (BCR) aktivering som involverer BLK , og T-celle-aktivering på grunn av HLA-følsomhet og IL-12-IFN-y-aksen.
Pasienter med ulik etnisk opprinnelse gjennomføre ulike HLA-resistens alleler , hvorav HLA-DR og HLA-DQ er involvert i patogenesen av Sjögrens syndrom. For eksempel viser pasienter fra Nord- og Vest -Europa og fra Nord -Amerika en høy forekomst av B8-, DRw52- og DR3 -gener. HLA klasse II -alleler er assosiert med tilstedeværelsen av spesifikke undersett av autoantistoffer , i stedet for med selve sykdommen. Autoantistoffer refererer til tap av B-celletoleranse som fører til produksjon av antistoffer rettet mot forskjellige organspesifikke og organspesifikke antigener. Foreningen mellom HLA og SS er begrenset til pasienter med anti-SSA/Ro- eller anti-SSB/La-antistoffer. Seropositivitet for anti-Ro og anti-La er forbundet med større alvorlighetsgrad og lengre varighet av sykdom, og funn av deres store mengde fra spyttkjertlene til Sjögrens pasienter antyder deres viktige rolle i patogenesen av SS.
Utover genetikk har epigenetisk abnormitet relatert til DNA -metylering , histonacetylering eller mikroRNA -uttrykk sannsynligvis en sentral rolle i patogenesen av autoimmune sykdommer, inkludert Sjögrens syndrom, selv om forskning på dette området er svært begrenset.
Miljøutløsere
Miljøfaktorer, slik som kjertel viral infeksjon , kunne føre til epitelceller for å aktivere den HLA-uavhengig medfødte immunsystemet gjennom toll-lignende reseptorer . Selv om en rekke smittsomme, eksogene midler har vært involvert i patogenesen av Sjögrens syndrom, for eksempel Epstein-Barr-virus (EBV), humant T-lymfotropisk virus 1 og hepatitt C-virus , virker deres tilknytning til Sjögrens syndrom svak. Mens EBV er tilstede i spyttkjertlene til normale individer, er det rapportert om høy forekomst av EBV -reaktivering hos Sjögrens pasienter med økte nivåer av EBV -DNA . Dette indikerer viral reaktivering og manglende evne til lymfoide infiltrater til å kontrollere EBV -replikasjon ved Sjögrens syndrom, noe som fører til initiering eller vedvarelse av en immunrespons i målorganene. Imidlertid gjenstår det å avklare nøyaktig hvordan reaktivering av EBV induseres i lesjoner av pasienter med Sjögrens syndrom, og hvilke spesifikke molekylære mekanismer som er involvert i prosessen med viral reaktivering.
Betennelse
Epitelceller i Sjögrens syndromlesjoner er aktive deltakere i induksjon og videreføring av den inflammatoriske prosessen. Miljø- og hormonelle faktorer, i samsvar med en passende genetisk bakgrunn, antas å utløse Sjögrens syndrom, som dysregulerer epitelceller og tillater avvikende homing og aktivering av dendritiske celler (DC), T -celler og B -celler. Dendritiske celler er antigenpresenterende celler som behandler antigenmateriale og presenterer det for andre T-celler. Etter migrasjon av lymfocytter inn i kjertlene som respons på kjemokiner og spesifikke vedheftsmolekyler , interagerer T -celler med epitelceller. Epitelceller aktiveres ytterligere av proinflammatoriske cytokiner (IL-1β, IFN-γ og TNF), som produseres av tilstøtende T-celler. Den tidlige akkumuleringen av plasmacytoide dendritiske celler i målvevet, som produserer høye nivåer av type 1 IFN, virker viktig, ettersom disse cellene ytterligere kan dysregulere immunresponsen gjennom unormal oppbevaring av lymfocytter i vevet og deres påfølgende aktivering. IFN-α stimulerer produksjonen av B-celleaktiverende faktor (BAFF) av epitelceller, DC-er og T-celler. BAFF stimulerer avvikende modning av B-celler, noe som fører til fremveksten av selvreaktive B-celler, som lokalt produserer autoantistoffer, i en germinal senterlignende struktur (GC-lignende), som også er stedet for lymfomagenese (opprinnelse til lymfom ).
Programmert celledød
Dysregulering av apoptose (programmert celledød) antas å spille en rolle i patogenesen av en rekke autoimmune sykdommer, selv om dens rolle i Sjögrens syndrom er kontroversiell. Både Fas- og Fas-ligandproteinene er overuttrykte hos primære Sjögrens pasienter, mens ekspresjon av BCL-1 , som er kjent for å nedregulere apoptose, ble funnet signifikant redusert i acinar- og duktale epitelceller hos Sjögrens pasienter sammenlignet med friske mennesker. Studier in situ viste ikke økt apoptose blant kjertelepitelceller, men viste redusert apoptose blant infiltrerende mononukleære celler. Redusert apoptose var også involvert i akkumulering av autoreaktive B-celler funnet i kjertlene. Forholdet mellom autoantistoffer uttrykt i Sjögrens syndrom og apoptose blir fortsatt undersøkt.
Hormonelle faktorer
Kjønnshormoner synes å påvirke humoral og cellemediert immunrespons, med østrogen som blir ansett som en av de viktigste faktorene som er ansvarlig for sex- immunologisk dimorphism . Østrogenmangel ser ut til å spille en rolle i utviklingen av Sjögrens syndrom. Det har blitt antatt at administrering av androgen til okulær overflate kan tjene som en effektiv behandling for tørre øyne.
Diagnose
Diagnostisering av Sjögrens syndrom (SS) er komplisert av symptomene som en pasient kan manifestere, og likheten mellom symptomer på Sjögrens syndrom og andre tilstander. Pasienter med SS -symptomer nærmer seg også forskjellige spesialiteter for behandling, noe som kan gjøre diagnosen vanskelig. Siden tørre øyne og tørr munn er svært vanlige symptomer, og ofte forekommer hos mennesker over 40, kan berørte mennesker tro at symptomene er aldersrelaterte, så ignorer dem. Noen medisiner kan forårsake symptomer som ligner på Sjögrens syndrom. Kombinasjonen av flere tester, som kan utføres i en serie, kan til slutt diagnostisere Sjögrens syndrom.
Blodprøver kan gjøres for å avgjøre om en pasient har høye nivåer av antistoffer som er tegn på tilstanden, for eksempel antinukleært antistoff (ANA) og revmatoid faktor (fordi Sjögrens syndrom ofte forekommer sekundært til revmatoid artritt), som er forbundet med autoimmune sykdommer . Typiske SS ANA-mønstre er SSA/Ro og SSB/La , hvorav anti-SSB/La er langt mer spesifikt; anti-SSA/Ro er assosiert med mange andre autoimmune tilstander, men er ofte tilstede i SS, men aAnti-SSA og anti-SSB tester er ofte ikke positive i SS.
Den rose bengal testen bruker en flekk som måler tilstand og funksjon av de lakrimalkjertlene . Denne testen innebærer å plassere den ikke -toksiske fargestoffrosen på øynene. Fargestoffets særegne farge hjelper til med å bestemme tilstanden og funksjonen til tårefilmen og tåredampningshastigheten. Enhver karakteristisk fargeendring kan indikere SS, men bekreftelse av tilstanden krever mange relaterte diagnostiske verktøy .
Schirmers test måler produksjon av tårer: en stripe med filterpapir holdes inne i det nedre øyelokket i fem minutter, og fuktigheten måles deretter med en linjal. Å produsere mindre enn 5 mm væske er vanligvis et tegn på SS. Denne måleanalysen varierer mellom mennesker, avhengig av andre øyerelaterte tilstander og medisiner som brukes når testen tas. En spaltelampeundersøkelse kan avsløre tørrhet på øyets overflate.
Symptomer på munntørrhet og tørrhet i munnhulen skyldes redusert spyttproduksjon fra spyttkjertlene ( parotidkjertel , submandibulær kjertel og sublingual kjertel ). For å kontrollere statusen til spyttkjertlene og produksjonen av spytt, utføres en spyttstrømningstest, der personen blir bedt om å spytte så mye som mulig i en kopp, og den resulterende spyttprøven blir samlet og veid. Denne testens resultater kan avgjøre om spyttkjertlene fungerer tilstrekkelig. Ikke nok spytt produsert kan bety at personen har SS. En alternativ test er ikke -stimulert samling av hele spyttflyt, der personen spytter i et reagensrør hvert minutt i 15 minutter. En resulterende samling på mindre enn 1,5 ml (0,053 imp fl oz; 0,051 US fl oz) regnes som et positivt resultat.
En leppe / spyttkjertel biopsi tar en vevsprøve som kan avsløre lymfocytter gruppert rundt spyttkjertler, og skade på disse kjertlene fra betennelse. Denne testen innebærer å fjerne en vevsprøve fra en persons indre leppe/spyttkjertel og undersøke den under et mikroskop . I tillegg utføres et sialogram , en spesiell røntgenundersøkelse for å se om det er blokkering i spyttkjertelkanalene (dvs. parotidkanal ) og mengden spytt som strømmer inn i munnen.
En radiologisk prosedyre er tilgjengelig som en pålitelig og nøyaktig test for Sjögrens syndrom. Et kontrastmiddel injiseres i parotidkanalen, som åpnes fra kinnet inn i munnens vestibyle motsatt halsen på den øvre andre molartannen . Histopatologiske studier skal vise fokal lymfocytisk sialadenitt . Objektive bevis på spyttkjertelintervensjon testes ved ultralydundersøkelser, nivået av ustimulerte helhet spyttstrømmen, en spyttkjertel sialografi eller spytt- scintigrafi , og autoantistoffer mot Ro (SSA) og / eller La (SSB) antigener.
Sjögrens syndrom kan utelukkes fra personer med tidligere strålebehandling i hode og nakke , ervervet immunsviktssyndrom , eksisterende lymfom , sarkoidose , transplantat-mot-vert-sykdom og bruk av antikolinerge legemidler .
Forebygging
Det finnes ingen forebyggende mekanisme for Sjögrens syndrom (SS) på grunn av kompleksiteten som en autoimmun lidelse, men endringer i livsstil kan redusere risikofaktorer knyttet til utvikling av SS eller redusere alvorlighetsgraden av tilstanden for pasienter som allerede har blitt diagnostisert. Kosthold er sterkt assosiert med betennelsen som ses i mange autoimmune sykdommer, inkludert SS. En eksperimentell studie konkluderte med at SS -pasienter ofte viser høy sensitivitet for gluten som direkte relaterer til betennelse. Moderat trening er også nyttig for SS -pasienter, og reduserer hovedsakelig effekten av lungebetennelse.
Behandling
Hverken en kur eller en spesifikk behandling for Sjogrens syndrom Det er kjent at permanent gjenopprette kjertel sekresjon . I stedet er behandlingen generelt symptomatisk og støttende.
Øyebehandling
Fuktbyttebehandlinger som kunstige tårer kan lette symptomene på tørre øyne. Noen pasienter med mer alvorlige problemer bruker vernebriller for å øke lokal luftfuktighet eller får satt inn punkteringsplugger for å beholde tårer på okulær overflate i lengre tid.
I tillegg er syklosporin (Restasis) tilgjengelig på resept for å behandle kronisk tørt øye ved å undertrykke betennelsen som forstyrrer tåresekresjon. Reseptbelagte legemidler er også tilgjengelige som bidrar til å stimulere spyttstrømmen, for eksempel cevimeline (Evoxac) og pilocarpine. Salagen , en produsert form for pilokarpin , kan brukes til å produsere tårer, samt spytt i munn og tarm. Den er avledet fra jaborandi -planten .
Vaginal tørrhet
Hos kvinner med Sjögrens syndrom rapporteres ofte tørrhet i skjeden, vulvodyni og dyspareuni (smertefullt samleie ); personlige smøremidler anbefales for å redusere irritasjon eller smerter som kan skyldes tørrhet i vaginale og vulvale områder.
Muskel -skjelett
Ikke-steroide antiinflammatoriske legemidler (NSAIDs) kan brukes til å behandle muskuloskeletale symptomer. For personer med alvorlige komplikasjoner kan kortikosteroider eller immunsuppressive legemidler foreskrives, og noen ganger intravenøse immunglobuliner . Også, sykdomsmodifiserende antireumatiske legemidler slik som metotreksat , kan være nyttig. Hydroksyklorokin (Plaquenil) er et annet alternativ og anses generelt som sikrere enn metotreksat. Disse foreskrevne legemidlene har imidlertid en rekke bivirkninger som kvalme , tap av matlyst , svimmelhet , hårtap , magesmerter/kramper , hodepine , levertoksisitet og økt risiko for infeksjoner . Også de som tar medisiner for å undertrykke immunsystemet, er mer sannsynlig å utvikle kreft senere.
Systematisk
For systemiske symptomer, inkludert tretthet, leddsmerter, myosit og nevropati , brukes ofte biologiske immunsuppressive legemidler som rituximab og belimumab som virker via B- cellepatologi og har mindre toksiske profiler enn tradisjonelle immunsuppressive regimer.
Tannhelse
Forebyggende tannbehandling er også nødvendig (og ofte oversett av pasienten), ettersom mangel på spytt forbundet med xerostomia skaper et ideelt miljø for spredning av bakterier som forårsaker hulrom . Behandlinger inkluderer hjemmelaget aktuell fluorapplikasjon for å styrke tannemaljen og hyppige tenner rengjøring av en tannhygienist. Eksisterende hulrom må også behandles, ettersom hulrom som strekker seg inn i tannen ikke kan behandles effektivt med tannrensing alene, og har stor risiko for å spre seg inn i tannmassen , noe som fører til tap av vitalitet og behov for ekstraksjon eller rot kanalbehandling . Dette behandlingsregimet er det samme som for alle xerostomipasienter, for eksempel for de som gjennomgår strålebehandling i hode og nakke, noe som ofte skader spyttkjertlene; disse kjertlene er mer utsatt for stråling enn andre kroppsvev.
Prognose
Publiserte studier om overlevelse av pasienter med Sjögrens syndrom er begrenset på forskjellige måter, kanskje på grunn av de relativt små utvalgsstørrelsene, og det faktum at sekundært Sjögrens syndrom er forbundet med andre autoimmune sykdommer. Resultater fra en rekke studier indikerer at, i forhold til andre autoimmune sykdommer, er Sjögrens syndrom assosiert med en spesielt høy forekomst av ondartet non-Hodgkin lymfom , kreft i hvite blodlegemer. Omtrent 5% av pasientene med SS utvikler en eller annen form for lymfoid malignitet . Pasienter med alvorlige tilfeller er mye mer sannsynlig å utvikle lymfomer enn pasienter med milde eller moderate tilfeller. De vanligste lymfomene er spyttekstranodale marginale sone B-cellelymfomer ( MALT-lymfomer i spyttkjertlene) og diffust stort B-cellelymfom .
Lymfomagenese hos pasienter med primær Sjögrens syndrom betraktes som en flertrinnsprosess, hvor det første trinnet er kronisk stimulering av autoimmune B -celler, spesielt B -celler som produserer revmatoid faktor på steder som er rettet mot sykdommen. Dette øker frekvensen av onkogen mutasjon , noe som fører til dysfunksjon ved sjekkpunkter for autoimmun B-celleaktivering for å transformere til malignitet. En undersøkelses funn har konkludert med den kontinuerlige stimuleringen av autoimmune B -celler, noe som fører til subtile germinale abnormiteter i gener som har spesifikke konsekvenser i B -celler, som ligger til grunn for mottakeligheten for lymfom.
Bortsett fra denne spesielt høyere forekomsten av ondartet NHL, viser Sjögrens pasienter bare beskjeden eller klinisk ubetydelig forverring av spesifikk organrelatert funksjon, noe som forklarer den eneste lille økningen i dødeligheten hos Sjögrens pasienter sammenlignet med resten av befolkningen.
Sjögrens syndrom er forbundet med en høy sykdomsbyrde, og har vist seg å redusere livskvaliteten (QoL) markant , med en betydelig innvirkning på arbeidsevnen som følge av økt funksjonshemming. Reduksjonen i QoL er lik den man ser ved andre kroniske tilstander som revmatoid artritt , lupus og fibromyalgi .
Epidemiologi
Sjögrens syndrom (SS) er den nest vanligste revmatiske autoimmune lidelsen, bak revmatoid artritt og systemisk lupus erythematosus . Det er ingen geografiske forskjeller i frekvensen av SS. Sjögrens syndrom er rapportert i alle områder av verden, selv om regionale priser ikke er godt studert. Avhengig av kriteriene for å bestemme prevalens, estimerer studier forekomsten av SS til mellom 500 000 og to millioner mennesker i USA. Bredere studier av SS -prevalens spenner vidt, med noen rapporter om opptil en prevalens på 3% av befolkningen. Noen få studier har rapportert at forekomsten av syndromet varierer mellom tre og seks per 100 000 per år.
Ni av ti SS -pasienter er kvinner. I tillegg til prevalens hos kvinner, har en førstegrads slektning med en autoimmun sykdom og tidligere svangerskap blitt identifisert som epidemiologiske risikofaktorer. Til tross for lavere risiko for menn, har primær SS hos menn en tendens til å representere en mer alvorlig form for sykdommen. Rasens og etnisitetens rolle i forekomsten av sykdommen er ukjent.
Selv om Sjögrens syndrom forekommer i alle aldersgrupper, er gjennomsnittsalderen for oppstart mellom 40 og 60 år, selv om så mange som halvparten av alle tilfellene kan stå udiagnostiserte eller urapporterte. Forekomsten av SS øker vanligvis med alderen.
Sjögrens syndrom er rapportert hos 30-50% av personer med revmatoid artritt og hos 10-25% med systemisk lupus erythematosus.
Historie
Jan Mikulicz-Radecki (1850–1905) får generelt den første beskrivelsen av SS. I 1892 beskrev han en 42 år gammel mann med utvidelse av parotid og tårekjertler forbundet med en rund-celle infiltrere og acinar atrofi . Kriteriene som Mikulicz fastsatte for diagnose førte imidlertid ofte til feildiagnostisering av Mikulicz syndrom . Mange tilstander, som tuberkulose , infeksjoner, sarkoidose og lymfom, har lignende tilstander som de som tilskrives Mikulicz syndrom. Likevel brukes begrepet "Mikulicz syndrom" fortsatt noen ganger for å beskrive utseendet til lymfocytiske infiltrater på spyttkjertelbiopsier.
I 1930 observerte Henrik Sjögren (1899–1986), en øyelege i Jönköping , Sverige , en pasient med lave sekreter fra tårene og spyttkjertlene. Sjögren introduserte begrepet keratoconjunctivitis sicca for symptomet på tørre øyne ( keratoconjunctivitis ). I 1933 publiserte han sin doktoravhandling som beskriver 19 kvinner, hvorav de fleste var postmenopausale og hadde leddgikt, som viste kliniske og patologiske manifestasjoner av syndromet. Sjögren presiserte at keratoconjunctivitis sicca, som følge av vannmangel, ikke hadde noe forhold til xerophthalmia , som følge av vitamin A -mangel. Sjögrens avhandling ble ikke godt mottatt ettersom eksamensnemnda kritiserte noen kliniske aspekter.
Etter omfattende forskning og datainnsamling publiserte Sjögren et essensielt papir i 1951, som beskriver 80 pasienter med keratoconjunctivitis sicca , hvorav 50 også hadde leddgikt. Hans påfølgende oppfølgingskonferanser knyttet til avisen hans førte til en internasjonal interesse for Sjögrens syndrom. Begrepet "keratoconjunctivitis sicca" ble laget av Sjögren selv og begynte å bli identifisert som Sjögrens syndrom i litteraturen, selv om det nå kan ha mer generell bruk.
Forskning

Forskning på multifaktorielle autoimmune sykdommer som SS fokuserer på å utvide kunnskapen rundt lidelsen, forbedre diagnostiske verktøy og finne måter å forebygge, håndtere og kurere lidelsen. Det britiske primære Sjögrens syndromregister, en vevsbiobank av prøver tatt for forskning, støttet av Medical Research Council, Storbritannia , ble opprettet i 2010. Den støtter kliniske studier og genetiske studier av Sjögrens syndrom og er åpen for de som ønsker å delta i forskningsstudier og til forskere som studerer sykdommen.
Som med andre autoimmune sykdommer påvirkes følsomheten for Sjögrens syndrom sterkt av det humane leukocyttantigenet. DQA1*05: 01, DQB1*02: 01 og DRB1*03: 01 -alleler ble identifisert som risikofaktorer , mens DQA1*02: 01, DQA1*03: 01 og DQB1*05: 01 -alleler ble funnet å være beskyttende faktorer for sykdommen. Forholdet mellom alleler og spesifikk rase ble også etablert. HLA-DQ2 og HLA-B8 finnes vanligvis hos kaukasiske pasienter, mens HLA-DR5 er relatert til greske og israelske pasienter. Flere genomsøkende assosiasjonsskanninger kan utføres i fremtiden for å identifisere viktige risikovarianter.
Virus som har vært assosiert med Sjögrens syndrom inkluderer humant T-lymfotropisk virus type 1 ( HTLV-1 ), Epstein-Barr-virus (EBV), humant immunsviktvirus (HIV), hepatitt delta-virus (HDV) og hepatitt C-virus (HCV) .
Noen undersøkelser har vist at mangel på vitamin A og vitamin D er forbundet med sykdommen. Vitamin D -mangel ble funnet å være relatert til nevrologiske manifestasjoner og tilstedeværelsen av lymfom blant pasienter, men vitamin A -nivåer var omvendt forbundet med ekstraglandulære manifestasjoner av sykdommen.
Spytt er et potensielt diagnostisk verktøy for Sjögrens syndrom fordi spyttkomponenten endres etter sykdomsutbruddet. Med den nye miniatyriseringsteknologien , kalt lab on a chip , kan diagnosen være mer praktisk.
Når det gjelder terapi, ble flere monoklonale antistoffer undersøkt i 2007. Det mest lovende syntes å være anti- CD20 rituximab og anti- CD22 epratuzumab , mens anti- TNF-α og IFN-α virket mindre effektive.
I 2014 kunngjorde Sjögrens syndromstiftelse et femårig mål om å halvere sykdommens gjennomsnittlige tid til diagnose.
Bemerkelsesverdige tilfeller
- Shannon Boxx ( amerikansk olympisk fotballspiller ) har både Sjögrens syndrom og lupus .
- Carrie Ann Inaba (sanger-skuespiller) er den nasjonale bevissthetsambassadøren og talspersonen for Sjögrens syndromstiftelse.
- Venus Williams (verdensmester tennisspiller ) har fått diagnosen Sjögrens syndrom og sa at hun hadde slitt med tretthet i årevis.
- Stephen McPhail (profesjonell fotballspiller for Irland, Leeds og Cardiff City) ble diagnostisert med lymfom og Sjögrens syndrom i en alder av 29 år.
Referanser
Eksterne linker
- Sjögren syndrom ved NHS Choices
- Sjögren syndrom - US National Institute of Arthritis og muskuloskeletale og hudsykdommer
- US Sjögrens stiftelse
- Pris, EJ; Rauz, S; Tappuni, AR; Sutcliffe, N; Hackett, KL; Barone, F; Granata, G; Ng, WF; Fisher, BA; Bombardieri, M; Astorri, E; Empson, B; Larkin, G; Crampton, B; Bowman, SJ; British Society for Rheumatology Standards, Guideline and Audit Working, Group. (1. oktober 2017). "British Society for Rheumatology -retningslinjen for behandling av voksne med primært Sjögrens syndrom" . Revmatologi . 56 (10): e24 – e48. doi : 10.1093/revmatologi/kex166 . PMID 28957550 .
| Klassifisering | |
|---|---|
| Eksterne ressurser |


