Syntetisk biologi - Synthetic biology
| Del av en serie artikler om |
| Syntetisk biologi |
|---|
| Syntetiske biologiske kretser |
| Genomredigering |
| Kunstige celler |
| Xenobiologi |
| Andre temaer |

Syntetisk biologi ( SynBio ) er et tverrfaglig forskningsområde som søker å lage nye biologiske deler, enheter og systemer, eller å redesigne systemer som allerede finnes i naturen.
Det er en vitenskapsgren som omfatter et bredt spekter av metoder fra ulike disipliner, for eksempel bioteknologi , genteknologi , molekylærbiologi , molekylær ingeniørfag , systembiologi , membranvitenskap , biofysikk , kjemisk og biologisk ingeniørfag , elektro- og datateknikk , kontrollteknikk og evolusjonær biologi .
På grunn av kraftigere gentekniske evner og reduserte DNA -syntese og sekvenseringskostnader , vokser feltet syntetisk biologi raskt. I 2016 var mer enn 350 selskaper fordelt på 40 land aktivt engasjert i applikasjoner for syntetisk biologi; alle disse selskapene hadde en estimert nettoverdi på 3,9 milliarder dollar i det globale markedet.
Definisjon
Syntetisk biologi har for tiden ingen allment akseptert definisjon. Her er noen eksempler:
- "bruk av en blanding av fysikk og genteknologi for å skape nye (og derfor syntetiske) livsformer"
- "et voksende forskningsfelt som tar sikte på å kombinere kunnskap og metoder innen biologi, ingeniørfag og relaterte disipliner i utformingen av kjemisk syntetisert DNA for å skape organismer med nye eller forbedrede egenskaper og egenskaper"
- "å designe og konstruere biologiske moduler , biologiske systemer og biologiske maskiner eller, re-design av eksisterende biologiske systemer for nyttige formål"
- "Å anvende ingeniørparadigmet for systemdesign på biologiske systemer for å produsere forutsigbare og robuste systemer med nye funksjoner som ikke eksisterer i naturen" (Europakommisjonen, 2005) Dette kan inkludere muligheten for en molekylær assembler , basert på biomolekylære systemer slik som ribosomet
Syntetisk biologi har tradisjonelt blitt delt inn i to forskjellige tilnærminger: topp ned og ned.
- The top down tilnærming innebærer å bruke metabolske og genetiske engineering teknikker for å formidle nye funksjoner til levende celler.
- Den nedenfra og opp fremgangsmåte innebærer å skape nye biologiske systemer in vitro ved å bringe sammen 'ikke-levende' biomolekylære komponenter, ofte med sikte på å bygge en kunstig celle .
Biologiske systemer settes dermed sammen modul for modul. Cellefrie proteinuttrykkssystemer brukes ofte, det samme er membranbaserte molekylære maskiner. Det er en økende innsats for å bygge bro mellom disse tilnærmingene ved å danne hybrid levende/syntetiske celler, og ingeniørkommunikasjon mellom levende og syntetiske cellepopulasjoner.
Historie
1910: Første identifiserbare bruk av begrepet "syntetisk biologi" i Stéphane Leducs publikasjon Théorie physico-chimique de la vie et générations spontanées . Han bemerket også dette begrepet i en annen publikasjon, La Biologie Synthétique i 1912.
1961: Jacob og Monod postulerer cellulær regulering av molekylære nettverk fra studiet av lac operon i E. coli og så for seg muligheten til å montere nye systemer fra molekylære komponenter.
1973: Første molekylære kloning og amplifikasjon av DNA i et plasmid er publisert i PNAS av Cohen, Boyer et al. som utgjør begynnelsen av syntetisk biologi.
1978: Arber , Nathans og Smith vinner Nobelprisen i fysiologi eller medisin for oppdagelsen av restriksjonsenzymer , noe som får Szybalski til å tilby en redaksjonell kommentar i tidsskriftet Gene :
Arbeidet med restriksjonsnukleaser lar oss ikke bare enkelt konstruere rekombinante DNA -molekyler og analysere individuelle gener, men har også ledet oss inn i den nye æra av syntetisk biologi der ikke bare eksisterende gener beskrives og analyseres, men også nye genordninger kan konstrueres og evaluert.
1988: Første DNA -amplifikasjon ved polymerasekjedereaksjonen (PCR) ved bruk av en termostabil DNA -polymerase er publisert i Science av Mullis et al. Dette unngikk å legge til nytt DNA -polymerase etter hver PCR -syklus, noe som forenklet DNA -mutagenese og montering i stor grad.
2000: To artikler i Nature rapporterer syntetiske biologiske kretser , en genetisk bryter og en biologisk klokke, ved å kombinere gener i E. coli -celler.
2003: De mest brukte standardiserte DNA -delene, BioBrick -plasmider, ble oppfunnet av Tom Knight . Disse delene vil bli sentrale i den internasjonale Genetically Engineered Machine -konkurransen (iGEM) som ble grunnlagt på MIT året etter.
2003: Forskere konstruerer en artemisinin -forløpervei i E. coli .
2004: Den første internasjonale konferansen for syntetisk biologi, Synthetic Biology 1.0 (SB1.0), holdes ved Massachusetts Institute of Technology, USA.
2005: Forskere utvikler en lysfølende krets i E. coli . En annen gruppe designer kretser som er i stand til dannelse av flercellede mønstre.
2006: Forskere konstruerer en syntetisk krets som fremmer bakteriell invasjon av tumorceller.
2010: Forskere publiserer i Science det første syntetiske bakterielle genomet, kalt M. mycoides JCVI-syn1.0. Genomet er laget av kjemisk syntetisert DNA ved bruk av gjærrekombinasjon.
2011: Funksjonelle syntetiske kromosomarmer er konstruert i gjær.
2012: Laboratorier i Charpentier og Doudna publiserer i Science programmeringen av bakteriell immunitet mot CRISPR-Cas9 for målrettet DNA-spaltning. Denne teknologien forenklet og utvidet eukaryot genredigering.
2019: Forskere ved ETH Zürich rapporterer etableringen av det første bakterielle genomet , kalt Caulobacter ethensis-2.0 , laget helt av en datamaskin, selv om en relatert levedyktig form av C. ethensis-2.0 ennå ikke eksisterer.
2019: forskere rapporterer fremstilling av et nytt syntetisk (muligens kunstig ) form av levedyktige levetid , en variant av bakterien Escherichia coli , ved å redusere det naturlige tallet av 64 kodoner i det bakterielle genomet til 59 kodoner i stedet for å kode 20 amino- syrer .
Perspektiver
Ingeniører ser på biologi som en teknologi (med andre ord, et gitt system inkluderer bioteknologi eller dets biologiske prosjektering ) Syntetisk biologi inkluderer den brede omdefinisjonen og utvidelsen av bioteknologi, med de endelige målene om å kunne designe og bygge konstruerte levende biologiske systemer som behandler informasjon , manipulere kjemikalier, fremstille materialer og strukturer, produsere energi, skaffe mat og vedlikeholde og forbedre menneskers helse, samt fremme grunnleggende kunnskap om biologiske systemer (se biomedisinsk ingeniørfag ) og miljøet vårt.
Studier i syntetisk biologi kan deles inn i brede klassifiseringer i henhold til tilnærmingen de tar til problemet: standardisering av biologiske deler, biomolekylær ingeniørfag, genomteknikk, metabolsk prosjektering.
Biomolekylær konstruksjon inkluderer tilnærminger som tar sikte på å lage et verktøykasse med funksjonelle enheter som kan introduseres for å presentere nye teknologiske funksjoner i levende celler. Genteknologi inkluderer tilnærminger for å konstruere syntetiske kromosomer eller minimale organismer som Mycoplasma laboratorium .
Biomolekylær design refererer til den generelle ideen om de novo -design og additiv kombinasjon av biomolekylære komponenter. Hver av disse tilnærmingene har en lignende oppgave: å utvikle en mer syntetisk enhet på et høyere kompleksitetsnivå ved oppfinnsomt å manipulere en enklere del på forrige nivå.
På den annen side er "omforfattere" syntetiske biologer som er interessert i å teste ureduserbarheten til biologiske systemer. På grunn av kompleksiteten i naturlige biologiske systemer, ville det være enklere å gjenoppbygge de naturlige systemene av interesse fra grunnen av; For å tilby konstruerte surrogater som er lettere å forstå, kontrollere og manipulere. Forfattere henter inspirasjon fra refactoring , en prosess som noen ganger brukes til å forbedre dataprogramvare.
Aktiverende teknologier
Flere nye aktiverende teknologier var avgjørende for suksessen til syntetisk biologi. Konseptene inkluderer standardisering av biologiske deler og hierarkisk abstraksjon for å tillate bruk av disse delene i syntetiske systemer. Grunnleggende teknologier inkluderer å lese og skrive DNA (sekvensering og fabrikasjon). Målinger under flere forhold er nødvendig for nøyaktig modellering og dataassistert design (CAD).
DNA og gensyntese
Drevet av dramatiske reduksjoner i kostnadene ved oligonukleotidsyntese ("oligos") og fremkomsten av PCR, har størrelsene på DNA -konstruksjoner fra oligoer økt til genomisk nivå. I 2000 rapporterte forskere syntese av Hepatitt C -virusgenomet på 9,6 kbp (kilo bp) fra kjemisk syntetisert 60 til 80 meter. I 2002 lyktes forskere ved Stony Brook University i å syntetisere 7741 bp poliovirus genomet fra den publiserte sekvensen, og produserte det andre syntetiske genomet, som strekker seg over to år. I 2003 ble 5386 bp -genomet til bakteriofagen Phi X 174 satt sammen på omtrent to uker. I 2006 konstruerte og patenterte det samme teamet ved J. Craig Venter Institute et syntetisk genom til en ny minimal bakterie, Mycoplasma laboratorium og arbeidet med å få det til å fungere i en levende celle.
I 2007 ble det rapportert at flere selskaper tilbød syntese av genetiske sekvenser opp til 2000 basepar (bp) lange, for en pris på omtrent $ 1 per bp og en behandlingstid på mindre enn to uker. Oligonukleotider høstet fra en fotolitografisk eller blekkskriverprodusert DNA-chip kombinert med PCR og DNA-mismatch-feilkorrigering tillater rimelige store endringer av kodoner i genetiske systemer for å forbedre genuttrykk eller inkorporere nye aminosyrer (se George M. Church 's og Anthony Forsters syntetiske celleprosjekter.) Dette favoriserer en syntese-fra-grunn-tilnærming.
I tillegg har CRISPR/Cas -systemet fremstått som en lovende teknikk for genredigering. Den ble beskrevet som "den viktigste nyvinningen innen det syntetiske biologiske rommet på nesten 30 år". Mens andre metoder tar måneder eller år å redigere gensekvenser, hastigheter CRISPR den tiden opp til uker. På grunn av brukervennligheten og tilgjengeligheten har den imidlertid reist etiske bekymringer, spesielt rundt bruken i biohacking .
Sekvensering
DNA -sekvensering bestemmer rekkefølgen på nukleotidbaser i et DNA -molekyl. Syntetiske biologer bruker DNA -sekvensering i arbeidet på flere måter. For det første fortsetter storskala genom-sekvenseringstiltak for å gi informasjon om naturlig forekommende organismer. Denne informasjonen gir et rikt underlag hvorfra syntetiske biologer kan konstruere deler og enheter. For det andre kan sekvensering verifisere at det fabrikkerte systemet er etter hensikten. For det tredje kan rask, billig og pålitelig sekvensering lette rask oppdagelse og identifisering av syntetiske systemer og organismer.
Mikrofluidikk
Mikrofluidikk , spesielt dråpemikrofluidikk, er et fremvoksende verktøy som brukes til å konstruere nye komponenter, og for å analysere og karakterisere dem. Det er mye brukt i screeninganalyser.
Modularitet
De mest brukte standardiserte DNA -delene er BioBrick -plasmider, oppfunnet av Tom Knight i 2003. Biobricks lagres på Registry of Standard Biological Parts i Cambridge, Massachusetts. BioBrick -standarden har blitt brukt av tusenvis av studenter over hele verden i den internasjonale konkurransen Genetically Engineered Machine (iGEM).
Mens DNA er viktigst for informasjonslagring, utføres en stor brøkdel av cellens aktiviteter av proteiner. Verktøy kan sende proteiner til bestemte områder av cellen og koble forskjellige proteiner sammen. Interaksjonsstyrken mellom proteinpartnere bør være justerbar mellom en levetid på sekunder (ønskelig for dynamiske signalhendelser) opp til en irreversibel interaksjon (ønskelig for enhetsstabilitet eller motstandsdyktig mot tøffe forhold). Interaksjoner som spolede spoler , SH3 -domene -peptidbinding eller SpyTag/SpyCatcher tilbyr slik kontroll. I tillegg er det nødvendig å regulere protein-protein-interaksjoner i celler, for eksempel med lys (ved bruk av lys-oksygen-spenning-sensing domener ) eller cellepermeable små molekyler ved kjemisk indusert dimerisering .
I en levende celle er molekylære motiver innebygd i et større nettverk med oppstrøms og nedstrøms komponenter. Disse komponentene kan endre signalegenskapene til modelleringsmodulen. Når det gjelder ultrasensitive moduler, kan følsomhetsbidraget til en modul avvike fra sensitiviteten som modulen opprettholder isolert.
Modellering
Modeller informerer utformingen av konstruerte biologiske systemer ved å bedre forutsi systematferd før fabrikasjon. Syntetisk biologi drar fordel av bedre modeller for hvordan biologiske molekyler binder substrater og katalyserer reaksjoner, hvordan DNA koder for informasjonen som trengs for å spesifisere cellen og hvordan multi-komponent integrerte systemer oppfører seg. Flerskala modeller av genregulerende nettverk fokuserer på applikasjoner av syntetisk biologi. Simuleringer kan modellere alle biomolekylære interaksjoner ved transkripsjon , oversettelse , regulering og induksjon av genregulerende nettverk.
Syntetiske transkripsjonsfaktorer
Studier har vurdert komponentene i DNA -transkripsjonsmekanismen . Et ønske fra forskere som lager syntetiske biologiske kretser, er å kunne kontrollere transkripsjonen av syntetisk DNA i encellede organismer ( prokaryoter ) og i flercellede organismer ( eukaryoter ). En studie testet justerbarheten av syntetiske transkripsjonsfaktorer (sTF) i områder med transkripsjonsutgang og samarbeidsevne blant flere transkripsjonsfaktorkomplekser. Forskere var i stand til å mutere funksjonelle regioner kalt sinkfingre , den DNA-spesifikke komponenten i sTF, for å redusere deres affinitet for spesifikke operatør-DNA-sekvenssteder, og dermed redusere den tilhørende stedsspesifikke aktiviteten til sTF (vanligvis transkripsjonsregulering). De brukte videre sinkfingrene som komponenter i kompleksdannende sTFer, som er de eukaryote oversettelsesmekanismene .
applikasjoner
Biologiske datamaskiner
En biologisk datamaskin refererer til et konstruert biologisk system som kan utføre datalignende operasjoner, som er et dominerende paradigme innen syntetisk biologi. Forskere bygde og karakteriserte en rekke logiske porter i en rekke organismer, og demonstrerte både analog og digital beregning i levende celler. De demonstrerte at bakterier kan konstrueres for å utføre både analog og/eller digital beregning. I menneskelige celler viste forskning en universell logikkevaluerer som opererer i pattedyrceller i 2007. Deretter brukte forskere dette paradigmet for å demonstrere en proof-of-concept-terapi som bruker biologisk digital beregning for å oppdage og drepe humane kreftceller i 2011. En annen gruppe forskere demonstrerte i 2016 at prinsipper for datateknikk kan brukes til å automatisere design av digitale kretser i bakterieceller. I 2017 demonstrerte forskere systemet `` boolsk logikk og aritmetikk gjennom DNA -eksisjon '' (BLADE) for å konstruere digital beregning i menneskelige celler. I 2019 implementerte forskere en perceptron i biologiske systemer som åpnet for maskinlæring i disse systemene.
Biosensorer
En biosensor refererer til en konstruert organisme, vanligvis en bakterie, som er i stand til å rapportere noen fenomener i omgivelsene, for eksempel tilstedeværelse av tungmetaller eller giftstoffer. Ett slikt system er det lux operonet av Aliivibrio fischeri , som koder for enzymet som er kilden for bakteriell bioluminescens , og kan plasseres etter motpart promoter for å uttrykke de luminiserende gener som respons på et spesifikt miljø stimulus. En slik sensor er laget, besto av et bioluminescent bakteriebelegg på et lysfølsomt databrikke til å oppdage visse oljeforurensninger . Når bakteriene aner forurensningen, lyser de. Et annet eksempel på en lignende mekanisme er påvisning av landminer av en konstruert E.coli -reporterstamme som er i stand til å påvise TNT og dets viktigste nedbrytningsprodukt DNT , og følgelig produsere et grønt fluorescerende protein ( GFP ).
Modifiserte organismer kan føle miljøsignaler og sende utgangssignaler som kan oppdages og tjene diagnostiske formål. Mikrokohorter har blitt brukt.
Celle transformasjon
Celler bruker samspillende gener og proteiner, som kalles genkretser, for å implementere mangfoldig funksjon, for eksempel å svare på miljøsignaler, beslutningstaking og kommunikasjon. Tre viktige komponenter er involvert: DNA, RNA og syntetisk biolog designet genkretser som kan kontrollere genuttrykk fra flere nivåer, inkludert transkripsjonelle, post-transkripsjonelle og translasjonsnivåer.
Tradisjonell metabolsk prosjektering har blitt styrket av introduksjonen av kombinasjoner av fremmede gener og optimalisering av styrt evolusjon. Dette inkluderer konstruksjon av E. coli og gjær for kommersiell produksjon av en forløper til det malariahemmende stoffet , Artemisinin .
Hele organismer har ennå ikke blitt skapt fra bunnen av, selv om levende celler kan transformeres med nytt DNA. Flere måter tillater konstruksjon av syntetiske DNA -komponenter og til og med hele syntetiske genomer , men når den ønskede genetiske koden er oppnådd, integreres den i en levende celle som forventes å manifestere de ønskede nye evnene eller fenotypene mens den vokser og blomstrer. Celletransformasjon brukes til å lage biologiske kretser , som kan manipuleres for å gi ønskede utganger.
Ved å integrere syntetisk biologi med materialvitenskap , ville det være mulig å bruke celler som mikroskopiske molekylære støperier for å produsere materialer med egenskaper hvis egenskaper var genetisk kodet. Re-engineering har produsert Curli-fibre, amyloidkomponenten i ekstracellulært materiale av biofilm , som en plattform for programmerbart nanomateriale . Disse nanofibrene ble genetisk konstruert for spesifikke funksjoner, inkludert vedheft til underlag, nanopartikkelmaler og proteinimmobilisering.
Designede proteiner
Naturlige proteiner kan for eksempel konstrueres ved rettet evolusjon , nye proteinstrukturer som matcher eller forbedrer funksjonaliteten til eksisterende proteiner, kan produseres. En gruppe genererte en helixbunt som var i stand til å binde oksygen med lignende egenskaper som hemoglobin , men bindte ikke karbonmonoksid . En lignende proteinstruktur ble generert for å støtte en rekke oksidoreduktaseaktiviteter , mens en annen dannet en strukturelt og sekvensielt ny ATPase . En annen gruppe genererte en familie av G-proteinkoblede reseptorer som kunne aktiveres av det inerte småmolekylet clozapine N-oksid, men ufølsomt for den native liganden , acetylkolin ; disse reseptorene er kjent som DREADDs . Nye funksjoner eller proteinspesifisitet kan også konstrueres ved hjelp av beregningsmessige tilnærminger. En studie var i stand til å bruke to forskjellige beregningsmetoder - en bioinformatikk og molekylær modelleringsmetode for å gruve sekvensdatabaser, og en beregningsmetode for enzymdesign for å omprogrammere enzymspesifisitet. Begge metodene resulterte i designet enzymer med mer enn 100 ganger spesifisitet for produksjon av lengre kjede alkoholer fra sukker.
En annen vanlig undersøkelse er utvidelse av det naturlige settet med 20 aminosyrer . Utenom stoppkodoner er 61 kodoner identifisert, men bare 20 aminosyrer er generelt kodet i alle organismer. Enkelte kodoner er konstruert for å kode for alternative aminosyrer inkludert: ikke-standardiserte aminosyrer som O- metyltyrin ; eller eksogene aminosyrer som 4-fluorfenylalanin. Vanligvis disse prosjektene gjøre bruk av re-kodet tull suppressor tRNA - Aminoacyl tRNA syntetase par fra andre organismer, men i de fleste tilfeller betydelig ingeniør er nødvendig.
Andre forskere undersøkte proteinstruktur og funksjon ved å redusere det normale settet med 20 aminosyrer. Begrensede proteinsekvensbiblioteker lages ved å generere proteiner der grupper av aminosyrer kan erstattes av en enkelt aminosyre. For eksempel kan flere upolare aminosyrer i et protein alle erstattes med en enkelt upolar aminosyre. Ett prosjekt viste at en konstruert versjon av Chorismate -mutase fortsatt hadde katalytisk aktivitet når bare 9 aminosyrer ble brukt.
Forskere og selskaper praktiserer syntetisk biologi for å syntetisere industrielle enzymer med høy aktivitet, optimale utbytter og effektivitet. Disse syntetiserte enzymene tar sikte på å forbedre produkter som vaskemidler og laktosefrie meieriprodukter, samt gjøre dem mer kostnadseffektive. Forbedringene av stoffskifte av syntetisk biologi er et eksempel på en bioteknologisk teknikk som brukes i industrien for å oppdage legemidler og fermenterende kjemikalier. Syntetisk biologi kan undersøke modulære banesystemer i biokjemisk produksjon og øke utbyttet av metabolsk produksjon. Kunstig enzymatisk aktivitet og påfølgende effekter på metabolske reaksjonshastigheter og utbytter kan utvikle "effektive nye strategier for å forbedre celleegenskaper ... for industrielt viktig biokjemisk produksjon".
Designede nukleinsyresystemer
Forskere kan kode digital informasjon på en enkelt tråd av syntetisk DNA . I 2012 kodet George M. Church en av bøkene hans om syntetisk biologi i DNA. 5.3 Mb data var mer enn 1000 ganger større enn den tidligere største mengden informasjon som skulle lagres i syntetisert DNA. Et lignende prosjekt kodet de komplette sonettene til William Shakespeare i DNA. Mer generelt muliggjør algoritmer som NUPACK, ViennaRNA, Ribosome Binding Site Calculator, Cello og Non-Repetitive Parts Calculator design av nye genetiske systemer.
Mange teknologier er utviklet for å inkorporere unaturlige nukleotider og aminosyrer i nukleinsyrer og proteiner, både in vitro og in vivo . For eksempel kunngjorde forskere i mai 2014 at de med hell hadde introdusert to nye kunstige nukleotider i bakterielt DNA. Ved å inkludere individuelle kunstige nukleotider i kulturmediene, var de i stand til å utveksle bakteriene 24 ganger; de genererte ikke mRNA eller proteiner som var i stand til å bruke de kunstige nukleotidene.
Utforsking av verdensrommet
Syntetisk biologi økte NASAs interesse da det kunne bidra til å produsere ressurser for astronauter fra en begrenset portefølje av forbindelser sendt fra jorden. Spesielt på Mars kan syntetisk biologi føre til produksjonsprosesser basert på lokale ressurser, noe som gjør den til et kraftig verktøy i utviklingen av bemannede utposter med mindre avhengighet av jorden. Det er arbeidet med å utvikle plantestammer som er i stand til å takle det harde Mars -miljøet, ved å bruke lignende teknikker som de som brukes for å øke motstandskraften mot visse miljøfaktorer i landbruksavlinger.
Syntetisk liv
Et viktig tema i syntetisk biologi er syntetisk liv , som er opptatt av hypotetiske organismer skapt in vitro fra biomolekyler og/eller kjemiske analoger derav . Syntetiske livseksperimenter prøver å enten undersøke livets opprinnelse , studere noen av livets egenskaper, eller mer ambisiøst å gjenskape liv fra ikke-levende ( abiotiske ) komponenter. Syntetisk livsbiologi prøver å skape levende organismer som kan utføre viktige funksjoner, fra produksjon av legemidler til avgiftning av forurenset land og vann. Innen medisin gir det muligheter for å bruke designerbiologiske deler som utgangspunkt for nye klasser av terapier og diagnostiske verktøy.
En levende "kunstig celle" er definert som en helt syntetisk celle som kan fange energi , opprettholde ionegradienter , inneholde makromolekyler samt lagre informasjon og ha evnen til å mutere . Ingen har klart å lage en slik celle.
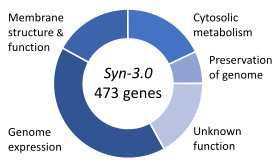
Et helt syntetisk bakteriekromosom ble produsert i 2010 av Craig Venter , og teamet hans introduserte det for genomisk tømte bakterielle vertsceller. Vertscellene var i stand til å vokse og replikere. Den Mycoplasma laboratorium er den eneste levende organisme med helt konstruert genom.
Den første levende organismen med 'kunstig' utvidet DNA -kode ble presentert i 2014; teamet brukte E. coli som hadde sitt genom ekstrahert og erstattet med et kromosom med en utvidet genetisk kode. De nukleosider lagt er d5SICS og dNaM .
I mai 2019 forskere, i en milepæl innsats, rapporterte dannelsen av en ny syntetisk (muligens kunstig ) form av levedyktige levetid , en variant av bakterier Escherichia coli , ved å redusere det naturlige tallet av 64 kodoner i det bakterielle genomet til 59 kodoner i stedet for å kode 20 aminosyrer .
I 2017 ble det internasjonale Build-a-Cell -forskningssamarbeidet for bygging av syntetisk levende celle startet, etterfulgt av nasjonale syntetiske celleorganisasjoner i flere land, inkludert FabriCell, MaxSynBio og BaSyC. Den europeiske innsatsen for syntetiske celler ble samlet i 2019 som SynCellEU -initiativ.
Legemiddelleveringsplattformer
Konstruert bakteriebasert plattform
Bakterier har lenge vært brukt i kreftbehandling. Bifidobacterium og Clostridium koloniserer selektivt svulster og reduserer størrelsen. Nylig omprogrammerte syntetiske biologer bakterier for å føle og svare på en bestemt krefttilstand. Oftest brukes bakterier for å levere et terapeutisk molekyl direkte til svulsten for å minimere effekter utenfor målet. For å målrette tumorcellene ble peptider som spesifikt kan gjenkjenne en svulst uttrykt på overflatene til bakterier. Peptider som brukes inkluderer et affibody -molekyl som spesifikt retter seg mot reseptor 2 for epidermal vekstfaktor hos mennesker og et syntetisk adhesin . Den andre måten er å la bakterier fornemme svulstmikromiljøet , for eksempel hypoksi, ved å bygge en OG logisk port inn i bakterier. Bakteriene frigjør da bare terapeutiske målmolekyler til svulsten gjennom enten lysis eller bakteriesekresjonssystemet . Lysis har fordelen at den kan stimulere immunsystemet og kontrollere vekst. Flere typer sekresjonssystemer kan brukes og andre strategier også. Systemet kan induceres av eksterne signaler. Indusere inkluderer kjemikalier, elektromagnetiske eller lysbølger.
Flere arter og stammer blir anvendt i disse terapiene. Mest brukte bakterier er Salmonella typhimurium , Escherichia Coli , Bifidobacteria , Streptococcus , Lactobacillus , Listeria og Bacillus subtilis . Hver av disse artene har sin egen eiendom og er unik for kreftbehandling når det gjelder vevskolonisering, interaksjon med immunsystemet og enkel påføring.
Cellebasert plattform
Immunsystemet spiller en viktig rolle i kreft og kan utnyttes for å angripe kreftceller. Cellebaserte terapier fokuserer på immunterapier , for det meste ved å konstruere T-celler .
T -celle reseptorer ble konstruert og 'trent' for å oppdage kreftepitoper . Kimære antigenreseptorer (CAR) er sammensatt av et fragment av et antistoff smeltet til intracellulære T -cellesignaleringsdomener som kan aktivere og utløse spredning av cellen. En andre generasjon CAR-basert terapi ble godkjent av FDA.
Genbrytere ble designet for å øke sikkerheten ved behandlingen. Drepbrytere ble utviklet for å avslutte behandlingen hvis pasienten skulle vise alvorlige bivirkninger. Mekanismer kan finere kontrollere systemet og stoppe og aktivere det på nytt. Siden antall T-celler er viktige for terapiens utholdenhet og alvorlighetsgrad, blir veksten av T-celler også kontrollert for å slå effekten og sikkerheten til terapier.
Selv om flere mekanismer kan forbedre sikkerhet og kontroll, inkluderer begrensninger vanskeligheten med å indusere store DNA -kretser inn i cellene og risiko forbundet med å introdusere fremmede komponenter, spesielt proteiner, i celler.
Etikk
Opprettelsen av nytt liv og manipulering av eksisterende liv har reist etiske bekymringer innen syntetisk biologi og diskuteres aktivt.
Vanlige etiske spørsmål inkluderer:
- Er det moralsk riktig å tukle med naturen?
- Spiller man Gud når han skaper nytt liv?
- Hva skjer hvis en syntetisk organisme ved et uhell slipper unna?
- Hva om en person misbruker syntetisk biologi og skaper en skadelig enhet (f.eks. Et biologisk våpen)?
- Hvem skal ha kontroll over og tilgang til produktene av syntetisk biologi?
- Hvem vil tjene på disse innovasjonene? Investorer? Medisinske pasienter? Industrielle bønder?
- Tillater patentsystemet patenter på levende organismer? Hva med deler av organismer, som HIV -resistensgener hos mennesker?
- Hva om en ny skapelse fortjener moralsk eller juridisk status?
De etiske aspektene ved syntetisk biologi har tre hovedtrekk: biosikkerhet, biosikkerhet og skapelse av nye livsformer. Andre etiske spørsmål som er nevnt inkluderer regulering av nye kreasjoner, patentbehandling av nye kreasjoner, fordeling av fordeler og forskningsintegritet.
Etiske spørsmål har dukket opp for rekombinant DNA og genetisk modifiserte organismer (GMO) teknologier og omfattende forskrifter for genteknologi og patogenforskning var på plass i mange jurisdiksjoner. Amy Gutmann , tidligere sjef for Presidential Bioethics Commission, hevdet at vi bør unngå fristelsen til å overregulere syntetisk biologi generelt, og genteknologi spesielt. Ifølge Gutmann, "Regulatory parsimony er spesielt viktig i nye teknologier ... hvor fristelsen til å kvele innovasjon på grunnlag av usikkerhet og frykt for det ukjente er spesielt stor. De sløvede instrumentene for lovfestet og regulatorisk begrensning kan ikke bare hemme fordelingen nye fordeler, men kan være kontraproduktivt for sikkerhet og sikkerhet ved å hindre forskere i å utvikle effektive sikkerhetstiltak. ".
Livets "skapelse"
Et etisk spørsmål er om det er akseptabelt å lage nye livsformer, noen ganger kjent som "å spille Gud". Foreløpig er opprettelsen av nye livsformer som ikke er tilstede i naturen i liten skala, de potensielle fordelene og farene er ukjente, og nøye vurdering og tilsyn er sikret for de fleste studier. Mange talsmenn uttrykker den store potensielle verdien - blant annet for landbruk, medisin og akademisk kunnskap - ved å lage kunstige livsformer. Opprettelse av nye enheter kan utvide vitenskapelig kunnskap langt utover det som for tiden er kjent fra å studere naturfenomener. Likevel er det bekymring for at kunstige livsformer kan redusere naturens "renhet" (dvs. at naturen på en eller annen måte kan bli ødelagt av menneskelig inngrep og manipulasjon) og potensielt påvirke vedtakelsen av mer ingeniørlignende prinsipper i stedet for biologisk mangfold og naturfokuserte idealer. Noen er også bekymret for at hvis en kunstig livsform skulle slippes ut i naturen, kan det hemme biologisk mangfold ved å slå ut naturlige arter for ressurser (i likhet med hvordan algeblomster dreper marine arter). En annen bekymring innebærer etisk behandling av nyopprettede enhetene hvis de tilfeldigvis følelse smerte , sentience og selvoppfatning. Skal slikt liv gis moralske eller juridiske rettigheter? I så fall, hvordan?
Biosikkerhet og bioinnhold
Hva er mest etisk hensiktsmessig når man vurderer biosikkerhetstiltak? Hvordan kan man unngå utilsiktet introduksjon av syntetisk liv i det naturlige miljøet? Mye etisk omtanke og kritisk tanke har blitt gitt til disse spørsmålene. Biosikkerhet refererer ikke bare til biologisk inneslutning; det refererer også til fremskritt for å beskytte publikum mot potensielt farlige biologiske agenser. Selv om slike bekymringer er viktige og forblir ubesvarte, er det ikke alle produkter av syntetisk biologi som bekymrer seg for biologisk sikkerhet eller negative konsekvenser for miljøet. Det argumenteres for at de fleste syntetiske teknologier er godartede og ikke er i stand til å blomstre i omverdenen på grunn av deres "unaturlige" egenskaper, ettersom det ennå ikke er et eksempel på en transgen mikrobe som har en treningsfordel i naturen.
Generelt anses eksisterende farekontroller , risikovurderingsmetoder og forskrifter utviklet for tradisjonelle genetisk modifiserte organismer (GMOer) som tilstrekkelige for syntetiske organismer. " Ekstrinsiske " bioinneslutningsmetoder i laboratoriekontekst inkluderer fysisk inneslutning gjennom biosikkerhetsskap og hanskerom , samt personlig verneutstyr . I en landbrukssammenheng inkluderer de isolasjonsavstander og pollen barrierer, i likhet med fremgangsmåter for biocontainment av GMO . Syntetiske organismer kan tilby økt farekontroll fordi de kan konstrueres med "iboende" bioinneslutningsmetoder som begrenser deres vekst i et ubehandlet miljø, eller forhindrer horisontal genoverføring til naturlige organismer. Eksempler på indre biocontainment omfatter auxotrofi , biologiske drepe brytere , manglende evne til organismen for å replikere eller for å passere modifiserte eller syntetiske gener til avkom, og bruken av xenobiological organismer ved bruk av alternative biokjemi, for eksempel ved anvendelse av kunstig xeno nukleinsyrer (XNA) i stedet for DNA . Når det gjelder auxotrofi, kan bakterier og gjær konstrueres til å ikke være i stand til å produsere histidin , en viktig aminosyre for alt liv. Slike organismer kan dermed bare dyrkes på histidinrike medier under laboratorieforhold, noe som opphever frykten for at de kan spre seg til uønskede områder.
Biosikkerhet
Noen etiske spørsmål angår biosikkerhet, der biosyntetiske teknologier bevisst kan brukes til å skade samfunnet og/eller miljøet. Siden syntetisk biologi reiser etiske spørsmål og biosikkerhetsspørsmål, må menneskeheten vurdere og planlegge hvordan de skal håndtere potensielt skadelige skapninger, og hva slags etiske tiltak som eventuelt kan brukes for å avskrekke fryktelige biosyntetiske teknologier. Med unntak av regulering av syntetiske biologiske og bioteknologiske selskaper, blir problemstillingene imidlertid ikke sett på som nye fordi de ble tatt opp under tidligere rekombinant DNA og genetisk modifiserte organismer (GMO) debatter og omfattende forskrifter for genteknologi og patogenforskning er allerede på plass i mange jurisdiksjoner.
Den Europeiske Union
Det EU -finansierte prosjektet SYNBIOSAFE har gitt ut rapporter om hvordan man håndterer syntetisk biologi. Et papir fra 2007 identifiserte viktige spørsmål innen sikkerhet, sikkerhet, etikk og grensesnittet mellom vitenskap og samfunn, som prosjektet definerte som offentlig utdanning og pågående dialog mellom forskere, bedrifter, myndigheter og etikkere. De viktigste sikkerhetsspørsmålene som SYNBIOSAFE identifiserte, involverte engasjerende selskaper som selger syntetisk DNA og biohacking -samfunnet av amatørbiologer. Sentrale etiske spørsmål gjaldt opprettelsen av nye livsformer.
En påfølgende rapport fokuserte på biosikkerhet, spesielt den såkalte dual-use- utfordringen. Selv om syntetisk biologi for eksempel kan føre til mer effektiv produksjon av medisinske behandlinger, kan det også føre til syntese eller modifikasjon av skadelige patogener (f.eks. Kopper ). Biohackingsamfunnet er fortsatt en kilde til spesiell bekymring, ettersom den distribuerte og diffuse naturen til bioteknologi med åpen kildekode gjør det vanskelig å spore, regulere eller dempe potensielle bekymringer om biosikkerhet og biosikkerhet.
COZY, et annet europeisk initiativ, fokuserer på offentlig oppfatning og kommunikasjon. For bedre å kommunisere syntetisk biologi og dens samfunnsmessige konsekvenser til et bredere publikum, publiserte COZY og SYNBIOSAFE SYNBIOSAFE , en 38 minutter lang dokumentarfilm, i oktober 2009.
International Association Synthetic Biology har foreslått selvregulering. Dette foreslår spesifikke tiltak som den syntetiske biologiindustrien, spesielt DNA -synteseselskaper, bør iverksette. I 2007 publiserte en gruppe ledet av forskere fra ledende DNA-synteseselskaper en "praktisk plan for å utvikle et effektivt tilsynsramme for DNA-synteseindustrien".
forente stater
I januar 2009 finansierte Alfred P. Sloan Foundation Woodrow Wilson Center , Hastings Center og J. Craig Venter Institute for å undersøke offentlig oppfatning, etikk og politiske implikasjoner av syntetisk biologi.
9. - 10. juli 2009 innkalte National Academies 'Committee of Science, Technology & Law til et symposium om "Opportunities and Challenges in the Emerging Field of Synthetic Biology".
Etter utgivelsen av den første syntetiske genomet og medfølgende medieoppslag om "liv" som blir opprettet, president Barack Obama etablerte Presidential Commission for studier av bioetiske spørsmål å studere syntetisk biologi. Kommisjonen innkalte til en serie møter og ga ut en rapport i desember 2010 med tittelen "New Directions: The Ethics of Synthetic Biology and Emerging Technologies." Kommisjonen uttalte at "mens Venters prestasjon markerte et betydelig teknisk fremskritt for å demonstrere at et relativt stort genom kunne nøyaktig syntetiseres og erstattes med et annet, utgjorde det ikke" livets opprettelse ". Det bemerket at syntetisk biologi er et voksende felt , som skaper potensielle risikoer og fordeler. Kommisjonen anbefalte ikke endringer i retningslinjer eller tilsyn og ba om fortsatt finansiering av forskningen og nye midler til overvåking, studier av nye etiske spørsmål og offentlig utdannelse.
Syntetisk biologi, som et viktig verktøy for biologiske fremskritt, resulterer i "potensialet for å utvikle biologiske våpen, mulige uforutsette negative effekter på menneskers helse ... og potensiell miljøpåvirkning". Spredning av slik teknologi kan også gjøre produksjonen av biologiske og kjemiske våpen tilgjengelig for et bredere spekter av statlige og ikke-statlige aktører . Disse sikkerhetsspørsmålene kan unngås ved å regulere industriens bruk av bioteknologi gjennom politikklovgivning. Føderale retningslinjer for genetisk manipulasjon blir foreslått av "Presidentens bioetiske kommisjon ... som svar på den kunngjorte opprettelsen av en selvreplikerende celle fra et kjemisk syntetisert genom, fremmet 18 anbefalinger, ikke bare for å regulere vitenskapen ... for å utdanne offentligheten".
Motstand
13. mars 2012 ga over 100 miljø- og sivilsamfunnsgrupper, inkludert Friends of the Earth , International Center for Technology Assessment og ETC Group ut manifestet The Principles for the Oversight of Syntetic Biology . Dette manifestet krever et verdensomspennende moratorium for frigjøring og kommersiell bruk av syntetiske organismer inntil mer robuste forskrifter og strenge biosikkerhetstiltak er etablert. Gruppene krever spesielt et direkte forbud mot bruk av syntetisk biologi på det menneskelige genomet eller det menneskelige mikrobiomet . Richard Lewontin skrev at noen av sikkerhetsprinsippene for tilsyn som er omtalt i The Principles for the Oversight of Synthetic Biology er rimelige, men at hovedproblemet med anbefalingene i manifestet er at "publikum generelt mangler evnen til å håndheve noen meningsfull erkjennelse av disse anbefalingene ".
Helse og sikkerhet
Farene ved syntetisk biologi inkluderer farer for biosikkerhet for arbeidere og publikum, farer for biosikkerhet som følge av bevisst konstruksjon av organismer for å forårsake skade, og miljøfarer. Biosikkerhetsrisikoen er lik den for eksisterende bioteknologiske felt, hovedsakelig eksponering for patogener og giftige kjemikalier, selv om nye syntetiske organismer kan ha nye farer. For biosikkerhet er det bekymring for at syntetiske eller redesignede organismer teoretisk sett kan brukes til bioterrorisme . Potensielle risikoer inkluderer å gjenskape kjente patogener fra bunnen av, konstruere eksisterende patogener for å være farligere og konstruere mikrober for å produsere skadelige biokjemikalier. Til slutt inkluderer miljøfarer negative effekter på biologisk mangfold og økosystemtjenester , inkludert potensielle endringer i arealbruken som følge av landbruksbruk av syntetiske organismer.
Eksisterende risikoanalysesystemer for GMO anses generelt som tilstrekkelige for syntetiske organismer, selv om det kan være vanskeligheter for en organisme som er bygget "bottom-up" fra individuelle genetiske sekvenser. Syntetisk biologi faller generelt under eksisterende forskrifter for GMO og bioteknologi generelt, og eventuelle forskrifter som eksisterer for kommersielle produkter nedstrøms, selv om det vanligvis ikke er noen forskrifter i noen jurisdiksjon som er spesifikke for syntetisk biologi.
Se også
- ACS Synthetic Biology (tidsskrift)
- Bioingeniør
- Biomimikk
- Carlson Curve
- Chiral livskonsept
- Beregningsbiologi
- Beregningsmessig biomodellering
- DNA digital datalagring
- Ingeniørbiologi
- Internasjonal genetisk konstruert maskin
- Ikke-cellulært liv
- Åpen syntetisk biologi
- Regenerativ medisin
- Syntetisk intelligens
- Syntetisk morfologi
- Syntetisk virologi
- Systems and Synthetic Biology (tidsskrift)
- Vevsteknikk
- Xenobiologi
Referanser
Bibliografi
- Church, George; Regis, Ed (2012). Hvordan syntetisk biologi vil gjenoppfinne naturen og oss selv . New York, NY: Basic Books . ISBN 978-0465021758.
- Europakommisjonen (2016) Syntetisk biologi og biologisk mangfold ; Science for Environmental Policy (2016); Fremtidsbeskrivelse 15. Produsert for EU -kommisjonens generaldirektorat for miljø av Science Communication Unit, UWE, Bristol. [1] , PDF, 36 sider.
- Venter, Craig (2013). Livet med lysets hastighet: The Double Helix and the Dawn of Digital Life . New York, NY: Penguin Books. ISBN 978-0670025404.
Eksterne linker
- Syntetiske biologibøker populærvitenskapelige bøker og lærebøker
- Innledende oppsummering av syntetisk biologi . Kortfattet oversikt over syntetiske biologikonsepter, utvikling og applikasjoner
- Kollaborativ oversiktsartikkel om syntetisk biologi
- Kontroversiell oppstart av DNA ønsker å la kundene lage skapninger (2015-01-03), San Francisco Chronicle
- It's Alive, but Is It Life: Synthetic Biology and the Future of Creation (28. september 2016), World Science Festival