Tuberkulose -Tuberculosis
| Tuberkulose | |
|---|---|
| Andre navn | Phthisis, phthisis pulmonalis, forbruk, stor hvit pest |
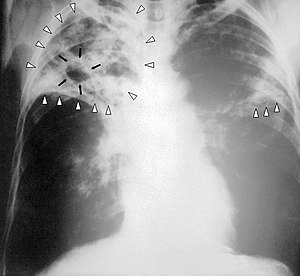 | |
| Røntgen thorax av en person med avansert tuberkulose: Infeksjon i begge lungene er markert med hvite pilspisser, og dannelsen av et hulrom er markert med svarte piler. | |
| Spesialitet | Infeksiøs sykdom , lungesykdommer |
| Symptomer | Kronisk hoste , feber , hoste med blodig slim , vekttap |
| Årsaker | Mycobacterium tuberculosis |
| Risikofaktorer | Røyking, HIV/AIDS |
| Diagnostisk metode | CXR , kultur , tuberkulin hudtest , QuantiFERON |
| Differensialdiagnose | Lungebetennelse , histoplasmose , sarkoidose , coccidioidomycosis |
| Forebygging | Screening av de med høy risiko, behandling av de smittede, vaksinasjon med basillen Calmette-Guérin (BCG) |
| Behandling | Antibiotika |
| Frekvens | 25 % av menneskene (latent TB) |
| Dødsfall | 1,5 millioner (2020) |
Tuberkulose ( TB ) er en infeksjonssykdom vanligvis forårsaket av Mycobacterium tuberculosis (MTB) bakterier . Tuberkulose påvirker vanligvis lungene , men det kan også påvirke andre deler av kroppen. De fleste infeksjoner viser ingen symptomer, i så fall er det kjent som latent tuberkulose . Rundt 10 % av latente infeksjoner utvikler seg til aktiv sykdom som, hvis den ikke behandles, dreper omtrent halvparten av de som rammes. Typiske symptomer på aktiv tuberkulose er kronisk hoste med blodholdig slim , feber , nattesvette og vekttap . Det ble historisk referert til som forbruk på grunn av vekttapet forbundet med sykdommen. Infeksjon av andre organer kan forårsake et bredt spekter av symptomer.
Tuberkulose spres fra en person til en annen gjennom luften når personer som har aktiv tuberkulose i lungene hoster, spytter, snakker eller nyser . Personer med latent tuberkulose sprer ikke sykdommen. Aktiv infeksjon forekommer oftere hos personer med hiv/aids og hos de som røyker . Diagnose av aktiv tuberkulose er basert på røntgen thorax , samt mikroskopisk undersøkelse og dyrking av kroppsvæsker. Diagnose av latent TB er avhengig av tuberkulin hudtest (TST) eller blodprøver.
Forebygging av tuberkulose innebærer screening av personer med høy risiko, tidlig oppdagelse og behandling av tilfeller, og vaksinasjon med basillen Calmette-Guérin (BCG) vaksine. De med høy risiko inkluderer husholdning, arbeidsplass og sosiale kontakter til personer med aktiv tuberkulose. Behandling krever bruk av flere antibiotika over lang tid. Antibiotikaresistens er et økende problem med økende forekomst av multippel medikamentresistent tuberkulose (MDR-TB).
I 2018 ble en fjerdedel av verdens befolkning antatt å ha en latent infeksjon av tuberkulose. Nye infeksjoner forekommer i omtrent 1 % av befolkningen hvert år. I 2020 utviklet anslagsvis 10 millioner mennesker aktiv tuberkulose, noe som resulterte i 1,5 millioner dødsfall, noe som gjør det til den nest største dødsårsaken fra en smittsom sykdom etter COVID-19 . Fra og med 2018 skjedde de fleste tuberkulosetilfellene i regionene i Sørøst-Asia (44%), Afrika (24%) og det vestlige Stillehavet (18%), med mer enn 50% av tilfellene diagnostisert i syv land: India (27 %), Kina (9 %), Indonesia (8 %), Filippinene (6 %), Pakistan (6 %), Nigeria (4 %) og Bangladesh (4 %). Innen 2021 gikk antallet nye tilfeller hvert år ned med rundt 2 % årlig. Omtrent 80 % av mennesker i mange asiatiske og afrikanske land tester positivt, mens 5–10 % av befolkningen i USAs befolkning tester positivt via tuberkulintesten. Tuberkulose har vært tilstede hos mennesker siden antikken .
Tegn og symptomer
Tuberkulose kan infisere hvilken som helst del av kroppen, men forekommer oftest i lungene (kjent som lungetuberkulose). Ekstrapulmonal TB oppstår når tuberkulose utvikler seg utenfor lungene, selv om ekstrapulmonal TB kan eksistere samtidig med lunge-TB.
Generelle tegn og symptomer inkluderer feber, frysninger , nattesvette, tap av matlyst , vekttap og tretthet . Betydelig negleklubbing kan også forekomme.
Pulmonal
Hvis en tuberkuloseinfeksjon blir aktiv, involverer den oftest lungene (i omtrent 90 % av tilfellene). Symptomer kan inkludere brystsmerter og langvarig hoste som produserer oppspytt. Omtrent 25 % av menneskene har kanskje ingen symptomer (dvs. de forblir asymptomatiske). Noen ganger kan folk hoste opp blod i små mengder, og i svært sjeldne tilfeller kan infeksjonen erodere inn i lungearterien eller en Rasmussens aneurisme , noe som resulterer i massiv blødning. Tuberkulose kan bli en kronisk sykdom og forårsake omfattende arrdannelse i øvre lungelapper. De øvre lungelappene er hyppigere rammet av tuberkulose enn de nedre. Årsaken til denne forskjellen er ikke klar. Det kan skyldes enten bedre luftstrøm, eller dårlig lymfedrenasje i de øvre lungene.
Ekstrapulmonal
I 15–20 % av de aktive tilfellene sprer infeksjonen seg utenfor lungene og forårsaker andre typer tuberkulose. Disse er samlet betegnet som ekstrapulmonal tuberkulose. Ekstrapulmonal TB forekommer oftere hos personer med svekket immunforsvar og små barn. Hos de med HIV forekommer dette i mer enn 50 % av tilfellene. Bemerkelsesverdige ekstrapulmonale infeksjonssteder inkluderer pleura (i tuberkuløs pleuritt), sentralnervesystemet (i tuberkuløs meningitt ), lymfesystemet (i scrofula i nakken), genitourinærsystemet (i urogenital tuberkulose ) og bein og ledd (i Pott sykdom i ryggraden), blant andre. En potensielt mer alvorlig, utbredt form for tuberkulose kalles "utbredt tuberkulose", det er også kjent som miliær tuberkulose . Miliær tuberkulose utgjør i dag omtrent 10 % av ekstrapulmonale tilfeller.
Årsaker
Mykobakterier

Hovedårsaken til tuberkulose er Mycobacterium tuberculosis (MTB), en liten, aerob , ikke -bevegelig basill . Det høye lipidinnholdet til dette patogenet står for mange av dets unike kliniske egenskaper. Den deler seg hver 16. til 20. time, som er en ekstremt langsom hastighet sammenlignet med andre bakterier, som vanligvis deler seg på mindre enn en time. Mykobakterier har et ytre membran- lipid-dobbeltlag. Hvis en Gram-farging utføres, farger MTB enten svært svakt "Gram-positiv" eller beholder ikke fargestoffet som følge av det høye lipid- og mykolsyreinnholdet i celleveggen. MTB tåler svake desinfeksjonsmidler og overlever i tørr tilstand i flere uker. I naturen kan bakterien bare vokse innenfor cellene til en vertsorganisme , men M. tuberculosis kan dyrkes i laboratoriet .
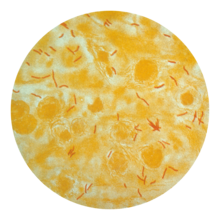
Ved å bruke histologiske flekker på ekspektorerte prøver fra slim (også kalt sputum), kan forskere identifisere MTB under et mikroskop. Siden MTB beholder visse flekker selv etter å ha blitt behandlet med sur løsning, er den klassifisert som en syrefast basill . De vanligste syrefaste fargingsteknikkene er Ziehl–Neelsen- beisen og Kinyoun-flekken , som farger syrefaste basiller en knallrød som skiller seg ut mot en blå bakgrunn. Auramin-rhodamin-farging og fluorescensmikroskopi brukes også.
M. tuberculosis - komplekset ( MTBC ) inkluderer fire andre TB-forårsakende mykobakterier : M. bovis , M. africanum , M. canetti og M. microti . M. africanum er ikke utbredt, men det er en betydelig årsak til tuberkulose i deler av Afrika. M. bovis var en gang en vanlig årsak til tuberkulose, men introduksjonen av pasteurisert melk har nesten eliminert dette som et folkehelseproblem i utviklede land. M. canetti er sjelden og ser ut til å være begrenset til Afrikas horn , selv om noen få tilfeller har blitt sett hos afrikanske emigranter. M. microti er også sjelden og sees nesten bare hos personer med immundefekt, selv om prevalensen kan være betydelig undervurdert.
Andre kjente patogene mykobakterier inkluderer M. leprae , M. avium og M. kansasii . De to sistnevnte artene er klassifisert som " ikke-tuberkuløse mykobakterier " (NTM) eller atypiske mykobakterier. NTM forårsaker verken TB eller spedalskhet , men de forårsaker lungesykdommer som ligner TB.
Overføring
Når personer med aktiv lunge-TB hoster, nyser, snakker, synger eller spytter, utviser de smittsomme aerosoldråper med en diameter på 0,5 til 5,0 µm . Et enkelt nys kan frigjøre opptil 40 000 dråper. Hver av disse dråpene kan overføre sykdommen, siden den smittsomme dosen av tuberkulose er svært liten (innånding av færre enn 10 bakterier kan forårsake en infeksjon).
Risiko for overføring
Personer med langvarig, hyppig eller nær kontakt med mennesker med tuberkulose har spesielt høy risiko for å bli smittet, med en anslått infeksjonsrate på 22 %. En person med aktiv, men ubehandlet tuberkulose kan smitte 10–15 (eller flere) andre per år. Smitte bør kun skje fra personer med aktiv tuberkulose – de med latent infeksjon antas ikke å være smittsom. Sannsynligheten for overføring fra en person til en annen avhenger av flere faktorer, inkludert antall smittsomme dråper som sendes ut av bæreren, effektiviteten av ventilasjon, varigheten av eksponeringen, virulensen til M. tuberculosis - stammen , nivået av immunitet i uinfisert person og andre. Kaskaden av spredning fra person til person kan omgås ved å skille de med aktiv ("åpen") TB og sette dem på anti-TB medikamentregimer. Etter omtrent to uker med effektiv behandling forblir ikke personer med ikke-resistente aktive infeksjoner generelt smittsomme for andre. Hvis noen blir smittet, tar det vanligvis tre til fire uker før den nylig smittede personen blir smittsom nok til å overføre sykdommen til andre.
Risikofaktorer
En rekke faktorer gjør individer mer utsatt for tuberkuloseinfeksjon og/eller sykdom.
Aktiv sykdomsrisiko
Den viktigste risikofaktoren globalt for å utvikle aktiv tuberkulose er samtidig HIV-infeksjon; 13 % av de med tuberkulose er også smittet med HIV. Dette er et spesielt problem i Afrika sør for Sahara , hvor HIV-infeksjonsratene er høye. Av de uten HIV-infeksjon som er smittet med tuberkulose, utvikler omtrent 5–10 % aktiv sykdom i løpet av livet; i motsetning til dette utvikler 30 % av de som samtidig er infisert med HIV den aktive sykdommen.
Bruk av visse medisiner, som kortikosteroider og infliksimab (et anti-αTNF monoklonalt antistoff), er en annen viktig risikofaktor, spesielt i den utviklede verden .
Andre risikofaktorer inkluderer: alkoholisme , diabetes mellitus (3 ganger økt risiko), silikose (30 ganger økt risiko), tobakksrøyking (2 ganger økt risiko), innendørs luftforurensning , underernæring, ung alder, nylig ervervet tuberkuloseinfeksjon, rekreasjonsbruk av rusmidler, alvorlig nyresykdom, lav kroppsvekt, organtransplantasjon, hode- og nakkekreft og genetisk følsomhet (den generelle betydningen av genetiske risikofaktorer er fortsatt udefinert).
Infeksjonsfølsomhet
Tobakksrøyking øker risikoen for infeksjoner (i tillegg til å øke risikoen for aktiv sykdom og død). Ytterligere faktorer som øker infeksjonsfølsomheten inkluderer ung alder.
Patogenese

Omtrent 90 % av de som er infisert med M. tuberculosis har asymptomatiske , latente TB-infeksjoner (noen ganger kalt LTBI), med bare 10 % livstids sjanse for at den latente infeksjonen vil utvikle seg til åpenbar, aktiv tuberkuløs sykdom. Hos de med HIV øker risikoen for å utvikle aktiv tuberkulose til nesten 10 % i året. Hvis effektiv behandling ikke gis, er dødsraten for aktive tuberkulosetilfeller opptil 66 %.

TB-infeksjon begynner når mykobakteriene når de alveolære luftsekkene i lungene, hvor de invaderer og replikeres i endosomene til alveolære makrofager . Makrofager identifiserer bakterien som fremmed og forsøker å eliminere den ved fagocytose . Under denne prosessen blir bakterien innhyllet av makrofagen og lagret midlertidig i en membranbundet vesikkel som kalles et fagosomet. Fagosomet kombineres deretter med et lysosom for å lage et fagolysosom. I fagolysosomet forsøker cellen å bruke reaktive oksygenarter og syre for å drepe bakterien. Imidlertid har M. tuberculosis en tykk, voksaktig mykolsyrekapsel som beskytter den mot disse giftige stoffene. M. tuberculosis er i stand til å formere seg inne i makrofagen og vil til slutt drepe immuncellen.
Det primære infeksjonsstedet i lungene, kjent som Ghon-fokuset , er vanligvis plassert enten i den øvre delen av den nedre lappen eller den nedre delen av den øvre lappen . Tuberkulose i lungene kan også oppstå via infeksjon fra blodstrømmen. Dette er kjent som et Simon-fokus og finnes vanligvis i toppen av lungen. Denne hematogene overføringen kan også spre infeksjon til fjernere steder, for eksempel perifere lymfeknuter, nyrene, hjernen og bein. Alle deler av kroppen kan bli påvirket av sykdommen, men av ukjente årsaker påvirker den sjelden hjertet , skjelettmuskulaturen , bukspyttkjertelen eller skjoldbruskkjertelen .
Tuberkulose er klassifisert som en av de granulomatøse inflammatoriske sykdommene. Makrofager , epiteloidceller , T-lymfocytter , B-lymfocytter og fibroblaster aggregerer for å danne granulomer, med lymfocytter som omgir de infiserte makrofagene. Når andre makrofager angriper den infiserte makrofagen, smelter de sammen for å danne en gigantisk multinukleær celle i alveolarlumen. Granulomet kan forhindre spredning av mykobakterier og gi et lokalt miljø for interaksjon av celler i immunsystemet. Nyere bevis tyder imidlertid på at bakteriene bruker granulomene for å unngå ødeleggelse av vertens immunsystem. Makrofager og dendrittiske celler i granulomene er ikke i stand til å presentere antigen til lymfocytter; dermed undertrykkes immunresponsen. Bakterier inne i granulomet kan bli sovende, noe som resulterer i latent infeksjon. Et annet trekk ved granulomene er utviklingen av unormal celledød ( nekrose ) i midten av tuberkler . For det blotte øye har denne teksturen av myk, hvit ost og kalles kaseøs nekrose .
Hvis TB-bakterier kommer inn i blodstrømmen fra et område med skadet vev, kan de spre seg over hele kroppen og sette opp mange infeksjonspunkter, som alle fremstår som små, hvite tuberkler i vevet. Denne alvorlige formen for tuberkulose, vanligst hos små barn og de med HIV, kalles miliær tuberkulose. Personer med denne spredte TB har en høy dødelighet selv med behandling (omtrent 30 %).
Hos mange mennesker vokser og avtar infeksjonen. Vevsødeleggelse og nekrose balanseres ofte av tilheling og fibrose . Berørt vev erstattes av arrdannelse og hulrom fylt med kaseøst nekrotisk materiale. Under aktiv sykdom er noen av disse hulrommene forbundet med luftkanalene ( bronkiene ) og dette materialet kan hostes opp. Den inneholder levende bakterier og kan dermed spre infeksjonen. Behandling med passende antibiotika dreper bakterier og lar helbredelse finne sted. Ved kurering blir berørte områder til slutt erstattet av arrvev.
Diagnose
Aktiv tuberkulose
Å diagnostisere aktiv tuberkulose kun basert på tegn og symptomer er vanskelig, det samme er å diagnostisere sykdommen hos de som har et svekket immunsystem. En diagnose av tuberkulose bør imidlertid vurderes hos de med tegn på lungesykdom eller konstitusjonelle symptomer som varer lenger enn to uker. Røntgen av thorax og flere sputumkulturer for syrefaste basiller er vanligvis en del av den første evalueringen. Interferon-γ-frigjøringsanalyser og tuberkulin-hudprøver er til liten nytte i det meste av utviklingsland. Interferon gamma-frigjøringsanalyser (IGRA) har lignende begrensninger hos de med HIV.
En definitiv diagnose av TB stilles ved å identifisere M. tuberculosis i en klinisk prøve (f.eks. sputum , puss eller en vevsbiopsi ). Imidlertid kan den vanskelige dyrkingsprosessen for denne saktevoksende organismen ta to til seks uker for blod- eller sputumkultur. Behandlingen starter derfor ofte før kulturer er bekreftet.
Nukleinsyreamplifikasjonstester og adenosindeaminasetesting kan tillate rask diagnose av tuberkulose. Blodprøver for å oppdage antistoffer er ikke spesifikke eller sensitive , så de anbefales ikke.
Latent tuberkulose
Mantoux tuberkulin hudtest brukes ofte til å screene personer med høy risiko for tuberkulose. De som tidligere har blitt vaksinert med Bacille Calmette-Guerin-vaksinen kan ha et falskt positivt testresultat. Testen kan være falskt negativ hos de med sarkoidose , Hodgkins lymfom , underernæring og spesielt aktiv tuberkulose. Interferon gamma-frigjøringsanalyser, på en blodprøve, anbefales for de som er positive til Mantoux-testen. Disse påvirkes ikke av immunisering eller de fleste miljømessige mykobakterier , så de genererer færre falske positive resultater. Imidlertid er de påvirket av M. szulgai , M. marinum og M. kansasii . IGRA-er kan øke følsomheten når de brukes i tillegg til hudtesten, men kan være mindre følsomme enn hudtesten når de brukes alene.
US Preventive Services Task Force ( USPSTF ) har anbefalt screening av personer som har høy risiko for latent tuberkulose med enten tuberkulin-hudprøver eller interferon-gamma-frigjøringsanalyser. Mens noen har anbefalt å teste helsepersonell, er bevis på nytte for dette dårlig fra og med 2019. Centers for Disease Control and Prevention (CDC) sluttet å anbefale årlig testing av helsepersonell uten kjent eksponering i 2019.
Forebygging
Tuberkuloseforebygging og -kontroll er først og fremst avhengig av vaksinering av spedbarn og påvisning og hensiktsmessig behandling av aktive tilfeller. Verdens helseorganisasjon (WHO) har oppnådd en viss suksess med forbedrede behandlingsregimer, og en liten nedgang i antall tilfelle. Noen land har lovgivning for å ufrivillig arrestere eller undersøke de som mistenkes for å ha tuberkulose, eller ufrivillig behandle dem hvis de er smittet.
Vaksiner
Den eneste tilgjengelige vaksinen per 2021 er bacillus Calmette-Guérin (BCG). Hos barn reduseres risikoen for å få infeksjonen med 20 % og risikoen for at infeksjonen blir til aktiv sykdom med nesten 60 %.
Det er den mest brukte vaksinen på verdensbasis, med mer enn 90 % av alle barn som er vaksinert. Immuniteten det induserer avtar etter omtrent ti år. Ettersom tuberkulose er uvanlig i det meste av Canada, Vest-Europa og USA, administreres BCG bare til personer med høy risiko. Noe av begrunnelsen mot bruk av vaksinen er at den gjør tuberkulinhudtesten falsk positiv, noe som reduserer testens nytte som screeningsverktøy. Flere vaksiner er under utvikling.
Intradermal MVA85A-vaksine i tillegg til BCG-injeksjon er ikke effektiv for å forhindre tuberkulose.
Folkehelse
Folkehelsekampanjer som har fokusert på overbefolkning, offentlig spytting og vanlig sanitær (inkludert håndvask) i løpet av 1800-tallet bidro til å enten avbryte eller bremse spredningen, som i kombinasjon med kontaktsporing, isolasjon og behandling bidro til å dramatisk dempe overføringen av både tuberkulose og annet. luftbårne sykdommer som førte til eliminering av tuberkulose som et stort folkehelseproblem i de fleste utviklede økonomier. Andre risikofaktorer som forverret spredning av tuberkulose som underernæring ble også forbedret, men siden fremveksten av HIV var en ny populasjon av immunkompromitterte individer tilgjengelig for tuberkulose å infisere.
Verdens helseorganisasjon (WHO) erklærte tuberkulose som en "global helsenødsituasjon" i 1993, og i 2006 utviklet Stop TB-partnerskapet en global plan for å stoppe tuberkulose som hadde som mål å redde 14 millioner liv mellom lanseringen og 2015. En rekke mål de fastsatte ble ikke oppnådd innen 2015, hovedsakelig på grunn av økningen i HIV-assosiert tuberkulose og fremveksten av multippel medikamentresistent tuberkulose. Et tuberkuloseklassifiseringssystem utviklet av American Thoracic Society brukes først og fremst i folkehelseprogrammer. I 2015 lanserte den End TB-strategien for å redusere dødsfall med 95 % og forekomst med 90 % før 2035. Målet om tuberkulose-eliminering er hemmet av mangelen på rask testing, på korte og effektive behandlingsforløp og av fullstendig effektive vaksiner .
Fordelene og risikoene ved å gi anti-tuberkulære legemidler til de som er utsatt for MDR-TB er uklare. Å gjøre HAART-terapi tilgjengelig for HIV-positive individer reduserer risikoen for progresjon til en aktiv TB-infeksjon betydelig med opptil 90 % og kan redusere spredningen gjennom denne populasjonen.
Behandling
Behandling av TB bruker antibiotika for å drepe bakteriene. Effektiv behandling av tuberkulose er vanskelig, på grunn av den uvanlige strukturen og kjemiske sammensetningen av mykobakteriell cellevegg, som hindrer inntreden av legemidler og gjør mange antibiotika ineffektive.
Aktiv tuberkulose behandles best med kombinasjoner av flere antibiotika for å redusere risikoen for at bakteriene utvikler antibiotikaresistens . Den rutinemessige bruken av rifabutin i stedet for rifampicin hos HIV-positive mennesker med tuberkulose er av uklar fordel fra og med 2007.
Latent TB
Latent tuberkulose behandles med enten isoniazid eller rifampin alene, eller en kombinasjon av isoniazid med enten rifampicin eller rifapentin.
Behandlingen tar tre til ni måneder avhengig av medisinene som brukes. Personer med latente infeksjoner behandles for å hindre dem i å utvikle seg til aktiv tuberkulose senere i livet.
Utdanning eller rådgivning kan forbedre fullføringsraten for latent tuberkulosebehandling.
Ny oppstart
Den anbefalte behandlingen av nyoppstått lungetuberkulose, fra og med 2010, er seks måneder med en kombinasjon av antibiotika som inneholder rifampicin, isoniazid, pyrazinamid og etambutol de første to månedene, og kun rifampicin og isoniazid de siste fire månedene. Der resistens mot isoniazid er høy, kan etambutol tilsettes de siste fire månedene som et alternativ. Behandling med anti-TB-medisiner i minst 6 måneder gir høyere suksessrate sammenlignet med behandling mindre enn 6 måneder, selv om forskjellen er liten. Kortere behandlingsregime kan anbefales for de med compliance-problemer. Det er heller ingen bevis for å støtte kortere anti-tuberkulosebehandlingsregimer sammenlignet med et 6-måneders behandlingsregime. Nylig tyder imidlertid resultater fra en internasjonal, randomisert, kontrollert klinisk studie på at et fire måneders daglig behandlingsregime som inneholder høydose, eller "optimalisert", rifapentin med moxifloxacin (2PHZM/2PHM) er like trygt og effektivt som den eksisterende standard seks. -måneds daglig diett for å kurere medikamentfølsom tuberkulose (TB).
Tilbakevendende sykdom
Hvis tuberkulose oppstår igjen, er det viktig å teste for å finne ut hvilke antibiotika den er følsom for før behandlingen bestemmes. Hvis multippel medikamentresistent TB (MDR-TB) påvises, anbefales behandling med minst fire effektive antibiotika i 18 til 24 måneder.
Medisinadministrasjon
Direkte observert terapi , dvs. å la en helsepersonell se på at personen tar medisinene sine, anbefales av Verdens helseorganisasjon (WHO) i et forsøk på å redusere antallet personer som ikke tar antibiotika på riktig måte. Beviset for å støtte denne praksisen over at folk bare tar medisinene sine uavhengig er av dårlig kvalitet. Det er ingen sterke bevis som indikerer at direkte observert terapi forbedrer antall personer som ble helbredet eller antall personer som fullfører medisinen. Moderat kvalitetsbevis tyder på at det heller ikke er noen forskjell om folk blir observert hjemme versus på en klinikk, eller av et familiemedlem kontra en helsepersonell. Metoder for å minne folk om viktigheten av behandling og avtaler kan resultere i en liten, men viktig forbedring. Det er heller ikke nok bevis for å støtte intermitterende rifampicin-holdig behandling gitt to til tre ganger i uken har lik effektivitet som daglig doseregime for å forbedre helbredelsesraten og redusere tilbakefallsfrekvensen. Det er heller ikke nok bevis på effektiviteten av å gi intermitterende to- eller tre ganger ukentlig kortkurregime sammenlignet med daglig doseringsregime ved behandling av barn med tuberkulose.
Medisineresistens
Primær resistens oppstår når en person blir infisert med en resistent tuberkulosestamme. En person med fullt mottakelig MTB kan utvikle sekundær (ervervet) resistens under behandlingen på grunn av utilstrekkelig behandling, ikke å ta det foreskrevne regimet på riktig måte (manglende etterlevelse), eller bruke medisiner av lav kvalitet. Medikamentresistent tuberkulose er et alvorlig folkehelseproblem i mange utviklingsland, siden behandlingen er lengre og krever dyrere legemidler. MDR-TB er definert som resistens mot de to mest effektive førstelinje-TB-medisinene: rifampicin og isoniazid. Utstrakt legemiddelresistent tuberkulose er også resistent mot tre eller flere av de seks klassene av andrelinjemedikamenter. Totalt legemiddelresistent tuberkulose er resistent mot alle legemidler som brukes i dag. Den ble først observert i 2003 i Italia, men ble ikke rapportert mye før i 2012, og har også blitt funnet i Iran og India. Det er en viss effekt for linezolid for å behandle de med XDR-TB, men bivirkninger og seponering av medisiner var vanlige. Bedaquilin støttes foreløpig for bruk ved multippel medikamentresistent tuberkulose.
XDR-TB er et begrep som noen ganger brukes for å definere omfattende resistent TB, og utgjør ett av ti tilfeller av MDR-TB. Tilfeller av XDR TB er identifisert i mer enn 90 % av landene.
For de med kjent rifampicin eller MDR-TB, kan molekylære tester som Genotype® MTBDRsl-analysen (utført på kulturisolater eller utstrykspositive prøver) være nyttige for å oppdage andrelinje anti-tuberkulær medikamentresistens.
Prognose

|
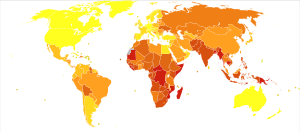
ingen data
≤10
10–25
25–50
50–75
75–100
100–250 |
250–500
500–750
750–1000
1000–2000
2000–3000
≥ 3000 |
Progresjon fra TB-infeksjon til åpen TB-sykdom skjer når basillene overvinner immunsystemets forsvar og begynner å formere seg. Ved primær TB-sykdom (omtrent 1–5 % av tilfellene) skjer dette kort tid etter den første infeksjonen. Men i de fleste tilfeller oppstår en latent infeksjon uten åpenbare symptomer. Disse sovende basillene produserer aktiv tuberkulose i 5–10 % av disse latente tilfellene, ofte mange år etter infeksjon.
Risikoen for reaktivering øker med immunsuppresjon , slik som forårsaket av infeksjon med HIV. Hos personer med samtidig M. tuberculosis og HIV øker risikoen for reaktivering til 10 % per år. Studier med DNA-fingeravtrykk av M. tuberculosis - stammer har vist at reinfeksjon bidrar mer vesentlig til tilbakevendende tuberkulose enn tidligere antatt, med anslag på at det kan utgjøre mer enn 50 % av reaktiverte tilfeller i områder der tuberkulose er vanlig. Sjansen for død fra et tilfelle av tuberkulose er omtrent 4 % fra 2008, ned fra 8 % i 1995.
Hos personer med utstryk-positiv lunge-TB (uten HIV-ko-infeksjon), dør 50-60 % etter 5 år uten behandling mens 20-25 % oppnår spontan oppløsning (kur). TB er nesten alltid dødelig hos de med ubehandlet HIV-kombinasjon, og dødsraten øker selv med antiretroviral behandling av HIV.
Epidemiologi
Omtrent en fjerdedel av verdens befolkning har blitt infisert med M. tuberculosis , med nye infeksjoner som forekommer hos omtrent 1 % av befolkningen hvert år. De fleste infeksjoner med M. tuberculosis forårsaker imidlertid ikke sykdom, og 90–95 % av infeksjonene forblir asymptomatiske. I 2012 var anslagsvis 8,6 millioner kroniske tilfeller aktive. I 2010 ble 8,8 millioner nye tilfeller av tuberkulose diagnostisert, og 1,20–1,45 millioner dødsfall skjedde (de fleste av disse forekommer i utviklingsland ). Av disse forekommer om lag 0,35 millioner hos de som også er smittet med HIV. I 2018 var tuberkulose den ledende dødsårsaken på verdensbasis fra et enkelt smittestoff. Det totale antallet tuberkulosetilfeller har vært synkende siden 2005, mens nye tilfeller har gått ned siden 2002.
Tuberkuloseforekomsten er sesongbasert, med topper hver vår og sommer. Årsakene til dette er uklare, men kan ha sammenheng med D-vitaminmangel om vinteren. Det er også studier som knytter tuberkulose til forskjellige værforhold som lav temperatur, lav luftfuktighet og lite nedbør. Det har blitt antydet at forekomsten av tuberkulose kan være knyttet til klimaendringer.
Risikogrupper
Tuberkulose er nært knyttet til både overbefolkning og underernæring , noe som gjør den til en av de viktigste sykdommene i fattigdom . De med høy risiko inkluderer således: personer som injiserer illegale rusmidler, innbyggere og ansatte i lokaliteter der sårbare mennesker samles (f.eks. fengsler og hjemløse krisesentre), medisinsk underprivilegerte og ressurssvake lokalsamfunn, høyrisiko-etniske minoriteter, barn i nær kontakt med pasienter i høyrisikokategori og helsepersonell som betjener disse pasientene.
Graden av tuberkulose varierer med alderen. I Afrika rammer det først og fremst ungdom og unge voksne. Men i land der forekomsten har gått dramatisk ned (som USA), er tuberkulose hovedsakelig en sykdom hos eldre og immunsvekket (risikofaktorer er listet opp ovenfor). På verdensbasis opplever 22 "høybelastningsstater" eller land til sammen 80 % av tilfellene samt 83 % av dødsfallene.
I Canada og Australia er tuberkulose mange ganger mer vanlig blant urbefolkningen , spesielt i avsidesliggende områder. Faktorer som bidrar til dette inkluderer høyere forekomst av disponerende helsetilstander og atferd, og overbefolkning og fattigdom. I noen kanadiske aboriginalgrupper kan genetisk følsomhet spille en rolle.
Sosioøkonomisk status (SES) påvirker TB risiko sterkt. Personer med lav SES er både mer sannsynlig å pådra seg tuberkulose og å bli mer alvorlig påvirket av sykdommen. De med lav SES er mer sannsynlig å bli påvirket av risikofaktorer for å utvikle tuberkulose (f.eks. underernæring, innendørs luftforurensning, HIV samtidig infeksjon, etc.), og er i tillegg mer sannsynlig å bli utsatt for overfylte og dårlig ventilerte rom. Mangelfull helsehjelp betyr også at personer med aktiv sykdom som legger til rette for spredning ikke blir diagnostisert og behandlet raskt; syke mennesker forblir dermed i smittsom tilstand og (fortsetter å) spre infeksjonen.
Geografisk epidemiologi
Fordelingen av tuberkulose er ikke ensartet over hele kloden; Omtrent 80 % av befolkningen i mange afrikanske, karibiske, sørasiatiske og østeuropeiske land tester positivt i tuberkulintester, mens bare 5–10 % av den amerikanske befolkningen tester positivt. Håpet om fullstendig kontroll av sykdommen har blitt dramatisk dempet på grunn av mange faktorer, inkludert vanskeligheten med å utvikle en effektiv vaksine, den dyre og tidkrevende diagnostiske prosessen, nødvendigheten av mange måneders behandling, økningen i HIV-assosiert tuberkulose, og fremveksten av narkotikaresistente tilfeller på 1980-tallet.
I utviklede land er tuberkulose mindre vanlig og finnes hovedsakelig i urbane områder. I Europa falt dødsfall fra tuberkulose fra 500 av 100 000 i 1850 til 50 av 100 000 innen 1950. Forbedringer i folkehelsen reduserte tuberkulose selv før antibiotikaen kom, selv om sykdommen forble en betydelig trussel mot folkehelsen, slik at når Medical Research Council ble dannet i Storbritannia i 1913, og dets første fokus var tuberkuloseforskning.
I 2010 var prisene per 100 000 mennesker i forskjellige områder av verden: globalt 178, Afrika 332, Amerika 36, Øst-Middelhavet 173, Europa 63, Sørøst-Asia 278 og Vest-Stillehavet 139.
Russland
Russland har oppnådd spesielt dramatisk fremgang med en nedgang i sin tuberkulosedødelighet – fra 61,9 per 100 000 i 1965 til 2,7 per 100 000 i 1993; dødeligheten økte imidlertid til 24 per 100 000 i 2005 og falt deretter tilbake til 11 per 100 000 innen 2015.
Kina
Kina har oppnådd spesielt dramatiske fremskritt, med omtrent 80 % reduksjon i TB-dødeligheten mellom 1990 og 2010. Antall nye tilfeller har gått ned med 17 % mellom 2004 og 2014.
Afrika
I 2007 var landet med den høyeste estimerte forekomsten av TB Eswatini , med 1200 tilfeller per 100 000 mennesker. I 2017 var landet med den høyeste estimerte forekomsten som en % av befolkningen Lesotho , med 665 tilfeller per 100 000 mennesker.
India
Fra og med 2017 hadde India den største totale forekomsten, med anslagsvis 2 740 000 tilfeller. I følge Verdens helseorganisasjon (WHO) falt Indias estimerte dødelighet i 2000–2015 fra 55 til 36 per 100 000 innbyggere per år, med anslagsvis 480 tusen mennesker døde av tuberkulose i 2015. I India blir en stor andel av tuberkulosepasientene behandles av private samarbeidspartnere og private sykehus. Bevis tyder på at den nasjonale tuberkuloseundersøkelsen ikke representerer antallet tilfeller som er diagnostisert og registrert av private klinikker og sykehus i India.
Nord Amerika
I USA har indianere fem ganger høyere dødelighet av tuberkulose, og rasemessige og etniske minoriteter sto for 84 % av alle rapporterte tuberkulosetilfeller.
I USA var den totale tuberkulosetilfellet 3 per 100 000 personer i 2017. I Canada er tuberkulose fortsatt endemisk i enkelte landlige områder.
Vest-Europa
I 2017, i Storbritannia, var landsgjennomsnittet 9 per 100 000 og de høyeste forekomstratene i Vest-Europa var 20 per 100 000 i Portugal.
Historie
Tuberkulose har eksistert siden antikken . Den eldste entydig påviste M. tuberculosis gir bevis på sykdommen i restene av bison i Wyoming datert til rundt 17 000 år siden. Hvorvidt tuberkulose oppsto i storfe, deretter overført til mennesker, eller om både bovin og menneskelig tuberkulose avviket fra en felles stamfar, er fortsatt uklart. En sammenligning av genene til M. tuberculosis -komplekset (MTBC) hos mennesker med MTBC hos dyr tyder på at mennesker ikke fikk MTBC fra dyr under dyrdomestisering, slik forskere tidligere trodde. Begge stammene av tuberkulosebakteriene deler en felles stamfar, som kunne ha infisert mennesker allerede før den neolitiske revolusjonen . Skjelettrester viser at noen forhistoriske mennesker (4000 f.Kr. ) hadde tuberkulose, og forskere har funnet tuberkulært forfall i ryggraden til egyptiske mumier fra 3000 til 2400 f.Kr. Genetiske studier tyder på tilstedeværelsen av tuberkulose i Amerika fra ca 100 e.Kr.
Før den industrielle revolusjonen assosierte folklore ofte tuberkulose med vampyrer . Når ett medlem av en familie døde av sykdommen, ville de andre infiserte medlemmene miste helsen sakte. Folk trodde dette var forårsaket av at den opprinnelige personen med tuberkulose tappet livet fra de andre familiemedlemmene.
Selv om Richard Morton etablerte lungeformen assosiert med tuberkler som en patologi i 1689, på grunn av mangfoldet av symptomene, ble TB ikke identifisert som en enkelt sykdom før på 1820-tallet. Benjamin Marten antok i 1720 at forbruk var forårsaket av mikrober som ble spredt av mennesker som bodde i nærheten av hverandre. I 1819 hevdet René Laennec at tuberkler var årsaken til lungetuberkulose. JL Schönlein publiserte først navnet "tuberkulose" (tysk: Tuberkulose ) i 1832. Mellom 1838 og 1845 brakte John Croghan, eieren av Mammoth Cave i Kentucky fra 1839 og utover, en rekke mennesker med tuberkulose inn i hulen i håp om kurere sykdommen med konstant temperatur og renhet av huleluften; hver døde innen et år. Hermann Brehmer åpnet det første TB- sanatoriet i 1859 i Görbersdorf (nå Sokołowsko ) i Schlesien . I 1865 demonstrerte Jean Antoine Villemin at tuberkulose kunne overføres, via inokulering, fra mennesker til dyr og blant dyr. (Villemins funn ble bekreftet i 1867 og 1868 av John Burdon-Sanderson .)
Robert Koch identifiserte og beskrev basillen som forårsaker tuberkulose, M. tuberculosis , 24. mars 1882. Han mottok Nobelprisen i fysiologi eller medisin i 1905 for denne oppdagelsen. Koch trodde ikke at storfe- og tuberkulosesykdommene var like, noe som forsinket anerkjennelsen av infisert melk som en smittekilde. I løpet av første halvdel av 1900-tallet ble risikoen for overføring fra denne kilden dramatisk redusert etter bruk av pasteuriseringsprosessen . Koch annonserte et glyserinekstrakt av tuberkelbasiller som et "middel" mot tuberkulose i 1890, og kalte det "tuberkulin". Selv om det ikke var effektivt, ble det senere vellykket tilpasset som en screeningtest for tilstedeværelse av presymptomatisk tuberkulose. Verdens tuberkulosedag markeres 24. mars hvert år, årsdagen for Kochs opprinnelige vitenskapelige kunngjøring.
Albert Calmette og Camille Guérin oppnådde den første ekte suksessen i immunisering mot tuberkulose i 1906, ved å bruke svekket tuberkulose av storfe. Den ble kalt bacille Calmette–Guérin (BCG). BCG-vaksinen ble først brukt på mennesker i 1921 i Frankrike, men oppnådde bred aksept i USA, Storbritannia og Tyskland først etter andre verdenskrig.
Tuberkulose forårsaket utbredt offentlig bekymring på 1800- og begynnelsen av 1900-tallet da sykdommen ble vanlig blant de fattige i byene. I 1815 skyldtes ett av fire dødsfall i England "forbruk". I 1918 forårsaket tuberkulose fortsatt én av seks dødsfall i Frankrike. Etter at tuberkulose ble fastslått å være smittsom, på 1880-tallet, ble den satt på en meldepliktig sykdomsliste i Storbritannia; kampanjer begynte å stoppe folk fra å spytte på offentlige steder, og de smittede fattige ble "oppmuntret" til å gå inn på sanatorier som lignet fengsler (sanatoriene for middel- og overklassen tilbød utmerket omsorg og konstant legehjelp). Uansett fordelene med "frisk luft" og arbeid i sanatoriene, selv under de beste forhold, døde 50 % av de som kom inn i løpet av fem år ( ca. 1916). Da Medical Research Council ble dannet i Storbritannia i 1913, fokuserte det først på tuberkuloseforskning.
I Europa begynte tuberkuloseraten å stige tidlig på 1600-tallet til et toppnivå på 1800-tallet, da det forårsaket nesten 25 % av alle dødsfall. På 1700- og 1800-tallet hadde tuberkulose blitt en epidemi i Europa , og viste et sesongmønster. På 1950-tallet hadde dødeligheten i Europa sunket med rundt 90 %. Forbedringer i sanitet, vaksinasjon og andre folkehelsetiltak begynte å redusere antallet tuberkulose betydelig selv før streptomycin og andre antibiotika kom, selv om sykdommen forble en betydelig trussel. I 1946 gjorde utviklingen av antibiotikumet streptomycin effektiv behandling og helbredelse av tuberkulose til en realitet. Før introduksjonen av denne medisinen var den eneste behandlingen kirurgisk inngrep, inkludert " pneumothorax - teknikken", som innebar å kollapse en infisert lunge for å "hvile" den og la tuberkuløse lesjoner gro.
På grunn av fremveksten av multiresistent tuberkulose (MDR-TB) , har kirurgi blitt gjeninnført for visse tilfeller av TB-infeksjoner. Det innebærer fjerning av infiserte brysthuler ("bullae") i lungene for å redusere antall bakterier og for å øke eksponeringen av de gjenværende bakteriene for antibiotika i blodet. Håpet om å eliminere tuberkulose endte med fremveksten av medikamentresistente stammer på 1980-tallet. Den påfølgende gjenoppblomstringen av tuberkulose resulterte i erklæringen om en global helsekrise av Verdens helseorganisasjon (WHO) i 1993.
Samfunn og kultur
Navn
Tuberkulose har vært kjent under mange navn fra det tekniske til det kjente. Phthisis ( Φθισις ) er et gresk ord for konsum, en gammel betegnelse for lungetuberkulose; rundt 460 f.Kr. beskrev Hippokrates phthisis som en sykdom i tørre årstider. Forkortelsen TB er en forkortelse for tuberkelbasill . Konsum var det vanligste engelske ordet fra det nittende århundre for sykdommen. Den latinske roten con som betyr 'fullstendig' er knyttet til sumere som betyr 'å ta opp fra under'. I The Life and Death of Mr Badman av John Bunyan kaller forfatteren forbruket "kapteinen på alle disse dødsmennene." "Stor hvit pest" har også blitt brukt.
Kunst og litteratur

Tuberkulose var i århundrer assosiert med poetiske og kunstneriske kvaliteter blant de smittede, og ble også kjent som «den romantiske sykdommen». Store kunstneriske skikkelser som dikterne John Keats , Percy Bysshe Shelley og Edgar Allan Poe , komponisten Frédéric Chopin , dramatikeren Anton Chekhov , romanforfatterne Franz Kafka , Katherine Mansfield , Charlotte Brontë , Fyodor Dostoevsky , Thomas Mann , W. Somerset Maugham , George Orwell og Robert Louis Stevenson , og artistene Alice Neel , Jean-Antoine Watteau , Elizabeth Siddal , Marie Bashkirtseff , Edvard Munch , Aubrey Beardsley og Amedeo Modigliani hadde enten sykdommen eller var omgitt av mennesker som gjorde det. En utbredt oppfatning var at tuberkulose hjalp kunstnerisk talent. Fysiske mekanismer som ble foreslått for denne effekten inkluderte den lette feberen og toksemien som den forårsaket, og angivelig hjalp dem til å se livet klarere og handle besluttsomt.
Tuberkulose dannet et ofte gjenbrukt tema i litteraturen , som i Thomas Manns The Magic Mountain , satt i et sanatorium ; i musikk , som i Van Morrisons sang " TB Sheets "; i opera , som i Puccinis La bohème og Verdis La Traviata ; i kunst , som i Monets maleri av sin første kone Camille på dødsleiet; og i film , for eksempel The Bells of St. Mary's fra 1945 med Ingrid Bergman i hovedrollen som nonne med tuberkulose.
Folkehelseinnsats
I 2014 vedtok WHO strategien "End TB" som har som mål å redusere TB-forekomsten med 80 % og TB-dødsfallene med 90 % innen 2030. Strategien inneholder en milepæl for å redusere TB-forekomsten med 20 % og TB-dødsfallene med 35 % innen 2020. Innen 2020 ble det imidlertid bare oppnådd en reduksjon på 9 % i forekomst per befolkning globalt, med den europeiske regionen som oppnådde 19 % og den afrikanske regionen oppnådde 16 % reduksjoner. Tilsvarende falt antallet dødsfall bare med 14 %, og gikk glipp av 2020-milepælen med en reduksjon på 35 %, med noen regioner som gjorde bedre fremgang (31 % reduksjon i Europa og 19 % i Afrika). Tilsvarende ble også behandlings-, forebyggings- og finansieringsmilepæler savnet i 2020, for eksempel ble bare 6,3 millioner mennesker startet på TB-forebygging under målet på 30 millioner.
Verdens helseorganisasjon (WHO), Bill og Melinda Gates Foundation og den amerikanske regjeringen subsidierer en hurtigvirkende diagnostisk tuberkulosetest for bruk i lav- og mellominntektsland fra og med 2012. I tillegg til å være hurtigvirkende, testen kan avgjøre om det er resistens mot antibiotikumet rifampicin som kan indikere multiresistent tuberkulose og er nøyaktig hos de som også er infisert med HIV. Mange ressurssvake steder har per 2011 tilgang til kun sputummikroskopi.
India hadde det høyeste totale antallet TB-tilfeller på verdensbasis i 2010, delvis på grunn av dårlig sykdomsbehandling innen privat og offentlig helsevesen. Programmer som Revised National Tuberculosis Control Program jobber for å redusere TB-nivået blant personer som mottar offentlig helsehjelp.
En EIU -helserapport fra 2014 viser at det er behov for å adressere apati og oppfordrer til økt finansiering. Rapporten siterer blant andre Lucica Ditui "[TB] er som et foreldreløst barn. Det har blitt neglisjert selv i land med høy byrde og ofte glemt av givere og de som investerer i helseintervensjoner."
Langsom fremgang har ført til frustrasjon, uttrykt av administrerende direktør for det globale fondet for å bekjempe AIDS, tuberkulose og malaria - Mark Dybul: "vi har verktøyene for å få slutt på TB som en pandemi og folkehelsestrussel på planeten, men vi er ikke gjør det." Flere internasjonale organisasjoner presser på for mer åpenhet i behandlingen, og flere land implementerer obligatorisk rapportering av saker til myndighetene fra og med 2014, selv om tilslutningen ofte varierer. Kommersielle behandlere kan til tider overskrive andrelinjemedisiner samt tilleggsbehandling, noe som fremmer krav om ytterligere reguleringer. Regjeringen i Brasil gir universell TB-omsorg, noe som reduserer dette problemet. Motsatt kan fallende forekomst av TB-infeksjon ikke være relatert til antall programmer rettet mot å redusere infeksjonsraten, men kan være knyttet til økt utdanningsnivå, inntekt og helse for befolkningen. Kostnadene ved sykdommen, som beregnet av Verdensbanken i 2009, kan overstige 150 milliarder dollar per år i land med "høy byrde". Mangel på fremgang for å utrydde sykdommen kan også skyldes manglende pasientoppfølging – som blant de 250 millioner migrantene på landsbygda i Kina .
Det er utilstrekkelig data til å vise at aktiv kontaktsporing bidrar til å forbedre antall tilfeller av tuberkulose. Intervensjoner som hus-til-hus-besøk, pedagogiske brosjyrer, massemediestrategier, pedagogiske økter kan øke tuberkulosedeteksjonsraten på kort sikt. Det er ingen studie som sammenligner nye metoder for kontaktsporing som sosial nettverksanalyse med eksisterende kontaktsporingsmetoder.
Stigma
Langsom fremgang i forebygging av sykdommen kan delvis skyldes stigma forbundet med tuberkulose. Stigma kan skyldes frykt for overføring fra berørte individer. Dette stigmaet kan i tillegg oppstå på grunn av sammenhenger mellom tuberkulose og fattigdom, og i Afrika, AIDS . Slik stigmatisering kan være både reell og oppfattet; for eksempel, i Ghana, er individer med tuberkulose forbudt å delta på offentlige sammenkomster.
Stigma mot tuberkulose kan føre til forsinkelser i å søke behandling, lavere behandlingsoverholdelse og familiemedlemmer som holder dødsårsaken hemmelig – slik at sykdommen kan spre seg videre. Derimot var stigma i Russland assosiert med økt behandlingsoverholdelse. TB-stigma rammer også sosialt marginaliserte individer i større grad og varierer mellom regioner.
En måte å redusere stigma på kan være gjennom promotering av «TB-klubber», der de som er smittet kan dele erfaringer og tilby støtte, eller gjennom rådgivning. Noen studier har vist at TB-opplæringsprogrammer er effektive for å redusere stigma, og kan dermed være effektive for å øke behandlingsoverholdelse. Til tross for dette mangler studier på forholdet mellom redusert stigma og dødelighet fra og med 2010, og lignende forsøk på å redusere stigma rundt AIDS har vært minimalt effektive. Noen har hevdet stigmaet er verre enn sykdommen, og helsepersonell kan utilsiktet forsterke stigmaet, ettersom de med tuberkulose ofte oppfattes som vanskelige eller på annen måte uønskede. En større forståelse av de sosiale og kulturelle dimensjonene ved tuberkulose kan også bidra til å redusere stigma.
Undersøkelser
BCG-vaksinen har begrensninger, og forskning for å utvikle nye TB-vaksiner pågår. En rekke potensielle kandidater er for tiden i fase I og II kliniske studier . To hovedtilnærminger brukes for å forsøke å forbedre effektiviteten til tilgjengelige vaksiner. En tilnærming innebærer å legge til en underenhetsvaksine til BCG, mens den andre strategien er å forsøke å lage nye og bedre levende vaksiner. MVA85A , et eksempel på en underenhetsvaksine, er i forsøk i Sør-Afrika fra og med 2006, og er basert på et genmodifisert vacciniavirus . Vaksiner er håpet å spille en betydelig rolle i behandlingen av både latent og aktiv sykdom.
For å oppmuntre til ytterligere oppdagelser, fremmer forskere og beslutningstakere nye økonomiske modeller for vaksineutvikling fra 2006, inkludert premier, skatteinsentiver og fremme markedsforpliktelser . En rekke grupper, inkludert Stop TB Partnership , South African Tuberculosis Vaccine Initiative og Aeras Global TB Vaccine Foundation , er involvert i forskning. Blant disse mottok Aeras Global TB Vaccine Foundation en gave på mer enn $280 millioner (US) fra Bill og Melinda Gates Foundation for å utvikle og lisensiere en forbedret vaksine mot tuberkulose for bruk i land med høy belastning.
En rekke medisiner blir studert fra og med 2012 for multiresistent tuberkulose, inkludert bedaquilin og delamanid . Bedaquiline mottok godkjenning fra US Food and Drug Administration (FDA) sent i 2012. Sikkerheten og effektiviteten til disse nye midlene er usikker fra og med 2012, fordi de er basert på resultatene av relativt små studier. Eksisterende data tyder imidlertid på at pasienter som tar bedaquilin i tillegg til standard TB-behandling har fem ganger større sannsynlighet for å dø enn de uten det nye stoffet, noe som har resultert i medisinske tidsskriftartikler som reiser helsepolitiske spørsmål om hvorfor FDA godkjente stoffet og hvorvidt det er økonomisk. bånd til selskapet som lager bedaquilin påvirket legers støtte til bruken.
Steroider tilleggsbehandling har ikke vist noen fordeler for aktiv lungetuberkuloseinfeksjon.
Andre dyr
Mykobakterier infiserer mange forskjellige dyr, inkludert fugler, fisk, gnagere og krypdyr. Underarten Mycobacterium tuberculosis er imidlertid sjelden til stede i ville dyr. Et forsøk på å utrydde bovin tuberkulose forårsaket av Mycobacterium bovis fra storfe- og hjortebesetningene på New Zealand har vært relativt vellykket. Innsatsen i Storbritannia har vært mindre vellykket.
Fra og med 2015 ser tuberkulose ut til å være utbredt blant fangede elefanter i USA. Det antas at dyrene opprinnelig ervervet sykdommen fra mennesker, en prosess som kalles omvendt zoonose . Fordi sykdommen kan spre seg gjennom luften for å infisere både mennesker og andre dyr, er den et folkehelseproblem som påvirker sirkus og dyrehager .
Referanser
Eksterne linker
- Tuberkulose hos Curlie
- "Tuberkulose (TB)" . Centers for Disease Control and Prevention (CDC). 24. oktober 2018.
- "Tuberkulose (TB)" . London: Health Protection Agency . Arkivert fra originalen 5. juli 2007.
- WHOs globale TB-rapport for 2016 (infografikk)
- WHO tuberkulose landsprofiler
- "Tuberkulose blant afroamerikanere" , 1990-11-01, In Black America ; KUT Radio , American Archive of Public Broadcasting ( WGBH og Library of Congress)
- Arbeidsgruppe for nye TB-legemidler , sporing av kliniske studier og medikamentkandidater







![Antall nye tilfeller av tuberkulose per 100 000 personer i 2016. [157]](https://upload.wikimedia.org/wikipedia/commons/thumb/a/a8/Tuberculosis_incidence_%28per_100%2C000_people%29%2C_OWID.svg/298px-Tuberculosis_incidence_%28per_100%2C000_people%29%2C_OWID.svg.png)
![Tuberkulosedødsfall etter region, 1990 til 2017. [158]](https://upload.wikimedia.org/wikipedia/commons/thumb/b/bb/Tuberculosis_deaths_by_region%2C_OWID.svg/298px-Tuberculosis_deaths_by_region%2C_OWID.svg.png)

