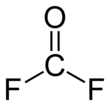
Karbonylfluorid - Carbonyl fluoride
|
|
|||
| Navn | |||
|---|---|---|---|
|
Foretrukket IUPAC-navn
Karbonyldifluorid |
|||
| Andre navn
Fluorfosgen; Karbondifluoridoksid; Fluormetanoylfluorid
|
|||
| Identifikatorer | |||
|
3D-modell ( JSmol )
|
|||
| ChemSpider | |||
| ECHA InfoCard |
100,005,941 |
||
| EF-nummer | |||
|
PubChem CID
|
|||
| RTECS-nummer | |||
| UNII | |||
| FN-nummer | 2417 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eiendommer | |||
| COF 2 | |||
| Molarmasse | 66,01 g mol −1 | ||
| Utseende | Fargeløs gass | ||
| Tetthet | 2,698 g / L (gass), 1,139 g / cm 3 (væske ved smeltepunkt) | ||
| Smeltepunkt | −111,26 ° C (−168,27 ° F, 161,89 K) | ||
| Kokepunkt | −84,57 ° C (−120,23 ° F, 188,58 K) | ||
| reagerer voldsomt med vann | |||
| Damptrykk | 55,4 atm (20 ° C) | ||
| Struktur | |||
| C 2v | |||
| 0,95 D | |||
| Farer | |||
| Viktigste farer | Dødelig ved innånding, reagerer med vann | ||
| GHS-piktogrammer |
   
|
||
| GHS Signalord | Fare | ||
| H280 , H290 , H314 , H330 , H331 , H370 | |||
| P234 , P260 , P261 , P264 , P270 , P271 , P280 , P284 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P307 + 311 , P310 , P311 , P320 , P321 , P363 , P390 , P403 + 233 , P404 , P405 , P410 + 403 , P501 | |||
| NFPA 704 (branndiamant) | |||
| Flammepunkt | Ikke brennbar | ||
| NIOSH (amerikanske helseeksponeringsgrenser): | |||
|
PEL (tillatt)
|
ingen | ||
|
REL (anbefalt)
|
TWA 2 ppm (5 mg / m 3 ) ST 5 ppm (15 mg / m 3 ) | ||
|
IDLH (umiddelbar fare)
|
ND | ||
| Beslektede forbindelser | |||
|
Beslektede forbindelser
|
Fosgen Karbonyl bromid Formyl fluor Thiocarbonyldiimida klorid Aceton Urea Kullsyre |
||
|
Med mindre annet er angitt, blir data gitt for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infoboksreferanser | |||
Karbonylfluorid er en kjemisk forbindelse med formelen COF 2 . Denne gassen er, i likhet med det analoge fosgenet , fargeløst og svært giftig. Molekylet er plan med C 2v- symmetri .
Klargjøring og egenskaper
Karbonylfluorid fremstilles vanligvis som et nedbrytningsprodukt av fluorerte hydrokarboner i den termiske nedbrytningen derav, for eksempel fra trifluormetanol eller tetrafluormetan i nærvær av vann:
-
CF
4+ H
2O → COF
2+ 2 HF
Karbonylfluorid kan også fremstilles ved omsetning av fosgen med hydrogenfluorid og oksydasjon av karbonmonoksid , selv om sistnevnte har en tendens til å resultere i overoksidasjon til karbontetrafluorid . Oksidasjonen av karbonmonoksid med sølvdifluorid er praktisk:
-
CO + 2 AgF
2→ COF
2+ 2 AgF
Karbonylfluorid er ustabilt i nærvær av vann, hydrolyserer til karbondioksid og hydrogenfluorid :
-
COF
2+ H
2O → CO
2+ 2 HF
Sikkerhet
Karbonylfluorid er giftig med en anbefalt eksponeringsgrense på 2 ppm som 8-timers tidsvektet gjennomsnitt og 5 ppm som kortvarig (15-minutters gjennomsnitt) eksponering.
Referanser
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "# 0108" . National Institute for Occupational Safety and Health (NIOSH).
- ^ MW Farlow; EH Man; CW Tullock (1960). "Karbonylfluorid". Uorganiske synteser . Uorganiske synteser. 6 . s. 155–158. doi : 10.1002 / 9780470132371.ch48 . ISBN 9780470132371.
- ^ "Karbonylfluorid" . NIOSH Pocket Guide til kjemiske farer . CDC sentre for sykdomskontroll og forebygging . Hentet 10.10.2013 .