Klorsyre - Chloric acid
|
|

|
|
| Navn | |
|---|---|
| Andre navn
Klorsyre (V)
|
|
| Identifikatorer | |
|
3D-modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.029.303 |
| EF-nummer | |
|
PubChem CID
|
|
| UNII | |
| FN-nummer | 2626 |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eiendommer | |
| HClO 3 | |
| Molarmasse | 84,45914 g mol −1 |
| Utseende | fargeløs løsning |
| Tetthet | 1 g / ml, oppløsning (omtrentlig) |
| > 40 g / 100 ml (20 ° C) | |
| Surhet (p K a ) | ~ −1 |
| Konjugert base | Klorat |
| Struktur | |
| pyramideformet | |
| Farer | |
| Viktigste farer | Oksidant, etsende |
| Sikkerhetsdatablad | Se: datasiden |
| GHS-piktogrammer |
 
|
| GHS Signalord | Fare |
| H271 , H314 | |
| P210 , P220 , P221 , P260 , P264 , P280 , P283 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P306 + 360 , P310 , P321 , P363 , P370 + 378 , P371 + 380 + 375 , P405 , P501 | |
| NFPA 704 (branndiamant) | |
| Beslektede forbindelser | |
|
Andre anioner
|
bromsyre jodsyre |
|
Andre kationer
|
ammonium- klorat natriumklorat kaliumklorat |
|
Beslektede forbindelser
|
saltsyre underklorsyrling klorsyrling perklorsyre |
| Supplerende dataside | |
|
Brytningsindeks ( n ), Dielektrisk konstant (ε r ), etc. |
|
|
Termodynamiske
data |
Faseadferd fast – flytende – gass |
| UV , IR , NMR , MS | |
|
Med mindre annet er angitt, blir data gitt for materialer i standardtilstand (ved 25 ° C, 100 kPa). |
|
| Infoboksreferanser | |
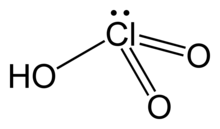
Klorsyre , H Cl O 3 , er en oksosyre med klor , og den formelle forløper av klorat salter. Det er en sterk syre ( p K a ≈ −2.7) og oksidasjonsmiddel .
Eiendommer
Klorsyre er termodynamisk ustabil med hensyn til disproporsjonering .
Klorsyre er stabil i kald vandig oppløsning opp til en konsentrasjon på ca. 30%, og oppløsning på opptil 40% kan fremstilles ved forsiktig fordampning under redusert trykk. Over disse konsentrasjonene nedbrytes klorsyreoppløsninger for å gi en rekke produkter, for eksempel:
- 8 HClO 3 → 4 HClO 4 + 2 H 2 O + 2 Cl 2 + 3 O to
- 3 HClO 3 → HClO 4 + H 2 O + 2 ClO 2
Farer
Klorsyre er et kraftig oksidasjonsmiddel. De fleste organiske stoffer og brennbare stoffer vil tømme ved kontakt.
Produksjon
Det kan fremstilles ved omsetning av svovelsyre med bariumklorat , idet det uoppløselige bariumsulfatet fjernes ved utfelling:
- Ba (ClO 3 ) 2 + H 2 SO 4 → 2 HClO 3 + BaSO 4
En annen metode er oppvarming av hypoklorsyre, og produserer klorsyre og hydrogenklorid :
- 3 HClO → HClO 3 + 2 HC1
Se også
Referanser
- Greenwood, Norman N .; Earnshaw, Alan (1997). Elementenes kjemi (2. utgave). Butterworth-Heinemann . ISBN 978-0-08-037941-8 .
- R. Bruce King, red. (1994). "Klorsyre". Encyclopedia of Inorganic Chemistry . 2 . Chichester: Wiley. s. 658. ISBN 0-471-93620-0 .

