Koordineringsgeometri - Coordination geometry
Begrepet koordinasjonsgeometri brukes i en rekke relaterte felt innen kjemi og faststoffkjemi / fysikk.
innhold
molekyler
Koordinasjonsgeometrien til et atom er det geometriske mønsteret som dannes av atomer rundt det sentrale atomet.
Uorganiske koordinasjonskomplekser
Innenfor uorganiske koordinasjonskomplekser er det det geometriske mønsteret som dannes av atomene i ligandene som er bundet til det sentrale atomet i et molekyl eller et koordinasjonskompleks . Det geometriske arrangementet vil variere i henhold til antall og type ligander bundet til metallsenteret, og til koordinasjonspreferansen til det sentrale atom, typisk et metall i et koordinasjonskompleks . Antallet bundne atomer (dvs. antall σ-bindinger mellom sentrale atom og ligander) betegnes som koordinasjonsnummer . Det geometriske mønsteret kan beskrives som en polyhedron der toppunktene til polyhedronen er sentrene for koordinerende atomer i ligandene.
Koordinasjonspreferansen til et metall varierer ofte med oksidasjonstilstanden. Antall koordineringsobligasjoner ( koordinasjonsnummer ) kan variere fra to så høye som 20 i Th (η 5- C 5 H 5 ) 4 .
En av de vanligste koordineringsgeometrier er oktaedralen , der seks ligander er koordinert til metallet i en symmetrisk fordeling, noe som fører til dannelse av en oktaedron hvis linjer ble trukket mellom ligandene. Andre vanlige koordineringsgeometrier er tetraedriske og firkantede plane .
Krystallfeltteori kan brukes til å forklare den relative stabiliteten til overgangsmetallforbindelser med forskjellig koordinasjonsgeometri, så vel som tilstedeværelsen eller fraværet av paramagnetisme , mens VSEPR kan brukes til komplekser av hovedgruppeelement for å forutsi geometri.
Bruk av krystallografi
I en krystallstruktur er koordinasjonsgeometrien til et atom det geometriske mønsteret for koordinering av atomer der definisjonen av koordinerende atomer avhenger av bindingsmodellen som brukes. For eksempel har hver natriumatom i bergsaltionisk struktur seks nærliggende kloridioner i en oktaedrisk geometri, og hvert klorid har tilsvarende seks nærliggende natriumioner i nærheten av en oktaedrisk geometri. I metaller med kroppen sentrert kubisk (bcc) struktur har hvert atom åtte nærmeste naboer i en kubisk geometri. I metaller med den ansiktet sentrerte kubikkstrukturen (fcc) har hvert atom tolv nærmeste naboer i en kuboktaedrisk geometri.
Tabell over koordineringsgeometrier
En tabell over de koordineringsgeometrier som er påvist er vist nedenfor med eksempler på forekomst av disse i komplekser funnet som diskrete enheter i forbindelser og koordinasjonssfærer rundt atomer i krystaller (hvor det ikke er noe diskret kompleks).
| Koordineringsnummer | Geometry | Eksempler på diskret (finitt) kompleks | Eksempler i krystaller (uendelige faste stoffer) | |
|---|---|---|---|---|
| 2 | lineær |
|
Ag (CN) 2 - i KAg (CN) 2 | Ag i sølvcyanid , Au i AUI |
| 3 | trigonal planar |

|
HgI 3 - | O i TiO 2 rutilstruktur |
| 4 | tetrahedral |

|
CoCl 4 2− | Zn og S i sinksulfid , Si i silisiumdioksid |
| 4 | firkantet plan |

|
AgF 4 - | CuO |
| 5 | trigonal bipyramidale |

|
SnCl 5 - | |
| 5 | firkantet pyramidal |

|
InCl 5 2− in (NEt 4 ) 2 InCl 5 | |
| 6 | octahedral |

|
Fe (H 2 O) 6 2+ | Na og Cl i NaCl |
| 6 | trigonal prismatisk |

|
W (CH 3 ) 6 | Som i NiAs , Mo i MoS 2 |
| 7 | femkantede bipyramidale |

|
ZrF 7 3− in (NH 4 ) 3 ZrF 7 | Pa i PaCl 5 |
| 7 | avkortet oktaedralen |

|
MoF 7 - | La in A-La 2 O 3 |
| 7 | avkortet trigonal prismatisk |
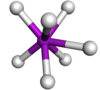
|
TaF 7 2− i K 2 TaF 7 | |
| 8 | firkantet antiprismatisk |

|
TaF 8 3- i Na 3 taF 8 Zr (H 2 O) 8 4+ aqua kompleks |
Thorium (IV) jodid |
| 8 |
dodekahedralen (merk: mens dette er betegnelsen som vanligvis brukes, er det riktige uttrykket "bisdisphenoid" eller " snub disphenoid " da denne polyhedronen er en deltahedron ) |

|
Mo (CN) 8 4− in K 4 [Mo (CN) 8 ] .2H 2 O | Zr i K 2 ZrF 6 |
| 8 | bicappet trigonal prismatisk |
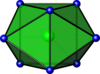
|
ZrF 8 4− | PuBr 3 |
| 8 | kubikk | Cesiumklorid , kalsiumfluorid | ||
| 8 | sekskantet bipyramidalt |
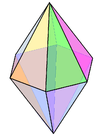
|
N i Li 3 N | |
| 8 | oktaedrisk, trans-bicapped | Ni i nikkel-arsenit , NiAs; 6 Som naboer + 2 Ni-avdekking | ||
| 8 | trigonal prismatisk, trekantet ansikt bicappet | Ca i CaFe 2 O 4 | ||
| 9 | trikappet trigonal prismatisk |
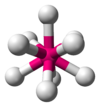
|
[ReH 9 ] 2- i kalium nonahydridorhenate Th (H 2 O) 9 4+ aqua kompleks |
SrCl 2 .6H 2 O, Th i RbTh 3 F 13 |
| 9 | avkortet firkantet antiprismatisk |

|
[Th (tropolonate) 4 (H 2 O)] | La i LaTe 2 |
| 10 | bicapped firkantet antiprismatisk | Th (C 2 O 4 ) 4 2− | ||
| 11 | Th i [Th IV (NO 3 ) 4 (H 2 O) 3 ] (NO 3 - er bidentat) | |||
| 12 | ikosaeder |

|
Th in Th (NO 3 ) 6 2- ion in Mg [Th (NO 3 ) 6 ] .8H 2 O | |
| 12 | kuboktaeder |

|
Zr IV (η 3 - (BH 4 ) 4 ) | atomer i fcc metaller f.eks Ca |
| 12 | antikuboktaeder ( trekantet orthobicupola ) |

|
atomer i hcp-metaller f.eks. Sc | |
| 12 | tohåndsheksagonal antiprismatisk | U (BH 4 ) 4 |
Navngivelse av uorganiske forbindelser
IUPAC har introdusert det poledriske symbolet som en del av deres IUPAC-nomenklatur for uorganisk kjemi 2005-anbefalinger for å beskrive geometrien rundt et atom i en forbindelse.
IUCr har foreslått et symbol som er vist som et påskrift i firkantede parenteser i den kjemiske formelen. For eksempel ville CaF 2 være Ca [8cb] F 2 [4t] , der [8cb] betyr kubisk koordinering og [4t] betyr tetraedrisk. De ekvivalente symbolene i IUPAC er henholdsvis CU −8 og T −4.
IUPAC-symbolet er anvendelig på komplekser og molekyler, mens IUCr-forslaget gjelder krystallinske faste stoffer.
