Heksametylfosforamid - Hexamethylphosphoramide
|
|

|
|
| Navn | |
|---|---|
|
Foretrukket IUPAC-navn
Heksametylfosforsyre triamid |
|
| Andre navn
Heksametylfosforamid
heksametapol HMPA Fosfor tris (dimetylamid) (ikke anbefalt) HMPT |
|
| Identifikatorer | |
|
3D-modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.010.595 |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eiendommer | |
| C 6 H 18 N 3 O P | |
| Molarmasse | 179,20 g / mol |
| Utseende | klar, fargeløs væske |
| Lukt | aromatisk, mild, aminlignende |
| Tetthet | 1,03 g / cm 3 |
| Smeltepunkt | 7,20 ° C (44,96 ° F; 280,35 K) |
| Kokepunkt | 232,5 ° C (450,5 ° F; 505,6 K) CRC |
| blandbare | |
| Damptrykk | 0,03 mmHg (4,0 Pa) ved 20 ° C |
| Farer | |
| Viktigste farer | Mistenkt kreftfremkallende |
| Sikkerhetsdatablad | Oxford MSDS |
| Flammepunkt | 104,4 ° C (219,9 ° F; 377,5 K) |
| NIOSH (amerikanske helseeksponeringsgrenser): | |
|
PEL (tillatt)
|
ingen |
|
REL (anbefalt)
|
Ca |
|
IDLH (umiddelbar fare)
|
Ca [ND] |
|
Med mindre annet er angitt, blir data gitt for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infoboksreferanser | |
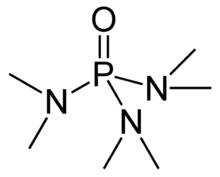
Heksametylfosforamid , ofte forkortet HMPA , er et fosforamid (et amid av fosforsyre ) med formelen [(CH 3 ) 2- N] 3 PO. Denne fargeløse væsken er et nyttig reagens i organisk syntese .
Struktur og reaktivitet
HMPA er oksydet til det svært basiske tertiære fosfinheksametylfosfor-triamidet (HMPT), P (NMe 2 ) 3 . Som andre fosfinoksider (som trifenylfosfinoksid ), har molekylet en tetrahedral kjerne og en P = O-binding som er sterkt polarisert, med betydelig negativ ladning på oksygenatomet.
Forbindelser som inneholder en nitrogen- fosforbinding nedbrytes vanligvis av saltsyre for å danne et protonert amin og fosfat.
Den løser opp alkalimetaller som danner blå løsninger som er stabile i noen timer. Solvatiserte elektroner er til stede i disse blå løsningene.
applikasjoner
HMPA er en spesialitet løsningsmiddel for polymerer , gasser , og metallorganiske forbindelser . Det forbedrer selektiviteten til litieringsreaksjoner ved å bryte opp oligomerer av litiumbaser som butyllitium . Fordi HMPA selektivt løser kationer, akselererer den ellers langsomme S N 2-reaksjoner ved å generere mer bare anioner. De grunnleggende nitrogensentrene i HMPA koordinerer sterkt til Li + .
HMPA er en ligand i de nyttige reagenser basert på molybden peroksyd komplekser, for eksempel, MoO (O 2 ) 2 (HMPA) (H 2 O) anvendes som et oksidasjonsmiddel i organisk syntese.
Alternative reagenser
Dimetylsulfoksid kan ofte brukes i stedet for HMPA som et samløsningsmiddel. Begge er sterke hydrogenbindingsakseptorer , og oksygenatomene deres binder metallkationer . Andre alternativer til HMPA inkluderer N , N '-tetraalkylurea DMPU (dimetylpropylenurea) eller DMI (1,3-dimetyl-2-imidazolidinon). Tripyrrolidinophosphoric syretriamid (TPPA) har blitt rapportert å være en god erstatning reagens for HMPA i reduksjoner med samarium-dijodid og som en Lewis-base additiv til mange reaksjoner som involverer samarium ketyls .
Toksisitet
HMPA er bare lett giftig, men har vist seg å forårsake kreft hos rotter. HMPA kan nedbrytes ved virkning av saltsyre .
Referanser
Eksterne linker
- "Heksametylfosforamid CAS-nr. 680-31-9" (PDF) . Rapport om kreftfremkallende stoffer (12. utg.). Nasjonalt toksikologiprogram, Institutt for helse og menneskelige tjenester. 2011.
- "Heksametylfosforamid" . NIOSH Pocket Guide til kjemiske farer . Senter for sykdomskontroll og forebygging, Institutt for helse og menneskelige tjenester. 2011.
- Merck indeks . 4761 (12. utgave).
