Molekylær anerkjennelse - Molecular recognition
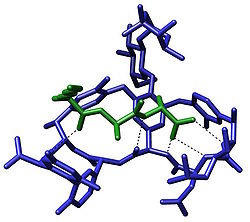

Begrepet molekylær gjenkjenning refererer til den spesifikke interaksjonen mellom to eller flere molekyler gjennom ikke-kovalent binding slik som hydrogenbinding , metallkoordinering , hydrofobe krefter , van der Waals-krefter , π-π-interaksjoner , halogenbinding eller resonante interaksjonseffekter . I tillegg til disse direkte interaksjonene kan løsningsmidler spille en dominerende indirekte rolle for å drive molekylær gjenkjenning i løsning. Den vert og gjest er involvert i molekylær gjenkjennelse oppviser molekyl komplementaritet . Unntak er molekylære beholdere, inkludert f.eks. Nanorør , der portaler i hovedsak styrer selektivitet.
Biologiske systemer

Molekylær gjenkjenning spiller en viktig rolle i biologiske systemer og observeres mellom reseptor -ligand, antigen - antistoff , DNA - protein , sukker - lektin , RNA - ribosom , etc. Et viktig eksempel på molekylær gjenkjenning er antibiotika vancomycin som selektivt binder seg til de peptider med terminal D-alanyl-D-alanin i bakterieceller gjennom fem hydrogenbindinger. Vankomycinet er dødelig for bakteriene, siden det når det har bundet seg til disse peptidene, ikke kan brukes til å konstruere bakteriens cellevegg .
Syntetisk molekylær gjenkjenning
Nyere arbeid antyder at molekylære gjenkjennelseselementer kan produseres syntetisk på nanoskala, og omgå behovet for naturlig forekommende molekylære gjenkjennelseselementer for utvikling av sanseverktøy for små molekyler. Bio-mimetiske polymerer som peptoider kan brukes til å gjenkjenne større biologiske mål som proteiner og konjugering av polymerer til syntetiske fluorescerende nanomaterialer kan generere syntetiske makromolekylære strukturer som fungerer som syntetiske antistoffer for optisk proteingjenkjenning og deteksjon.
Supramolekylære systemer
Kjemikere har demonstrert at mange kunstige supramolekylære systemer kan utformes som viser molekylær gjenkjenning. Et av de tidligste eksemplene på et slikt system er kronetere som er i stand til selektivt å binde spesifikke kationer. Imidlertid har en rekke kunstige systemer blitt etablert siden.
Statisk vs. dynamisk
Molekylær gjenkjenning kan deles inn i statisk molekylær gjenkjenning og dynamisk molekylær gjenkjenning . Statisk molekylær gjenkjenning sammenlignes med samspillet mellom en nøkkel og et nøkkelhull; det er en 1: 1 type komplekseringsreaksjon mellom et vertsmolekyl og et gjestemolekyl for å danne et vert -gjest -kompleks . For å oppnå avansert statisk molekylær gjenkjenning, er det nødvendig å lage gjenkjennelsessteder som er spesifikke for gjestemolekyler.
I tilfelle av dynamisk molekylær gjenkjenning påvirker bindingen av den første gjesten til det første bindingsstedet til en vert assosiasjonskonstanten til en andre gjest med et andre bindingssted. som fører til bindende samarbeid . I tilfelle av positive allosteriske systemer øker bindingen av den første gjesten assosiasjonskonstanten til den andre gjesten. Mens for negative allosteriske systemer reduserer bindingen av den første gjesten assosiasjonskonstanten med den andre. Den dynamiske naturen til denne typen molekylær gjenkjenning er spesielt viktig siden den gir en mekanisme for å regulere binding i biologiske systemer. Dynamisk molekylær gjenkjenning kan forbedre evnen til å skille mellom flere konkurrerende mål via den konformasjonelle korrekturlesingsmekanismen . Dynamisk molekylær gjenkjenning studeres også for bruk i svært funksjonelle kjemiske sensorer og molekylære enheter .
Kompleksitet
En nylig studie basert på molekylære simuleringer og samsvarskonstanter beskriver molekylær anerkjennelse som et fenomen av organisering. Selv for små molekyler som karbohydrater, kan gjenkjennelsesprosessen ikke forutsies eller utformes selv om vi antar at hver enkelt hydrogenbindings styrke er nøyaktig kjent. Imidlertid, som Mobley et al. konkludert, må den nøyaktige forutsigelsen av de molekylære gjenkjenningshendelsene gå utover det statiske øyeblikksbildet av en enkelt ramme mellom gjesten og verten. Entropier er viktige bidragsytere til bindende termodynamikk og må redegjøres for å kunne forutsi gjenkjennelsesprosessen mer nøyaktig. Entropier er sjelden observerbare i enkeltbundne strukturer (statisk øyeblikksbilde).
Intragen komplementering
Jehle påpekte at ladningsfluktuasjonskrefter, når de er nedsenket i en væske og blandes med andre molekyler, favoriserer assosiasjon av identiske molekyler som nærmeste naboer. I samsvar med dette prinsippet gjennomgår de mange kopiene av et polypeptid som er kodet av et gen ofte molekylær gjenkjenning med hverandre for å danne en ordnet multipolypeptidproteinstruktur. Når et slikt protein dannes av polypeptider produsert av to forskjellige mutante alleler av et bestemt gen, kan proteinet sammensatt av en blanding av polypeptider utvise større funksjonell aktivitet enn multipolypeptidproteinet dannet av hver av mutantene alene. I et slikt tilfelle omtales fenomenet som intragenisk komplementering .
Intragenisk komplementering (også kalt interallel komplementering) har blitt påvist i mange forskjellige gener i en rekke organismer. Crick og Orgel analyserte resultatene av slike studier og kom til den konklusjon at intragenisk komplementering generelt oppstår fra samspillet mellom forskjellige defekte polypeptidmonomerer når de danner et ordnet aggregat som de kaller en "multimer."
Se også
- Journal of Molecular Recognition
- SAMPL -utfordring
- Ikke -kovalente interaksjoner
- Supramolekylær kjemi
- Allostery
- Samarbeid
- Molekylær montør
Referanser
Eksterne linker
- http://www.mdpi.org/ijms/sections/molecular-recognition.htm Spesialutgave om molekylær anerkjennelse i Int. J. Mol. Sci.

