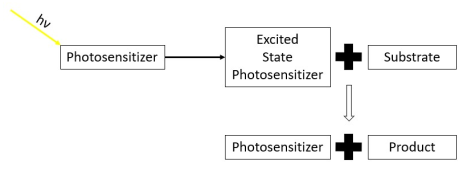
Fotosensibilisator - Photosensitizer

Fotosensibilisatorer produserer en fysisk-kjemisk endring i et nabomolekyl ved enten å donere et elektron til substratet eller ved å abstrahere et hydrogenatom fra substratet. På slutten av denne prosessen går fotosensibilisereren til slutt tilbake til bakken , hvor den forblir kjemisk intakt til fotosensibilisereren absorberer mer lys. Dette betyr at fotosensibilisatoren forblir uendret før og etter den energiske utvekslingen, omtrent som heterogen fotokatalyse . En gren av kjemi som ofte bruker fotosensibiliserende midler er polymerkjemi , ved bruk av fotosensibilisatorer i reaksjoner som fotopolymerisering , fototverrbinding og fotnedbrytning . Fotosensibiliserende midler brukes også til å generere langvarige eksiterte elektroniske tilstander i organiske molekyler ved bruk i fotokatalyse , fotonoppkonvertering og fotodynamisk terapi . Generelt absorberer fotosensibilisatorer elektromagnetisk stråling bestående av infrarød stråling , synlig lysstråling og ultrafiolett stråling og overfører absorbert energi til nabomolekyler. Denne absorpsjonen av lys er mulig med fotosensibiliserende store avlokaliserte π-systemer , som senker energien fra HOMO- og LUMO- orbitaler for å fremme fotoexcitasjon . Mens mange fotosensibiliserende midler er organiske eller metallorganiske forbindelser, er det også eksempler på bruk av halvleder kvanteprikker som fotosensibilisatorer.
Teori
Definisjon
Fotosensibiliserende stoffer er molekyler som absorberer lys (hν) og overfører energien fra det innfallende lyset til et annet nærliggende molekyl. Dette lyset er ofte innenfor det synlige spekteret eller det infrarøde spekteret , ettersom enhver elektromagnetisk stråling med høyere energi kan resultere i den fotoelektriske effekten . Ved å absorbere fotoner av stråling fra innfallende lys, er fotosensibilisatorer i stand til å fremme et jordtilstandselektron til en eksit singletilstand . Denne elektronen i den eksiterte singlettilstanden vender deretter i sin indre spinntilstand via Intersystem-kryssing for å bli en opphisset triplettilstandselektron . Elektronens levetid i den eksiterte tilstanden forlenges ved å snurre i tripletilstanden. Langvarige triplettilstander gir fotosensibiliserende molekyler en økt sannsynlighet for å samhandle med andre molekyler i nærheten. Fotosensibilisatorer opplever varierende effektivitetsnivåer for intersystemkrysning ved forskjellige bølgelengder av lys basert på den indre elektroniske strukturen til molekylet.
Parametere
For at et molekyl skal betraktes som et fotosensibilisator:
- Fotosensibilisatoren må gi en fysisk-kjemisk endring på et substrat etter at det har absorbert innfallende lys.
- Etter å ha gitt en kjemisk endring, går fotosensibilisereren tilbake til sin opprinnelige kjemiske form.
Det er viktig å skille lysfølsomme midler fra andre fotokjemiske interaksjoner, inkludert, men ikke begrenset til, fotoinitiatorer , fotokatalysatorer , fotosyrer og fotopolymerisasjoner . Fotosensibilisatorer bruker lys for å vedta en kjemisk endring i et substrat; etter den kjemiske endringen, går fotosensibilisereren tilbake til sin opprinnelige tilstand, og forblir kjemisk uendret fra prosessen. Fotoinitiatorer absorberer lys for å bli en reaktiv art, vanligvis en radikal eller et ion , der den reagerer med en annen kjemisk art. Disse fotoinitiatorene endres ofte kjemisk etter reaksjonen. Fotokatalysatorer fremskynder kjemiske reaksjoner som er avhengige av lys. Mens noen fotosensibiliserende midler kan fungere som fotokatalysatorer, kan ikke alle fotokatalysatorer fungere som lysfølsomme midler. Fotosyrer (eller fotobaser) er molekyler som blir surere (eller basiske) ved absorpsjon av lys. Fotosyrer øker surheten når de absorberer lys og kobles termisk tilbake til sin opprinnelige form når de slapper av. Fotosyregeneratorer gjennomgår en irreversibel forandring for å bli en sur art ved lysabsorpsjon. Fotopolymerisering kan skje på to måter. Fotopolymerisering kan forekomme direkte hvor monomerene absorberer det innfallende lyset og begynner å polymerisere, eller det kan skje gjennom en fotosensibiliseringsmediert prosess der fotosensibilisereren absorberer lyset først før den overfører energi til monomerer.
Historie
Fotosensibiliserende midler har eksistert i naturlige systemer så lenge klorofyll og andre lysfølsomme molekyler har vært en del av plantelivet, men studier av lysfølsomme midler startet allerede på 1900-tallet, hvor forskere observerte fotosensibilisering i biologiske underlag og i behandling av kreft. Mekanistiske studier relatert til fotosensibilisatorer begynte med forskere som analyserte resultatene av kjemiske reaksjoner der fotosensibiliserende foto-oksiderte molekylært oksygen til peroksidarter. Resultatene ble forstått ved å beregne kvanteffektivitet og fluorescerende utbytter ved varierende bølgelengder av lys og sammenligne disse resultatene med utbyttet av reaktive oksygenarter . Imidlertid var det først på 1960-tallet at elektrondoneringsmekanismen ble bekreftet gjennom forskjellige spektroskopiske metoder, inkludert reaksjons-mellomstudier og luminescensstudier .
Begrepet fotosensibilisator vises ikke i vitenskapelig litteratur før på 1960-tallet. I stedet vil forskere referere til fotosensibiliserende midler som sensibiliserende stoffer som brukes i foto-oksidasjons- eller foto-oksygeneringsprosesser. Studier i løpet av denne tidsperioden med fotosensibiliserende stoffer benyttet organiske fotosensibiliserende midler, bestående av aromatiske hydrokarbonmolekyler , som kunne lette syntetiske kjemiske reaksjoner. Imidlertid, på 1970- og 1980-tallet, fikk fotosensibiliserende tiltrekningskraft i det vitenskapelige samfunnet for sin rolle innen biologiske prosesser og enzymatiske prosesser. Foreløpig blir fotosensibilisatorer studert for deres bidrag til felt som energihøsting, fotoredoksikatalyse i syntetisk kjemi og kreftbehandling.
Type fotosensibiliseringsprosesser
Det er to hovedveier for lysfølsomme reaksjoner.
Type I
I type I lysfølsomme reaksjoner blir fotosensibilisatoren begeistret av en lyskilde til en triplettilstand. Den eksiterte fotosensibilisatoren i tripletilstand reagerer deretter med et substratmolekyl som ikke er molekylært oksygen for både å danne et produkt og reformere fotosensibilisatoren. Type I lysfølsomme reaksjoner resulterer i at fotosensibilisatoren slukkes av et annet kjemisk substrat enn molekylært oksygen.
Type II
I lysfølsjerte reaksjoner av type II blir fotosensibiliseringsapparatet begeistret av en lyskilde til en triplettilstand. Den glade fotosensibiliserende reagerer deretter med et grunntilstand, triplet oksygenmolekyl . Dette exciterer oksygenmolekylet i singlettilstand, noe som gjør det til en reaktiv oksygenart . Ved eksitering reagerer oksygenmolekylet i singlet med et substrat for å danne et produkt. Type II lysfølsom reaksjon resulterer i at fotosensibilisatoren slukkes av et oksygenmolekyl fra bakken, som deretter reagerer med et substrat for å danne et produkt.
Sammensetning av fotosensibilisatorer
Fotosensibilisatorer kan plasseres i 3 generaliserte domener basert på deres molekylære struktur. Disse tre domenene er organometalliske fotosensibilisatorer, organiske fotosensibiliserende stoffer og nanomateriale fotosensibiliserende midler.
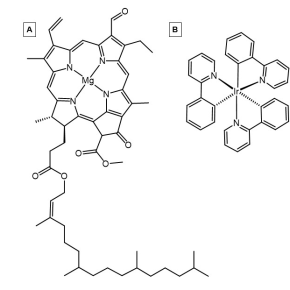
Organometallic
Organometalliske fotosensibiliserende stoffer inneholder et metallatom som er chelatert til minst en organisk ligand . Den fotosensibiliserende kapasiteten til disse molekylene skyldes elektroniske interaksjoner mellom metallet og liganden (e). Populære elektronrike metallsentre for disse kompleksene inkluderer Iridium , Ruthenium og Rhodium . Disse metallene, så vel som andre, er vanlige metallsentre for lysfølsomme midler på grunn av deres høyt fylte d-orbitaler , eller høye d-elektronantall , for å fremme overføring av metall til ligandladning fra pi-elektronakseptante ligander. Denne interaksjonen mellom metallsenteret og liganden fører til et stort kontinuum av orbitaler i både den høyest okkuperte molekylære orbitalen (HOMO) og den laveste ubebodde molekylære orbitalen (LUMO) som tillater opphissede elektroner å bytte multiplikasjoner via kryssing av intersystem.
Mens mange organometalliske fotosensibiliserende forbindelser er fremstilt syntetisk, eksisterer det også naturlig forekommende, lyshøstende organometalliske fotosensibilisatorer. Noen relevante naturlig forekommende eksempler på organometalliske fotosensibilisatorer inkluderer klorofyll a og klorofyll B .
Organisk
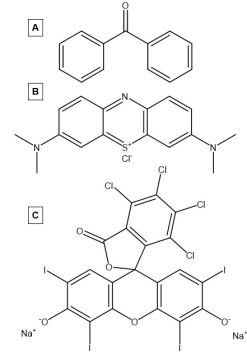
Organiske fotosensibilisatorer er karbonbaserte molekyler som er i stand til fotosensibilisering. De tidligste studerte fotosensibilisatorene var aromatiske hydrokarboner som absorberte lys i nærvær av oksygen for å produsere reaktive oksygenarter. Disse organiske fotosensibilisatorene består av sterkt konjugerte systemer som fremmer elektrondelokalisering . På grunn av deres høye konjugasjon har disse systemene et mindre gap mellom den høyest okkuperte molekylære orbitalen (HOMO) og den laveste ledige molekylære orbitalen (LUMO), så vel som et kontinuum av orbitaler i HOMO og LUMO. Det mindre båndgapet og kontinuiteten til orbitaler i både ledningsbåndet og valensbåndet tillater at disse materialene går inn i triplettilstanden mer effektivt, noe som gjør dem til bedre fotosensibiliserende. Noen bemerkelsesverdige organiske fotosensibiliserende stoffer som har blitt studert grundig, inkluderer benzofenoner, metylenblått og rose Bengal.
Nanomaterialer
Quantum Dots
Kolloidale kvantepunkter er halvledermaterialer i nanoskala med svært avstemmbare optiske og elektroniske egenskaper. Kvantprikker fotosensibiliserer via samme mekanisme som organometalliske fotosensibiliserende og organiske fotosensibiliserende midler, men deres nanoskalaegenskaper tillater større kontroll i særegne aspekter. Noen viktige fordeler ved bruk av kvantepunkter som fotosensibiliserende stoffer inkluderer deres lille, avstemmbare båndgap som muliggjør effektive overganger til triplettilstanden, og deres uløselighet i mange løsningsmidler som muliggjør enkel henting fra en syntetisk reaksjonsblanding.
Nanorods
Nanorods , som er like store som kvanteprikker, har justerbare optiske og elektroniske egenskaper. Basert på størrelse og materialesammensetning er det mulig å stille inn den maksimale absorpsjonstoppen for nanorods under syntesen. Denne kontrollen har ført til opprettelsen av fotosensibiliserende nanoroder.
applikasjoner
Medisinsk
Fotodynamisk terapi
Fotodynamisk terapi benytter lysfølsomme midler av type II for å høste lys for å nedbryte svulster eller kreftmasser. Denne oppdagelsen ble først observert tilbake i 1907 av Hermann von Tappeiner da han brukte eosin til å behandle hudtumorer. Den fotodynamiske prosessen er overveiende en ikke-invasiv teknikk hvor fotosensibiliserende legges i en pasient slik at den kan akkumuleres i svulsten eller kreften. Når fotosensibilisatoren når svulsten eller kreften, skinner bølgelengdespesifikt lys på utsiden av pasientens berørte område. Dette lyset (fortrinnsvis nær infrarød frekvens, da dette tillater inntrengning av huden uten akutt toksisitet) stimulerer lysfølsomhetselektronene til tripletilstanden. Ved eksitering begynner fotosensibilisatoren å overføre energi til nærliggende bakken tilstand triplet oksygen for å generere eksit singlet oksygen . De resulterende eksiterte oksygenarter nedbryter deretter selektivt svulsten eller kreftmassen.
I februar 2019 kunngjorde medisinske forskere at iridium festet til albumin , som skaper et fotosensibilisert molekyl, kan trenge gjennom kreftceller og, etter å ha blitt bestrålt med lys (en prosess som kalles fotodynamisk terapi ), ødelegge kreftcellene.
Energikilder
Fargestoffsensibiliserte solceller
I 1972 oppdaget forskere at klorofyll kunne absorbere sollys og overføre energi til elektrokjemiske celler. Denne oppdagelsen førte til slutt til bruk av lysfølsomme midler som høsting av sollys i solceller, hovedsakelig gjennom bruk av lysfølsomme fargestoffer. Fargestoffsensibiliserte solceller bruker disse lysfølsomme fargestoffene til å absorbere fotoner fra sollys og overføre energirike elektroner til det nærliggende halvledermaterialet for å generere elektrisk energiutgang. Disse fargestoffene fungerer som dopemidler til halvlederoverflater som muliggjør overføring av lysenergi fra fotosensibilisatoren til elektronisk energi i halvlederen. Disse fotosensibiliserende stoffene er ikke begrenset til fargestoffer. De kan ha form av en hvilken som helst lysfølsom struktur, avhengig av halvledermaterialet som de er festet til.
Hydrogengenererende katalysatorer
Via absorpsjon av lys kan fotosensibilisatorer bruke tripletilstandsoverføring for å redusere små molekyler, for eksempel vann, for å generere hydrogengass. Fra nå av har fotosensibiliserende stoffer generert hydrogengass ved å dele vannmolekyler i liten laboratorieskala.
Syntetisk kjemi
Photoredox Chemistry
Tidlig på 1900-tallet observerte kjemikere at forskjellige aromatiske hydrokarboner i nærvær av oksygen kunne absorbere bølgelengdespesifikt lys for å generere en peroksidart. Denne oppdagelsen av oksygenreduksjonen med en fotosensibilisator førte til at kjemikere studerte fotosensibiliserende midler som fotoredoksikatalysatorer for deres roller i katalysen av perisykliske reaksjoner og andre reduksjons- og oksidasjonsreaksjoner . Fotosensibiliserende stoffer i syntetisk kjemi tillater manipulering av elektroniske overganger i molekyler gjennom en eksternt anvendt lyskilde. Disse fotosensibiliserende stoffene som brukes i redokskjemi, kan være organiske, organometalliske eller nanomaterialer avhengig av de fysiske og spektrale egenskapene som kreves for reaksjonen.
Se også
- Kunstig fotosyntese
- Lysfølsomhet
- Fotodynamisk terapi
- Fotokatalyse
- Fargestoffsensibilisert solcelle
- Photoredox Catalysis
- Lette høstingsmaterialer
- Photoswitch