Dimetylsulfat - Dimethyl sulfate
|
|
|
|
| Navn | |
|---|---|
|
Foretrukket IUPAC -navn
Dimetylsulfat |
|
| Andre navn
Dimetylsulfat; Svovelsyredimetylester; Me 2 SO 4 ; DMSO 4 ; Dimetylester av svovelsyre; Metylsulfat
|
|
| Identifikatorer | |
|
3D -modell ( JSmol )
|
|
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.000.963 |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C 2 H 6 O 4 S | |
| Molar masse | 126,13 g/mol |
| Utseende | Fargeløs, fet væske |
| Lukt | svak, løkaktig |
| Tetthet | 1,33 g/ml, flytende |
| Smeltepunkt | −32 ° C (−26 ° F; 241 K) |
| Kokepunkt | 188 ° C (370 ° F; 461 K) (brytes ned) |
| Reagerer | |
| Løselighet | Metanol , diklormetan , aceton |
| Damptrykk | 0,1 mmHg (20 ° C) |
| -62,2 · 10 −6 cm 3 /mol | |
| Farer | |
| viktigste farer | Ekstremt giftig, kontaktfare, innåndingsfare, etsende, miljøfare, kreftfremkallende, mutagent |
| GHS -piktogrammer |
  
|
| GHS Signalord | Fare |
| H301 , H314 , H317 , H330 , H335 , H341 , H350 | |
| NFPA 704 (brann diamant) | |
| Flammepunkt | 83 ° C; 182 ° F; 356 K |
| Dødelig dose eller konsentrasjon (LD, LC): | |
|
LC 50 ( median konsentrasjon )
|
8,6 ppm (rotte, 4 timer) 75 ppm (marsvin, 20 min) 53 ppm (mus) 32 ppm (marsvin, 1 time) |
|
LC Lo ( lavest publisert )
|
97 spm (menneske, 10 min) |
| NIOSH (amerikanske helseeksponeringsgrenser): | |
|
PEL (tillatt)
|
TWA 1 ppm (5 mg/m 3 ) [hud] |
|
REL (anbefalt)
|
Ca TWA 0,1 ppm (0,5 mg/m 3 ) [hud] |
|
IDLH (Umiddelbar fare)
|
Ca [7 spm] |
| Relaterte forbindelser | |
|
Relaterte forbindelser
|
Dietylsulfat , metyltriflat , dimetylkarbonat |
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox -referanser | |
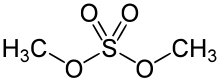
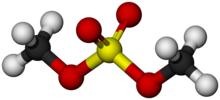
Dimetylsulfat er en kjemisk forbindelse med formel (CH 3 O) 2 SO 2 . Som diester av metanol og svovelsyre , er dens formel ofte skrevet som ( CH 3 ) 2 SO 4 eller Me 2 SO 4 , hvor CH 3 eller Me er metyl . Me 2 SO 4 brukes hovedsakelig som et metyleringsmiddel i organisk syntese .
Me 2 SO 4 er en fargeløs oljeaktig væske med en liten løklignende lukt (selv om det lukter ville det representere betydelig eksponering). Som alle sterke alkyleringsmidler er Me 2 SO 4 ekstremt giftig . Bruken som et laboratoriereagens har blitt erstattet i en viss grad ved metyltriflat , CF 3 SO 3 CH 3 , metylesteren av trifluormetansulfonsyre .
Historie
Dimetylsulfat ble oppdaget på begynnelsen av 1800 -tallet i en uren form. JP Claesson studerte senere grundig forberedelsen. Den ble brukt i kjemisk krigføring under første verdenskrig.
Produksjon
Dimetylsulfat kan syntetiseres i laboratoriet ved mange forskjellige metoder, den enkleste er forestringen av svovelsyre med metanol :
- 2 CH 3 OH + H 2 SO 4 → (CH 3 ) 2 SO 4 + 2 H 2 O
En annen mulig syntese innebærer destillasjon av metylhydrogensulfat:
- 2 CH 3 HSO 4 → H 2 SO 4 + (CH 3 ) 2 SO 4
Metylnitritt og metylklorsulfonat resulterer også i dimetylsulfat:
- CH 3 ONO + (CH 3 ) OSO 2 Cl → (CH 3 ) 2 SO 4 + NOCl
Me 2 SO 4 har blitt produsert kommersielt siden 1920 -tallet. En vanlig prosess er den kontinuerlige reaksjonen av dimetyleter med svoveltrioksyd .
- (CH 3 ) 2 O + SO 3 → (CH 3 ) 2 SO 4
Bruker
Dimetylsulfat er best kjent som et reagens for metylering av fenoler , aminer og tioler . En metylgruppe overføres raskere enn den andre. Metyloverføring antas å skje via en S N 2 -reaksjon. Sammenlignet med andre metyleringsmidler foretrekkes dimetylsulfat av industrien på grunn av dets lave kostnader og høye reaktivitet.
Metylering ved oksygen
Hyppigst Me 2 SO 4 anvendes for å metylat fenoler. Noen enkle alkoholer er også hensiktsmessig metylert, som illustrert ved omdannelsen av tert -butanol til t -butylmetyleter :
- 2 (CH 3 ) 3 COH + (CH 3 O) 2 SO 2 → 2 (CH 3 ) 3 COCH 3 + H 2 SO 4
Alkoksid -salter metyleres raskt:
- RO - Na + + (CH 3 O) 2 SO 2 → ROCH 3 + Na (CH 3 ) SO 4
Metyleringen av sukker kalles Haworth -metylering .
Metylering ved amin -nitrogen
Me 2 SO 4 brukes til å fremstille både kvaternære ammoniumsalter eller tertiære aminer :
- C 6 H 5 CH = NC 4 H 9 + (CH 3 O) 2 SO 2 → C 6 H 5 CH = N + (CH 3 ) C 4 H 9 + CH 3 OSO 3 -
Kvaterniserte fettammoniumforbindelser brukes som et overflateaktivt middel eller tøymykner. Metylering for å lage et tertiært amin er illustrert som:
- CH 3 (C 6 H 4 ) NH 2 + (CH 3 O) 2 SO 2 (i NaHCO 3 aq.) → CH 3 (C 6 H 4 ) N (CH 3 ) 2 + Na (CH 3 ) SO 4
Metylering ved svovel
I likhet med metylering av alkoholer blir merkaptidsalte lett metylert av Me 2 SO 4 :
- RS - Na + + (CH 3 O) 2 SO 2 → RSCH 3 + Na (CH 3 ) SO 4
Et eksempel er:
- p-CH 3 C 6 H 4 SO 2 Na + (CH 3 O) 2 SO 2 → p-CH 3 C 6 H 4 SO 2 CH 3 + Na (CH 3 ) SO 4
Denne metoden har blitt brukt til å forberede tioestere:
- RC (O) SH + (CH 3 O) 2 SO 2 → RC (O) S (CH 3 ) + HOSO 3 CH 3
Reaksjoner med nukleinsyrer
Dimetylsulfat (DMS) brukes til å bestemme den sekundære strukturen til RNA . Ved nøytral pH metylerer DMS uparede adenin- og cytosinrester på sine kanoniske Watson-Crick-ansikter, men det kan ikke metylere baseparrede nukleotider. Ved å bruke metoden kjent som DMS-MaPseq , inkuberes RNA med DMS for å metylere uparede baser. Deretter transkriberes RNA; den reverse transkriptase legger ofte feil DNA base når den støter på en denaturert RNA base. Disse mutasjonene kan påvises via sekvensering , og RNA antas å være enkeltstrenget ved baser med mutasjonshastigheter over bakgrunnen.
Dimetylsulfat kan påvirke den basespesifikke spaltningen av DNA ved å angripe imidazolringene som finnes i guanin. Dimetylsulfat metylerer også adenin i enkeltstrengede deler av DNA (f.eks. De med proteiner som RNA-polymerase som gradvis smelter og annealer DNA). Ved nyglødning forstyrrer disse metylgruppene adenin-guanin-baseparring. Nuklease S1 kan deretter brukes til å kutte DNA i enkeltstrengede områder (hvor som helst med et metylert adenin). Dette er en viktig teknikk for å analysere protein-DNA-interaksjoner.
Alternativer
Selv om dimetylsulfat er svært effektivt og rimelig, har dets toksisitet oppmuntret til bruk av andre metyleringsreagenser. Metyljodid er et reagens som brukes til O-metylering, som dimetylsulfat, men er mindre farlig og dyrere. Dimetylkarbonat , som er mindre reaktivt, har langt lavere toksisitet sammenlignet med både dimetylsulfat og metyljodid. Høytrykk kan brukes for å akselerere metylering med dimetylkarbonat. Generelt er toksisiteten til metyleringsmidler korrelert med deres effektivitet som metyloverføringsreagenser.
Sikkerhet
Dimetylsulfat er kreftfremkallende og mutagent , svært giftig , etsende og miljøfarlig . Dimetylsulfat absorberes gjennom huden, slimhinner og mage -tarmkanalen, og kan forårsake dødelig forsinket luftveisreaksjon. En okulær reaksjon er også vanlig. Det er ingen sterk lukt eller umiddelbar irritasjon for å advare om dødelig konsentrasjon i luften. Den LD50 (akutt, oral) er 205 mg / kg (rotte) og 140 mg / kg (mus), og LC50 (akutt) er 45 ppm / 4 timer (rotte). Damptrykket på 65 Pa er tilstrekkelig stort til å produsere en dødelig konsentrasjon i luft ved fordampning ved 20 ° C. Forsinket toksisitet tillater potensielt dødelig eksponering før utvikling av advarselssymptomer. Symptomene kan bli forsinket 6–24 timer. Konsentrerte oppløsninger av baser (ammoniakk, alkalier) kan brukes til å hydrolysere mindre søl og rester på forurenset utstyr, men reaksjonen kan bli voldsom med større mengder dimetylsulfat (se ICSC). Selv om forbindelsen hydrolyserer, kan behandling med vann ikke antas å dekontaminere dimetylsulfat.

