Strålebehandling utvendig stråle - External beam radiotherapy
| Strålebehandling utvendig stråle | |
|---|---|
| |
| Andre navn | Teleterapi |
| ICD-9-CM | 92,21 - 92,26 |
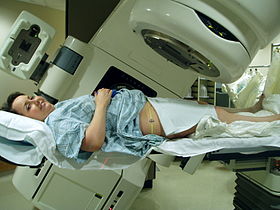
Ekstern strålebehandling ( EBRT ) er den vanligste formen for strålebehandling ( strålebehandling ). Pasienten sitter eller ligger på en sofa og en ekstern kilde til ioniserende stråling peker mot en bestemt del av kroppen. I motsetning til brachyterapi (forseglet kilde strålebehandling) og uforseglet kilde strålebehandling , der strålingskilden er inne i kroppen, leder ekstern strålebehandling strålingen mot svulsten fra utsiden av kroppen. Orthovoltage ("overfladisk") røntgen brukes for behandling av hudkreft og overfladiske strukturer. Megavoltage røntgenstråler brukes til å behandle dypsittende svulster (f.eks. Blære, tarm, prostata, lunge eller hjerne), mens megavoltage elektronstråler vanligvis brukes til å behandle overfladiske lesjoner som strekker seg til en dybde på omtrent 5 cm (økende stråleenergi tilsvarer til større penetrasjon). Røntgenstråler og elektronstråler er de klart mest brukte kildene for ekstern strålebehandling. Et lite antall sentre driver eksperimentelle og pilotprogrammer som bruker bjelker av tyngre partikler, spesielt protoner , på grunn av den raske nedgangen i absorbert dose under dybden av målet.
Røntgen og gammastråler

Konvensjonelt uttrykkes energien til diagnostiske og terapeutiske gamma- og røntgenstråler i kilovolt eller mega volt (kV eller MV), mens energien til terapeutiske elektroner uttrykkes i form av mega elektronvolt (MeV). I det første tilfellet er denne spenningen det maksimale elektriske potensialet som brukes av en lineær akselerator for å produsere fotonstrålen . Strålen består av et spekter av energier: maksimal energi er omtrent lik bjelkens maksimale elektriske potensial ganger elektronladningen. Dermed vil en 1 MV stråle produsere fotoner på ikke mer enn omtrent 1 MeV. Den gjennomsnittlige X-ray energi er bare ca 1/3 av maksimal energi. Strålekvalitet og hardhet kan forbedres med røntgenfiltre , noe som forbedrer homogeniteten til røntgenspekteret.
Medisinsk nyttige røntgenstråler produseres når elektroner akselereres til energier der enten den fotoelektriske effekten dominerer (for diagnostisk bruk, siden den fotoelektriske effekten gir relativt god kontrast med effektivt atomnummer Z ) eller Compton-spredning og parproduksjon dominerer (ved energier over ca. 200 keV for førstnevnte og 1 MeV for sistnevnte), for terapeutiske røntgenstråler. Noen eksempler på røntgenenergier brukt i medisin er:
- Svært lavenergi overfladiske røntgenstråler- 35 til 60 keV (mammografi, som prioriterer bløtvevskontrast, bruker kV-røntgener med svært lav energi)
- Overfladisk røntgenstråling-60 til 150 keV
- Diagnostiske røntgenstråler- 20 til 150 keV (mammografi til CT); dette er utvalget av fotonergier der den fotoelektriske effekten, som gir maksimal bløtvevskontrast, dominerer.
- Orthovoltage røntgenstråler- 200 til 500 keV
- Superspenningsrøntgenstråler- 500 til 1000 keV
- Megavoltage X-stråler -1 til 25 MeV (i praksis er nominelle energier over 15 MV uvanlige i klinisk praksis).
Megavoltage røntgen er langt vanligst innen strålebehandling for behandling av et bredt spekter av kreftformer. Overfladiske og ortovoltiske røntgenstråler har anvendelse for behandling av kreft på eller i nærheten av hudoverflaten. Vanligvis velges megavoltage-røntgenstråler med høyere energi når det er ønskelig å maksimere "hudsparende" (siden den relative dosen til huden er lavere for slike højenergibjelker).
Medisinsk nyttige fotonstråler kan også stammer fra en radioaktiv kilde som iridium-192 , cesium-137 eller radium -226 (som ikke lenger brukes klinisk) eller kobolt-60 . Slike fotonstråler, avledet fra radioaktivt forfall, er mer eller mindre monokromatisk og kalles riktig gammastråler . Det vanlige energiområdet er mellom 300 keV til 1,5 MeV, og er spesifikt for isotopen. Spesielt er fotonstråler fra radioisotoper omtrent monoenergetiske, i motsetning til det kontinuerlige bremsstrahlungspekteret fra en linac.
Terapeutisk stråling genereres hovedsakelig i strålebehandlingsavdelingen ved hjelp av noe av følgende utstyr:
- Overflatestrålebehandling (SRT) -maskiner produserer røntgenstråler med lav energi i samme energiområde som diagnostiske røntgenapparater, 20-150 kV, for å behandle hudlidelser.
- Orthovoltage røntgenmaskiner, som produserer røntgenstråler med høyere energi i området 200–500 kV. Denne strålingen ble kalt "dyp" fordi den kunne behandle svulster på dybder der "overfladisk" stråling med lavere energi (ovenfor) var uegnet. Orthovoltage-enheter har i hovedsak samme design som diagnostiske røntgenapparater . Disse maskinene er generelt begrenset til mindre enn 600 kV.
- Lineære akseleratorer ("linacs") som produserer megavoltage røntgenstråler. Den første bruken av en linac for medisinsk strålebehandling var i 1953 (se også strålebehandling ). Kommersielt tilgjengelige medisinske linakker produserer røntgenstråler og elektroner med et energiområde fra 4 MeV til rundt 25 MeV. Røntgenstrålene i seg selv produseres av den raske retardasjonen av elektroner i et målmateriale, vanligvis en wolframlegering , som produserer et røntgenspektrum via bremsstrahlung- stråling. Formen og intensiteten til strålen produsert av en linac kan modifiseres eller kollimeres på forskjellige måter. Dermed produseres konvensjonell, konform, intensitetsmodulert, tomografisk og stereotaktisk strålebehandling av spesialmodifiserte lineære akseleratorer.
- Koboltenheter som bruker stråling fra radioisotopkobolt -60, produserer stabile, dikromatiske stråler på 1,17 og 1,33 MeV, noe som resulterer i en gjennomsnittlig stråleenergi på 1,25 MeV. Koboltenhetens rolle har i stor grad blitt erstattet av den lineære akseleratoren, som kan generere høyere energistråling. Koboltbehandling har fortsatt en nyttig rolle å spille i visse applikasjoner (for eksempel Gamma Knife ) og er fremdeles i utbredt bruk over hele verden, siden maskinen er relativt pålitelig og enkel å vedlikeholde sammenlignet med den moderne lineære akseleratoren.

Elektroner
Røntgenstråler genereres ved å bombardere et materiale med høyt atomnummer med elektroner. Hvis målet fjernes (og strålestrømmen reduseres) oppnås en elektron med høy energi. Elektronstråler er nyttige for behandling av overfladiske lesjoner fordi maksimal doseavsetning skjer nær overflaten. Dosen reduseres deretter raskt med dybde og sparer underliggende vev. Elektronstråler har vanligvis nominelle energier i området 4–20 MeV. Avhengig av energien betyr dette et behandlingsområde på omtrent 1–5 cm (i vannekvivalent vev). Energier over 18 MeV brukes svært sjelden. Selv om røntgenmålet fjernes i elektronmodus, må strålen viftes ut med sett med tynne spredende folier for å oppnå flate og symmetriske doseprofiler i det behandlede vevet.
Mange lineære akseleratorer kan produsere både elektroner og røntgenstråler.
Hadron -terapi
Hadronterapi innebærer terapeutisk bruk av protoner , nøytroner og tyngre ioner (fullt ioniserte atomkjerner). Av disse er protonterapi den desidert vanligste, men fortsatt ganske sjeldne sammenlignet med andre former for ekstern strålebehandling, siden det krever stort og dyrt utstyr. Portalen (delen som roterer rundt pasienten) er en struktur i flere etasjer, og et protonterapisystem kan koste (fra 2009) opptil 150 millioner dollar.
Kollimator med flere blader
Moderne lineære akseleratorer er utstyrt med multileaf kollimatorer (MLC) som kan bevege seg innenfor strålingsfeltet når linac -portalen roterer, og blokkerer feltet etter behov i henhold til portalen. Denne teknologien gir planleggere for strålebehandling stor fleksibilitet når det gjelder å beskytte organer i fare (OARS), samtidig som den sikrer at den foreskrevne dosen blir levert til målet (e). En typisk flerbladskollimator består av to sett med 40 til 80 blader, hver rundt 5 mm til 10 mm tykke og flere centimeter i de to andre dimensjonene. Nyere MLC -er har nå opptil 160 blader. Hvert blad i MLC er parallelt med strålingsfeltet og kan flyttes uavhengig for å blokkere en del av feltet. Dette gjør at dosimetristen kan matche strålingsfeltet til svulstens form (ved å justere posisjonen til bladene), og dermed minimere mengden sunt vev som blir utsatt for stråling. På eldre linacer uten MLC må dette utføres manuelt ved hjelp av flere håndlagde blokker.
Intensitetsmodulert strålebehandling

A.) en internasjonal standard kildeholder (vanligvis bly),
B.) en holdering og
C.) en teleterapi "kilde" sammensatt av
D.) to nestede rustfrie stålbeholdere sveiset til
E.) to lokk i rustfritt stål som omgir
F.) et indre beskyttende skjold (vanligvis uranmetall eller en wolframlegering) og
G.) en sylinder av radioaktivt kildemateriale, ofte men ikke alltid kobolt-60 . Diameteren på "kilden" er 30 mm.
Intensitetsmodulert strålebehandling (IMRT) er en avansert strålebehandlingsteknikk som brukes for å minimere mengden normalt vev som bestråles i behandlingsfeltet. I noen systemer oppnås denne intensitetsmodulasjonen ved å flytte bladene i MLC i løpet av behandlingen, og derved levere et strålingsfelt med en ujevn (dvs. modulert) intensitet. Med IMRT er strålingsonkologer i stand til å bryte opp strålingsstrålen i mange "stråler". Dette tillater stråling onkologi for å variere intensiteten av hver beamlet. Med IMRT kan leger ofte begrense mengden stråling som mottas av sunt vev i nærheten av svulsten. Leger har funnet ut at dette noen ganger tillot dem å trygt gi en høyere dose stråling til svulsten, noe som potensielt øker sjansen for en kur.
Volumetrisk modulert lysbue terapi
Volumetric modulated arc therapy (VMAT) er en forlengelse av IMRT der den lineære akseleratoren i tillegg til MLC -bevegelse vil bevege seg rundt pasienten under behandlingen. Dette betyr at i stedet for at stråling kommer inn i pasienten gjennom bare et lite antall faste vinkler, kan den komme inn gjennom mange vinkler. Dette kan være gunstig for noen behandlingssteder der målvolumet er omgitt av en rekke organer som må spares for stråledose.
Utflatingsfilter gratis
Intensiteten til røntgenstrålene produsert i en megavoltage linac er mye høyere i midten av strålen sammenlignet med kanten. For å motvirke dette brukes et utflatingsfilter. Et utflatende filter er en kjegle av metall (vanligvis wolfram); etter at røntgenstrålen har passert gjennom utflatningsfilteret vil det ha en mer jevn profil, siden utflatingsfilteret er formet for å kompensere for forspenningen i momentumet til elektronene som faller på det. Dette gjør behandlingsplanleggingen enklere, men reduserer også intensiteten til strålen betydelig. Med større datakraft og mer effektive behandlingsplanleggingsalgoritmer reduseres behovet for enklere behandlingsplanleggingsteknikker ("fremoverplanlegging", der planleggeren direkte instruerer linacen om hvordan den foreskrevne behandlingen skal leveres). Dette har ført til økt interesse for utflating av filterfrie behandlinger (FFF).
Fordelen med FFF -behandlinger er den økte maksimale doseraten, med en faktor på opptil fire, noe som tillater reduserte behandlingstider og en reduksjon i effekten av pasientbevegelse på behandlingens levering. Dette gjør FFF til et område av spesiell interesse for stereotaktiske behandlinger. , der den reduserte behandlingstiden kan redusere pasientbevegelsen, og brystbehandlinger, der det er potensial for å redusere pustebevegelse.
Bildestyrt strålebehandling
Bildestyrt strålebehandling (IGRT) forsterker strålebehandling med bildediagnostikk for å øke nøyaktigheten og presisjonen av mållokalisering, og dermed redusere mengden sunt vev i behandlingsfeltet. Jo mer avanserte behandlingsteknikkene blir når det gjelder doseavsetning, desto høyere blir kravene til IGRT. For å la pasientene dra fordel av sofistikerte behandlingsteknikker som IMRT eller hadronterapi, blir pasientjusteringsnøyaktigheter på 0,5 mm og mindre ønskelige. Derfor beriker nye metoder som stereoskopisk digital kilovoltage-avbildningsbasert pasientposisjonskontroll (PPVS) for justeringsestimering basert på in-situ cone-beam computertomografi (CT) utvalget av moderne IGRT-tilnærminger.
Se også
- Brachyterapi
- Cyberknife
- Gamma Knife , en type radiokirurgi
- Intraoperativ elektronstrålebehandling
- Intraoperativ strålebehandling
- Nøytronfangstbehandling av kreft
- Strålebehandling
- Tomoterapi
Referanser
Generelle referanser
- Strålebehandling fysikk i praksis , redigert av JR Williams og DI Thwaites, Oxford University Press UK (2. utgave 2000), ISBN 0-19-262878-X
- Linear Particle Accelerator (Linac) Animation av Ionactive
- Overfladisk strålebehandling
- Nasjonalt institutt for radiologisk vitenskap (Japan)
