Nanosensor - Nanosensor
| Del av en serie artikler om |
| Nanoteknologi |
|---|
| Effekt og applikasjoner |
| Nanomaterialer |
| Molekylær selvmontering |
| Nanoelektronikk |
| Nanometrologi |
| Molekylær nanoteknologi |
Nanosensorer er nanoskalaenheter som måler fysiske størrelser og konverterer disse til signaler som kan oppdages og analyseres. Det er flere måter som foreslås i dag for å lage nanosensorer; disse inkluderer ovenfra og ned litografi, nedenfra og opp montering og molekylær selvmontering . Det finnes forskjellige typer nanosensorer i markedet og under utvikling for ulike applikasjoner, spesielt innen forsvars-, miljø- og helsevirksomhet. Disse sensorene deler den samme grunnleggende arbeidsflyten: en selektiv binding av en analyt, signalgenerering fra interaksjonen mellom nanosensoren og bioelementet, og prosessering av signalet til nyttige beregninger.
Kjennetegn
Nanomaterialbaserte sensorer har flere fordeler i følsomhet og spesifisitet i forhold til sensorer laget av tradisjonelle materialer, på grunn av nanomaterialefunksjoner som ikke er tilstede i bulk materiale som oppstår i nanoskalaen. Nanosensorer kan ha økt spesifisitet fordi de opererer i samme skala som naturlige biologiske prosesser, og tillater funksjonalisering med kjemiske og biologiske molekyler, med gjenkjennelseshendelser som forårsaker påviselige fysiske endringer. Forbedringer i følsomhet stammer fra det høye forholdet mellom overflate og volum av nanomaterialer, samt nye fysiske egenskaper til nanomaterialer som kan brukes som grunnlag for påvisning, inkludert nanofotonikk . Nanosensorer kan også potensielt integreres med nanoelektronikk for å legge til naturlig prosesseringsevne til nanosensoren.
I tillegg til sensitivitet og spesifisitet, gir nanosensorer betydelige fordeler i pris og responstid, noe som gjør dem egnet for applikasjoner med høy kapasitet. Nanosensorer gir sanntidsovervåking sammenlignet med tradisjonelle deteksjonsmetoder som kromatografi og spektroskopi. Disse tradisjonelle metodene kan ta dager til uker for å oppnå resultater og krever ofte investering i kapitalkostnader samt tid til prøveutarbeidelse.
Endimensjonale nanomaterialer som nanotråder og nanorør er godt egnet for bruk i nanosensorer, sammenlignet med plane eller tynne film plane enheter. De kan fungere både som svingere og ledninger for å overføre signalet. Deres høye overflateareal kan forårsake store signalendringer ved binding av en analyt. Deres lille størrelse kan muliggjøre omfattende multipleksing av individuelt adresserbare sensorenheter i en liten enhet. Driften deres er også "etikettfri" i den forstand at den ikke krever fluorescerende eller radioaktive markeringer på analyttene. Sinkoksyd nanotråd brukes til gassfølingsapplikasjoner, gitt at den har høy følsomhet overfor lav gasskonsentrasjon under omgivelsesforhold og lett kan fremstilles med lave kostnader.
Det er flere utfordringer for nanosensorer, inkludert å unngå drift og tilsmussing , utvikle reproduserbare kalibreringsmetoder, bruke forkonsentrasjons- og separasjonsmetoder for å oppnå en riktig analytkonsentrasjon som unngår metning og integrere nanosensoren med andre elementer i en sensorpakke på en pålitelig produserbar måte. Fordi nanosensorer er en relativt ny teknologi, er det mange ubesvarte spørsmål angående nanotoksikologi, som for tiden begrenser deres anvendelse i biologiske systemer.
Potensielle applikasjoner for nanosensorer inkluderer medisin, påvisning av forurensninger og patogener, og overvåking av produksjonsprosesser og transportsystemer. Ved å måle endringer i fysiske egenskaper ( volum , konsentrasjon , forskyvning og hastighet , gravitasjon , elektriske og magnetiske krefter, trykk eller temperatur ) kan nanosensorer være i stand til å skille mellom og gjenkjenne visse celler på molekylært nivå for å levere medisin eller overvåke utvikling til bestemte steder i kroppen. Typen signaltransduksjon definerer det viktigste klassifiseringssystemet for nanosensorer. Noen av hovedtyper av nanosensoravlesninger inkluderer optiske, mekaniske, vibrasjonsmessige eller elektromagnetiske.
Som et eksempel på klassifisering kan nanosensorer som bruker molekylært påtrykte polymerer (MIP) deles inn i tre kategorier, som er elektrokjemiske , piezoelektriske eller spektroskopiske sensorer. Elektrokjemiske sensorer induserer en endring i de elektrokjemiske egenskapene til sensormaterialet, som inkluderer ladning , ledningsevne og elektrisk potensial . Piezoelektriske sensorer konverterer mekanisk kraft til elektrisk kraft eller omvendt. Denne kraften blir deretter overført til et signal. MIP spektroskopiske sensorer kan deles inn i tre underkategorier, som er kjemiluminescerende sensorer, overflateplasmonresonanssensorer og fluorescenssensorer . Som navnet antyder, produserer disse sensorene lysbaserte signaler i form av kjemiluminescens, resonans og fluorescens. Som beskrevet i eksemplene, avhenger typen endring som sensoren oppdager, og typen signal den induserer av sensortypen
Driftsmekanismer
Det er flere mekanismer som en gjenkjenningshendelse kan overføres til et målbart signal; generelt utnytter disse nanomaterialets følsomhet og andre unike egenskaper for å oppdage en selektivt bundet analyt.
Elektrokjemiske nanosensorer er basert på å oppdage en motstandsendring i nanomaterialet ved binding av en analyt på grunn av endringer i spredning eller til uttømming eller akkumulering av ladningsbærere . En mulighet er å bruke nanotråder som karbon-nanorør , ledende polymerer eller metalloksyd-nanotråder som porter i felt-effekt-transistorer , selv om de ennå ikke hadde blitt demonstrert i forhold til den virkelige verden. Kjemiske nanosensorer inneholder et kjemisk gjenkjenningssystem (reseptor) og en fysiokjemisk transduser, der reseptoren samhandler med analyt for å produsere elektriske signaler. I ett tilfelle hadde den nanoporøse transduseren, etter interaksjon av analytten med reseptoren, en endring i impedans som ble bestemt som sensorsignalet. Andre eksempler inkluderer elektromagnetiske eller plasmoniske nanosensorer, spektroskopiske nanosensorer som overflateforbedret Raman-spektroskopi , magnetoelektroniske eller spintroniske nanosensorer og mekaniske nanosensorer.
Biologiske nanosensorer består av en bio-reseptor og en svinger. Den valgte transduksjonsmetoden er for tiden fluorescens på grunn av den høye følsomheten og den relative måling. Målingen kan oppnås ved å bruke følgende metoder: binding av aktive nanopartikler til aktive proteiner i cellen, ved bruk av stedstyrt mutagenese for å produsere indikatorproteiner, muliggjør målinger i sanntid, eller ved å lage et nanomateriale (f.eks. Nanofibre) med festeanlegg for bio-reseptorene. Selv om elektrokjemiske nanosensorer kan brukes til å måle intracellulære egenskaper, er de vanligvis mindre selektive for biologiske målinger, da de mangler den høye spesifisiteten til bio-reseptorer (f.eks. Antistoff, DNA).
Fotoniske enheter kan også brukes som nanosensorer for å kvantifisere konsentrasjoner av klinisk relevante prøver. Et driftsprinsipp for disse sensorene er basert på den kjemiske moduleringen av et hydrogelfilmvolum som inneholder et Bragg-gitter . Når hydrogelen svulmer eller krymper ved kjemisk stimulering, endrer Bragg-gitteret farge og diffrakterer lys ved forskjellige bølgelengder. Det diffrakterte lyset kan korreleres med konsentrasjonen av en målanalyt.
En annen type nanosensor er en som fungerer på en kolorimetrisk basis. Her forårsaker tilstedeværelsen av analytten en kjemisk reaksjon eller morfologisk endring for at en synlig fargeendring skal skje. En slik applikasjon er at nanopartikler i gull kan brukes til påvisning av tungmetaller. Mange skadelige gasser kan også oppdages ved en kolorimetrisk endring, for eksempel gjennom den kommersielt tilgjengelige Dräger Tube . Disse gir et alternativ til store, lab-skala systemer, da disse kan miniatyriseres for å brukes til punkt-of-sample-enheter. For eksempel er mange kjemikalier regulert av Environmental Protection Agency og krever omfattende testing for å sikre at nivået av forurensning ligger innenfor de riktige grensene. Kolorimetriske nanosensorer gir en metode for bestemmelse av mange forurensninger på stedet.
Produksjonsmetoder
Produksjonsmetoden spiller en sentral rolle i å bestemme egenskapene til den produserte nanosensoren ved at nanosensorens funksjon kan gjøres ved å kontrollere overflaten til nanopartikler. Det er to hovedtilnærminger ved produksjon av nanosensorer: top-down-metoder, som begynner med et mønster generert i større skala, og deretter redusert til mikroskala. Bunn-opp-metoder starter med atomer eller molekyler som bygger opp til nanostrukturer.
Top-down metoder
Litografi
Det innebærer å starte med en større blokk med noe materiale og hugge ut ønsket form. Disse skåret ut enheter, særlig tatt i bruk i spesifikke mikroelektromekaniske systemer brukes som mikrosensorer, som regel bare når micro størrelse, men den siste av disse har begynt å innlemme nanostørrelse komponenter. En av de vanligste metodene kalles elektronstrålelitografi. Selv om det er veldig kostbart, danner denne teknikken effektivt en fordeling av sirkulære eller ellipsoide plotter på den todimensjonale overflaten. En annen metode er elektroavsetting, som krever ledende elementer for å produsere miniatyriserte enheter.
Fibertrekking
Denne metoden består i å bruke en strekkanordning for å strekke hovedaksen til en fiber mens den varmes opp, for å oppnå skalaer i nanostørrelse. Denne metoden er spesielt brukt i optisk fiber for å utvikle optisk-fiberbaserte nanosensorer.
Kjemisk etsning
To forskjellige typer kjemisk etsning er rapportert. I Turner-metoden etses en fiber til et punkt mens den plasseres i menisken mellom flussyre og et organisk overlag . Denne teknikken har vist seg å produsere fibre med store koniske vinkler (og dermed øke lyset som når fiberspissen) og spissdiameter som kan sammenlignes med trekkemetoden. Den andre metoden er røretsing, som innebærer etsning av en optisk fiber med en enkeltkomponentløsning av hydrogenfluorid . En silisiumfiber, omgitt av en organisk kledning , poleres og den ene enden plasseres i en beholder med fluorsyre. Syren begynner deretter å etse bort fiberspissen uten å ødelegge kledningen. Når silisiumfiberen er etset vekk, fungerer polymerbekledningen som en vegg og skaper mikrostrømmer i flussyre som, sammen med kapillærvirkning , får fiberen til å etses i form av en kjegle med store, glatte tapers. Denne metoden viser mye mindre mottakelighet for miljøparametere enn Turner-metoden.
Bottom-up-metoder
Denne typen metoder innebærer å montere sensorene ut av mindre komponenter, vanligvis individuelle atomer eller molekyler. Dette gjøres ved å arrangere atomer i spesifikke mønstre, noe som er oppnådd i laboratorietester ved bruk av atomkraftmikroskopi , men som fremdeles er vanskelig å oppnå en masse og ikke er økonomisk levedyktig.
Selvmontering
Også kjent som "voksende", innebærer denne metoden oftest et allerede komplett sett med komponenter som automatisk monteres i et ferdig produkt. Nøyaktig å kunne reprodusere denne effekten for en ønsket sensor i et laboratorium, ville innebære at forskere kunne produsere nanosensorer mye raskere og potensielt langt billigere ved å la mange molekyler montere seg selv med liten eller ingen innflytelse utenfor, i stedet for å måtte montere hver sensor manuelt .
Selv om konvensjonelle fabrikasjonsteknikker har vist seg å være effektive, kan ytterligere forbedringer i produksjonsmetoden føre til minimering av kostnader og forbedring av ytelsen. Utfordringer med dagens produksjonsmetoder inkluderer ujevn fordeling, størrelse og form på nanopartikler, som alle fører til begrensning i ytelse. I 2006 patenterte forskere i Berlin oppfinnelsen av en ny diagnostisk nanosensor produsert med nanosfærelitografi (NSL), som gir nøyaktig kontroll over størrelse og form på nanopartikler og skaper nano-øyer. De metalliske nanoområdene produserte en økning i signaltransduksjon og dermed økt følsomhet til sensoren. Resultatene viste også at sensitiviteten og spesifikasjonen til den diagnostiske nanosensoren avhenger av størrelsen på nanopartiklene, at å redusere nanopartikkelstørrelsen øker følsomheten.
applikasjoner
Et av de første arbeidseksemplene på en syntetisk nanosensor ble bygget av forskere ved Georgia Institute of Technology i 1999. Det involverte å feste en enkelt partikkel på enden av et karbon-nanorør og måle vibrasjonsfrekvensen til nanorøret både med og uten partikkelen . Avviket mellom de to frekvensene tillot forskerne å måle massen av den festede partikkelen.
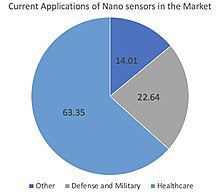
Siden da har økende mengder forskning gått inn i nanosensorer, der moderne nanosensorer er utviklet for mange applikasjoner. Foreløpig inkluderer applikasjonene av nanosensorer i markedet: helsetjenester, forsvar og militær, og andre som mat, miljø og jordbruk.
Forsvar og militær
Nanovitenskap som helhet har mange potensielle anvendelser i forsvars- og militærsektoren - inkludert kjemisk deteksjon, dekontaminering og rettsmedisin. Noen nanosensorer under utvikling for forsvarsapplikasjoner inkluderer nanosensorer for påvisning av eksplosiver eller giftige gasser. Slike nanosensorer fungerer på prinsippet om at gassmolekyler kan skilles ut basert på deres masse ved hjelp av for eksempel piezoelektriske sensorer. Hvis et gassmolekyl adsorberes på overflaten av detektoren, endres resonansfrekvensen til krystallet, og dette kan måles som en endring i elektriske egenskaper. I tillegg kan felteffekt-transistorer, brukt som potensiometre , oppdage giftige gasser hvis porten blir følsom for dem.
I en lignende applikasjon kan nanosensorer brukes i militær og rettshåndhevende klær og utstyr. Navy Research Laboratory's Institute for Nanoscience har studert kvanteprikker for anvendelse i nanofotonikk og identifisering av biologiske materialer. Nanopartikler lagdelt med polymerer og andre reseptormolekyler vil endre farge når de kommer i kontakt med analytter som giftige gasser. Dette varsler brukeren om at de er i fare. Andre prosjekter innebærer å legge inn klær med biometriske sensorer for å videreformidle informasjon om brukerens helse og vitalitet, noe som vil være nyttig for å overvåke soldater i kamp.
Overraskende nok er noen av de mest utfordrende aspektene ved å skape nanosensorer for forsvar og militær bruk, politiske i stedet for tekniske. Mange forskjellige offentlige etater må jobbe sammen for å fordele budsjetter og dele informasjon og fremgang i testing; dette kan være vanskelig med så store og komplekse institusjoner. I tillegg kan visum og innvandringsstatus bli et tema for utenlandske forskere - siden emnet er veldig følsomt, kan det noen ganger kreves godkjenning fra myndighetene. Endelig er det for tiden ikke veldefinerte eller klare forskrifter om nanosensortesting eller applikasjoner i sensorindustrien, noe som bidrar til vanskeligheter med implementering.
Mat og miljø
Nanosensorer kan forbedre ulike underområder innen mat- og miljøsektorer, inkludert matforedling, jordbruk, luft- og vannkvalitetsovervåking, samt emballasje og transport. På grunn av deres følsomhet, samt avstemmbarhet og resulterende bindingsselektivitet, er nanosensorer veldig effektive og kan utformes for et bredt utvalg av miljøapplikasjoner. Slike anvendelser av nanosensorer hjelper til med en praktisk, rask og ultrafølsom vurdering av mange typer miljøforurensende stoffer.
Kjemiske sensorer er nyttige for å analysere lukt fra matprøver og oppdage atmosfæriske gasser. Den "elektroniske nesen" ble utviklet i 1988 for å bestemme kvaliteten og friskheten til matprøver ved hjelp av tradisjonelle sensorer, men mer nylig har sensorfilmen blitt forbedret med nanomaterialer. En prøve plasseres i et kammer der flyktige forbindelser konsentreres i gassfasen, hvorved gassen pumpes gjennom kammeret for å føre aromaen til sensoren som måler dens unike fingeravtrykk. Forholdet mellom høyt overflateareal og volum for nanomaterialene muliggjør større interaksjon med analytter, og nanosensorens raske responstid muliggjør separasjon av forstyrrende responser. Også kjemiske sensorer er bygget med nanorør for å oppdage forskjellige egenskaper til gassformige molekyler. Mange karbon-nanorørbaserte sensorer er designet som felteffekt-transistorer, og utnytter følsomheten. Den elektriske ledningsevnen til disse nanorørene vil endres på grunn av ladningsoverføring og kjemisk doping fra andre molekyler, noe som gjør det mulig å oppdage dem. For å forbedre selektiviteten, involverer mange av disse et system der nanosensorer er bygget for å ha en bestemt lomme for et annet molekyl. Karbon-nanorør har blitt brukt for å registrere ionisering av gassformige molekyler mens nanorør laget av titan har blitt brukt for å oppdage atmosfæriske konsentrasjoner av hydrogen på molekylært nivå. Noen av disse er designet som felteffekttransistorer, mens andre utnytter optiske sensorfunksjoner. Selektiv analytbinding oppdages gjennom spektralforskyvning eller fluorescensmodulering. På en lignende måte har Flood et al. har vist at supramolecular host-guest chemistry tilbyr kvantitativ sensing ved bruk av Raman-spredt lys så vel som SERS .
Andre typer nanosensorer, inkludert kvanteprikker og nanopartikler i gull , blir for tiden utviklet for å oppdage forurensende stoffer og giftstoffer i miljøet. Disse utnytter den lokaliserte overflateplasmonresonansen (LSPR) som oppstår i nanoskalaen, noe som resulterer i bølgelengdespesifikk absorpsjon. Dette LSPR-spekteret er spesielt følsomt, og dets avhengighet av nanopartikkelstørrelse og miljø kan brukes på forskjellige måter for å designe optiske sensorer. For å dra nytte av LSPR-spektrumskiftet som oppstår når molekyler binder seg til nanopartikkelen, kan overflatene deres funksjonaliseres for å diktere hvilke molekyler som vil binde og utløse en respons. For miljøapplikasjoner kan kvantepunktoverflater modifiseres med antistoffer som binder spesifikt til mikroorganismer eller andre forurensende stoffer. Spektroskopi kan deretter brukes til å observere og kvantifisere dette spektrumskiftet, noe som muliggjør presis påvisning, potensielt i størrelsesorden molekyler. På samme måte kan fluorescerende halvledende nanosensorer dra nytte av fluorescensresonans energioverføring (FRET) for å oppnå optisk deteksjon. Kvanteprikker kan brukes som givere, og vil overføre elektronisk eksitasjonsenergi når de er plassert nær akseptormolekyler, og dermed miste fluorescensen. Disse kvanteprikkene kan funksjonaliseres for å bestemme hvilke molekyler som vil binde, hvorpå fluorescens vil bli gjenopprettet. Gull nanopartikkelbaserte optiske sensorer kan brukes til å oppdage tungmetaller veldig presist; for eksempel nivåer av kvikksølv så lave som 0,49 nanometer. Denne senseringsmodaliteten utnytter FRET, der tilstedeværelsen av metaller hemmer samspillet mellom kvanteprikker og gullnanopartikler, og slukker FRET-responsen. En annen potensiell implementering utnytter størrelsesavhengigheten til LSPR-spekteret for å oppnå ioneføling. I en studie, Liu et al. funksjonaliserte gullnanopartikler med et Pb 2+ sensitivt enzym for å produsere en blysensor. Generelt ville gullnanopartiklene samle seg når de nærmet seg hverandre, og endringen i størrelse ville resultere i en fargeendring. Interaksjoner mellom enzymet og Pb 2+ ionene ville hemme denne aggregeringen, og dermed kunne tilstedeværelsen av ioner påvises.
Den viktigste utfordringen knyttet til bruk av nanosensorer i mat og miljø er å bestemme deres tilknyttede toksisitet og generelle effekt på miljøet. Foreløpig er det ikke tilstrekkelig kunnskap om hvordan implementeringen av nanosensorer vil påvirke jord, planter og mennesker på lang sikt. Dette er vanskelig å håndtere fullstendig fordi nanopartikkeltoksisitet avhenger sterkt av typen, størrelsen og doseringen av partikkelen, samt miljøvariabler inkludert pH, temperatur og fuktighet. For å redusere potensiell risiko forskes det på å produsere trygge, ikke-giftige nanomaterialer, som en del av en samlet innsats mot grønn nanoteknologi.
Helsevesen
Nanosensorer har stort potensial for diagnostisk medisin, som muliggjør tidlig identifisering av sykdom uten å stole på observerbare symptomer. Ideelle nanosensorimplementeringer ser ut til å etterligne responsen til immunceller i kroppen, og inneholder både diagnostiske og immunresponsfunksjonaliteter, mens de overfører data for å muliggjøre overvåking av sensorinngangen og responsen. Imidlertid er denne modellen fortsatt et langsiktig mål, og forskning er for tiden fokusert på nanosensors umiddelbare diagnostiske evner. Den intracellulære implementeringen av nanosensor syntetisert med biologisk nedbrytbare polymerer induserer signaler som muliggjør overvåking i sanntid og baner dermed vei for fremgang innen medikamentlevering og -behandling.
Et eksempel på disse nanosensorer innebærer å bruke fluorescens-egenskapene til kadmiumselenid kvanteprikker som sensorer for å avdekke svulster i kroppen. En ulempe med kadmiumselenidprikkene er imidlertid at de er svært giftige for kroppen. Som et resultat jobber forskere med å utvikle alternative prikker laget av et annet, mindre giftig materiale mens de fortsatt beholder noen av fluorescensegenskapene. Spesielt har de undersøkt de spesielle fordelene med sinksulfidkvanteprikker som, selv om de ikke er like fluorescerende som kadmiumselenid, kan forstørres med andre metaller inkludert mangan og forskjellige lantanidelementer . I tillegg blir disse nyere kvantepunktene mer fluorescerende når de binder seg til målcellene.
En annen anvendelse av nanosensorer innebærer bruk av silisium-nanotråder i IV-linjer for å overvåke organs helse. Nanotrådene er følsomme for å oppdage sporbiomarkører som diffunderer inn i IV-linjen gjennom blod som kan overvåke nyre- eller organsvikt. Disse nanotrådene vil tillate kontinuerlig biomarkørmåling, noe som gir noen fordeler når det gjelder tidsmessig følsomhet over tradisjonelle biomarkørkvantifiseringsanalyser som ELISA.
Nanosensorer kan også brukes til å oppdage forurensning i organimplantater. Nanosensoren er innebygd i implantatet og oppdager forurensning i cellene som omgir implantatet gjennom et elektrisk signal sendt til en kliniker eller helsepersonell. Nanosensoren kan oppdage om cellene er sunne, inflammatoriske eller forurenset med bakterier. Imidlertid er en største ulempe funnet ved langvarig bruk av implantatet, der vev vokser på toppen av sensorene, noe som begrenser deres evne til å komprimere. Dette hindrer produksjonen av elektriske ladninger, og forkorter dermed levetiden til disse nanosensorene, ettersom de bruker den piezoelektriske effekten til selvkraft.
På samme måte som de som brukes til å måle atmosfæriske forurensninger, brukes gullpartikkelbaserte nanosensorer for å gi en tidlig diagnose til flere typer kreft ved å oppdage flyktige organiske forbindelser (VOC) i pusten, da tumorvekst er assosiert med peroksidering av cellemembranen. En annen kreftrelatert applikasjon, men fremdeles i musesonderingsstadium, er bruken av peptidbelagte nanopartikler som aktivitetsbaserte sensorer for å oppdage lungekreft. De to viktigste fordelene ved bruk av nanopartikler for å oppdage sykdommer er at det muliggjør påvisning av tidlig stadium, da det kan oppdage svulster i størrelsesorden millimeter. Det gir også et kostnadseffektivt, brukervennlig, bærbart og ikke-invasivt diagnostisk verktøy.
En nylig innsats mot fremgang innen nanosensorteknologi har brukt molekylær avtrykk , som er en teknikk som brukes til å syntetisere polymermatriser som fungerer som en reseptor i molekylær gjenkjenning. Analogt med enzymsubstratlåsen og nøkkelmodellen , bruker molekylær avtrykk malmolekyler med funksjonelle monomerer for å danne polymermatriser med spesifikk form som tilsvarer målmalmolekylene, og øker dermed matrisens selektivitet og affinitet. Denne teknikken har gjort det mulig for nanosensorer å oppdage kjemiske arter. Innen bioteknologi er molekylært påtrykte polymerer (MIP) syntetiserte reseptorer som har vist lovende, kostnadseffektive alternativer til naturlige antistoffer ved at de er konstruert for å ha høy selektivitet og affinitet. For eksempel viste et eksperiment med MI-sensor som inneholder nanotips med ikke-ledende polyfenol- nano-belegg (PPn-belegg) selektiv påvisning av E7-protein og demonstrerte dermed potensiell bruk av disse nanosensorene til påvisning og diagnose av humant papillomavirus, andre humane patogener og toksiner . Som vist ovenfor er nanosensorer med molekylær avtrykksteknikk i stand til selektivt å oppdage ultrafølsomme kjemiske arter ved at molekylær avtrykk øker affiniteten og selektiviteten ved kunstig modifisering av polymermatrisene. Selv om molekylært påtrykte polymerer gir fordeler ved selektiv molekylær gjenkjenning av nanosensorer, er selve teknikken relativt fersk, og det gjenstår fortsatt utfordringer som dempningssignaler, deteksjonssystemer som mangler effektive transdusere og overflater som mangler effektiv deteksjon. Videre undersøkelse og forskning på feltet av molekylært innprentede polymerer er avgjørende for utvikling av svært effektive nanosensorer.
For å utvikle smart helsevesen med nanosensorer, må det opprettes et nettverk av nanosensorer, ofte kalt nanonetwork, for å overvinne størrelsen og kraftbegrensningene til individuelle nanosensorer. Nanonetworks demper ikke bare de eksisterende utfordringene, men gir også mange forbedringer. Cellanivåoppløsning av nanosensorer vil gjøre det mulig for behandlinger å eliminere bivirkninger, muliggjøre kontinuerlig overvåking og rapportering av pasientenes forhold.
Nanonetworks krever videre studier ved at nanosensorer er forskjellige fra tradisjonelle sensorer. Den vanligste mekanismen til sensornettverk er gjennom elektromagnetisk kommunikasjon. Imidlertid er det nåværende paradigmet ikke aktuelt for nanomeenheter på grunn av deres lave rekkevidde og kraft. Optisk signaltransduksjon har blitt foreslått som et alternativ til klassisk elektromagnetisk telemetri og har overvåkingsapplikasjoner i menneskekropper. Andre foreslåtte mekanismer inkluderer bioinspirert molekylær kommunikasjon, kablet og trådløs aktiv transport i molekylær kommunikasjon, Forster energioverføring og mer. Det er viktig å bygge en effektiv nanonetwork slik at den kan brukes i felt som medisinske implantater, kroppsnett (BAN), internet av nano ting (IoNT), levering av legemidler og mer. Med et dyktig nanonettverk kan bioimplanterbare nanodeenheter gi høyere nøyaktighet, oppløsning og sikkerhet sammenlignet med makroskalaimplantater. Kroppsnettverk (BAN) gjør det mulig for sensorer og aktuatorer å samle fysiske og fysiologiske data fra menneskekroppen for bedre å forutse sykdommer, som dermed vil lette behandlingen. Potensielle anvendelser av BAN inkluderer overvåking av hjerte- og karsykdommer, insulinbehandling, kunstig syn og hørsel, og hormonbehandling. Internet of Bio-Nano Things refererer til nettverk av nanomeenheter som er tilgjengelige på internett. Utviklingen av IoBNT har banet vei for nye behandlinger og diagnostiske teknikker. Nanonetworks kan også hjelpe medikamentlevering ved å øke lokalisering og sirkulasjonstid for medisiner.
Eksisterende utfordringer med de nevnte applikasjonene inkluderer biokompatibilitet av nanoimplantatene, fysiske begrensninger som fører til mangel på strøm og minnelagring, og biokompatibilitet for sender- og mottakerdesignet til IoBNT. Nanonetwork-konseptet har mange forbedringsområder: disse inkluderer utvikling av nanomaskiner , problemer med protokollstabel, strømforsyningsteknikker og mer.
Det er fremdeles strenge regler på plass for utvikling av standarder for nanosensorer som skal brukes i medisinsk industri, på grunn av utilstrekkelig kunnskap om nanosensorers negative effekter samt potensielle cytotoksiske effekter av nanosensorer. I tillegg kan det være høye kostnader for råvarer som silisium, nanotråder og karbon-nanorør, som forhindrer kommersialisering og produksjon av nanosensorer som krever oppskalering for implementering. For å redusere ulempen med kostnadene, ser forskere på å produsere nanosensorer laget av mer kostnadseffektive materialer. Det er også en høy grad av presisjon som trengs for å produsere nanosensorer på reproduserbar måte, på grunn av deres lille størrelse og følsomhet for forskjellige synteseteknikker, noe som skaper flere tekniske utfordringer som skal overvinnes.