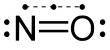Nitrogenoksid - Nitric oxide

|
|||
|
|
|||
| Navn | |||
|---|---|---|---|
|
IUPAC navn
Nitrogenoksid
|
|||
|
Systematisk IUPAC -navn
Oksidonitrogen (•) (tilsetningsstoff) |
|||
| Andre navn
Nitrogenoksid
Nitrogenmonoksid Nitrogen (II) oksid Oxonitrogen |
|||
| Identifikatorer | |||
|
3D -modell ( JSmol )
|
|||
| 3DMet | |||
| ChEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.030.233 |
||
| EC -nummer | |||
| 451 | |||
| KEGG | |||
|
PubChem CID
|
|||
| RTECS -nummer | |||
| UNII | |||
| FN -nummer | 1660 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| N O | |||
| Molar masse | 30,006 g · mol −1 | ||
| Utseende | Fargeløs gass | ||
| Tetthet | 1,3402 g/L | ||
| Smeltepunkt | −164 ° C (−263 ° F; 109 K) | ||
| Kokepunkt | −152 ° C (−242 ° F; 121 K) | ||
| 0,0098 g / 100 ml (0 ° C) 0,0056 g / 100 ml (20 ° C) |
|||
|
Brytningsindeks ( n D )
|
1.0002697 | ||
| Struktur | |||
| lineær ( punktgruppe C ∞ v ) | |||
| Termokjemi | |||
|
Std molar
entropi ( S |
210,76 J/(K · mol) | ||
|
Std
formasjonsentalpi (Δ f H ⦵ 298 ) |
91,29 kJ/mol | ||
| Farmakologi | |||
| R07AX01 ( WHO ) | |||
| Lisensdata | |||
| Innånding | |||
| Farmakokinetikk : | |||
| god | |||
| via lungekapillærseng | |||
| 2–6 sekunder | |||
| Farer | |||
| viktigste farer | |||
| Sikkerhetsdatablad | Eksternt SDS | ||
| GHS -piktogrammer |
   
|
||
| GHS Signalord | Fare | ||
| H270 , H280 , H330 , H314 | |||
| P244 , P260 , P220 , P280 , P304+340+315 , P303+361+353+315 , P305+351+338+315 , P370+376 , P403 , P405 | |||
| NFPA 704 (brann diamant) | |||
| Dødelig dose eller konsentrasjon (LD, LC): | |||
|
LC 50 ( median konsentrasjon )
|
315 ppm (kanin, 15 min ) 854 ppm (rotte, 4 t ) 2500 ppm (mus, 12 min) |
||
|
LC Lo ( lavest publisert )
|
320 sppm (mus) | ||
| Relaterte forbindelser | |||
|
Relaterte nitrogenoksider
|
Dinitrogenpentoksid Dinitrogentetroksid |
||
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infobox -referanser | |||
Nitrogenoksid ( nitrogenoksid eller nitrogenmonoksid) er en fargeløs gass med formelen NO . Det er et av de viktigste nitrogenoksidene . Nitrogenoksid er et fritt radikal : det har et uparret elektron , som noen ganger er markert med en prikk i den kjemiske formelen (· N = O eller · NO). Nitrogenoksid er også et heteronukleært diatomisk molekyl , en klasse av molekyler hvis studie skapte tidlige moderne teorier om kjemisk binding .
Et viktig mellomprodukt i industriell kjemi , nitrogenoksid dannes i forbrenningssystemer og kan genereres av lyn i tordenvær. Hos pattedyr, inkludert mennesker, er nitrogenoksid et signalmolekyl i mange fysiologiske og patologiske prosesser. Det ble utropt til " Årets molekyl " i 1992. Nobelprisen i fysiologi eller medisin i 1998 ble tildelt for å oppdage nitrogenoksidets rolle som et kardiovaskulært signalmolekyl.
Nitrogenoksid bør ikke forveksles med nitrogendioksid (NO 2 ), en brun gass og store luftforurensninger , og heller ikke med lystgass (N 2 O), et bedøvelsesmiddel .
Reaksjoner
Med di- og triatomiske molekyler
Ved kondensering til en væske dimeriserer nitrogenoksid til dinitrogendioksid , men assosiasjonen er svak og reversibel. N – N -avstanden i krystallinsk NO er 218 pm, nesten to ganger N -O -avstanden.
Siden dannelsesvarmen av · NO er endoterm , kan NO dekomponeres til elementene. Katalysatorer i biler utnytter denne reaksjonen:
- 2 NO → O 2 + N 2
Når den utsettes for oksygen , omdannes nitrogenoksid til nitrogendioksid :
- 2 NO + O 2 → 2 NO 2
Denne konverteringen er spekulert i at den skjer via ONOONO -mellomproduktet.
I vann reagerer nitrogenoksid med oksygen og danner salpetersyre (HNO 2 ). Reaksjonen antas å fortsette via følgende støkiometri :
- 4 NO + O 2 + 2 H 2 O → 4 HNO 2
Nitrogenoksid reagerer med fluor , klor og brom for å danne nitrosylhalogenider, for eksempel nitrosylklorid :
- 2 NO + Cl 2 → 2 NOCl
Med NO 2 , også en radikal, kombineres NO for å danne det intenst blå dinitrogentrioksidet :
- NO + NO 2 ⇌ ON − NO 2
Organisk kjemi
Tilsetningen av en nitrogenoksid -del til et annet molekyl blir ofte referert til som nitrosylation . Den Traube reaksjon er tilsetning av en to ekvivalenter av nitrogenoksid på et enolat , som gir en diazeniumdiolate (også kalt en nitrosohydroxylamine ). Produktet kan gjennomgå en påfølgende retroaldolreaksjon , noe som gir en samlet prosess som ligner haloformreaksjonen . For eksempel reagerer nitrogenoksid med aceton og et alkoksid for å danne et diazeniumdiolat på hver α-posisjon , med påfølgende tap av metylacetat som et biprodukt :
Denne reaksjonen, som ble oppdaget omkring 1898, rester av interesse i nitrogenoksid prodrug forskning. Nitrogenoksid kan også reagere direkte med natriummetoksyd , og til slutt danne natriumformiat og lystgass ved hjelp av et N -metoksydiazeniumdiolat.
Koordineringskomplekser
Nitrogenoksid reagerer med overgangsmetaller for å gi komplekser som kalles metallnitrosyler . Den vanligste bindemåten for nitrogenoksid er den terminale lineære typen (M − NO). Alternativt kan nitrogenoksid fungere som et ett-elektron pseudohalid. I slike komplekser er M − N − O -gruppen preget av en vinkel mellom 120 ° og 140 °. NO -gruppen kan også bygge bro mellom metalsentre gjennom nitrogenatomet i en rekke geometrier.
Produksjon og forberedelse
I kommersielle omgivelser produseres nitrogenoksid ved oksidasjon av ammoniakk ved 750–900 ° C (normalt ved 850 ° C) med platina som katalysator i Ostwald -prosessen :
- 4 NH 3 + 5 O 2 → 4 NO + 6 H 2 O
Den ukatalyserte endoterme reaksjonen av oksygen (O 2 ) og nitrogen (N 2 ), som utføres ved høy temperatur (> 2000 ° C) ved lyn, har ikke blitt utviklet til en praktisk kommersiell syntese (se Birkeland – Eyde -prosessen ):
- N 2 + O 2 → 2 NO
Laboratoriemetoder
I laboratoriet genereres nitrogenoksid praktisk ved reduksjon av fortynnet salpetersyre med kobber :
- 8 HNO 3 + 3 Cu → 3 Cu (NO 3 ) 2 + 4 H 2 O + 2 NO
En alternativ rute innebærer reduksjon av salpetersyre i form av natriumnitritt eller kaliumnitritt :
- 2 NaNO 2 + 2 NaI + 2 H 2 SO 4 → I 2 + 2 Na 2 SO 4 + 2 H20 + 2 NO
- 2 NaNO 2 + 2 FeSO 4 + 3 H 2 SO 4 → Fe 2 (SO 4 ) 3 + 2 NaHSO 4 + 2 H20 + 2 NO
- 3 KNO 2 + KNO 3 + Cr 2 O 3 → 2 K 2 CrO 4 + 4 NO
Jern (II) sulfatveien er enkel og har blitt brukt i laboratorieeksperimenter. Såkalte NONOate- forbindelser brukes også til produksjon av nitrogenoksid.
Påvisning og analyse

Nitrogenoksidkonsentrasjon kan bestemmes ved bruk av en kjemiluminescerende reaksjon som involverer ozon . En prøve som inneholder nitrogenoksid blandes med en stor mengde ozon. Nitrogenoksidet reagerer med ozonet for å produsere oksygen og nitrogendioksid , ledsaget av lysutslipp ( kjemiluminescens ):
- NO + O 3 → NO 2 + O 2 + hν
som kan måles med en fotodetektor . Mengden lys som produseres er proporsjonal med mengden av nitrogenoksid i prøven.
Andre metoder for testing inkluderer elektroanalyse (amperometrisk tilnærming), der · NO reagerer med en elektrode for å indusere en strøm- eller spenningsendring. Påvisning av NO -radikaler i biologiske vev er spesielt vanskelig på grunn av den korte levetiden og konsentrasjonen av disse radikalene i vev. En av de få praktiske metoder er spinnoppfangende av nitrogenoksid med jern- ditiokarbamat- komplekser og påfølgende deteksjon av den mono-nitrosyl-jernkompleks med elektron-paramagnetisk resonans (EPR).
Det finnes en gruppe fluorescerende fargestoffindikatorer som også er tilgjengelige i acetylert form for intracellulære målinger. Den vanligste forbindelsen er 4,5-diaminofluorescein (DAF-2).
Miljøeffekter
Sur nedbør
Nitrogenoksid reagerer med hydroperoksyradikalet (HO 2 • ) for å danne nitrogendioksid (NO 2 ), som deretter kan reagere med et hydroksylradikal ( • OH ) for å produsere salpetersyre (HNO 3 ):
- · NO + HO 2 • → • NO 2 + • OH
- · NO 2 + • OH → HNO 3
Salpetersyre, sammen med svovelsyre , bidrar til sur nedbør .
Ozonforringelse
· NO deltar i nedbrytning av ozonlaget . Nitrogenoksid reagerer med stratosfærisk ozon for å danne O 2 og nitrogendioksid:
- · NO + O 3 → NO 2 + O 2
Denne reaksjonen brukes også til å måle konsentrasjoner av · NO i kontrollvolumer.
Forløper til NO 2
Som vist i avsnittet Acid deposition, kan nitrogenoksid transformere til nitrogendioksid (dette kan skje med hydroperoksyradikalet, HO 2 • eller diatomisk oksygen, O 2 ). Symptomer på kortsiktig nitrogendioksideksponering inkluderer kvalme, dyspné og hodepine. Langtidseffekter kan inkludere nedsatt immun- og respirasjonsfunksjon .
Biologiske funksjoner
NO er et gassformig signalmolekyl . Det er en viktig biologisk budbringer for virveldyr , som spiller en rolle i en rekke biologiske prosesser. Det er et bioprodukt i nesten alle typer organismer, inkludert bakterier, planter, sopp og dyreceller.
Nitrogenoksid, en endotelavledet avslappende faktor (EDRF), biosyntetiseres endogent fra L -arginin , oksygen og NADPH av forskjellige nitrogenoksydsyntase (NOS) enzymer . Reduksjon av uorganisk nitrat kan også lage nitrogenoksid. Et av de viktigste enzymatiske målene for nitrogenoksid er guanylylsyklase . Binding av nitrogenoksid til enzymets hemregion fører til aktivering i nærvær av jern. Nitrogenoksid er svært reaktivt (har en levetid på noen få sekunder), men diffunderer fritt over membraner. Disse attributtene gjør nitrogenoksid ideelt for et forbigående parakrin (mellom tilstøtende celler) og autokrine (i en enkelt celle) signalmolekyl. Når nitrogenoksid er omdannet til nitrater og nitritt av oksygen og vann, er cellesignalering deaktivert.
Den endotel (indre foring) av blodkar bruker nitrogenoksid for å signalisere den omliggende glatt muskulatur til å slappe av, noe som resulterer i vasodilatasjon og øker blodstrømmen. Sildenafil (Viagra) er et stoff som bruker nitrogenoksidveien. Sildenafil produserer ikke nitrogenoksid, men forbedrer signalene som er nedstrøms nitrogenoksidveien ved å beskytte syklisk guanosinmonofosfat (cGMP) mot nedbrytning av cGMP-spesifikk fosfodiesterase type 5 (PDE5) i corpus cavernosum , slik at signalet kan være forbedret, og dermed vasodilatasjon . Et annet endogent gassformig senderen, hydrogensulfid (H 2 S) arbeider med ingen for å indusere vasodilatasjon og angiogenese i et samvirkende vis.
Nasal pust produserer nitrogenoksid i kroppen, mens pusten i munnen ikke gjør det.
Sikkerhet og helse
I USA har Occupational Safety and Health Administration (OSHA) satt den lovlige grensen ( tillatt eksponeringsgrense ) for nitrogenoksideksponering på arbeidsplassen til 25 ppm (30 mg/m 3 ) over en 8-timers arbeidsdag. The National Institute for Occupational Safety and Health (NIOSH) har satt en anbefalt eksponeringsgrense (REL) på 25 ppm (30 mg / m 3 ) over en åtte timers arbeidsdag. Ved nivåer på 100 ppm er nitrogenoksid umiddelbart farlig for liv og helse .
Referanser
Videre lesning
- Butler A. og Nicholson R .; "Liv, død og NEI." Cambridge 2003. ISBN 978-0-85404-686-7 .
- van Faassen, EE; Vanin, AF (red.); "Radikaler for livet: De forskjellige formene for nitrogenoksid." Elsevier, Amsterdam 2007. ISBN 978-0-444-52236-8 .
- Ignarro, LJ (red.); "Nitrogenoksid: biologi og patobiologi." Academic Press, San Diego 2000. ISBN 0-12-370420-0 .
Eksterne linker
- Internasjonalt kjemisk sikkerhetskort 1311
- "Nitrogenoksid og dets rolle i helse og diabetes" . 21. oktober 2015.
- Gasskjemi i mikroskala: Eksperimenter med nitrogenoksider
- Hjernen din starter opp som en datamaskin - ny innsikt om nitrogenoksidets biologiske rolle.
- Vurdere potensialet for nitrogenoksid i diabetesfoten
- Nye funn om nitrogenoksid kan gi medisiner mot schizofreni
- Nitrogenoksid i den kjemiske databasen
- "Umiddelbart farlig for livs- eller helsekonsentrasjoner (IDLH): nitrogenoksid" . Nasjonalt institutt for arbeidssikkerhet og helse . 2. november 2018.