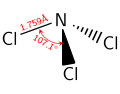Nitrogen triklorid - Nitrogen trichloride
|
|
|||

|
|||
| Navn | |||
|---|---|---|---|
| Andre navn
Trichloramine
Agene Nitrogen (III) klorid Trichloroazane Trichlorine nitrid |
|||
| Identifikatorer | |||
|
3D-modell ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100.030.029 |
||
| EF-nummer | |||
| 1840 | |||
|
PubChem CID
|
|||
| RTECS-nummer | |||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eiendommer | |||
| NCl 3 | |||
| Utseende | gul oljeaktig væske | ||
| Lukt | klor -lignende | ||
| Tetthet | 1,653 g / ml | ||
| Smeltepunkt | −40 ° C (−40 ° F; 233 K) | ||
| Kokepunkt | 71 ° C (160 ° F; 344 K) | ||
| blandbar sakte nedbrytes |
|||
| Løselighet | løselig i benzen , kloroform , CCl 4 , CS 2 , PCl 3 | ||
| Struktur | |||
| ortorombisk (under −40 ° C) | |||
| trigonal pyramidal | |||
| 0,6 D | |||
| Termokjemi | |||
|
Std. Entalpi av
dannelse (Δ f H ⦵ 298 ) |
232 kJ / mol | ||
| Farer | |||
|
EU-klassifisering (DSD) (utdatert)
|
ikke listet | ||
| NFPA 704 (branndiamant) | |||
| 93 ° C (199 ° F; 366 K) | |||
| Beslektede forbindelser | |||
|
Andre anioner
|
Nitrogen trifluoride Nitrogen tribromide Nitrogen triiodide |
||
|
Andre kationer
|
Fosfor-triklorid Arseniklorid |
||
|
Relaterte kloraminer
|
Monokloramin dikloramin |
||
|
Beslektede forbindelser
|
Nitrosylklorid | ||
|
Med mindre annet er angitt, blir data gitt for materialer i standardtilstand (ved 25 ° C, 100 kPa). |
|||
|
|
|||
| Infoboksreferanser | |||
Nitrogentriklorid , også kjent som trichloramine , er den kjemiske forbindelsen med formel NCl 3 . Denne gule, oljeaktige, skarp luktende og eksplosive væsken opptrer oftest som et biprodukt av kjemiske reaksjoner mellom ammoniakk- derivater og klor (for eksempel i svømmebassenger ). Ved siden av monokloramin og dikloramin er trikloramin ansvarlig for den særegne 'klorlukten' assosiert med svømmebassenger, hvor forbindelsen lett dannes som et produkt fra hypoklorsyre som reagerer med ammoniakk og andre nitrogenholdige stoffer i vannet, slik som urea fra urin .
Forberedelse og struktur
Forbindelsen fremstilles ved behandling av ammoniumsalter, slik som ammoniumnitrat med klor.
Mellomprodukter ved denne omdanningen innbefatter monochloramine og dikloramin , NH 2 Cl og N HCl 2 , henholdsvis.
I likhet med ammoniakk er NCl 3 et pyramidemolekyl . N-Cl-avstandene er 1,76 Å, og Cl-N-Cl-vinklene er 107 °.
Reaksjoner og bruksområder
Kjemien til NCl 3 er godt utforsket. Det er moderat polar med et dipolmoment på 0,6 D. Nitrogensenteret er basisk, men mye mindre enn ammoniakk. Den hydrolyseres av varmt vann for å frigjøre ammoniakk og saltsyre .
- NCI 3 + 3 H 2 O → NH 3 + 3 HOCl
NCI 3 eksploderer for å gi N- 2 og klorgass. Denne reaksjonen inhiberes for fortynnede gasser.
Nitrogentriklorid kan dannes i små mengder når offentlig vannforsyning desinfiseres med monokloramin , og i svømmebassenger ved å desinfisere klor som reagerer med urea i urin og svette fra badende.
Nitrogentriklorid, varemerket Agene , ble en gang brukt til å bleke mel , men denne fremgangsmåten ble forbudt i USA i 1949 på grunn av sikkerhetshensyn.
Sikkerhet
Nitrogentriklorid kan irritere slimhinner - det er et lachrymatory agent , men har aldri blitt brukt som sådan. Det rene stoffet (sjelden påtruffet) er et farlig eksplosivt stoff som er følsomt for lys, varme, til og med moderat støt og organiske forbindelser. Pierre Louis Dulong forberedte den først i 1812, og mistet to fingre og et øye i to eksplosjoner. I 1813 blindet en NCl 3- eksplosjon Sir Humphry Davy midlertidig og fikk ham til å ansette Michael Faraday som medarbeider. De ble begge skadet i en annen NCl 3- eksplosjon kort tid etter.
Se også
Referanser
Videre lesning
- Jander, J. (1976). Nylig undersøkelse av kjemi og struktur av nitrogentriiodid, tribromid, triklorid og relaterte forbindelser . Fremskritt innen uorganisk kjemi . Fremskritt innen uorganisk kjemi og radiokjemi. 19 . s. 1–63. doi : 10.1016 / S0065-2792 (08) 60070-9 . ISBN 9780120236190 .
- Kovacic, P .; Lowery, MK; Field, KW (1970). "Kjemi av N-bromaminer og N-kloraminer". Kjemiske anmeldelser . 70 (6): 639–665. doi : 10.1021 / cr60268a002 .
- Hartl, H .; Schöner, J .; Jander, J .; Schulz, H. (1975). "Die Struktur des Festen Stickstofftrichlorids (−125 ° C)". Zeitschrift für Anorganische und Allgemeine Chemie . 413 (1): 61–71. doi : 10.1002 / zaac.19754130108 .
- Cazzoli, G .; Favero, PG; Dal Borgo, A. (1974). "Molecular Structure, Nuclear Quadrupole Coupling Constant and Dipole Moment of Nitrogen Trichloride from Microwave Spectroscopy". Journal of Molecular Spectroscopy . 50 (1–3): 82–89. Bibcode : 1974JMoSp..50 ... 82C . doi : 10.1016 / 0022-2852 (74) 90219-7 .
- Bayersdorfer, L .; Engelhardt, U .; Fischer, J .; Höhne, K .; Jander, J. (1969). "Untersuchungen an Stickstoff – Chlor-Verbindungen. V. Infrarot- und RAMAN-Spektren von Stickstofftrichlorid". Zeitschrift für Anorganische und Allgemeine Chemie . 366 (3–4): 169–179. doi : 10.1002 / zaac.19693660308 .
Eksterne linker
|
NH 3 N 2 H 4 |
Han (N 2 ) 11 | ||||||||||||||||
| Li 3 N | Vær 3 N 2 | BN |
β-C 3 N 4 g-C 3 N 4 C x N y |
N 2 | N x O y | NF 3 | Ne | ||||||||||
| Na 3 N | Mg 3 N 2 | AlN | Si 3 N 4 |
PN P 3 N 5 |
S x N y SN S 4 N 4 |
NCl 3 | Ar | ||||||||||
| K 3 N | Ca 3 N 2 | ScN | Tinn | VN |
CrN Cr 2 N |
Mn x N y | Fe x N y | Lure | Ni 3 N | CuN | Zn 3 N 2 | GaN | Ge 3 N 4 | Som | Se | NBr 3 | Kr |
| Rb | Sr 3 N 2 | YN | ZrN | NbN | β-Mo 2 N | Tc | Ru | Rh | PdN | Ag 3 N | CdN | Vertshus | Sn | Sb | Te | NI 3 | Xe |
| Cs | Ba 3 N 2 | Hf 3 N 4 | TaN | WN | Re | Os | Ir | Pt | Au | Hg 3 N 2 | TlN | Pb | BiN | Po | På | Rn | |
| Fr | Ra 3 N 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| La | CeN | Pr | Nd | Pm | Sm | Eu | GdN | Tb | Dy | Ho | Er | Tm | Yb | Lu | |||
| Ac | Th | Pa | U 2 N 3 | Np | Pu | Er | Cm | Bk | Jf | Es | Fm | Md | Nei | Lr | |||