Fruktose -bisfosfat aldolase - Fructose-bisphosphate aldolase
| Fruktose-bisfosfat aldolase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Fruktose-bisfosfat aldolase oktamer, Human
| |||||||||
| Identifikatorer | |||||||||
| EF -nr. | 4.1.2.13 | ||||||||
| CAS -nr. | 9024-52-6 | ||||||||
| Databaser | |||||||||
| IntEnz | IntEnz -visning | ||||||||
| BRENDA | BRENDA -oppføring | ||||||||
| ExPASy | NiceZyme utsikt | ||||||||
| KEGG | KEGG -oppføring | ||||||||
| MetaCyc | metabolsk vei | ||||||||
| PRIAM | profil | ||||||||
| PDB -strukturer | RCSB PDB PDBe PDBsum | ||||||||
| Genontologi | AmiGO / QuickGO | ||||||||
| |||||||||
| Fruktose-bisfosfat aldolase klasse-I | |||||||||
|---|---|---|---|---|---|---|---|---|---|
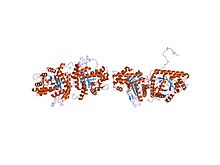 fruktose 1,6-bisfosfat aldolase fra kaninlever
| |||||||||
| Identifikatorer | |||||||||
| Symbol | Glykolytisk | ||||||||
| Pfam | PF00274 | ||||||||
| InterPro | IPR000741 | ||||||||
| PROSIT | PDOC00143 | ||||||||
| SCOP2 | 1ald / SCOPe / SUPFAM | ||||||||
| CDD | cd00344 | ||||||||
| |||||||||
| Fruktose-bisfosfat aldolase klasse-II | |||||||||
|---|---|---|---|---|---|---|---|---|---|
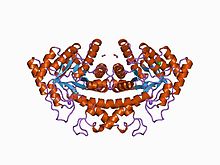 klasse II fruktose-1,6-bisfosfat aldolase i kompleks med fosfoglykolhydroksamat
| |||||||||
| Identifikatorer | |||||||||
| Symbol | F_bP_aldolase | ||||||||
| Pfam | PF01116 | ||||||||
| Pfam klanen | CL0036 | ||||||||
| InterPro | IPR000771 | ||||||||
| PROSIT | PDOC00523 | ||||||||
| SCOP2 | 1dos / SCOPe / SUPFAM | ||||||||
| CDD | cd00453 | ||||||||
| |||||||||
Fruktose-bisfosfat aldolase ( EC 4.1.2.13 ), ofte bare aldolase , er et enzym som katalyserer en reversibel reaksjon som deler aldolen , fruktose 1,6-bisfosfat , i triose fosfater dihydroksyacetonfosfat (DHAP) og glyseraldehyd 3-fosfat (G3P ). Aldolase kan også produsere DHAP fra andre (3S, 4R) -ketose 1-fosfater som fruktose 1-fosfat og sedoheptulose 1,7-bisfosfat . Glukoneogenese og Calvin -syklusen , som er anabole veier , bruker omvendt reaksjon. Glykolyse , en katabolisk vei , bruker fremoverreaksjonen. Aldolase er delt inn i to klasser etter mekanisme.
Ordet aldolase refererer også mer generelt til et enzym som utfører en aldolreaksjon (skaper en aldol ) eller dens revers (spalting av en aldol), for eksempel Sialinsyre aldolase , som danner sialinsyre . Se listen over aldolaser .
Mekanisme og struktur
Klasse I-proteinene danner en protonert Schiff-base mellomliggende binding av en høyt konservert aktive setet lysin med den DHAP karbonyl karbon. I tillegg er tyrosinrester avgjørende for denne mekanismen for å fungere som stabiliserende hydrogenakseptorer. Klasse II -proteiner bruker en annen mekanisme som polariserer karbonylgruppen med en divalent kation som Zn 2+ . Den Escherichia coli galaktitol operon protein, gatY, og N-acetyl-galaktosamin -operonet protein, agay, som er tagatose-aldolase , er homologer av klasse II-fruktose-aldolase. To histidin- residuer i den første halvdel av sekvensen av disse homologer er blitt vist å være involvert i binding sink.
De protein subenheter av begge klasser hver har en α / β domene foldet inn i et TIM tønne inneholdende det aktive sete. Flere underenheter er satt sammen til det komplette proteinet . De to klassene deler liten sekvensidentitet .
Med få unntak er det bare funnet klasse I -proteiner hos dyr , planter og grønne alger . Med få unntak er det bare funnet klasse II -proteiner i sopp . Begge klassene har blitt funnet mye i andre eukaryoter og hos bakterier . De to klassene er ofte tilstede sammen i samme organisme. Planter og alger har plastidal aldolase, noen ganger en levning av endosymbiose , i tillegg til den vanlige cytosoliske aldolase. En bifunksjonell fruktose-bisfosfat aldolase/fosfatase, med klasse I-mekanisme, har blitt funnet mye i archaea og i noen bakterier. Det aktive stedet for denne arkeiske aldolasen er også i en TIM -fat.
I glukoneogenese og glykolyse
Glukoneogenese og glykolyse deler en serie med seks reversible reaksjoner. Ved glukoneogenese reduseres glyseraldehyd-3-fosfat til fruktose 1,6-bisfosfat med aldolase. I glykolyse blir fruktose 1,6-bisfosfat gjort til glyseraldehyd-3-fosfat og dihydroksyacetonfosfat ved bruk av aldolase. Aldolasen som brukes i glukoneogenese og glykolyse er et cytoplasmatisk protein.
Tre former for klasse I -protein finnes hos virveldyr . Aldolase A uttrykkes fortrinnsvis i muskler og hjerne; aldolase B i lever, nyre og i enterocytter ; og aldolase C i hjernen. Aldolaser A og C er hovedsakelig involvert i glykolyse , mens aldolase B er involvert i både glykolyse og glukoneogenese. Noen defekter i aldolase B forårsaker arvelig fruktoseintoleranse . Metabolismen av fri fruktose i leveren utnytter aldolase Bs evne til å bruke fruktose 1-fosfat som et substrat . Archaeal fruktose-bisfosfat aldolase/fosfatase er antagelig involvert i glukoneogenese fordi produktet er fruktose 6-fosfat.
I Calvin -syklusen
Den Calvin syklusen er en karbon-fiksering ledningen; det er en del av fotosyntesen, som omdanner karbondioksid og andre forbindelser til glukose. Det og glukoneogenese deler en serie med fire reversible reaksjoner. I begge veier reduseres 3-fosfoglyserat (3-PGA eller 3-PG) til fruktose 1,6-bisfosfat med aldolase som katalyserer den siste reaksjonen. En femte reaksjon, katalysert i begge veier av fruktose 1,6-bisfosfatase , hydrolyserer fruktose 1-6-bisfosfatet til fruktose 6-fosfat og uorganisk fosfat. Den store nedgangen i fri energi gjør denne reaksjonen irreversibel. I Calvin-syklusen katalyserer aldolase også produksjonen av sedoheptulose 1,7-bisfosfat fra DHAP og erytrose 4-fosfat . Hovedproduktene i Calvin-syklusen er triose fosfat (TP), som er en blanding av DHAP og G3P, og fruktose 6-fosfat. Begge er også nødvendig for å regenerere RuBP . Aldolasen som brukes av planter og alger i Calvin-syklusen er vanligvis et plastid-målrettet protein kodet av et kjernefysisk gen.
Reaksjoner
Aldolase katalyserer
- fruktose 1,6-bisfosfat ⇌ DHAP + G3P
og også
- sedoheptulose 1,7-bisfosfat ⇌ DHAP + erytrose 4-fosfat
- fruktose 1-fosfat ⇌ DHAP + glyseraldehyd
Aldolase brukes i den reversible stammen av glukoneogenese/glykolyse
- 2 ( PEP + NADH + H + + ATP + H 2 O) ⇌ fruktose 1,6-bisfosfat + 2 (NAD + + ADP + P i )
Aldolase brukes også i den delen av Calvin-syklusen som deles med glukoneogenese, med irreversibel fosfathydrolyse på slutten katalysert av fruktose 1,6-bisfosfatase
- 2 ( 3-PG + NADPH + H + + ATP + H 2 O) ⇌ fruktose 1,6-bisfosfat + 2 (NADP + + ADP + P i )
- fruktose 1,6-bisfosfat + H 2 O → fruktose-6-fosfat + P i
I glukoneogenese produseres 3-PG av enolase og fosfoglyseratmutase som virker i serie
- PEP + H 2 O ⇌ 2-PG ⇌ 3-PG
I Calvin-syklusen er 3-PG produsert av RuBisCO
- RuBP + CO 2 + H 2 O → 2 (3-PG)
G3P produseres ved at fosfoglyseratkinase virker i serie med glyseraldehyd-3-fosfat dehydrogenase (GAPDH) i glukoneogenese, og i serie med glyseraldehyd-3-fosfat dehydrogenase (NADP+) (fosforylering) i Calvin-syklusen
- 3-PG + ATP ⇌ 1,3-bisfosfoglyserat + ADP
- 1,3-bisfosfoglyserat + NAD (P) H + H + ⇌ G3P + P i + NAD (P) +
Triose-fosfat isomerase opprettholder DHAP og G3P i nær likevekt, og produserer blandingen som kalles triose fosfat (TP)
- G3P, DHAP
Dermed er både DHAP og G3P tilgjengelig for aldolase.
Måneskinnsegenskaper
Aldolase har også vært implisert i mange "måneskinnende" eller ikke-katalytiske funksjoner, basert på dets bindingsaffinitet for flere andre proteiner, inkludert F-actin , α-tubulin , lett kjededynin , WASP , Band 3 anionbytter, fosfolipase D ( PLD2 ) , glukosetransportør GLUT4 , inositoltrisfosfat , V-ATPase og ARNO (et guaninnukleotid utveksling faktor av ARF6 ). Disse assosiasjonene antas å være hovedsakelig involvert i cellulær struktur, men involvering i endocytose, parasittinvasjon, omplacering av cytoskjelett, cellemotilitet, membranproteinhandel og resirkulering, signaltransduksjon og vevsoppdeling er blitt undersøkt.
Referanser
Videre lesning
- Berry A, Marshall KE (februar 1993). "Identifikasjon av sinkbindende ligander i klasse II fruktose-1,6-bisfosfat aldolase av Escherichia coli" . FEBS Lett . 318 (1): 11–6. doi : 10.1016/0014-5793 (93) 81317-S . PMID 8436219 . S2CID 7682431 .
- Freemont PS, Dunbar B, Fothergill-Gilmore LA (februar 1988). "Den komplette aminosyresekvensen for human skjelett-muskel fruktose-bisfosfat aldolase" . Biochem. J . 249 (3): 779–88. doi : 10.1042/bj2490779 . PMC 1148774 . PMID 3355497 .
- Galkin A, Li Z, Li L, Kulakova L, Pal LR, Dunaway-Mariano D, Herzberg O (2009). "Strukturell innsikt i substratbinding og stereoselektivitet av giardia fruktose-1,6-bisfosfat aldolase" . Biokjemi . 48 (14): 3186–96. doi : 10.1021/bi9001166 . PMC 2666783 . PMID 19236002 .
- Marsh JJ, Lebherz HG (mars 1992). "Fruktose-bisfosfat aldolaser: en evolusjonær historie". Trender Biochem. Sci . 17 (3): 110–3. doi : 10.1016/0968-0004 (92) 90247-7 . PMID 1412694 .
- Perham RN (april 1990). "Fruktose-1,6-bisfosfat aldolaser: samme reaksjon, forskjellige enzymer". Biochem. Soc. Trans . 18 (2): 185–7. doi : 10.1042/bst0180185 . PMID 2199259 .
Eksterne linker
-
 Medier relatert til fruktose-bisfosfat aldolase på Wikimedia Commons
Medier relatert til fruktose-bisfosfat aldolase på Wikimedia Commons - Tolan Laboratory ved Boston University
|
ATP
ADP
ATP
ADP
+ +
2 × 3-fosfoglyserat 2 × 2-fosfoglyserat 2 × fosfoenolpyruvat ADP
ATP
2 × Pyruvat |










