Azulene - Azulene
|
|
|||
| Navn | |||
|---|---|---|---|
|
Foretrukket IUPAC-navn
Azulene |
|||
|
Systematisk IUPAC-navn
Bicyclo [5.3.0] dekapentaen |
|||
| Identifikatorer | |||
|
3D-modell ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100,005,449 |
||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eiendommer | |||
| C 10 H 8 | |||
| Molarmasse | 128,174 g · mol −1 | ||
| Smeltepunkt | 99 til 100 ° C (210 til 212 ° F; 372 til 373 K) | ||
| Kokepunkt | 242 ° C (468 ° F; 515 K) | ||
| -98,5 · 10 −6 cm 3 / mol
g / l |
|||
| Termokjemi | |||
|
Std
forbrenningsentalpi (Δ c H ⦵ 298 ) |
−1266,5 kcal / mol | ||
|
Med mindre annet er angitt, blir data gitt for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infoboksreferanser | |||
Azulene er en organisk forbindelse og en isomer av naftalen . Mens naftalen er fargeløs, er azulen mørk blå. To terpenoider, vetivazulen (4,8-dimetyl-2-isopropylazulene) og guaiazulen (1,4-dimetyl-7-isopropylazulene), som inneholder azulenskelettet, finnes i naturen som bestanddeler av pigmenter i sopp, guaiac-treolje og noen marine virvelløse dyr.
Azulene har en lang historie, og dateres tilbake til 1400-tallet som den azurblå kromoforen oppnådd ved dampdestillasjon av tysk kamille . Kromoforen ble oppdaget i ryllik og malurt og ble oppkalt i 1863 av Septimus Piesse. Dens struktur ble først rapportert av Lavoslav Ružička , etterfulgt av dens organiske syntese i 1937 av Placidus Plattner.
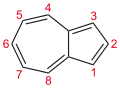
Struktur og liming

Azulene blir vanligvis sett på som et resultat av fusjon av cyklopentadien- og cykloheptatrienringer . Som naftalen og cyklodekapentaen er det et 10 pi-elektronsystem . Den har aromatiske egenskaper: (i) de perifere bindingene har lignende lengder og (ii) den gjennomgår Friedel-Crafts- lignende erstatninger. Stabilitetsgevinsten fra aromatisitet er anslått til å være halvparten av naftalen.
Dens dipolmoment er 1,08 D , i motsetning til naftalen, som har et dipolmoment på null. Denne polariteten kan forklares ved å betrakte azulen som fusjonen av et 6 π-elektron cyklopentadienylanion og et 6 π-elektron tropylium-kation : et elektron fra den syvleddede ringen overføres til den femleddede ringen for å gi hver ring aromatisk stabilitet av Hückels styre . Reaktivitetsstudier bekrefter at syvleddet ring er elektrofil og femleddet er nukleofil .
Grunntilstandens dipolære natur gjenspeiles i dens dype farge, noe som er uvanlig for små umettede aromatiske forbindelser. Et annet bemerkelsesverdig trekk ved azulen er at det bryter Kashas regel ved å utvise fluorescens fra en øvre eksitert tilstand (S 2 → S 0 ).
Organisk syntese
Syntetiske ruter til azulen har lenge vært av interesse på grunn av dens uvanlige struktur. I 1939 ble den første metoden rapportert av St. Pfau og Plattner med utgangspunkt i indan og etyldiazoacetat .
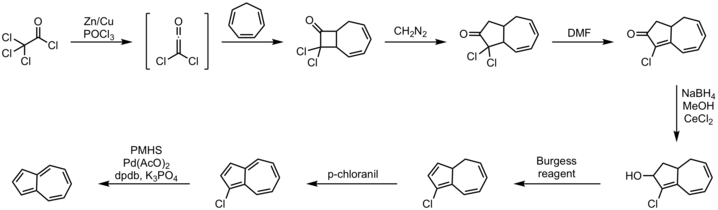
En effektiv one-pot rute medfører annuleringen av cyklopentadien med umettet C 5 - syntoner . Den alternative tilnærmingen fra cykloheptatrien har lenge vært kjent, en illustrativ metode er vist nedenfor.
Fremgangsmåte:
- cykloheptatrien 2 + 2 cykloaddition med diklorketen
- diazometan innsettingsreaksjon
- dehydrohalogeneringsreaksjon med DMF
- Luche reduksjon til alkohol med natriumborhydrid
- eliminasjonsreaksjon med Burgess-reagens
- oksidasjon med p-kloranil
- dehalogenering med polymethylhydrosiloxane , palladium (II) acetat , kaliumfosfat og DPDB liganden
Organometalliske komplekser
I organometallisk kjemi tjener azulen som en ligand for metaller med lav verdi, som ellers er kjent for å danne π-komplekser med både cyklopentadienyl- og cykloheptatrienylligander. Illustrerende komplekser er (azulen) Mo 2 (CO) 6 og (azulen) Fe 2 (CO) 5 .
Beslektede forbindelser
1-hydroksyazulen er en ustabil grønn olje og viser ikke keto-enol tautomerisme . 2-hydroksyazulen oppnås ved hydrolyse av 2-metoksyazulen med hydrobromsyre. Den er stabil og viser keto-enol tautomerisme. Den p K en 2-hydroxyazulene i vann er 8,71. Det er surere enn fenol eller naftol . P K a av 6-hydroksyazulener i vann er 7,38, noe som gjør det også surere enn fenol eller naftol.
I naft [ a ] azulen blir en naftalen ring kondensert i 1,2-posisjonene til azulen. I et slikt system er deformasjon fra planaritet funnet lik tetrahelicen .
Guaiazulene (1,4-dimetyl-7-isopropylazulen) er et alkylert derivat av azulen med en nesten identisk intens blå farge. Den er kommersielt tilgjengelig for kosmetikkindustrien der den fungerer som et hudkondisjoneringsmiddel.