Massebalanse - Mass balance
En massebalanse , også kalt en materialbalanse , er en anvendelse av bevaring av masse til analyse av fysiske systemer. Ved å redegjøre for materiale som kommer inn og ut av et system, kan massestrømmer identifiseres som kan ha vært ukjent eller vanskelig å måle uten denne teknikken. Den eksakte bevaringsloven som ble brukt i analysen av systemet, avhenger av problemets kontekst, men alt dreier seg om massebevaring, det vil si at materie ikke kan forsvinne eller skapes spontant.
Derfor brukes massebalanser mye i ingeniør- og miljøanalyser . For eksempel brukes massebalanseteori til å designe kjemiske reaktorer , for å analysere alternative prosesser for å produsere kjemikalier, samt for å modellere forurensningsspredning og andre prosesser i fysiske systemer. Nært beslektede og komplementære analyseteknikker inkluderer befolkningsbalanse , energibalanse og den noe mer komplekse entropibalansen . Disse teknikkene er nødvendige for grundig design og analyse av systemer som kjølesyklusen .
I miljøovervåking brukes begrepet budsjettberegninger for å beskrive massebalanselasjoner der de brukes til å evaluere overvåkingsdataene (sammenligne input og output, etc.). I biologien gjør den dynamiske energibudsjettsteorien for metabolsk organisasjon eksplisitt bruk av masse- og energibalanse.
Introduksjon
Den generelle formen som er sitert for en massebalanse er massen som kommer inn i et system må ved bevaring av masse enten forlate systemet eller akkumulere i systemet .
Matematisk er massebalansen for et system uten en kjemisk reaksjon som følger:
Strengt tatt gjelder ligningen ovenfor også for systemer med kjemiske reaksjoner hvis begrepene i balanseligningen er referert til total masse, dvs. summen av alle kjemiske artene i systemet. I fravær av en kjemisk reaksjon vil mengden av enhver kjemisk art som strømmer inn og ut være den samme; dette gir opphav til en ligning for hver art som er tilstede i systemet. Imidlertid, hvis dette ikke er tilfelle, må massebalanse -ligningen endres for å muliggjøre generering eller uttømming (forbruk) av hver kjemisk art. Noen bruker ett begrep i denne ligningen for å redegjøre for kjemiske reaksjoner, som vil være negative for uttømming og positive for generering. Imidlertid er den konvensjonelle formen for denne ligningen skrevet for å ta hensyn til både et positivt generasjonsbegrep (dvs. produkt av reaksjon) og et negativt forbruksterm (reaktantene som brukes til å produsere produktene). Selv om ett begrep totalt sett står for den totale balansen på systemet, er begge vilkårene nødvendige for å bruke denne balanse ligningen på en enkelt art og deretter hele prosessen. Denne modifiserte ligningen kan brukes ikke bare for reaktive systemer, men for befolkningsbalanser som oppstår i partikkelmekaniske problemer. Ligningen er gitt nedenfor; Vær oppmerksom på at det forenkler den tidligere ligningen i tilfelle generasjonsbegrepet er null.
- I fravær av en atomreaksjon må antallet atomer som strømmer inn og ut forbli det samme, selv i nærvær av en kjemisk reaksjon.
- For at en balanse skal dannes, må systemets grenser være klart definert.
- Massebalanser kan overtas fysiske systemer i flere skalaer.
- Massebalanser kan forenkles med forutsetningen om steady state , der akkumuleringstiden er null.
Illustrerende eksempel
Et enkelt eksempel kan illustrere konseptet. Vurder situasjonen der en slam strømmer inn i en sedimenteringstank for å fjerne faststoffet i tanken. Tørrstoff samles i bunnen ved hjelp av et transportbånd som er delvis nedsenket i tanken, og vann kommer ut via et overløp.
I dette eksemplet er det to stoffer: faste stoffer og vann. Vannoverløpsutløpet bærer en økt konsentrasjon av vann i forhold til faste stoffer, sammenlignet med slurryinnløpet, og utgangen av transportbåndet bærer en økt konsentrasjon av faste stoffer i forhold til vann.
Antagelser
- Stabil
- Ikke-reaktivt system
Analyse
Anta at slurryinnløpssammensetningen (etter masse) er 50% fast og 50% vann, med en massestrøm på 100 kg / min . Tanken antas å fungere i steady state, og da slik akkumulering er null, må input og output være lik for både faste stoffer og vann. Hvis vi vet at fjerningseffektiviteten for oppslemningstanken er 60%, vil vannutløpet inneholde20 kg / min faststoff (40% ganger100 kg / min ganger 50% faste stoffer). Hvis vi måler strømningshastigheten til de kombinerte faste stoffene og vannet, og vannutløpet er vist65 kg / min , så må mengden vann som kommer ut via transportbåndet være5 kg / min . Dette tillater oss å fullstendig bestemme hvordan massen har blitt fordelt i systemet med bare begrenset informasjon og ved å bruke massebalanseforholdet på tvers av systemgrensene. Massebalansen for dette systemet kan beskrives i tabellform:
| Strøm | |||
|---|---|---|---|
| Materiale | Avklaringsinnløp | Avklart vannuttak | Ekstraherte Soilds |
| Fast stoff | 50 kg/min | 20 kg/min | 30 kg/min |
| Vann | 50 kg/min | 45 kg/min | 5 kg/min |
| Total | 100 kg/min | 65 kg/min | 35 kg/min |
Masse tilbakemelding (resirkuler)
Massebalanser kan utføres på tvers av systemer som har sykliske strømninger. I disse systemene blir utgangsstrømmer ført tilbake til inngangen til en enhet, ofte for videre behandling.
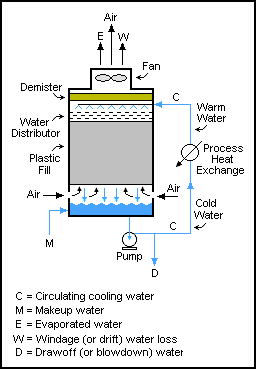
Slike systemer er vanlig i malekretser, hvor kornet knuses deretter siktet slik at bare fine partikler ut av kretsen og de større partikler returneres til valsemøllen (jeksel). Resirkuleringsstrømmer er imidlertid på ingen måte begrenset til solide mekaniske operasjoner; de brukes også i væske- og gassstrømmer. Et slikt eksempel er i kjøletårn , der vann pumpes gjennom et tårn mange ganger, med bare en liten mengde vann som trekkes ut ved hvert pass (for å forhindre oppbygging av faste stoffer) til det enten har fordampet eller gått ut med det avtappede vannet. Massebalansen for vann er M = D + W + E.
Bruken av resirkuleringen hjelper til med å øke den totale konverteringen av inputprodukter, noe som er nyttig for lav-per-pass konverteringsprosesser (for eksempel Haber-prosessen ).
Differensielle massebalanser
En massebalanse kan også tas differensielt . Konseptet er det samme som for en stor massebalanse, men det utføres i sammenheng med et begrensende system (for eksempel kan man vurdere det begrensende tilfellet i tid eller, mer vanlig, volum). En differensial massebalanse brukes til å generere differensialligninger som kan gi et effektivt verktøy for modellering og forståelse av målsystemet.
Differensialmassebalansen løses vanligvis i to trinn: Først må et sett med styrende differensialligninger oppnås, og deretter må disse ligningene løses, enten analytisk eller, for mindre behandlingsbare problemer, numerisk.
Følgende systemer er gode eksempler på anvendelsene av differensialmassebalansen:
- Ideell (omrørt) batchreaktor
- Ideell tankreaktor, også kalt Continuous Stirred Tank Reactor (CSTR)
- Ideal Plug Flow Reactor (PFR)
Ideell batchreaktor
Den ideelle fullstendig blandede batchreaktoren er et lukket system. Det antas isotermiske forhold , og blanding forhindrer konsentrasjonsgradienter ettersom reaktantkonsentrasjonene synker og produktkonsentrasjonene øker over tid. Mange lærebøker i kjemi antar implisitt at det studerte systemet kan beskrives som en batchreaktor når de skriver om reaksjonskinetikk og kjemisk likevekt . Massebalansen for et stoff A blir
hvor r A angir hastigheten stoffet A produseres med, V er volumet (som kan være konstant eller ikke), n A antall mol ( n ) av stoff A.
I en matet batch-reaktor tilsettes noen reaktanter/ingredienser kontinuerlig eller i pulser (sammenligne å lage grøt ved å først blande alle ingrediensene og deretter la det koke, som kan beskrives som en batchreaktor, eller ved først å blande bare vann og salt og får det til å koke før de andre ingrediensene tilsettes, som kan beskrives som en matet batch-reaktor). Massebalanser for matede batchreaktorer blir litt mer kompliserte.
Reaktivt eksempel
I det første eksemplet vil vi vise hvordan du bruker en massebalanse for å utlede et forhold mellom prosent luftoverskudd for forbrenning av en hydrokarbonbasert fyringsolje og prosent oksygen i forbrenningsproduktgassen. Først inneholder normal tørr luft0,2095 mol oksygen per mol luft, så det er en mol O
2 i 4,773 mol tørr luft. For støkiometrisk forbrenning er forholdet mellom luftmassen og massen til hvert brennbart element i en fyringsolje:
Med tanke på nøyaktigheten av typiske analytiske prosedyrer, er en ligning for luftmassen pr. Masse drivstoff ved støkiometrisk forbrenning:
hvor wC, wH, wS og wO refererer til massefraksjonen av hvert element i fyringsoljen, svovelforbrenning til SO2 og AFR- masse refererer til luft-drivstoff-forholdet i masseenheter.
Til 1 kg fyringsolje som inneholder 86,1% C, 13,6% H, 0,2% O og 0,1% S er den støkiometriske luftmassen14,56 kg , så AFR = 14,56. Forbrenningsproduktmassen er da15,56 kg . Ved nøyaktig støkiometri, O
2burde være fraværende. Ved 15 prosent overflødig luft er AFR = 16,75, og massen av forbrenningsproduktgassen er17,75 kg , som inneholder0,505 kg overflødig oksygen. Forbrenningsgassen inneholder dermed 2,84 prosent O
2etter masse. Forholdet mellom prosent overflødig luft og % O
2 i forbrenningsgassen uttrykkes nøyaktig med kvadratiske ligninger, gyldige i området 0–30 prosent overflødig luft:
I det andre eksemplet vil vi bruke loven om massevirkning for å utlede uttrykket for en kjemisk likevektskonstant .
Anta at vi har en lukket reaktor der følgende reversible reaksjon i væskefasen skjer:
Massebalansen for stoff A blir
Siden vi har en væskefasereaksjon kan vi (vanligvis) anta et konstant volum og siden vi får det
eller
I mange lærebøker er dette gitt som definisjonen på reaksjonshastighet uten å spesifisere den implisitte antagelsen om at vi snakker om reaksjonshastighet i et lukket system med bare en reaksjon. Dette er en uheldig feil som har forvirret mange studenter gjennom årene.
I henhold til loven om massehandling kan fremoverreaksjonshastigheten skrives som
og reaksjonshastigheten bakover som
Hastigheten stoffet A produseres med er dermed
og siden, ved likevekt, er konsentrasjonen av A konstant vi får
eller, omorganisert
Ideell tankreaktor/kontinuerlig omrørt tankreaktor
Den kontinuerlig blandede tankreaktoren er et åpent system med en innflytende strøm av reaktanter og en avløpsstrøm av produkter. En innsjø kan betraktes som en tankreaktor, og innsjøer med lange omsetningstider (f.eks. Med lave flux-til-volumforhold) kan for mange formål betraktes som kontinuerlig omrørt (f.eks. Homogen på alle måter). Massebalansen blir da
der Q 0 og Q angir den volumetriske strømmen inn og ut av henholdsvis systemet og C A, 0 og C A konsentrasjonen av A i henholdsvis tilsig og utstrømning. I et åpent system kan vi aldri nå en kjemisk likevekt. Vi kan imidlertid nå en stabil tilstand der alle tilstandsvariabler (temperatur, konsentrasjoner, etc.) forblir konstant ( ).
Eksempel
Tenk på et badekar der det er litt badesalt oppløst. Vi fyller på mer vann og beholder bunnpluggen. Hva skjer?
Siden det ikke er noen reaksjon, og siden det ikke er noen utstrømning . Massebalansen blir
eller
Ved å bruke en massebalanse for totalt volum, er det imidlertid tydelig at og det . Slik får vi
Merk at det ikke er noen reaksjon, og dermed ingen reaksjonshastighet eller hastighetsloven involvert, og likevel . Vi kan dermed trekke den konklusjon at reaksjonshastigheten ikke kan defineres på en generell måte ved hjelp av . Man må først skrive ned en massebalanse før en kobling mellom og reaksjonshastigheten kan bli funnet. Mange lærebøker definerer imidlertid reaksjonshastigheten som
uten å nevne at denne definisjonen implisitt forutsetter at systemet er lukket, har et konstant volum og at det bare er en reaksjon.
Ideell plug -flow reaktor (PFR)
Den idealiserte pluggstrømreaktoren er et åpent system som ligner et rør uten blanding i strømningsretningen, men perfekt blanding vinkelrett på strømningsretningen, ofte brukt for systemer som elver og vannrør hvis strømmen er turbulent. Når en massebalanse er laget for et rør, vurderer man først en uendelig liten del av røret og lager en massebalanse over den ved hjelp av den ideelle tankreaktormodellen. Denne massebalansen blir deretter integrert over hele reaktorvolumet for å oppnå:
I numeriske løsninger, f.eks. Ved bruk av datamaskiner, blir det ideelle røret ofte oversatt til en serie tankreaktorer, da det kan vises at en PFR tilsvarer et uendelig antall omrørte tanker i serier, men sistnevnte er ofte lettere å analysere , spesielt ved steady state.
Mer komplekse problemer
I virkeligheten er reaktorer ofte ikke-ideelle, der kombinasjoner av reaktormodellene ovenfor brukes til å beskrive systemet. Ikke bare kjemiske reaksjonshastigheter, men også masseoverføringshastigheter kan være viktige i den matematiske beskrivelsen av et system, spesielt i heterogene systemer.
Siden den kjemiske reaksjonshastigheten avhenger av temperaturen, er det ofte nødvendig å lage både en energibalanse (ofte en varmebalanse i stedet for en fullverdig energibalanse) samt massebalanser for å beskrive systemet fullt ut. En annen reaktormodell kan være nødvendig for energibalansen: Et system som er lukket med hensyn til masse kan være åpent med hensyn til energi, for eksempel siden varme kan komme inn i systemet gjennom ledning .
Kommersielt bruk
I industrielle prosessanlegg, ved å bruke det faktum at massen som kommer inn og ut av en hvilken som helst del av et prosessanlegg må balansere, kan datavalidering og avstemningsalgoritmer brukes til å korrigere målte strømmer, forutsatt at det er nok redundans av strømningsmålinger for å tillate statistisk avstemning og ekskludering av påviselig feilaktige målinger. Siden alle virkelige måleverdier inneholder iboende feil, gir de avstemte målingene et bedre grunnlag enn måleverdiene for finansiell rapportering, optimalisering og reguleringsrapportering. Det finnes programvarepakker for å gjøre dette kommersielt mulig daglig.
Se også
Referanser
Eksterne linker
- Materialbalanseberegninger
- Materialbalanse Grunnleggende
- Materialbalansen for kjemiske reaktorer
- Material- og energibalanse
- Varme- og materialbalansemetode for prosesskontroll for petrokjemiske anlegg og oljeraffinerier, USAs patent 6751527
- Morris, Arthur E .; Geiger, Gordon; Fine, H. Alan (2011). Håndbok om beregninger av materiale- og energibalanse i materialbehandling (3. utg.). Wiley . ISBN 978-1-118-06565-5.
















![r_1 = k_1 [\ mathrm {A}]^a [\ mathrm {B}]^b](https://wikimedia.org/api/rest_v1/media/math/render/svg/39705e7b067feb34083145780fca904558471a3d)
![{\ displaystyle r _ {-1} = k _ {-1} [\ mathrm {C}]^{c} [\ mathrm {D}]^{d}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/27a0bd516fe71d6b0f717db6bda90c725636c033)


![\ frac {k_1} {k _ {-1}} = \ frac {[\ mathrm {C}]^c [\ mathrm {D}]^d} {[\ mathrm {A}]^a [\ mathrm {B }]^b} = K_ {eq}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6ea19d7d091bc2086d115756eca8dadca790c6eb)












