Rodium (III) klorid - Rhodium(III) chloride
|
|

|
|

|
|
| Navn | |
|---|---|
| Andre navn
Rodiumtriklorid
|
|
| Identifikatorer | |
|
3D -modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.030.138 |
| EC -nummer | |
|
PubChem CID
|
|
| RTECS -nummer | |
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| RhCl 3 | |
| Molar masse | 209,26 g/mol |
| Utseende | mørkerødt fast delikat |
| Tetthet | 5,38 g / cm 3 , fast |
| Smeltepunkt | ca. 450 ° C (842 ° F; 723 K) |
| Kokepunkt | 717 ° C (1.323 ° F; 990 K) |
| uløselig | |
| Løselighet | løselig i hydroksyd- og cyanidløsninger , også løselig i vannregier |
| Surhet (p K a ) | sur i oppløsningen |
| −7,5 · 10 −6 cm 3 /mol | |
| Struktur | |
| Monoklinisk , mS16 | |
| C12/m1, nr. 12 | |
| oktaedrisk | |
| Termokjemi | |
|
Std
formasjonsentalpi (Δ f H ⦵ 298 ) |
−234 kJ/mol |
| Farer | |
| Sikkerhetsdatablad | ICSC 0746 |
| Flammepunkt | Ikke brennbar |
| Dødelig dose eller konsentrasjon (LD, LC): | |
|
LD 50 ( median dose )
|
> 500 mg/kg (rotte, oral) 1302 mg/kg (rotte, oral) |
| Relaterte forbindelser | |
|
Andre anioner
|
Rhodium (III) fluor Rhodium (III) bromide Rhodium (III) jodid |
|
Andre kationer
|
Kobolt (II) klorid Iridium (III) klorid |
|
Relaterte forbindelser
|
Rutenium (III) klorid Palladium (II) klorid |
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox -referanser | |
Rhodium (III) klorid refererer til uorganiske forbindelser med formel RhCl 3 (H 2 O) n , hvor n varierer fra 0 til 3. Disse er diamagnetiske faste stoffer Med oktaedriske Rh (III) sentre. Avhengig av verdien av n , er materialet enten et tett brunt fast stoff eller et oppløselig rødlig salt. Det oppløselige trihydrerte (n = 3) saltet er mye brukt for å fremstille forbindelser som brukes i homogen katalyse , særlig for industriell produksjon av eddiksyre og hydroformylering .
Strukturer
Vandige oppløsninger av RhCl 3 (H 2 O) 3 har vært preget av 103 Rh NMR-spektroskopi , noe som viser tilstedeværelsen av flere arter. Andelen som endres med tiden og avhenger av konsentrasjonen av klorid. Den relative fordelingen av disse artene bestemmer fargen på løsningene, som kan variere fra gult (hexaaquo-ionet) til "bringebærrødt". Noen av disse artene er [Rh (H 2 O) 6 ] 3+ , [RhCl (H 2 O) 5 ] 2+ , cis - og trans - [RhCl 2 (H 2 O) 4 ] + og [RhCl 3 (H 2 O) 3 ]. Individuelle ioner har blitt separert ved ionebytterkromatografi.
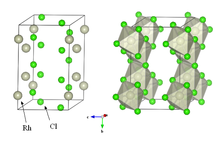
Vannfrie rhodiumklorid krystalliserer i YCL 3 og AlCl 3 motiv (se bilde i øverst til høyre). Metallsentrene er oktaedriske, og halogenidene er en dobbel bro. Det er et tett brunt fast stoff som er uløselig i vanlige løsningsmidler og har liten verdi i laboratoriet.
Forberedelse
RhCl 3 (H 2 O) 3 fremstilles av salter slik som Na 3 RhCl 6 , idet sistnevnte er oppnådd ved rensing av rhodium fra de andre platinagruppemetaller som platina og iridium. Natriumsaltet ble omdannet til H- 3 RhCl 6 ved ionebytterkromatografi . Omkrystallisering av dette sure saltet fra vann gir det hydratiserte trikloridet, noen ganger kalt "løselig rodiumtriklorid." Vannfritt RhCl 3 fremstilles ved omsetning av klor med rhodium svampmetall ved 200-300 ° C. Over 800 ° C går det vannfrie kloridet tilbake til Rh -metall og klor.
Ulike rodiumkloridkomplekser er mellomprodukter i rensing av rodium fra malmene.
Koordineringskomplekser
RhCl 3 (H 2 O) 3 er en forløper til en rekke komplekser , hvorav noen er kommersielt nyttig. Den reagerer med acetylaceton for å gi rodiumacetylacetonat .
Aminer og pyridin
Oppløsninger av RhCl 3 (H 2 O) 3 reagere med ammoniakk i nærvær av alkoholen under dannelse av saltet pentamminerhodium klorid , [RhCl (NH 3 ) 5 ] Cl 2 . Sink reduksjon av denne kation, etterfulgt av tilsetning av sulfat gir den fargeløse hydridkompleks [parets (NH 3 ) 5 ] SO 4 .
Ved koking i en blanding av etanol og pyridin (py), hydratiserte rhodiumtrikloridhydrat konverterer til trans - [RhCl 2 (py) 4 )] Cl . I fravær av et reduksjonsmiddel, er reaksjons gir fac - [RhCl 3 (py) 3 ], analogt med tioeterderivater. Oksidasjon av vandig etanolisk oppløsning av pyridin og RhCl 3 (H 2 O) 3 ved hjelp av luft gir en blå paramagnetisk oksygen-broforbindelsen, [Cl (py) 4 Rh-O 2 -Rh (py) 4 Cl] 5+ .
Tioetere og tertiære fosfiner
Etanoliske løsninger av hydrert rodiumtriklorid reagerer med dialkylsulfider .
- RhCl 3 (H 2 O) 3 + 3 SR 2 RhCl 3 (SR 2 ) 3 + 3 H 2 O
Både fac og mer stereoisomerer av slike forbindelser har blitt isolert.
Omsetning av RhCl 3 (H 2 O) 3 under milde betingelser med tertiære fosfiner gir addukter beslektet med den ovennevnte tioeter-komplekser. Når disse reaksjonene utføres i kokende etanoloppløsning, oppstår reduksjon av rodium (III), noe som fører til rodium (I) -derivater som [RhCl (PPh 3 ) 3 ], Wilkinsons katalysator , med oksidasjon av løsningsmidlet eller mer vanlig med et overskudd av fosfin:
Alkener og karbonmonoksid
Omsetning av RhCl 3 (H 2 O) 3 med olefiner, gir forbindelser av type Rh 2- Cl 2 (alken) 4 . Med 1,5-syklooktadien, RhCl 3 (H 2 O) 3 reagere i etanol for å gi cyklooktadien rhodiumklorid-dimer .

RhCl 3 (H 2 O) 3 i metanol, reagerer med karbonmonoksyd (1 bar) for å fremstille H [RhCl 2 (CO) 2 ], som inneholder dicarbonyldichloridorhodate (I) anion; videre karbonylering i nærvær av natriumcitrat fører til dannelsen av tetrarhodium dodecacarbonyl , Rh 4 (CO) 12 , en rhodium (0) klaseforbindelse . Behandling av fast RhCl 3 (H 2 O) 3 med strømmende CO gir den dimere rhodium (I) forbindelse rhodium karbonylklorid , [(CO) 2 Rh (μ-Cl)] 2 .
Mange Rh-CO-PR 3 (R = organiske grupper) forbindelser er blitt fremstilt i løpet av omfattende undersøkelser av hydroformyleringskatalyse . RhCl (PPh 3 ) 3 reagerer med CO og gir trans -RhCl (CO) (PPh 3 ) 2 , støkiometrisk analog til, men mindre reaktiv enn Vaskas kompleks . Trans -RhCl (CO) (PPh 3 ) 2 reagerer med en blanding av NaBH 4 og PPh 3 for å gi HRh (CO) (PPh 3 ) 3 , en svært aktiv katalysator for hydroformylering av alkener.
Ved behandling med cyclopentadienes eller dets derivater kan organometalliske halve sandwichforbindelser produseres. For eksempel fører reaksjon av trihydratet med pentametylsyklopentadien (Cp*H) i varm metanol til utfelling av pentametylsyklopentadienyl -rodiumdiklorid -dimeren , [Cp*RhCl 2 ] 2 :
- 2 Cp*H + 2 RhCl 3 (H 2 O) 3 [Cp*RhCl 2 ] 2 + 2 HCl + 6 H 2 O
Denne forbindelse ble først fremstilt fra heksametyl Dewar benzen og RhCl 3 (H 2 O) 3 . Hydrohalinsyren som er nødvendig for omorganisering av ringkontraksjonen genereres in situ i metanoliske oppløsninger av rodiumsaltet, og det andre trinnet har blitt utført separat, som bekrefter denne mekanistiske beskrivelsen. Reaksjonen finner sted ved dannelsen av 1,1-dimetoksyetan , CH 3 CH (OCH 3 ) 2 , og heksametylbenzen er produsere ved en sidereaksjon . Denne rodium (III) dimeren kan reduseres med sink i nærvær av CO for å produsere rodium (I) komplekset [Cp*Rh (CO) 2 ].
Katalyse
Begynnelsen spesielt i 1960, RhCl 3 (H 2 O) 3 ble påvist å være katalytisk aktiv for en rekke reaksjoner som omfatter CO, H 2 , og alkener . For eksempel, RhCl 3 (H 2 O) 3 ble vist å dimerise eten til en blanding av cis- og trans- 2-buten :
- 2 C 2 H 4 CH 3 -CH = CH -CH 3
Dessverre mislykkes denne reaksjonen for høyere alkener.
Etylendimerisering viste seg å involvere katalyse av den dimere rodium (I) -forbindelsen [(η 2 -C 2 H 4 ) 2 Rh (μ -Cl) 2 Rh (η 2 -C 2 H 4 ) 2 ] . Dette og mange relaterte funn næret det daværende unge feltet for homogen katalyse, hvor katalysatorene er oppløst i mediet med substratet. Før denne epoken var de fleste metallkatalysatorer "heterogene", dvs. katalysatorene var faste stoffer og substratene var enten flytende eller gasser. Et annet fremskritt i homogen katalyse var det funn at PPh 3 -avledede komplekser har vært aktive katalytisk, så vel som oppløselige i organiske oppløsningsmidler, det best kjente en slik katalysator er Wilkinsons katalysator som katalyserer hydrogenering og isomerisering av alkener. Hydroformyleringen av alkener katalyseres av den relaterte RhH (CO) (PPh 3 ) 3 . Katalyse av rhodium er så effektiv at den har fortrengt den tidligere teknologien betydelig basert på rimeligere koboltkatalysatorer.
Sikkerhet
Rodium (III) klorid er ikke oppført under vedlegg I til direktiv 67/548/EØF , men er vanligvis klassifisert som skadelig , R22 : Farlig ved svelging . Noen Rh-forbindelser har blitt undersøkt som legemidler mot kreft . Det er oppført i oversikten over kontrollloven for giftige stoffer (TSCA).

![{\ displaystyle {\ ce {-> [{\ ce {CH3CH2OH}}]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7a6552044024d3bcd2e07972f7ae82ca8ca646a1)
![{\ displaystyle {\ ce {-> [{\ ce {CH3CH2OH}} {\ text { / Δ}}]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/12a08389489aa7ab9fbd60f946daba3c1a06e582)
![{\ displaystyle {\ ce {-> [{\ ce {CH3OH}} {\ text { / Δ}}]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8b38287ac05102ae2efa8432ce004a22c2dc924e)
![Syntese av rhodium (III) dimeren [Cp*RhCl2] 2 fra heksametyl Dewar benzen](https://upload.wikimedia.org/wikipedia/commons/thumb/d/db/Hexamethyl_Dewar_benzene_reacting_with_rhodium_chloride_under_acidic_conditions.PNG/700px-Hexamethyl_Dewar_benzene_reacting_with_rhodium_chloride_under_acidic_conditions.PNG)
![{\ displaystyle {\ ce {-> [{\ ce {RhCl3 (H2O) 3}}]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/bb2c131af4d6b9deaacb2b34406a3bdff68a87cb)