Tyrosinaminotransferase - Tyrosine aminotransferase
| Tyrosintransaminase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
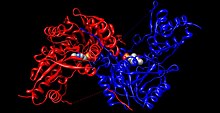
 Humant tyrosinaminotransferase (regnbuefarget, N-terminal = blå, C-terminal = rød) kompleksert med pyridoksalfosfat ( romfyllingsmodell ).
| |||||||||
| Identifikatorer | |||||||||
| EF -nr. | 2.6.1.5 | ||||||||
| CAS -nr. | 9014-55-5 | ||||||||
| Databaser | |||||||||
| IntEnz | IntEnz -visning | ||||||||
| BRENDA | BRENDA -oppføring | ||||||||
| ExPASy | NiceZyme utsikt | ||||||||
| KEGG | KEGG -oppføring | ||||||||
| MetaCyc | metabolsk vei | ||||||||
| PRIAM | profil | ||||||||
| PDB -strukturer | RCSB PDB PDBe PDBsum | ||||||||
| Genontologi | AmiGO / QuickGO | ||||||||
| |||||||||
Tyrosinaminotransferase (eller tyrosintransaminase ) er et enzym som finnes i leveren og katalyserer omdannelsen av tyrosin til 4-hydroksyfenylpyruvat .
Hos mennesker er tyrosinaminotransferaseproteinet kodet av TAT -genet . En mangel på enzymet hos mennesker kan resultere i det som kalles tyrosinemi av type II , hvor det er en mengde tyrosin som et resultat av at tyrosin ikke gjennomgår en aminotransferasereaksjon for å danne 4-hydroksyfenylpyruvat.
Mekanisme
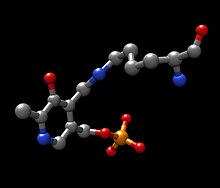
Strukturene til de tre hovedmolekylene som er involvert i kjemisk reaksjon katalysert av tyrosinaminotransferaseenzymet er vist nedenfor: aminosyren tyrosin , den protetiske gruppen pyridoksalfosfat og det resulterende produktet 4-hydroksyfenylpyruvat .
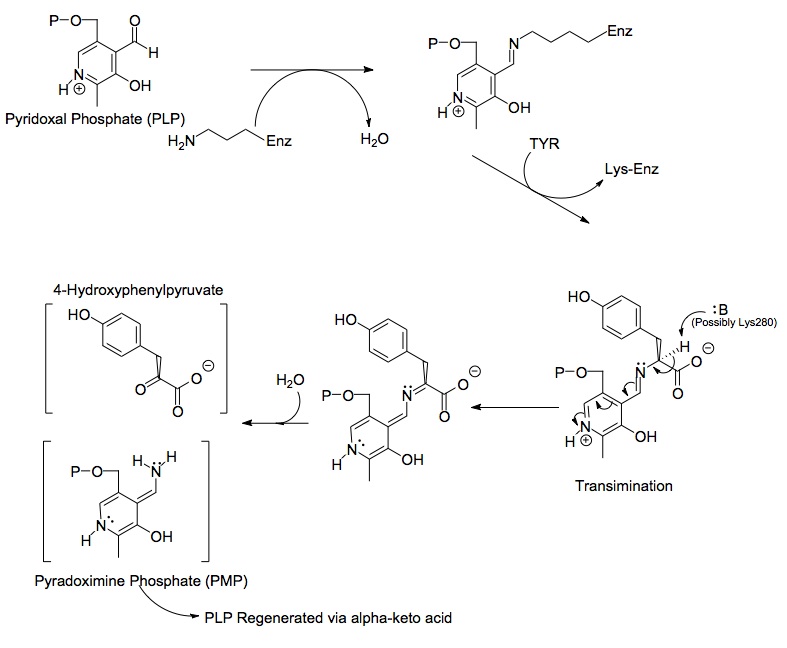
Hver side av dimerproteinet inkluderer pyridoksalfosfat (PLP) bundet til Lys280 -resten av tyrosinaminotransferasemolekylet. Amingruppen av tyrosin angriper alfakarbonet av iminet bundet til Lys280, danner et tetraederkompleks og sparker deretter i gang LYS-ENZ. Denne prosessen er kjent som transiminering ved å slå ut imingruppen som er bundet til PLP. Det nydannede PLP-TYR-molekylet blir deretter angrepet av en base.
En mulig kandidat for basen i mekanismen kan være Lys280 som nettopp ble presset av PLP, som sekvesterer den nydannede aminogruppen til PLP-TYR-molekylet. I en lignende mekanisme for aspartattransaminase virker lysinet som danner den første iminen til PLP senere som basen som angriper tyrosinet ved transiminering. Elektronene som er igjen etter tapet av protonen beveger seg ned for å danne en ny dobbeltbinding til iminen, som igjen skyver de allerede dobbeltbundne elektronene gjennom PLP og ender som et ensomt par på det positivt ladede nitrogenet i seksleddet ringen av molekylet. Vann angriper alfakarbonet av iminet av PLP-TYR og ved hjelp av acylsubstitusjon starter nitrogenet til PLP og danner pyridoksaminfosfat (PMP) og 4-hydroksyfenylpyruvat.
PMP regenereres deretter til PLP ved å overføre amingruppen til alfa-ketoglutarat, og reformere den aldehydfunksjonelle gruppen. Dette etterfølges av en annen substitusjonsreaksjon med Lys280-resten for å reformere dens iminbinding til enzymet og danne ENZ-PLP.
Aktiv side
Tyrosinaminotransferase som en dimer har to identiske aktive steder. Lys280 er festet til PLP, som holdes på plass via to upolare aminosyresidekjeder; fenylalanin og isoleucin (se miniatyrbildet til høyre). PLP holdes også på plass ved hydrogenbinding til omgivende molekyler hovedsakelig av fosfatgruppen.
Nedenfor vises et aktivt nettsted med tre forskjellige forstørrelser:

Patologi
Tyrosinemi er den vanligste metabolske sykdommen forbundet med tyrosinaminotransferase. Sykdommen skyldes mangel på hepatisk tyrosinaminotransferase. Tyrosinemi type II (Richner-Hanhart syndrom, RHS) er en sykdom med autosomal recessiv arv preget av keratitt, palmoplantar hyperkeratose, mental retardasjon og forhøyede blodtyrosinnivåer. Keratitt hos pasienter med tyrosinemi type II er forårsaket av avsetning av tyrosinkrystaller i hornhinnen og resulterer i betennelse i hornhinnen. TAT-genet er lokalisert på humant kromosom 16q22-24 og strekker seg over 10,9 kilobaser (kb) som inneholder 12 eksoner, og dets 3,0 kb mRNA koder for et 454-aminosyreprotein på 50,4 kDa. Tolv forskjellige TAT -genmutasjoner er rapportert.
Referanser
Molekylære grafikkbilder ble produsert ved hjelp av UCSF Chimera-pakken fra Resource for Biocomputing, Visualization, and Informatics ved University of California, San Francisco (støttet av NIH P41 RR-01081).
Eksterne linker
- Tyrosin+aminotransferase ved US National Library of Medicine Medical Subject Headings (MeSH)
- PDBe-KB gir en oversikt over all strukturinformasjon som er tilgjengelig i PDB for humant tyrosinaminotransferase