Antrasen - Anthracene

|
|

|
|

|
|
| Navn | |
|---|---|
|
Foretrukket IUPAC -navn
Antrasen |
|
|
Systematisk IUPAC -navn
Tricyklo [8.4.0.0 3,8 ] tetradeca-1,3,5,7,9,11,13-heptaene |
|
| Identifikatorer | |
|
3D -modell ( JSmol )
|
|
| 1905429 | |
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100.003.974 |
| EC -nummer | |
| 67837 | |
| KEGG | |
|
PubChem CID
|
|
| RTECS -nummer | |
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C 14 H 10 | |
| Molar masse | 178,234 g · mol −1 |
| Utseende | Fargeløs |
| Lukt | Svak aromatisk |
| Tetthet | 1,28 g/cm 3 (25 ° C) 0,969 g/cm 3 (220 ° C) |
| Smeltepunkt | 216 ° C (421 ° F; 489 K) ved 760 mmHg |
| Kokepunkt | 341,3 ° C (646,3 ° F; 614,5 K) ved 760 mmHg |
| 0,022 mg/L (0 ° C) 0,044 mg/L (25 ° C) 0,29 mg/L (50 ° C) 0,00045 vekt/vekt (100 ° C, 3,9 MPa) |
|
| Løselighet | Løselig i alkohol , (C 2 H 5 ) 2 O , aceton , C 6 H 6 , CHCl 3 , CS 2 |
| Løselighet i etanol | 0,76 g/kg (16 ° C) 1,9 g/kg (19,5 ° C) 3,28 g/kg (25 ° C) |
| Løselighet i metanol | 18 g/kg (19,5 ° C) |
| Løselighet i heksan | 3,7 g/kg |
| Løselighet i toluen | 9,2 g/kg (16,5 ° C) 129,4 g/kg (100 ° C) |
| Løselighet i karbontetraklorid | 7,32 g/kg |
| logg P | 4.56 |
| Damptrykk | 0,01 kPa (125,9 ° C) 0,1 kPa (151,5 ° C) 13,4 kPa (250 ° C) |
|
Henrys
lovkonstant ( k H ) |
0,0396 L · atm/mol |
| UV-vis (λ maks ) | 345,6 nm, 363,2 nm |
| −129,8 × 10 −6 cm 3 /mol | |
| Termisk ledningsevne | 0,1416 W/(m · K) (240 ° C) 0,1333 W/(m · K) (270 ° C) 0,1259 W/(m · K) (300 ° C) |
| Viskositet | 0,602 cP (240 ° C) 0,498 cP (270 ° C) 0,429 cP (300 ° C) |
| Struktur | |
| Monoklinisk (290 K) | |
| P2 1 /b | |
| D5 2 timer |
|
|
a = 8.562 Å, b = 6.038 Å, c = 11.184 Å
α = 90 °, β = 124,7 °, γ = 90 °
|
|
| Termokjemi | |
|
Varmekapasitet ( C )
|
210,5 J/(mol · K) |
|
Std molar
entropi ( S |
207,5 J/(mol · K) |
|
Std
formasjonsentalpi (Δ f H ⦵ 298 ) |
129,2 kJ/mol |
|
Std
forbrenningsentalpi (Δ c H ⦵ 298 ) |
7061 kJ/mol |
| Farer | |
| GHS -piktogrammer |
 
|
| GHS Signalord | Advarsel |
| H302 , H305 , H315 , H319 , H335 , H410 | |
| P261 , P273 , P305+351+338 , P501 | |
| NFPA 704 (brann diamant) | |
| Flammepunkt | 121 ° C (250 ° F; 394 K) |
| 540 ° C (1 004 ° F; 813 K) | |
| Dødelig dose eller konsentrasjon (LD, LC): | |
|
LD 50 ( median dose )
|
100-149 mg/kg (rotter, orale) |
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox -referanser | |
Antracen er et solid polysyklisk aromatisk hydrokarbon (PAH) med formel C 14 H 10 , som består av tre smeltede benzenringer . Det er en bestanddel av kulltjære . Antracen brukes i produksjonen av det røde fargestoffet alizarin og andre fargestoffer. Antracen er fargeløst, men viser en blå (400–500 nm topp) fluorescens under ultrafiolett stråling.
Forekomst og produksjon
Kultjære, som inneholder rundt 1,5% antracen, er fortsatt en viktig kilde til dette materialet. Vanlige urenheter er fenantren og karbazol . Mineralformen av antracen kalles freitalitt og er relatert til et kullforekomst. En klassisk laboratoriemetode for fremstilling av antracen er ved cyklodehydrering av o-metyl- eller o-metylensubstituerte diarylketoner i den såkalte Elbs-reaksjonen .
Reaksjoner
Reduksjon
Reduksjon av antracen med alkalimetaller gir de dypfargede radikale anionsaltene M + [antracen] - (M = Li, Na, K). Hydrogenering gir 9,10- dihydroantracen , og bevarer aromatikken til de to flankeringene.
Cycloadditions
Antracen fotodimeriserer ved virkningen av UV -lys:
Den dimer , kalt dianthracene (eller noen ganger paranthracene), er forbundet med et par nye karbon-karbonbindinger, resultatet av [4 + 4] cykloaddisjon . Det går tilbake til antracen termisk eller med UV -bestråling under 300 nm. Substituerte antracenderivater oppfører seg på samme måte. Reaksjonen påvirkes av tilstedeværelsen av oksygen .
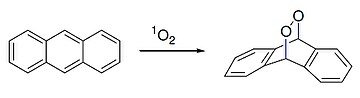
Antracen reagerer også med dienofil singlet oksygen i en [4+2] -cyklostdisjon ( Diels – Alder-reaksjon ):
Med elektrofiler
Kjemisk oksidasjon skjer lett, noe som gir antrakinon , C 14 H 8 O 2 (nedenfor), for eksempel ved bruk av hydrogenperoksid og vanadylacetylacetonat .
Elektrofil substitusjon av antracen skjer i 9 -stillingen. For eksempel gir formylering 9-antracenkarboksaldehyd . Substitusjon på andre stillinger utføres indirekte, for eksempel med antokinon. Brominering av antracen gir 9,10-dibromantranen.
Bruker
Antracen omdannes hovedsakelig til antrakinon , en forløper til fargestoffer.
Nisje
Antracen, en bred båndgap organisk halvleder brukes som en scintillator for detektorer av højenergifotoner , elektroner og alfapartikler . Plast, for eksempel polyvinyltoluen , kan dopes med antracen for å produsere en plastisk scintillator som er tilnærmet vannekvivalent for bruk i strålebehandling dosimetri . Antrasens utslippsspektrum topper seg mellom 400 nm og 440 nm.
Det er også brukt i tre konserveringsmidler , insektmidler , og beleggmateriale .
Antracen brukes ofte som UV -sporstoff i samsvarende belegg påført på trykte ledningsplater. Antracen -sporstoffet gjør at det konforme belegget kan inspiseres under UV -lys. Antrasen brukes også i produksjon av antrakinon.
Derivater

En rekke antracenderivater finner spesialiserte bruksområder. Derivater som har en hydroksylgruppe er 1-hydroksyantracen og 2-hydroksyantracen, homologe med fenol og naftoler , og hydroksyantracen (også kalt antrol og antrasenol) er farmakologisk aktive. Antracen kan også finnes med flere hydroksylgrupper, som i 9,10-dihydroksyantracen .
Hendelse
Antracen, som mange andre polysykliske aromatiske hydrokarboner , genereres under forbrenningsprosesser. Eksponering for mennesker skjer hovedsakelig gjennom tobakkrøyk og inntak av mat som er forurenset med forbrenningsprodukter.
Toksikologi
Mange undersøkelser indikerer at antracen er ikke -kreftfremkallende: "konsekvent negative funn i en rekke in vitro og in vivo genotoksisitetstester". Tidlige eksperimenter antydet noe annet fordi råprøver var forurenset med andre polycykliske aromatiske forbindelser . Videre nedbrytes det lett i jord. Det er spesielt utsatt for nedbrytning i nærvær av lys.
Se også
- 9,10-Ditioantracen , derivat med to tiolgrupper tilsatt den sentrale ringen
- Fenantren
- Tetracene
Referanser
Siterte kilder
- Haynes, William M., red. (2011). CRC Handbook of Chemistry and Physics (92. utgave). CRC Press . ISBN 978-1439855119.