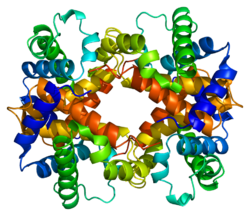
Hemoglobin subenhet beta - Hemoglobin subunit beta
Hemoglobin subenhet beta , ( beta-globin , β-globin , hemoglobin-beta , hemoglobin-beta ) er en globin protein , kodet for av HBB -genet, som sammen med alfa-globin ( HBA ), utgjør den mest vanlige formen av hemoglobin hos voksne mennesker , hemoglobin A (HbA). Den er 147 aminosyrer lang og har en molekylvekt på 15 867 Da . Normal voksen menneskelig HbA er en heterotetramer som består av to alfakjeder og to betakjeder.
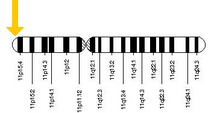
HBB er kodet av HBB -genet på humant kromosom 11 . Mutasjoner i genet produserer flere varianter av proteinene som er implisert med genetiske lidelser som sigdcellesykdom og beta-thalassemi , samt fordelaktige egenskaper som genetisk resistens mot malaria .
Genlokus
HBB-protein produseres av genet HBB som er lokalisert på multigen-locuset av β-globin-locus på kromosom 11 , spesielt på den korte armposisjonen 15.4. Uttrykk for beta-globin og de nærliggende globinene i β-globin-locus styres av enkelt- locus-kontrollregion (LCR), det viktigste regulatoriske elementet på locuset som ligger oppstrøms for globin-genene. Den normale allelvarianten er 1600 basepar (bp) lang og inneholder tre eksoner . Rekkefølgen på genene i beta-globinklyngen er 5 ' -epsilon - gamma-G - gamma-A - delta -beta-3'.
Interaksjoner
HBB samhandler med hemoglobin, alfa 1 (HBA1) for å danne hemoglobin A, det viktigste hemoglobinet hos voksne mennesker. Samspillet er todelt. Først kombineres en HBB og en HBA1, ikke-kovalent, for å danne en dimer. For det andre kombineres to dimerer for å danne firekjedet tetramer, og dette blir det funksjonelle hemolglobinet.
Tilknyttede genetiske lidelser
Betatalassemi
Betatalassemi er en arvelig genetisk mutasjon i en (Beta thalassemia minor) eller begge (Beta thalassemia major) av Beta globin-allelene på kromosom 11. De mutante allelene er delt inn i to grupper: β0, hvor ingen funksjonell β-globin dannes , og β+, der en liten mengde normalt β-globinprotein produseres. Betatalassemi mindre oppstår når en person arver en normal Beta -allel og en unormal Beta -allel (enten β0 eller β+). Beta thalassemi mindre resulterer i en mild mikrocytisk anemi som ofte er asymptomatisk eller kan forårsake tretthet og eller blek hud. Beta thalassemia major oppstår når en person arver to unormale alleler. Dette kan enten være to ß+ alleler, to β0 -alleler eller en av hver. Beta thalassemia major er en alvorlig medisinsk tilstand. En alvorlig anemi ses fra 6 måneders alder. Uten medisinsk behandling skjer døden ofte før du er 12. Beta thalassemia major kan behandles ved livslang blodoverføring eller benmargstransplantasjon .
I følge en nylig studie er stop gain-mutasjonen Gln40stop i HBB- genet en vanlig årsak til autosomal recessiv beta-thalassemi hos sardinske mennesker (nesten eksklusivt på Sardinia). Bærere av denne mutasjonen viser et forbedret antall røde blodlegemer. Som en kuriositet, var den samme mutasjonen også assosiert med en nedgang i serum -LDL -nivåer i bærere, så forfatterne antyder at det skyldes behovet for kolesterol for å regenerere cellemembraner.
Sigdcellesykdom
Mer enn tusen naturlig forekommende HBB -varianter er oppdaget. Den vanligste er HbS, som forårsaker sigdcellesykdom . HbS produseres av en punktmutasjon i HBB der kodonet GAG er erstattet av GTG. Dette resulterer i erstatning av hydrofil aminosyre glutaminsyre med den hydrofobe aminosyren valin i sjette posisjon (β6Glu → Val). Denne substitusjonen skaper et hydrofobt sted på utsiden av proteinet som fester seg til den hydrofobe regionen i et tilstøtende hemoglobinmolekyls betakjede. Dette forårsaker ytterligere klumping av HbS -molekyler i stive fibre, noe som forårsaker "sigd" av hele de røde blodcellene i den homozygote ( HbS/HbS ) tilstanden. Den homozygote allelen har blitt en av de dødeligste genetiske faktorene, mens mennesker heterozygote for den mutante allelen ( HbS/HbA ) er resistente mot malaria og utvikler minimale effekter av anemi.
Hemoglobin C.
Seglcellesykdom er nært knyttet til et annet mutant hemoglobin kalt hemoglobin C (HbC), fordi de kan arves sammen. HbC -mutasjon er i samme posisjon i HbS, men glutaminsyre erstattes av lysin (β6Glu → Lys). Mutasjonen er spesielt utbredt i vestafrikanske populasjoner. HbC gir nær full beskyttelse mot Plasmodium falciparum hos homozygote (CC) individer og mellomliggende beskyttelse hos heterozygote (AC) individer. Dette indikerer at HbC har sterkere innflytelse enn HbS, og er spådd å erstatte HbS i malaria-endemiske regioner.
Hemoglobin E.
En annen punktmutasjon i HBB, der glutaminsyre erstattes med lysin i posisjon 26 (β26Glu → Lys), fører til dannelse av hemoglobin E (HbE). HbE har en veldig ustabil α- og β-globinforening. Selv om det ustabile proteinet i seg selv har en mild effekt, arvet med HbS- og thalassemi-egenskaper, blir det til en livstruende form for β-thalassemi. Mutasjonen er av relativt nylig opprinnelse, noe som tyder på at den skyldes selektivt trykk mot alvorlig falciparum malaria, ettersom heterozygot allel forhindrer utvikling av malaria.
Menneskelig evolusjon
Malaria på grunn av Plasmodium falciparum er en viktig selektiv faktor i menneskelig evolusjon . Det har påvirket mutasjoner i HBB i forskjellige grader, noe som har resultert i eksistensen av mange HBB -varianter. Noen av disse mutasjonene er ikke direkte dødelige og gir i stedet motstand mot malaria, spesielt i Afrika hvor malaria er epidemi. Mennesker med afrikansk avstamning har utviklet seg til å ha høyere forekomst av mutant HBB fordi heterozygote individer har en feilformet rød blodcelle som forhindrer angrep fra malariaparasitter. Dermed er HBB-mutanter kildene til positivt utvalg i disse regionene og er viktige for deres langsiktige overlevelse. Slike seleksjonsmarkører er viktige for å spore menneskelige aner og diversifisering fra Afrika .
Se også
Referanser
Videre lesning
- Higgs DR, Vickers MA, Wilkie AO, Pretorius IM, Jarman AP, Weatherall DJ (1989). "En gjennomgang av den molekylære genetikken til den menneskelige alfa-globin-genklyngen" . Blod . 73 (5): 1081–104. doi : 10.1182/blood.V73.5.1081.1081 . PMID 2649166 .
- Giardina B, Messana I, Scatena R, Castagnola M (1995). "De flere funksjonene til hemoglobin". Crit. Rev. Biochem. Mol. Biol . 30 (3): 165–96. doi : 10.3109/10409239509085142 . PMID 7555018 .
- Salzano AM, Carbone V, Pagano L, Buffardi S, De RC, Pucci P (2002). "Hb Vila Real [beta36 (C2) Pro-> His] i Italia: karakterisering av aminosyresubstitusjonen og DNA-mutasjonen". Hemoglobin . 26 (1): 21–31. doi : 10.1081/HEM-120002937 . PMID 11939509 . S2CID 40757080 .
- Frischknecht H, Dutly F (2007). "En 65 bp duplisering/innsetting i ekson II av beta-globin-genet som forårsaker beta0-thalassemi" . Hematologisk . 92 (3): 423–4. doi : 10.3324/haematol.10785 . PMID 17339197 .