Irinotecan - Irinotecan
 | |
 | |
| Kliniske data | |
|---|---|
| Handelsnavn | Camptosar, Campto, Onivyde, andre |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a608043 |
| Lisensdata | |
| graviditet kategori |
|
| Veier administrasjon |
Intravenøs |
| ATC -kode | |
| Lovlig status | |
| Lovlig status | |
| Farmakokinetiske data | |
| Biotilgjengelighet | NA |
| Metabolisme | lever glukuronidering |
| Eliminering halveringstid | 6 til 12 timer |
| Utskillelse | Galle og nyre |
| Identifikatorer | |
| |
| CAS -nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.219.260 |
| Kjemiske og fysiske data | |
| Formel | C 33 H 38 N 4 O 6 |
| Molar masse | 586,689 g · mol −1 |
| 3D -modell ( JSmol ) | |
| |
| |
|
| |
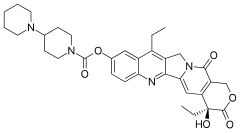
Irinotecan , blant annet solgt under merkenavnet Camptosar , er en medisin som brukes til å behandle tykktarmskreft og småcellet lungekreft . For tykktarmskreft brukes den enten alene eller sammen med fluorouracil . For småcellet lungekreft brukes den sammen med cisplatin . Det gis intravenøst .
Vanlige bivirkninger inkluderer diaré , oppkast , benmargsundertrykkelse , hårtap, kortpustethet og feber. Andre alvorlige bivirkninger inkluderer blodpropp , tarmbetennelse og allergiske reaksjoner . De med to kopier av UGT1A1*28 genvarianten har større risiko for bivirkninger. Bruk under graviditet kan føre til skade på babyen. Irinotecan er en topoisomerasehemmer - det blokkerer topoisomerase 1 -enzymet, noe som resulterer i DNA -skade og celledød .
Irinotecan ble godkjent for medisinsk bruk i USA i 1996. Det er på Verdens helseorganisasjons liste over essensielle medisiner . Den er laget av den naturlige forbindelsen camptothecin som finnes i det kinesiske prydetreet Camptotheca acuminata .
Medisinske bruksområder
Dets viktigste bruk er spesielt i tykktarmskreft i kombinasjon med andre kjemoterapimidler. Dette inkluderer diett FOLFIRI , som består av infusjons 5-fluorouracil , leucovorin og irinotecan. Behandlingen XELIRI består av capecitabin og irinotecan.
Det kan også brukes sammen med fluorouracil og folinsyre for kreft i bukspyttkjertelen etter mislykket startbehandling.
Bivirkninger
De mest signifikante bivirkningene av irinotecan inkluderer diaré, kvalme og oppkast, nøytropeni og feber, infeksjoner i blod eller lunger (sepsis, lungebetennelse), sjokk, dehydrering, nyresvikt og trombocytopeni (lave nivåer av blodplater).
Diaré
Irinotecan-assosiert diaré er alvorlig og klinisk signifikant, noe som noen ganger fører til alvorlig dehydrering som krever sykehusinnleggelse eller intensivavdeling. Denne bivirkningen håndteres med aggressiv bruk av antidiarrhealer som loperamid eller atropin med den første løse tarmbevegelsen.
Immunsuppresjon
Immunsystemet påvirkes negativt av irinotecan. Dette gjenspeiles i - noen ganger dramatisk - lavere hvite blodlegemer i blodet, spesielt nøytrofile . Pasienten kan oppleve nøytropeni (en klinisk signifikant nedgang i nøytrofiler i blodet).
Virkningsmekanismen
Camptothecin, en av de fire viktigste strukturelle klassifikasjonene av plante-avledede kreftfremkallende forbindelser, er et cytotoksisk alkaloid som består av en pentacyklisk ringstruktur som inneholder en pyrrol (3, 4 β) kinolindel, en S-konfigurert laktonform og en karboksylatform. Irinotecan aktiveres ved hydrolyse til SN-38 , en hemmer av topoisomerase I. Dette inaktiveres deretter ved glukuronidering av uridindifosfatglukuronosyltransferase 1A1 ( UGT1A1 ). Inhiberingen av topoisomerase I av den aktive metabolitten SN-38 fører til slutt til inhibering av både DNA-replikasjon og transkripsjon.
Den molekylære virkningen av irinotekan skjer ved å fange en delmengde av topoisomerase -1 -DNA -spaltningskomplekser, de med en guanin +1 i DNA -sekvensen. Ett irinotekanmolekyl stabler mot baseparene som flankerer det topoisomerase-induserte spaltingsstedet og forgifter (inaktiverer) topoisomerase 1-enzymet.
Interaktiv vei
Klikk på gener, proteiner og metabolitter nedenfor for å lenke til respektive artikler.
Farmakokinetikk
Administrasjon
Irinotecan kan administreres ved 30- eller 90-minutters intravenøs infusjon av enten 125 mg / m 2 ukentlig i fire av hver sjette uke eller 350 mg / m 2 hver tredje uke.
Fordeling
Irinotecan er en hydrofil forbindelse med et stort distribusjonsvolum (400 L/m 2 ). Ved fysiologisk pH er irinotecan og dets aktive metabolitt etyl-10-hydroksy-camptothecin (SN-38) tilstede i to pH-avhengige likevektsisoformer; den antitumoraktive laktonringen som hydrolyserte til karboksylatisoformen.
I plasma er flertallet av irinotecan og SN-38 bundet til albumin, noe som stabiliserer laktonformene. I blod er irinotecan og SN-38 bundet til blodplater og røde blodlegemer.
Irinotecan har en lineær farmakokinetikk. Befolkningens farmakokinetiske modeller antok en tre-roms modell for irinotecan og en to-kammers modell for SN-38.
SN-38 har en kort distribusjonshalveringstid (ca. 8 min). Den nådde sin høyeste plasmakonsentrasjon innen 2 timer etter infusjon. SN-38 viser også en andre topp i plasmakonsentrasjonen på grunn av dens enterohepatiske resirkulasjon og frigjøring fra erytrocytter.
Metabolisme
Aktivering av karboksylesteraser og butyrylkolinesteras
Omtrent 2–5% av legemidlet irinotecan hydrolyseres til sin aktive metabolitt SN-38 i leveren av to karboksylesterase-omdannende enzymer (CES1 og CES2) og i plasma av butyrylkolinesterase (hBChE). CES2 har en 12,5 ganger høyere affinitet for irinotecan enn CES1. Mens butyrylkolinesterase har en 6 ganger høyere aktivitet for irinotekan enn CES. Etter konvertering transporteres SN-38 aktivt til leveren av organisk aniontransporterende polypeptid (OATP) 1B1-transportør.
Inaktivering av uridindifosfatglukuronosyltransferaser
SN-38 inaktiveres ved glukuronidering til SN-38G (β-glukuronidkonjugat) av flere uridindifosfatglukuronosyltransferaseenzymer (UGT) i leveren (UGT1A1, UGT1A9) og ekstrahepatisk (UGT1A1, UGT1A7) og UGT1A7, UGT1A7, . Flere UGT -polymorfier påvirker farmakokinetikken til irinotecan, for eksempel kan den reduserte UGT1 -aktiviteten føre til alvorlig toksisitet. Også UGT1A1 -konjugater bilirubin og bilirubinglukuronidering er en annen risikofaktor for økt toksisitet
De-konjugering av β-glukuronidaser
Tarmbakteriene produserte β-glukuronidaser som de-konjugerer SN-38G til SN-38, noe som resulterer i entero-hepatisk resirkulasjon av SN-38.
Metabolisme av cytokrom P450 -enzymer
Irinotecan metaboliseres av intrahepatiske cytokrom P450-enzymer, CYP3A4 og CYP3A5 til inaktive metabolitter APC (7-etyl-10- [4-N- (5-aminopentansyre) -1-piperidino] karbonyloksykamptotecin) og NPC (7-etyl-10- [4-amino-1-piperidino] karbonyloksykamptotecin). NPC kan videre konverteres av CES1 og CES2 i leveren til SN-38. Induksjon eller inhibering av CYP3A -enzymer ved røyking, noen urter og medisiner kan resultere i interaksjoner med irinotecan.
Transport til galle
Irinotecan transporteres til galle av ATP-bindende kassett (ABC) transportproteiner: ABCB1, ABCC1, ABCC2 og ABCG2.
Eliminering
Irinotecans clearance er hovedsakelig galde (66%) og estimert 12–21 L/t/m 2 . Alle metabolitter, unntatt SN-38G, skilles hovedsakelig ut i avføring. Irinotekans eliminasjonshalveringstid ble rapportert mellom 5 til 18 timer. SN-38 halveringstider ble rapportert mellom 6 og 32 timer.
Det er høy (30%) interindividuell variasjon i farmakokinetiske parametere for irinotekan som kan endres av flere faktorer, inkludert alder, kjønn, dose, administreringstidspunkt, leverfunksjon, enzymaktivitet eller hematokritnivåer.
Farmakogenomikk
Irinotecan omdannes av et enzym til sin aktive metabolitt SN-38, som igjen inaktiveres av enzymet UGT1A1 ved glukuronidering.
*28 variantpasienter
Personer med varianter av UGT1A1 kalt TA 7 , også kjent som "*28 -varianten", uttrykker færre UGT1A1 -enzymer i leveren og har ofte Gilberts syndrom . Under cellegift får de effektivt en større dose enn forventet fordi kroppen ikke klarer å rydde irinotekan så raskt som andre. I studier tilsvarer dette høyere forekomst av alvorlig nøytropeni og diaré.
I 2004 ble det utført en klinisk studie som både prospektivt validerte assosiasjonen av varianten *28 med større toksisitet og evnen til genetisk testing for å forutsi denne toksisiteten før cellegiftbehandling.
I 2005 gjorde FDA endringer i merkingen av irinotecan for å legge til anbefalinger om farmakogenomikk , slik at irinotecan -mottakere med en homozygot (begge de to genkopiene) polymorfisme i UGT1A1 -genet, for å være spesifikk, *28 -varianten, bør vurderes for reduserte legemiddeldoser. Irinotecan er et av de første mye brukte kjemoterapimidlene som doseres i henhold til mottakerens genotype.
Samfunn og kultur
Godkjenning
Irinotecan mottok akselerert godkjenning fra US Food and Drug Administration (FDA) i 1996, og full godkjenning i 1998.
Navn
Under utviklingen ble det kjent som CPT-11.
Formuleringer
En liposominnkapslet versjon av irinotecan solgt som Onivyde av Merrimack Pharmaceuticals , ble godkjent av FDA i oktober 2015 for å behandle metastatisk kreft i bukspyttkjertelen . Den ble godkjent for medisinsk bruk i EU i oktober 2016.
Se også
- Etirinotecan pegol , et eksperimentelt derivat av irinotecan med lengre halveringstid i menneskekroppen
Referanser
Videre lesning
- Dean L (2015). "Irinotecan -terapi og UGT1A1 -genotype" . I Pratt VM, McLeod HL, Rubinstein WS, et al. (red.). Sammendrag av medisinsk genetikk . Nasjonalt senter for bioteknologisk informasjon (NCBI). PMID 28520360 . Bokhylle -ID: NBK294473.
Eksterne linker
- "Irinotecan" . Legemiddelinformasjonsportal . US National Library of Medicine.
- "Irinotecan hydroklorid" . Legemiddelinformasjonsportal . US National Library of Medicine.
- Irinotecan Pathway på PharmGKB

