Permanganat - Permanganate

|
|
|
|
| Navn | |
|---|---|
|
Systematisk IUPAC-navn
Permanganat |
|
| Identifikatorer | |
|
3D-modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eiendommer | |
|
MnO- 4 |
|
| Molarmasse | 118,934 g · mol −1 |
| Konjugat syre | Permangansyre |
|
Med mindre annet er angitt, blir data gitt for materialer i standardtilstand (ved 25 ° C, 100 kPa). |
|
| Infoboksreferanser | |
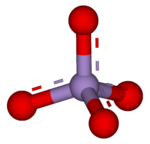
Et permanganat er det generelle navnet på en kjemisk forbindelse som inneholder manganat (VII) ion , ( MnO-
4). Fordi mangan er i +7 oksidasjonstilstand , er permanganat (VII) ion et sterkt oksidasjonsmiddel . Ionen har tetrahedral geometri . Permanganatløsninger er lilla i fargen og er stabile i nøytrale eller svakt alkaliske medier. Den eksakte kjemiske reaksjonen er avhengig av de organiske forurensningene som er tilstede og oksidanten som brukes. For eksempel, trikloretan (C- 2- H 3- Cl 3 ) oksideres ved permanganat-ioner for å danne karbondioksyd (CO 2 ), mangandioksyd (MnO 2 ), hydrogenioner (H + ), og klorioner (Cl - ).
- 8 MnO-
4+ 3 C
2H
3Cl
3→ 6 CO
2+ 8 MnO
2+ H+
+ 4 H
2O + 9 Cl-
I en sur løsning reduseres permanganat (VII) til den blekrosa +2 oksidasjonstilstanden til mangan (II) (Mn 2+ ) ionen.
- 8 H+
+ MnO-
4+ 5 e - → Mn 2+ + 4 H 2 O
I en sterkt basisk løsning reduseres permanganat (VII) til den grønne +6 oksidasjonstilstanden til manganationen , MnO2−
4.
-
MnO-
4+ e - → MnO2−
4
I et nøytralt medium, men det blir redusert til det brune 4 oksidasjonstilstanden av mangandioksyd MnO 2 .
- 2 H 2 O + MnO-
4+ 3 e - → MnO 2 + 4 OH -
Produksjon
Permanganater kan produseres ved oksidasjon av manganforbindelser som manganklorid eller mangansulfat av sterke oksidasjonsmidler, for eksempel natriumhypokloritt eller blydioksid :
- 2 MnCh 2 + 5 NaCIO + 6 NaOH → 2 NaMnO 4 + 9 NaCl + 3 H 2 O
- 2 MnSO 4 + 5 PbO 2 + 3 H 2 SO 4 → 2 HMnO 4 + 5 PbSO 4 + 2 H 2 O
Det kan også produseres ved disproporsjonering av manganater , med mangandioksid som et biprodukt:
- 3 Na 2 MnO 4 + 2 H 2 O → 2 NaMnO 4 + MnO 2 + 4 NaOH
De produseres kommersielt ved elektrolyse eller luftoksidasjon av alkaliske oppløsninger av manganatsalter ( MnO2−
4).
Eiendommer

Permanganater (VII) er salter av permangansyre . De har en dyp lilla farge på grunn av en overføringsladningsovergang . Permanganat (VII) er en sterk oksidasjonsmiddel , og ligner på perklorat . Det er derfor i vanlig bruk i kvalitativ analyse som involverer redoksreaksjoner ( permanganometri ). I følge teorien er permanganat sterkt nok til å oksidere vann, men dette skjer faktisk ikke i noen grad. Foruten dette er det stabilt.
Det er et nyttig reagens , men det er ikke veldig selektivt med organiske forbindelser. Kaliumpermanganat brukes som desinfeksjonsmiddel og tilsetningsmiddel for vannbehandling i havbruk.
Manganater (VII) er ikke veldig stabile termisk. For eksempel nedbrytes kaliumpermanganat ved 230 ° C til kaliummanganat og mangandioksid , og frigjør oksygengass :
- 2 KMnO 4 → K 2 MnO 4 + MnO 2 + O 2
Et permanganat kan oksidere et amin til en nitroforbindelse , en alkohol til et keton , et aldehyd til en karboksylsyre , en terminal alken til en karboksylsyre , oksalsyre til karbondioksid og et alken til en diol . Denne listen er ikke uttømmende.
I alkenoksidasjoner er ett mellomprodukt en syklisk Mn (V) art:
Forbindelser
- Ammoniumpermanganat , NH 4 MnO 4
- Kalsiumpermanganat , Ca (MnO 4 ) 2
- Kaliumpermanganat , KMnO 4
- Natriumpermanganat , NaMnO 4
- Silver permanganat , AgMnO 4
Se også
- Perklorat , et lignende ion med et klor (VII) senter
- Kromat , som er isoelektronisk med permanganat
- Pertechnetate


