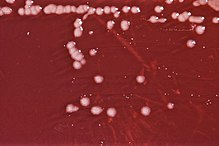
Pseudomonas -Pseudomonas
Pseudomonas er en slekt av gramnegative , Gammaproteobacteria , som tilhører familien Pseudomonadaceae og inneholder 191 gyldig beskrevne arter. Medlemmene av slekten demonstrerer mye metabolsk mangfold og er følgelig i stand til å kolonisere et bredt spekter av nisjer. Deres enkle kultur in vitro og tilgjengeligheten av et økende antall av Pseudomonas- stammen genomsekvenser har gjort slekten en utmerket fokus for vitenskapelig forskning; de best studerte artene inkluderer P. aeruginosa i sin rolle som et opportunistisk menneskelig patogen , plantepatogenet P. syringae , jordbakterien P. putida og plantevekstfremmende P. fluorescens , P. lini , P. migulae , og P. graminis .
På grunn av deres utbredte forekomst i vann og plantefrø, for eksempel dicots , ble pseudomonadene observert tidlig i mikrobiologiens historie . Den generiske navnet Pseudo opprettet for disse organismene ble definert i heller uklare vilkår av Walter Migula i 1894 og 1900 som en slekt av gram-negativ, stavformet, og polar- flagellert bakterier med noen sporedannende arter. Sistnevnte uttalelse ble senere vist seg feil og skyldtes brytningsgranulat av reserve materialer. Til tross for den vage beskrivelsen, viste typearten , Pseudomonas pyocyanea (basonym for Pseudomonas aeruginosa ), seg som den beste deskriptoren.
Klassifiseringshistorie
Som de fleste bakterieslekter levde pseudomonadens siste felles stamfar for hundrevis av millioner år siden. De ble opprinnelig klassifisert på slutten av 1800 -tallet da de først ble identifisert av Walter Migula . Etymologien til navnet ble ikke spesifisert på den tiden og dukket først opp i den syvende utgaven av Bergey's Manual of Systematic Bacteriology ( hovedmyndigheten i bakteriell nomenklatur) som greske pseudes (ψευδής) "falske" og -monas (μονάς/μονάδος) " en enkelt enhet ", som kan bety falsk enhet; Imidlertid mente Migula det muligens som falske Monas , en nanoflagellert protist (senere ble begrepet "monade" brukt i mikrobiologiens tidlige historie for å betegne encellede organismer). Snart ble andre arter som matchet Migulas noe vage opprinnelige beskrivelse isolert fra mange naturlige nisjer, og på den tiden ble mange tildelt slekten . Imidlertid har mange stammer siden blitt omklassifisert, basert på nyere metodikk og bruk av tilnærminger som involverer studier av konservative makromolekyler.
Nylig har 16S rRNA -sekvensanalyse omdefinert taksonomien til mange bakteriearter. Som et resultat inkluderer slekten Pseudomonas stammer som tidligere var klassifisert i slektene Chryseomonas og Flavimonas . Andre stammer som tidligere var klassifisert i slekten Pseudomonas, er nå klassifisert i slektene Burkholderia og Ralstonia .
I 2020 identifiserte en fylogenom analyse av 494 komplette Pseudomonas- genomer to veldefinerte arter ( P. aeruginosa og P. chlororaphis ) og fire bredere fylogenetiske grupper ( P. fluorescens, P. stutzeri, P. syringae, P. putida ) med en tilstrekkelig antall tilgjengelige proteomer. De fire bredere evolusjonære gruppene inkluderer mer enn en art, basert på artsdefinisjonen av gjennomsnittlige nukleotididentitetsnivåer. I tillegg identifiserte den fylogenomiske analysen flere stammer som ble feilmeldt til feil art eller evolusjonsgruppe. Dette feilanotasjonsproblemet har også blitt rapportert av andre analyser.
Genomikk
I 2000 ble den komplette genom -sekvensen til en Pseudomonas -art bestemt; mer nylig har sekvensen av andre stammer blitt bestemt, inkludert P. aeruginosa- stammer PAO1 (2000), P. putida KT2440 (2002), P. protegens Pf-5 (2005), P. syringae pathovar tomat DC3000 (2003), P. syringae pathovar syringae B728a (2005), P. syringae pathovar phaseolica 1448A (2005), P. fluorescens Pf0-1 og P. entomophila L48.
I 2016 hadde mer enn 400 stammer av Pseudomonas blitt sekvensert. Sekvensering av genomene til hundrevis av stammer avslørte svært divergerende arter i slekten. Faktisk deler mange genomer av Pseudomonas bare 50-60% av genene sine, f.eks. P. aeruginosa og P. putida deler bare 2971 proteiner av 5350 (eller ~ 55%).
I 2020 var mer enn 500 komplette Pseudomonas -genomer tilgjengelige i Genebank. En fylogenom analyse benyttet 494 komplette proteomer og identifiserte 297 kjerneortologer, delt av alle stammer. Dette settet med kjerneortologer på slektsnivå ble beriket for proteiner involvert i metabolisme, oversettelse og transkripsjon og ble brukt til å generere et fylogenomisk tre av hele slekten, for å avgrense forholdene mellom de store evolusjonsgruppene i Pseudomonas . I tillegg ble gruppespesifikke kjerneproteiner identifisert for de fleste evolusjonære grupper, noe som betyr at de var til stede i alle medlemmer av den spesifikke gruppen, men fraværende i andre Pseudomonads . For eksempel ble flere P. aeruginosa -spesifikke kjerneproteiner identifisert som er kjent for å spille en viktig rolle i denne artens patogenitet, for eksempel CntL, CntM, PlcB, Acp1, MucE, SrfA, Tse1, Tsi2, Tse3 og EsrC .
Kjennetegn
Medlemmer av slekten viser disse definerende egenskapene:
- Stangformet
- Gram-negativ
- Flagellum en eller flere, som gir bevegelighet
- Aerob
- Dannelse uten sporer
- Katalasepositiv
- Oksidase-positiv
Andre egenskaper som har en tendens til å være assosiert med Pseudomonas- arter (med noen unntak) inkluderer sekresjon av pyoverdin , en fluorescerende gulgrønn siderofor under jernbegrensende forhold. Visse Pseudomonas- arter kan også produsere flere typer av siderofor, slik som pyocyanin av Pseudomonas aeruginosa og thioquinolobactin av Pseudomonas fluorescens ,. Pseudomonas -arter gir også typisk et positivt resultat til oksidasetesten , fravær av gassdannelse fra glukose, glukose oksideres i oksidasjon/gjæringstest ved hjelp av Hugh og Leifson O/F -test, beta -hemolytisk (på blodagar ), indol -negativ , metyl rød negativ, Voges – Proskauer test negativ og sitrat positiv.
Pseudomonas kan være den vanligste kjernemassen for iskrystaller i skyer, og dermed være av største betydning for dannelsen av snø og regn rundt om i verden.
Biofilmdannelse
Alle arter og stammer av Pseudomonas har historisk blitt klassifisert som strenge aerober . Unntak fra denne klassifiseringen har nylig blitt oppdaget i Pseudomonas biofilm . Et betydelig antall celler kan produsere eksopolysakkarider assosiert med dannelse av biofilm. Sekresjon av eksopolysakkarider som alginat gjør det vanskelig for pseudomonader å bli fagocytosert av hvite blodlegemer i pattedyr . Eksopolysakkaridproduksjon bidrar også til overflatekoloniserende biofilmer som er vanskelige å fjerne fra matlagingsflater. Vekst av pseudomonader på ødeleggende matvarer kan generere en "fruktig" lukt.
Antibiotikaresistens
Mest Pseudomonas spp. er naturlig resistente mot penicillin og de fleste relaterte beta-laktam-antibiotika , men en rekke er følsomme for piperacillin , imipenem , ticarcillin eller ciprofloxacin . Aminoglykosider som tobramycin , gentamicin og amikacin er andre valg for behandling.
Denne evnen til å trives under tøffe forhold er et resultat av deres hardføre cellevegger som inneholder poriner . Motstanden mot de fleste antibiotika tilskrives efflux -pumper , som pumper ut noen antibiotika før de er i stand til å virke.
Pseudomonas aeruginosa blir i økende grad anerkjent som et fremvoksende opportunistisk patogen av klinisk relevans. En av de mest bekymringsfulle egenskapene er dens lave antibiotikaresistens. Denne lave følsomheten kan tilskrives en samordnet virkning av flammemedisinske utstrømmingspumper med kromosomalt kodede antibiotikaresistensgener (f.eks. MexAB-oprM , mexXY , etc.) og den lave permeabiliteten til de bakterielle cellekonvoluttene. I tillegg til egen resistensutvikler P. aeruginosa lett ervervet resistens enten ved mutasjon i kromosomalt kodede gener eller ved horisontal genoverføring av antibiotikaresistens determinanter. Utvikling av multiresistens av P. aeruginosa -isolater krever flere forskjellige genetiske hendelser som inkluderer anskaffelse av forskjellige mutasjoner og/eller horisontal overføring av antibiotikaresistensgener. Hypermutasjon favoriserer valg av mutasjonsdrevet antibiotikaresistens i P. aeruginosa- stammer som produserer kroniske infeksjoner, mens gruppering av flere forskjellige antibiotikaresistensgener i integroner favoriserer samordnet oppkjøp av antibiotikaresistens-determinanter. Noen nylige studier har vist fenotypisk resistens assosiert meddannelse av biofilm eller fremveksten av småkoloni-varianter, noe som kan være viktig i responsen fra P. aeruginosa- populasjoner til antibiotikabehandling .
Følsomhet for gallium
Selv om gallium ikke har noen naturlig funksjon i biologien, interagerer galliumioner med cellulære prosesser på en måte som ligner jern (III). Når galliumioner ved en feiltakelse tas opp i stedet for jern (III) av bakterier som Pseudomonas , forstyrrer ionene respirasjonen, og bakteriene dør. Dette skjer fordi jern er redoks-aktivt, noe som tillater overføring av elektroner under respirasjon, mens gallium er redoks-inaktivt.
Patogenitet
Dyrepatogener
Smittsomme arter inkluderer P. aeruginosa , P. oryzihabitans og P. plecoglossicida . P. aeruginosa blomstrer i sykehusmiljøer, og er et spesielt problem i dette miljøet, siden det er den nest vanligste infeksjonen hos sykehusinnlagte pasienter ( nosokomielle infeksjoner ). Denne patogenesen kan delvis skyldes proteinene som utskilles av P. aeruginosa . Bakterien har et bredt spekter av sekresjonssystemer , som eksporterer mange proteiner som er relevante for patogenesen av kliniske stammer. Interessant nok er flere gener involvert i patogenesen av P.aeruginosa, for eksempel CntL, CntM, PlcB, Acp1, MucE, SrfA, Tse1, Tsi2, Tse3 og EsrC kjernegruppespesifikke, noe som betyr at de deles av de aller fleste av P. aeruginosa -stammer, men de er ikke tilstede i andre Pseudomonads .
Plante patogener
P. syringae er et fruktbart plantepatogen . Den eksisterer som over 50 forskjellige patovarer , hvorav mange viser en høy grad av vert-plante-spesifisitet. Mange andre Pseudomonas- arter kan fungere som plantepatogener, særlig alle de andre medlemmene i undergruppen P. syringae , men P. syringae er den mest utbredte og best studerte.
Selv om det ikke strengt tatt er et plantepatogen, kan P. tolaasii være et stort jordbruksproblem, ettersom det kan forårsake bakteriell flekk av dyrket sopp . På samme måte kan P. agarici forårsake dryppende gjell i dyrket sopp.
Bruk som biokontrollmidler
Siden midten av 1980-tallet har visse medlemmer av slekten Pseudomonas blitt påført kornfrø eller påført direkte på jord som en måte å forhindre vekst eller etablering av avlingspatogener. Denne praksisen kalles generelt biokontroll . Biokontrollegenskapene til P. fluorescens og P. protegens- stammer (for eksempel CHA0 eller Pf-5) er for tiden best forstått, selv om det ikke er klart nøyaktig hvordan plantevekstfremmende egenskaper til P. fluorescens oppnås. Teorier inkluderer: bakteriene kan indusere systemisk resistens i vertsplanten, slik at de bedre kan motstå angrep fra et ekte patogen; bakteriene kan utkonkurrere andre (patogene) jordmikrober, f.eks. ved at sideroforer gir et konkurransefortrinn ved å fjerne jern; bakteriene kan produsere forbindelser som er antagonistiske mot andre jordmikrober, slik som fenazintype antibiotika eller hydrogencyanid . Eksperimentelle bevis støtter alle disse teoriene.
Andre kjente Pseudomonas- arter med BIOCONTROL egenskaper omfatter P. chlororaphis , som produserer en fenazin -type antibiotisk aktivt middel mot visse sopp plantepatogener, og de nært beslektede arter P. aurantiaca , som produserer di-2,4-diacetylfluoroglucylmethane, en forbindelse antibiotisk aktive mot Gram-positive organismer.
Bruk som bioremedieringsmiddel
Noen medlemmer av slekten er i stand til å metabolisere kjemiske forurensninger i miljøet, og kan derfor brukes til bioremediering . Bemerkelsesverdige arter demonstrert som egnet for bruk som bioremedieringsmidler inkluderer:
- P. alcaligenes , som kan bryte ned polysykliske aromatiske hydrokarboner .
- P. mendocina , som er i stand til å bryte ned toluen .
- P. pseudoalcaligenes , som er i stand til å bruke cyanid som nitrogenkilde .
- P. resinovorans , som kan nedbryte karbazol .
- P. veronii , som har vist seg å bryte ned en rekke enkle aromatiske organiske forbindelser .
- P. putida , som har evnen til å bryte ned organiske løsningsmidler som toluen . Minst en stamme av denne bakterien er i stand til å omdanne morfin i vandig oppløsning inn i den sterkere og noe kostbart å fremstille medikament hydromorfon (Dilaudid).
- Sil KC av P. stutzeri , som er i stand til å bryte ned karbontetraklorid .
Påvisning av matskader i melk
En måte å identifisere og kategorisere flere bakterielle organismer i en prøve er å bruke ribotyping. Ved ribotyping blir forskjellige lengder av kromosomalt DNA isolert fra prøver som inneholder bakteriearter og fordøyd til fragmenter. Lignende typer fragmenter fra forskjellige organismer visualiseres og lengden deres sammenlignes med hverandre ved Southern blotting eller ved den mye raskere metoden for polymerasekjedereaksjon (PCR) . Fragmenter kan deretter matches med sekvenser som finnes på bakteriearter. Ribotyping er vist å være en metode for å isolere bakterier som kan ødelegges. Rundt 51% av Pseudomonas -bakteriene som finnes i meieriprosesseringsanlegg er P. fluorescens , med 69% av disse isolatene som har proteaser, lipaser og lecitinaser som bidrar til nedbrytning av melkekomponenter og påfølgende ødeleggelse. Andre Pseudomonas -arter kan ha noen av proteasene, lipasene eller lecitinasene, eller ingen i det hele tatt. Lignende enzymatisk aktivitet utføres av Pseudomonas av samme ribotype, med hver ribotype som viser forskjellige grader av ødeleggelse av melk og effekter på smak. Antall bakterier påvirker intensiteten av ødeleggelse, med ikke-enzymatiske Pseudomonas- arter som bidrar til ødeleggelse i høyt antall.
Fordøyelse av mat er skadelig for næringsmiddelindustrien på grunn av produksjon av flyktige forbindelser fra organismer som metaboliserer de ulike næringsstoffene som finnes i matvaren. Forurensning resulterer i helsefare fra produksjon av giftige forbindelser samt ubehagelig lukt og smak. Elektronisk neseteknologi tillater rask og kontinuerlig måling av ødeleggelse av mikrobiell mat ved å kjenne lukt fra disse flyktige stoffene. Elektronisk neseteknologi kan dermed brukes til å oppdage spor av Pseudomonas melkeskader og isolere de ansvarlige Pseudomonas -artene. Gassensoren består av en nesedel laget av 14 modifiserbare polymersensorer som kan detektere spesifikke melkedbrytningsprodukter produsert av mikroorganismer. Sensordata produseres ved endringer i elektrisk motstand for de 14 polymerene når de er i kontakt med målforbindelsen, mens fire sensorparametere kan justeres for å spesifisere responsen ytterligere. Svarene kan deretter forhåndsbehandles av et nevrale nettverk som deretter kan skille mellom melkeskader mikroorganismer som P. fluorescens og P. aureofaciens .
Arter som tidligere er klassifisert i slekten
Nylig omdefinerte 16S rRNA -sekvensanalyse taksonomien til mange bakteriearter som tidligere var klassifisert som å være i slekten Pseudomonas . Arter fjernet fra Pseudomonas er oppført nedenfor; Hvis du klikker på en art, vises den nye klassifiseringen. Begrepet 'pseudomonad' gjelder ikke strengt bare slekten Pseudomonas , og kan brukes til også å inkludere tidligere medlemmer som slektene Burkholderia og Ralstonia .
α Proteobacteria: P. abikonensis , P. aminovorans , P. azotocolligans , P. carboxydohydrogena , P. carboxidovorans , P. compransoris , P. diminuta , P. echinoides , P. extorquens , P. lindneri , P. mesophilica , P. paucimobilis , P. radiora , P. rhodos , P. riboflavina , P. rosea , P. vesicularis .
β proteobakterier: P. acidovorans , P. alliicola , P. antimicrobica , P. avenae , P. butanovorae , P. caryophylli , P. cattleyae , P. cepacia , P. cocovenenans , P. delafieldii , P. facilis , P. flava , P. gladioli , P. glathei , P. glumae , P. graminis , P. huttiensis , P. indigofera , P. lanceolata , P. lemoignei , B. mallei , P. mephitica , P. mixta , P. palleronii , P . fenaziniumsalter , P. pickettii , P. plantarii , P. pseudoflava , B. pseudomallei , P. pyrrocinia , P. rubrilineans , P. rubrisubalbicans , P. saccharophila , P. solanacearum , P. spinosa , P. syzygii , P. taeniospiralis , P. terrigena , P. testosteroni .
γ-β proteobakterier: P. beteli , P. boreopolis , P. cissicola , P. geniculata , P. hibiscicola , P. maltophilia , P. pictorum .
γ proteobakterier: P. beijerinckii , P. diminuta , P. doudoroffii , P. elongata , P. flectens , P. halodurans , P. halophila , P. iners , P. marina , P. nautica , P. nigrifaciens , P. pavonacea , P. piscicida , P. stanieri .
δ proteobakterier: P. formicans .
Bakteriofag
Det er en rekke bakteriofager som infiserer Pseudomonas , f.eks
- Pseudomonas fag Φ6
- Pseudomonas aeruginosa phage EL
- Pseudomonas aeruginosa fag ΦKMV
- Pseudomonas aeruginosa fag LKD16
- Pseudomonas aeruginosa fag LKA1
- Pseudomonas aeruginosa phage LUZ19
- Pseudomonas aeruginosa fag ΦKZ
- Pseudomonas putida phage gh-1
Se også
- Kultursamling for en liste over kultursamlinger