Sinkklorid - Zinc chloride

|
|

|
|
| Navn | |
|---|---|
|
IUPAC navn
Sinkklorid
|
|
| Andre navn
Sink (II) klorid
Sinkdiklorid Smør av sink |
|
| Identifikatorer | |
|
3D -modell ( JSmol )
|
|
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.028.720 |
| EC -nummer | |
|
PubChem CID
|
|
| RTECS -nummer | |
| UNII | |
| FN -nummer | 2331 |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| ZnCl 2 | |
| Molar masse | 136,315 g/mol |
| Utseende | hvit krystallinsk fast hygroskopisk og veldig delikat |
| Lukt | luktfri |
| Tetthet | 2,907 g/cm 3 |
| Smeltepunkt | 290 ° C (554 ° F; 563 K) |
| Kokepunkt | 732 ° C (1.350 ° F; 1.005 K) |
| 432,0 g/ 100 g (25 ° C) | |
| Løselighet | løselig i etanol , glyserol og aceton |
| Løselighet i alkohol | 430,0 g/100 ml |
| −65,0 · 10 −6 cm 3 /mol | |
| Struktur | |
| Tetrahedral , lineær i gassfasen | |
| Farmakologi | |
| B05XA12 ( WHO ) | |
| Farer | |
| Sikkerhetsdatablad | Eksternt HMS -datablad |
|
EU -klassifisering (DSD) (utdatert)
|
Farlig ( Xn ) Etsende ( C ) Miljøfarlig ( N ) |
| R-setninger (utdatert) | R22 , R34 , R50/53 |
| S-setninger (utdatert) | (S1/2) , S26 , S36/37/39 , S45 , S60 , S61 |
| NFPA 704 (brann diamant) | |
| Dødelig dose eller konsentrasjon (LD, LC): | |
|
LD 50 ( median dose )
|
350 mg/kg (rotte, oral) 350 mg/kg (mus, oral) 200 mg/kg (marsvin, oral) 1100 mg/kg (rotte, oral) 1250 mg/kg (mus, oral) |
|
LC 50 ( median konsentrasjon )
|
1260 mg/m 3 (rotte, 30 min) 1180 mg-min/m 3 |
| NIOSH (amerikanske helseeksponeringsgrenser): | |
|
PEL (tillatt)
|
TWA 1 mg/m 3 (røyk) |
|
REL (anbefalt)
|
TWA 1 mg/m 3 ST 2 mg/m 3 (røyk) |
|
IDLH (Umiddelbar fare)
|
50 mg/m 3 (røyk) |
| Relaterte forbindelser | |
|
Andre anioner
|
Sinkfluorid Sinkbromid sinkjodid |
|
Andre kationer
|
Kadmiumklorid Kvikksølv (II) klorid |
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox -referanser | |
Sinkklorid er navnet på kjemiske forbindelser med formelen ZnCl 2 og dets hydrater. Sinkklorider , hvorav ni krystallinske former er kjent, er fargeløse eller hvite og er svært løselige i vann. Dette hvite saltet er hygroskopisk og til og med delikat . Prøver bør derfor beskyttes mot fuktighetskilder, inkludert vanndampen som finnes i luften. Sinkklorid finner bred anvendelse i tekstilbehandling , metallurgiske flukser og kjemisk syntese. Intet mineral med denne kjemiske sammensetningen er kjent bortsett fra det svært sjeldne mineralet simonkolleitt , Zn 5 (OH) 8 Cl 2 · H 2 O.
Struktur og egenskaper
Fire krystallinske former ( polymorfer ) av ZnCl 2 er kjente: α, β, γ, og δ. Hver sak har tetraedriske Zn 2+ sentre.
| Skjema | Symmetri | Pearson -symbol | Gruppe | Nei | a (nm) | b (nm) | c (nm) | Z | ρ (g/cm 3 ) |
|---|---|---|---|---|---|---|---|---|---|
| α | tetragonal | tI12 | I 4 2d | 122 | 0,5398 | 0,5398 | 0,64223 | 4 | 3,00 |
| β | tetragonal | tP6 | P4 2 /nmc | 137 | 0.3696 | 0.3696 | 1.071 | 2 | 3.09 |
| γ | monoklinisk | mP36 | P2 1 /c | 14 | 0,654 | 1.131 | 1.23328 | 12 | 2,98 |
| δ | orthorhombic | oP12 | Pna2 1 | 33 | 0,6125 | 0,6443 | 0,7693 | 4 | 2,98 |
Her er a , b og c gitterkonstanter, Z er antall strukturenheter per celleenhet, og ρ er tettheten beregnet ut fra strukturparametrene.
Den ortorhombiske formen (δ) endres raskt til en av de andre formene ved eksponering for atmosfæren. En mulig forklaring er at OH - ionene som kommer fra det absorberte vannet letter omorganiseringen. Hurtig avkjøling av smeltet ZnCl 2 gir et glass .
Smeltet ZnCl 2 har en høy viskositet ved smeltepunktet og en relativt lav elektrisk ledningsevne, som øker markant med temperaturen. En Raman -spredningsstudie av smelten indikerte tilstedeværelsen av polymere strukturer, og en nøytronspredningsstudie indikerte tilstedeværelsen av tetraedriske {ZnCl 4 } -komplekser.
I gassfasen er ZnCl 2 -molekyler lineære med en bindingslengde på 205 pm.
Hydrater
Fem hydrater av sinkklorid er kjent: ZnCl 2 (H 2 O) n med n = 1, 1,5, 2,5, 3 og 4. tetrahydrat ZnCl 2 (H 2 O) 4 krystalliserer fra vandige oppløsninger av sinkklorid.
Forberedelse og rensing
Vannfri ZnCl 2 kan fremstilles av sink og hydrogenklorid :
- Zn + 2 HCl → ZnCl 2 + H 2
Hydrerte former og vandige oppløsninger kan lett fremstilles på samme måte ved å behandle Zn -metall, sinkkarbonat, sinkoksid og sinksulfid med saltsyre:
- ZnS + 2 HCl + 4 H 2 O → ZnCl 2 (H 2 O) 4 + H 2 S
I motsetning til mange andre elementer, eksisterer sink hovedsakelig i bare en oksidasjonstilstand, 2+, noe som forenkler rensingen av kloridet.
Kommersielle prøver av sinkklorid inneholder vanligvis vann og produkter fra hydrolyse som urenheter. Slike prøver kan renses ved omkrystallisering fra varmt dioksan . Vannfrie prøver kan renses ved sublimering i en strøm av hydrogenkloridgass , etterfulgt av oppvarming av sublimatet til 400 ° C i en strøm av tørr nitrogengass . Til slutt er den enkleste metoden avhengig av behandling av sinkklorid med tionylklorid .
Reaksjoner
Smeltet vannfri ZnCl 2 ved 500–700 ° C løser opp sinkmetall, og ved rask avkjøling av smelten dannes et gult diamagnetisk glass, som Raman -studier indikerer inneholder Zn2+
2 ion.
Et antall salter som inneholder tetrachlorozincate -anionen, Zn Cl2−
4, er kjent. "Caultons reagens", V 2 Cl 3 (thf) 6 Zn 2 Cl 6 er et eksempel på et salt som inneholder Zn 2 Cl2−
6. Forbindelsen Cs 3 ZnCl 5 inneholder tetraedrisk Zn Cl2−
4og Cl - anioner. Ingen forbindelser som inneholder Zn Cl4−
6 ion har blitt karakterisert.
Mens sinkklorid er meget oppløselig i vann, løsninger kan ikke anses å inneholde bare solvatiserte Zn 2+ ioner og Cl - ioner, ZnCI x H 2 O (4 x ) arter er også til stede. Vandige oppløsninger av ZnCl 2 er sure: en 6 M vandig oppløsning har en pH-verdi på 1. surhet av vandige ZnCl 2 oppløsninger i forhold til løsninger av andre Zn 2+ salter er på grunn av dannelsen av den tetraedriske, klor aqua komplekser hvor reduksjonen i koordinasjonstallet fra 6 til 4 reduserer styrken til O -H -bindingene i de oppløste vannmolekylene ytterligere.
I alkaliløsning i nærvær av OH - ion finnes forskjellige sinkhydroksykloridanioner i løsningen, f.eks. Zn (OH) 3 Cl 2− , Zn (OH) 2 Cl2−
2, ZnOH Cl2−
3Og Zn 5 (OH) 8 Cl 2 -H 2 O (simonkolleite) bunnfall.
Når ammoniakk bobles gjennom en løsning av sink-klorid, gjør hydroksyd ikke bunnfallet, istedenfor forbindelser som inneholder kompleksbundet ammoniakk (ammines) er produsert, Zn (NH 3 ) 4- Cl 2 -H 2 O og på konsentrasjonen ZnCl 2 (NH 3 ) 2 . Førstnevnte inneholder Zn (NH 3 ) 6 2+ -ionen, og sistnevnte er molekylær med en forvrengt tetraedral geometri. Arten i vandig oppløsning er undersøkt og viser at Zn (NH 3 ) 4 2+ er hovedarten som er tilstede med Zn (NH 3 ) 3 Cl + også tilstede ved lavere NH 3 : Zn -forhold.
Vandig sinkklorid reagerer med sinkoksid og danner en amorf sement som først ble undersøkt i 1855 av Stanislas Sorel . Sorel fortsatte senere med å undersøke den relaterte magnesiumoksyklorid -sementen , som bærer navnet hans.
Når hydrert sinkklorid oppvarmes, får man en rest av Zn (OH) Cl, f.eks
- ZnCl 2 · 2 H 2 O → ZnCl (OH) + HCI + H 2 O
Forbindelsen ZnCl 2 · Anmeldelse for 1. / 2 HCl-H 2 O, kan fremstilles ved forsiktig utfelling fra en oppløsning av ZnCl 2 surgjort med HCl. Den inneholder en polymer anion (Zn 2 Cl 5 - ) n med balanserende monohydrerte hydroniumioner , H 5 O 2 + ioner.
Dannelsen av svært reaktiv vannfri HCl -gass som dannes ved oppvarming av sinkkloridhydrat er grunnlaget for kvalitative uorganiske flekkprøver.
Bruken av sinkklorid som fluks, noen ganger i en blanding med ammoniumklorid (se også sinkammoniumklorid ), innebærer produksjon av HCl og dets påfølgende reaksjon med overflateoksider. Sinkklorid danner to salter med ammoniumklorid: (NH 4 ) 2 ZnCl 4 og (NH 4 ) 3 ClZnCl 4 , som brytes ned ved oppvarming av frigjørende HCl, akkurat som sinkkloridhydrat gjør. Virkningen av sink-klorid / ammoniumklorid flussmidler, for eksempel i varmforsinking fremgangsmåte gir H 2 gass og ammoniakkdamp.
Cellulose oppløses i vandige oppløsninger av ZnCl 2 , og sink-cellulose komplekser er blitt detektert. Cellulose også oppløses i smeltet ZnCl 2 hydrat og karboksylering og acetyleringen utført på den cellulosepolymer.
Således, selv om mange sinksalter har forskjellige formler og forskjellige krystallstrukturer , oppfører disse saltene seg veldig likt i vandig løsning. For eksempel kan oppløsninger som fremstilles fra et hvilket som helst av de polymorfer av ZnCl 2 , så vel som andre halogenider (bromid, jodid), og sulfatet kan ofte bli anvendt om hverandre for fremstilling av andre sinkforbindelser. Illustrativ er fremstillingen av sinkkarbonat:
applikasjoner
Som en metallurgisk fluks
Sinkklorid reagerer med metalloksider (MO) for å gi derivater av den idealiserte formelen MZnOCl 2 . Denne reaksjonen er relevant for bruken av ZnCl 2 -løsningen som fluss for lodding - den oppløser passiverende oksider og avslører den rene metalloverflaten. Flukser med ZnCl 2 som aktiv ingrediens kalles noen ganger "tinner's fluid".
I organisk syntese
Sinkklorid er en nyttig Lewis -syre i organisk kjemi. Smeltet sinkklorid katalyserer omdannelsen av metanol til heksametylbenzen :
- 15 CH
3OH → C
6(CH
3)
6+ 3 CH
4+ 15 H
2O
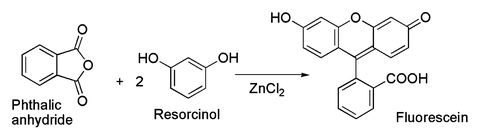
Andre eksempler inkluderer katalysering av (A) Fischer indolsyntesen , og (B) Friedel-Crafts acyleringsreaksjoner som involverer aktiverte aromatiske ringer
I slekt med sistnevnte er det klassiske preparatet av fargestoffet fluorescein fra ftalsyreanhydrid og resorcinol , som involverer en Friedel-Crafts-acylering . Denne transformasjonen er faktisk blitt oppnådd ved anvendelse av til og med den hydratiserte ZnCl 2 eksemplet vist på bildet ovenfor.
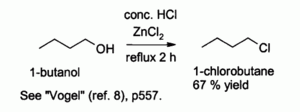
Kombinasjonen av saltsyre og ZnCl 2 , kjent som " Lucas-reagens ", er effektiv for fremstilling av alkyl-klorider fra alkoholer.
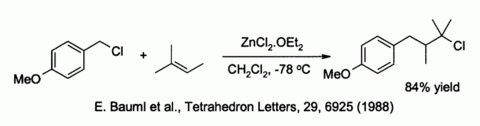
Sinkklorid aktiverer også benzyliske og allyliske halogenider mot substitusjon av svake nukleofiler som alkener :
På lignende måte, ZnCl 2 fremmer selektiv NaBH 3- CN reduksjon av tertiære, allyliske eller benzyliske halogenidene til de tilsvarende hydrokarboner.
Sinkklorid er også et nyttig utgangsreagens for syntese av mange organozinkreagenser , slik som de som brukes i den palladiumkatalyserte Negishi -koblingen med arylhalogenider eller vinylhalogenider . I slike tilfeller blir organosinkforbindelsen vanligvis fremstilt ved transmetallering fra et organolitium eller et Grignard -reagens , for eksempel:
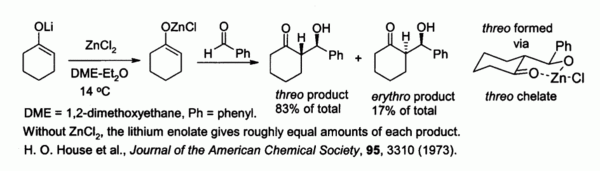
Sink enolater , fremstilt fra alkalimetall-enolater og ZnCl 2 , sørge for styring av stereokjemi i aldolkondensasjon reaksjoner på grunn av chelatering videre til sinken. I det eksempel som er vist nedenfor, den treo ble produktet favorisert over erytro med en faktor på 5: 1 når ZnCl 2 i DME / eter ble benyttet. Chelatet er mer stabil når den voluminøse fenylgruppen er pseudo- ekvatorial i stedet for pseudo- aksiale , dvs. treo snarere enn erythro .
I tekstil- og papirbehandling
Konsentrerte vandige oppløsninger av sinkklorid (mer enn 64% vekt/vekt sinkklorid i vann) har oppløselig stivelse , silke og cellulose .
Relevant for sin affinitet for disse materialene, brukes ZnCl 2 som et brannsikringsmiddel og i stoff "forfriskere" som Febreze. Vulkanisert fiber lages ved å suge papir i konsentrert sinkklorid.
Røykgranater
Den sinkklorid røykblanding ( "HC") som brukes i røykgranater inneholder sinkoksyd , heksakloretan og granulært aluminiumpulver, som, når den antennes, reagerer under dannelse av sink-klorid, karbon og aluminiumoksyd røk, en effektiv røykteppe .
Fingeravtrykksdeteksjon
Ninhydrin reagerer med aminosyrer og aminer for å danne en farget forbindelse "Ruhemanns lilla" (RP). Sprøyting med en sinkkloridoppløsning danner et 1: 1 kompleks RP: ZnCl (H 2 O) 2 , som er lettere gjenkjent som den fluorescerer mer intenst enn RP.
Desinfeksjonsmiddel og trebeskyttelse
Fortynnet vandig sinkklorid ble brukt som desinfeksjonsmiddel under navnet "Burnett's Desinfecting Fluid". Fra 1839 fremmet Sir William Burnett bruken som et desinfeksjonsmiddel så vel som et trebeskyttelsesmiddel. Royal Navy gjennomførte forsøk på bruk som desinfeksjonsmiddel på slutten av 1840 -tallet, inkludert under koleraepidemien i 1849 ; og samtidig ble det utført eksperimenter med konserveringsegenskapene som gjelder for skipsbyggings- og jernbaneindustrien. Burnett hadde noen kommersiell suksess med sin eponymous væske. Etter hans død ble bruken i stor grad erstattet av bruk av karbolsyre og andre proprietære produkter.
Alternativ hudkreftbehandling
Sinkklorid har blitt brukt i alternativ medisin for å forårsake hudskader , skorper av dødt vev, i et forsøk på å kurere hudkreft. Ulike produkter, for eksempel Cansema eller "black salve", som inneholder sinkklorid og selges som kreftkurer, er oppført av US Food and Drug Administration (FDA) som falske med advarselsbrev sendt til leverandører. Ardannelse og hudskade er forbundet med eskarotiske stoffer.
Sikkerhet
Sinkklorid er en kjemisk irritasjon for øyne, hud og luftveier.
Ytterligere lesning
- NN Greenwood, A. Earnshaw, Chemistry of the Elements , 2. utg., Butterworth-Heinemann, Oxford, Storbritannia, 1997.
- Lide, DR, red. (2005). CRC Handbook of Chemistry and Physics (86. utg.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- The Merck Index , 7. utgave, Merck & Co, Rahway, New Jersey, USA, 1960.
- D. Nicholls, Complexes and First-Row Transition Elements , Macmillan Press, London, 1973.
- J. March, Advanced Organic Chemistry , 4. utg., S. 723, Wiley, New York, 1992.
- GJ McGarvey, i Handbook of Reagents for Organic Synthesis, bind 1: Reagents, Auxiliaries and Catalysts for CC Bond Formation , (RM Coates, SE Denmark, red.), S. 220–3, Wiley, New York, 1999.