Piperidin - Piperidine
|
|
|||

|
|||
| Navn | |||
|---|---|---|---|
|
Foretrukket IUPAC -navn
Piperidin |
|||
| Andre navn
Hexahydropyridine
Azacyclohexane Pentamethyleneamine Azinane |
|||
| Identifikatorer | |||
|
3D -modell ( JSmol )
|
|||
| ChEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100.003.467 |
||
| EC -nummer | |||
| KEGG | |||
|
PubChem CID
|
|||
| RTECS -nummer | |||
| UNII | |||
| FN -nummer | 2401 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| C 5 H 11 N | |||
| Molar masse | 85,150 g · mol −1 | ||
| Utseende | Fargeløs væske | ||
| Lukt | Sædlignende, fishy-ammoniacal, skarp | ||
| Tetthet | 0,862 g/ml | ||
| Smeltepunkt | −7 ° C (19 ° F; 266 K) | ||
| Kokepunkt | 106 ° C (223 ° F; 379 K) | ||
| Blandbare | |||
| Surhet (p K a ) | 11.22 | ||
| -64,2 · 10 −6 cm 3 /mol | |||
| Viskositet | 1,573 cP ved 25 ° C | ||
| Farer | |||
| Sikkerhetsdatablad | MSDS1 , MSDS2 | ||
| GHS -piktogrammer |
  
|
||
| GHS Signalord | Fare | ||
| H225 , H311 , H314 , H331 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P260 , P261 , P264 , P271 , P280 , P301+330+331 , P302+352 , P303+361+353 , P304+340 , P305+351+338 , P310 , P311 , P312 , P321 , P322 , P361 , P363 , P370+378 , P403+233 | |||
| NFPA 704 (branndiamant) | |||
| Relaterte forbindelser | |||
|
Relaterte forbindelser
|
Pyridin Pyrrolidine Piperazine Phosphorinane Arsinane |
||
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infobox -referanser | |||
Piperidin er en organisk forbindelse med molekylformelen (CH 2 ) 5 NH. Denne heterocykliske aminen består av en seksleddet ring som inneholder fem metylenbroer (–CH 2- ) og en aminbro (–NH–). Det er en fargeløs væske med en lukt beskrevet som upassende og typisk for aminer . Navnet kommer fra slektsnavnet Piper , som er det latinske ordet for pepper . Selv om piperidin er en vanlig organisk forbindelse, er det best kjent som et representativt strukturelement i mange legemidler og alkaloider , for eksempel naturlig forekommende solenopsiner .
Produksjon
Piperidin ble først rapportert i 1850 av den skotske kjemikeren Thomas Anderson og igjen, uavhengig, i 1852 av den franske kjemikeren Auguste Cahours , som kalte den. Begge oppnådde piperidin ved å reagere piperin med salpetersyre.
Industrielt produseres piperidin ved hydrogenering av pyridin , vanligvis over en molybdendisulfidkatalysator :
- C 5 H 5 N + 3 H 2 → C 5 H 10 NH
Pyridin kan også reduseres til piperidin via en modifisert bjørkreduksjon ved bruk av natrium i etanol .
Naturlig forekomst av piperidin og derivater
Selve piperidin er hentet fra svart pepper , fra Psilocaulon absimile ( Aizoaceae ) og i Petrosimonia monandra .
Piperidin -strukturmotivet er tilstede i mange naturlige alkaloider . Disse inkluderer piperine , som gir svart pepper sin krydret smak. Dette ga forbindelsen sitt navn. Andre eksempler er de brann maur toksinet solenopsin , den nikotin analoge anabasin av tre tobakk ( Nicotiana glauca ), lobelin fra indisk tobakk , og det toksiske alkaloid koniin fra gift hemlock , som ble brukt til å sette Sokrates til døden.
Konfirmasjon
Piperidine foretrekker en stolkonformasjon , som ligner på cykloheksan . I motsetning til cykloheksan har piperidin to forskjellige stolkonformasjoner: den ene med N – H -bindingen i en aksial posisjon , og den andre i en ekvatoriell posisjon. Etter mye kontrovers i løpet av 1950-70 -årene ble ekvatorialkonformasjonen funnet å være mer stabil med 0,72 kcal/mol i gassfasen. I upolare løsningsmidler har et område mellom 0,2 og 0,6 kcal/mol blitt estimert, men i polare løsningsmidler kan den aksiale konformatoren være mer stabil. De to konformerne interkonverterer raskt gjennom nitrogeninversjon ; aktiveringsbarrieren for fri energi for denne prosessen, estimert til 6,1 kcal/mol, er vesentlig lavere enn 10,4 kcal/mol for ringinversjon . Når det gjelder N -metylpiperidin, er den ekvatoriale konformasjonen foretrukket av 3,16 kcal/mol, som er mye større enn preferansen i metylcykloheksan , 1,74 kcal/mol.
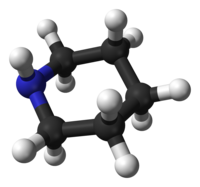 |

|
| aksial konformasjon | ekvatorial konformasjon |
Reaksjoner
Piperidin er en mye brukt for å konvertere ketoner til eminer . Enaminer avledet fra piperidin er substrater i Stork enamin alkyleringsreaksjonen .
Ved behandling med kalsiumhypokloritt , piperidin konvertert til N-klorpiperidin , et kloramin med formelen C 5 H 10 NCl. Det resulterende kloramin gjennomgår dehydrohalogenering for å gi det sykliske iminet.
NMR kjemiske skift
Bruker
Piperidin brukes som løsningsmiddel og som base . Det samme gjelder for visse derivater: N -formylpiperidin er et polart aprotisk løsningsmiddel med bedre hydrokarbonløselighet enn andre amidoppløsningsmidler, og 2,2,6,6 -tetrametylpiperidin er en sterisk sterkt hindret base, nyttig på grunn av lav nukleofilitet og høy løselighet i organiske løsningsmidler .
En betydelig industriell anvendelse av piperidin er for produksjon av dipiperidinyl dithiuram tetrasulfid, som benyttes som en akselerator for den svovelvulkaniseringen av gummi.
Liste over piperidinmedisiner
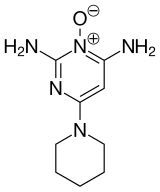
Piperidin og dets derivater er allestedsnærværende byggesteiner i legemidler og finkjemikalier. Piperidinstrukturen finnes i for eksempel:
- Icaridin (insektmiddel)
- SSRI ( selektive serotoninopptakshemmere )
- sentralstimulerende midler og nootropika :
- SERM ( selektive østrogenreseptormodulatorer )
- Vasodilatorer
- Antipsykotiske medisiner:
- Opioider :
-
Arylcykloheksylaminer :
- PCP og analoger
-
antikolinerge kjemiske våpen
- Ditran
- N- Metyl-3-piperidylbenzilat (JB-336, BZ)
Piperidin brukes også ofte i kjemiske nedbrytningsreaksjoner, for eksempel sekvensering av DNA ved spaltning av bestemte modifiserte nukleotider . Piperidin brukes også ofte som en base for avbeskyttelse av Fmoc - aminosyrer som brukes i fastfase -peptidsyntese .
Piperidin er oppført som en tabell II-forløper under FNs konvensjon mot ulovlig trafikk med narkotiske stoffer og psykotrope stoffer på grunn av bruken (toppet på 1970-tallet) i den hemmelige produksjonen av PCP (1- (1-fenylcykloheksyl) piperidin, også kjent som engelstøv, sherms, våt, etc.).
Referanser
Eksterne linker
-
 Media relatert til Piperidine på Wikimedia Commons
Media relatert til Piperidine på Wikimedia Commons



