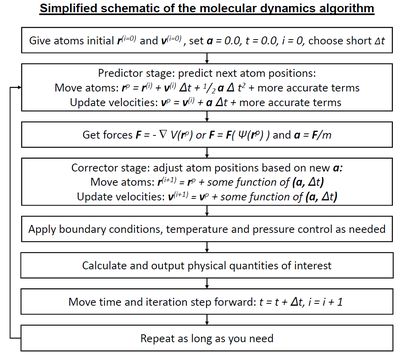
Molekylær dynamikk - Molecular dynamics

Molecular dynamics ( MD ) er en datasimuleringsmetode for å analysere de fysiske bevegelsene til atomer og molekyler . Atomer og molekyler får lov til å samhandle i en bestemt tidsperiode, noe som gir en oversikt over den dynamiske "utviklingen" av systemet. I den vanligste versjonen bestemmes atomer og molekylers baner ved numerisk å løse Newtons bevegelsesligninger for et system av interaktive partikler, hvor krefter mellom partiklene og deres potensielle energier ofte beregnes ved hjelp av interatomiske potensialer eller molekylær mekaniske kraftfelt . Metoden brukes mest i kjemisk fysikk , materialvitenskap og biofysikk .
Fordi molekylære systemer vanligvis består av et stort antall partikler, er det umulig å bestemme egenskapene til slike komplekse systemer analytisk; MD -simulering omgår dette problemet ved å bruke numeriske metoder. Imidlertid er lange MD-simuleringer matematisk dårlige , og genererer kumulative feil i numerisk integrasjon som kan minimeres med riktig valg av algoritmer og parametere, men ikke elimineres helt.
For systemer som følger den ergodiske hypotesen , kan utviklingen av en molekylær dynamikk -simulering brukes til å bestemme makroskopiske termodynamiske egenskaper til systemet: Tidsgjennomsnittene til et ergodisk system tilsvarer mikrokanoniske ensemblet gjennomsnitt. MD har også blitt betegnet som "statistisk mekanikk ved tall" og " Laplaces visjon om newtonsk mekanikk " om å forutsi fremtiden ved å animere naturens krefter og tillate innsikt i molekylær bevegelse på atomskala.
Historie
MD ble opprinnelig utviklet på begynnelsen av 1950 -tallet , etter de tidligere suksessene med Monte Carlo -simuleringer , som selv dateres tilbake til det attende århundre, for eksempel i Buffons nåleproblem , men ble populært for statistisk mekanikk ved Los Alamos National Laboratory av Rosenbluth og Metropolis i det som i dag er kjent som Metropolis - Hastings algoritme . Interessen for tidsutviklingen av N-kroppssystemer dateres mye tidligere til det syttende århundre, som begynte med Newton, og fortsatte inn i det følgende århundre stort sett med fokus på himmelsk mekanikk og spørsmål som solsystemets stabilitet. Mange av de numeriske metodene som ble brukt i dag, ble utviklet i løpet av denne tidsperioden, som er forut for bruk av datamaskiner; for eksempel ble den vanligste integreringsalgoritmen som brukes i dag, Verlet integreringsalgoritme , brukt allerede i 1791 av Jean Baptiste Joseph Delambre . Numeriske beregninger med disse algoritmene kan betraktes som MD "for hånd".
Allerede i 1941 ble integrering av bevegelsesligningene med mange kroppsformer utført med analoge datamaskiner. Noen påtok seg det arbeidskrevende arbeidet med å modellere atombevegelse ved å konstruere fysiske modeller, f.eks. Ved å bruke makroskopiske sfærer. Målet var å ordne dem på en slik måte at de gjengir strukturen til en væske og bruker denne til å undersøke dens oppførsel. JD Bernal sa, i 1962: " ... Jeg tok en rekke gummikuler og stakk dem sammen med stenger i et utvalg av forskjellige lengder fra 2,75 til 4 tommer. Jeg prøvde å gjøre dette i utgangspunktet så tilfeldig som mulig , jobbet på mitt eget kontor, ble avbrutt hvert femte minutt eller så og husket ikke hva jeg hadde gjort før avbruddet. "
Etter oppdagelsen av mikroskopiske partikler og utviklingen av datamaskiner, utvidet interessen seg utover gravitasjonssystemers bevisbare grunn til materiens statistiske egenskaper. I et forsøk på å forstå opprinnelsen til irreversibilitet, foreslo Fermi i 1953, og publiserte i 1955, bruk av MANIAC I , også ved Los Alamos National Laboratory , for å løse tidsutviklingen av bevegelsesligningene for et mangekroppssystemfag til flere valg av maktlover; i dag er dette sentrale verket kjent som Fermi - Pasta - Ulam - Tsingou -problemet . Tidsutviklingen av energien fra det originale verket er vist i figuren til høyre.
I 1957 brukte Alder og Wainwright en IBM 704 -datamaskin for å simulere perfekt elastiske kollisjoner mellom harde sfærer . I 1960, i den kanskje første realistiske simuleringen av materie, sa Gibson et al. simulert strålingsskade av fast kobber ved å bruke en Born – Mayer type frastøtende interaksjon sammen med en sammenhengende overflatekraft. I 1964 publiserte Rahman simuleringer av flytende argon som brukte et Lennard-Jones-potensial ; beregninger av systemegenskaper, for eksempel selvdiffusjonskoeffisienten , sammenlignet godt med eksperimentelle data.
Bruksområder og grenser
MD -metoden ble først brukt i teoretisk fysikk og ble populær innen materialvitenskap like etterpå, og siden 1970 -tallet er den også vanlig innen biokjemi og biofysikk . MD brukes ofte til å foredle tredimensjonale strukturer av proteiner og andre makromolekyler basert på eksperimentelle begrensninger fra røntgenkrystallografi eller NMR-spektroskopi . I fysikk brukes MD for å undersøke dynamikken i fenomener på atomnivå som ikke kan observeres direkte, for eksempel tynnfilmsvekst og ion-subplantasjon, og også for å undersøke de fysiske egenskapene til nanoteknologiske enheter som ikke har eller ikke kan opprettes ennå . I biofysikk og strukturbiologi brukes metoden ofte for å studere bevegelsene til makromolekyler som proteiner og nukleinsyrer , noe som kan være nyttig for å tolke resultatene av visse biofysiske eksperimenter og for å modellere interaksjoner med andre molekyler, som ved ligand -dokking . I prinsippet kan MD brukes til ab initio prediksjon av proteinstruktur ved å simulere folding av polypeptidkjeden fra tilfeldig spole .
Resultatene av MD -simuleringer kan testes gjennom sammenligning med eksperimenter som måler molekylær dynamikk, hvorav en populær metode er NMR -spektroskopi. MD-avledede strukturforutsigelser kan testes gjennom samfunnsdekkende eksperimenter i Critical Assessment of protein Structure Prediction ( CASP ), selv om metoden historisk sett har hatt begrenset suksess på dette området. Michael Levitt , som delte Nobelprisen delvis for anvendelse av MD på proteiner, skrev i 1999 at CASP -deltakere vanligvis ikke brukte metoden på grunn av " ... en sentral forlegenhet for molekylær mekanikk, nemlig at energiminimering eller molekylær dynamikk generelt fører til en modell som er mindre lik den eksperimentelle strukturen. "Forbedringer i beregningsressurser som tillater flere og lengre MD -baner, kombinert med moderne forbedringer i kvaliteten på kraftfeltparametere , har gitt noen forbedringer både i strukturforutsigelse og forfining av homologimodeller , uten nå poenget med praktisk nytteverdi på disse områdene; mange identifiserer kraftfeltparametere som et sentralt område for videre utvikling.
MD -simulering er rapportert for farmakoforutvikling og legemiddeldesign. For eksempel, Pinto et al. implementerte MD-simuleringer av Bcl-Xl-komplekser for å beregne gjennomsnittsposisjoner for kritiske aminosyrer involvert i ligandbinding. På den annen side, Carlson et al. implementert molekylær dynamikk simulering for å identifisere forbindelser som utfyller reseptoren samtidig som de forårsaker minimal forstyrrelse av konformasjonen og fleksibiliteten til det aktive stedet. Øyeblikksbilder av proteinet med konstante tidsintervaller under simuleringen ble lagt over for å identifisere konserverte bindingsområder (konservert i minst tre av elleve rammer) for farmakoforutvikling. Spyrakis et al. stolte på en arbeidsflyt med MD -simuleringer, fingeravtrykk for ligander og proteiner (FLAP) og lineær diskriminering -analyse for å identifisere de beste ligand -proteinkonformasjonene for å fungere som farmakoformaler basert på retrospektiv ROC -analyse av de resulterende farmakoforene. I et forsøk på å forbedre strukturbasert legemiddeloppdagelsesmodellering, overfor behovet for mange modellerte forbindelser, foreslo Hatmal et al. En kombinasjon av MD-simulering og ligand-reseptor intermolekylær kontaktanalyse for å skille mellom kritiske intermolekylære kontakter (bindingsinteraksjoner) fra overflødige i et enkelt ligand -proteinkompleks. Kritiske kontakter kan deretter konverteres til farmakoformodeller som kan brukes til virtuell screening.
Metodens grenser er relatert til parametersettene som brukes, og til de underliggende molekylære mekaniske kraftfeltene. Ett forsøk på en MD -simulering optimaliserer den potensielle energien , i stedet for proteinets frie energi , noe som betyr at alle entropiske bidrag til termodynamisk stabilitet av proteinstrukturen blir neglisjert, inkludert konformasjonsentropien til polypeptidkjeden (hovedfaktoren som destabiliserer proteinstrukturen ) og hydrofobe effekter (de viktigste drivkreftene ved proteinfolding). En annen viktig faktor er intramolekylære hydrogenbindinger , som ikke eksplisitt er inkludert i moderne kraftfelt, men beskrives som Coulomb -interaksjoner av atompunktladninger. Dette er en grov tilnærming fordi hydrogenbindinger har en delvis kvantemekanisk og kjemisk natur. Videre beregnes elektrostatiske interaksjoner vanligvis ved hjelp av vakuumets dielektriske konstant , selv om den omkringliggende vandige løsningen har en mye høyere dielektrisk konstant. Det er tvilsomt å bruke den makroskopiske dielektriske konstanten på korte interatomiske avstander. Til slutt er van der Waals interaksjoner i MD vanligvis beskrevet av Lennard-Jones potensialer basert på Fritz London- teorien som bare er anvendelig i et vakuum. Imidlertid er alle typer van der Waals -krefter til syvende og sist av elektrostatisk opprinnelse og er derfor avhengige av miljøets dielektriske egenskaper . Den direkte målingen av tiltrekningskrefter mellom forskjellige materialer (som Hamaker -konstant ) viser at "samspillet mellom hydrokarboner over vann er omtrent 10% av det på tvers av vakuum". Miljøavhengigheten til van der Waals-krefter blir neglisjert i standardsimuleringer, men kan inkluderes ved å utvikle polariserbare kraftfelt.
Designbegrensninger
Utformingen av en molekylær dynamikk -simulering bør stå for den tilgjengelige beregningskraften. Simuleringsstørrelse ( n = antall partikler), tidssteg og total tidsvarighet må velges slik at beregningen kan fullføres innen en rimelig tidsperiode. Imidlertid bør simuleringene være lange nok til å være relevante for tidsskalaene for de naturlige prosessene som studeres. For å gjøre statistisk gyldige konklusjoner fra simuleringene, bør tidsperioden som simuleres, stemme overens med kinetikken til den naturlige prosessen. Ellers er det analogt med å trekke konklusjoner om hvordan et menneske går når det bare ser på mindre enn ett fotspor. De fleste vitenskapelige publikasjoner om dynamikken i proteiner og DNA bruker data fra simuleringer som spenner over nanosekunder (10 - 9 s) til mikrosekunder (10 - 6 s). For å få disse simuleringene er det nødvendig med flere CPU-dager til CPU-år. Parallelle algoritmer lar lasten fordeles mellom CPUer; et eksempel er den romlige eller kraftige dekomponeringsalgoritmen.
Under en klassisk MD -simulering er den mest CPU -intensive oppgaven evaluering av potensialet som en funksjon av partiklenes interne koordinater. Innenfor denne energivurderingen er den dyreste delen den ikke-limte eller ikke-kovalente delen. I Big O-notasjon skalerer vanlige molekylære dynamikk-simuleringer etter om alle parvise elektrostatiske og van der Waals interaksjoner eksplisitt må redegjøres for. Denne beregningskostnaden kan reduseres ved å bruke elektrostatiske metoder som partikkelmaske Ewald-summering ( ), partikkel-partikkel-partikkel-maske ( P3M ) eller gode sfæriske cutoff-metoder ( ).
En annen faktor som påvirker den totale CPU -tiden som trengs av en simulering, er størrelsen på integrasjonstidspunktet. Dette er tidslengden mellom evalueringer av potensialet. Tidssteget må velges så lite at det ikke er mulig å gjøre diskretiseringsfeil (dvs. mindre enn perioden knyttet til raskeste vibrasjonsfrekvens i systemet). Typiske tidsskritt for klassisk MD er i størrelsesorden 1 femtosekund (10 - 15 s). Denne verdien kan utvides ved å bruke algoritmer som SHAKE -begrensningsalgoritmen , som fikser vibrasjonene til de raskeste atomene (f.eks. Hydrogener) på plass. Det er også utviklet flere tidsskala-metoder, som tillater forlengede tider mellom oppdateringer av langsommere langdistansekrefter.
For å simulere molekyler i et løsningsmiddel, bør det velges mellom eksplisitt og implisitt løsningsmiddel . Eksplisitte løsningsmiddelpartikler (for eksempel TIP3P , SPC/E og SPC-f vannmodellene ) må beregnes dyrt av kraftfeltet, mens implisitte løsningsmidler bruker en middelfeltmetode. Å bruke et eksplisitt løsningsmiddel er beregningsmessig dyrt, og krever å inkludere omtrent ti ganger flere partikler i simuleringen. Men granulariteten og viskositeten til eksplisitt løsningsmiddel er avgjørende for å reprodusere visse egenskaper til de oppløste molekylene. Dette er spesielt viktig for å reprodusere kjemisk kinetikk .
I alle slags molekylær dynamikk simuleringer må størrelsen på simuleringsboksen være stor nok til å unngå artefakter fra grensetilstand . Grenseforhold behandles ofte ved å velge faste verdier i kantene (som kan forårsake artefakter), eller ved å bruke periodiske grensebetingelser der den ene siden av simuleringen går tilbake til motsatt side, etterligner en bulkfase (som også kan forårsake artefakter) .
Mikrokanonisk ensemble (NVE)
I det mikrokanoniske ensemblet er systemet isolert fra endringer i mol (N), volum (V) og energi (E). Det tilsvarer en adiabatisk prosess uten varmeveksling. En mikrokanonisk molekylær dynamikkbane kan sees på som en utveksling av potensiell og kinetisk energi, med total energi som bevares. For et system av N -partikler med koordinater og hastigheter kan følgende par differensialligninger av første orden skrives i Newtons notasjon som
Systemets potensielle energifunksjon er en funksjon av partikkelkoordinatene . Det omtales ganske enkelt som potensialet i fysikk, eller kraftfeltet i kjemi. Den første ligningen kommer fra Newtons bevegelseslover ; kraften som virker på hver partikkel i systemet kan beregnes som den negative gradienten av .
For hvert trinn kan hver partikkels posisjon og hastighet integreres med en symplektisk integratormetode som Verlet -integrasjon . Tidsutviklingen av og kalles en bane. Gitt de opprinnelige posisjonene (f.eks. Fra teoretisk kunnskap) og hastigheter (f.eks. Randomisert Gauss), kan vi beregne alle fremtidige (eller tidligere) posisjoner og hastigheter.
En hyppig kilde til forvirring er betydningen av temperatur i MD. Vanligvis har vi erfaring med makroskopiske temperaturer, som involverer et stort antall partikler. Men temperatur er en statistisk mengde. Hvis det er et stort nok antall atomer, kan statistisk temperatur anslås ut fra den øyeblikkelige temperaturen , som blir funnet ved å likestille systemets kinetiske energi til nk B T /2 hvor n er antall frihetsgrader i systemet.
Et temperaturrelatert fenomen oppstår på grunn av det lille antallet atomer som brukes i MD-simuleringer. Vurder for eksempel å simulere veksten av en kobberfilm som starter med et substrat som inneholder 500 atomer og en avsetningsenergi på 100 eV. I den virkelige verden ville 100 eV fra det avsatte atomet raskt bli transportert gjennom og delt mellom et stort antall atomer ( eller flere) uten noen stor temperaturendring. Når det bare er 500 atomer, fordampes imidlertid substratet nesten umiddelbart av avsetningen. Noe lignende skjer i biofysiske simuleringer. Temperaturen i systemet i NVE økes naturlig når makromolekyler som proteiner gjennomgår eksoterme konformasjonsendringer og binding.
Kanonisk ensemble (NVT)
I det kanoniske ensemblet bevares mengden stoff (N), volum (V) og temperatur (T). Det kalles også noen ganger konstant temperatur molekylær dynamikk (CTMD). I NVT utveksles energien fra endotermiske og eksotermiske prosesser med en termostat.
En rekke termostatalgoritmer er tilgjengelige for å legge til og fjerne energi fra grensene for en MD -simulering på en mer eller mindre realistisk måte, tilnærmet til det kanoniske ensemblet . Populære metoder for å kontrollere temperaturen omfatte hastighet oppskalering, i nese-Hoover termostat , nese-Hoover kjeder, den Berendsen termostat , den Andersen termostaten og Langevin dynamikk . Berendsen -termostaten kan introdusere den flygende isterningseffekten , noe som fører til ufysiske oversettelser og rotasjoner av det simulerte systemet.
Det er ikke trivielt å oppnå en kanonisk ensemblefordeling av konformasjoner og hastigheter ved bruk av disse algoritmene. Hvordan dette avhenger av systemstørrelse, valg av termostat, termostatparametere, tidstrinn og integrator er gjenstand for mange artikler på feltet.
Isotermisk -isobarisk (NPT) ensemble
I det isotermiske - isobare ensemblet bevares mengden stoff (N), trykk (P) og temperatur (T). I tillegg til en termostat er det nødvendig med en barostat. Det tilsvarer nærmest laboratorieforhold med en kolbe åpen for omgivelsestemperatur og trykk.
I simuleringen av biologiske membraner er isotropisk trykkregulering ikke hensiktsmessig. For lipiddobbeltlag skjer trykkontroll under konstant membranareal (NPAT) eller konstant overflatespenning "gamma" (NPγT).
Generaliserte ensembler
Den replika utveksling metoden er en generalisert ensemble. Det ble opprinnelig opprettet for å håndtere den langsomme dynamikken i uordnede spinnsystemer. Det kalles også parallellherding. Replika-utvekslingen MD (REMD) -formuleringen prøver å overvinne multiple-minima-problemet ved å utveksle temperaturen på ikke-interagerende kopier av systemet som kjører ved flere temperaturer.
Potensialer i MD -simuleringer
En molekylær dynamikk -simulering krever definisjon av en potensiell funksjon , eller en beskrivelse av begrepene som partiklene i simuleringen vil samhandle med. I kjemi og biologi blir dette vanligvis referert til som et kraftfelt og i materialfysikk som et interatomisk potensial . Potensialer kan defineres på mange nivåer av fysisk nøyaktighet; de som vanligvis brukes i kjemi er basert på molekylær mekanikk og legemliggjør en klassisk mekanisk behandling av partikkel-partikkel interaksjoner som kan reprodusere strukturelle og konformasjonsmessige endringer, men vanligvis ikke kan reprodusere kjemiske reaksjoner .
Reduksjonen fra en fullstendig kvantebeskrivelse til et klassisk potensial innebærer to hovednæringer. Den første er Born -Oppenheimer -tilnærmingen , som sier at elektronenes dynamikk er så rask at de kan anses å reagere øyeblikkelig på bevegelsen til kjernene deres. Som en konsekvens kan de behandles separat. Den andre behandler kjernene, som er mye tyngre enn elektroner, som punktpartikler som følger klassisk newtonsk dynamikk. I klassisk molekylær dynamikk er effekten av elektronene tilnærmet som en potensiell energioverflate, som vanligvis representerer grunntilstanden.
Når det trengs finere detaljnivåer, brukes potensialer basert på kvantemekanikk ; noen metoder prøver å lage hybrid klassiske/kvantepotensialer der hoveddelen av systemet behandles klassisk, men et lite område blir behandlet som et kvantesystem, vanligvis under en kjemisk transformasjon.
Empiriske potensialer
Empiriske potensialer som brukes i kjemi kalles ofte kraftfelt , mens de som brukes i materialfysikk kalles interatomiske potensialer .
De fleste kraftfeltene i kjemi er empirisk og består av en summering av sammenbundne kreftene som oppstår ved kjemiske bindinger , bindingen vinkler, og bindingen dihedrals , og ikke-bundet kreftene som oppstår ved van der Waals-krefter og elektrostatisk ladning . Empiriske potensialer representerer kvantemekaniske effekter på en begrenset måte gjennom ad hoc funksjonelle tilnærminger. Disse potensialer inneholder frie parametere som atom ladning , van der Waals parametere som reflekterer estimater av atomradius , og likevektsbindingslengden , vinkel, og dieder; disse oppnås ved å passe mot detaljerte elektroniske beregninger (kvantekjemiske simuleringer) eller eksperimentelle fysiske egenskaper som elastiske konstanter , gitterparametere og spektroskopiske målinger.
På grunn av den ikke-lokale naturen til ikke-bundne interaksjoner, involverer de minst svake interaksjoner mellom alle partikler i systemet. Beregningen er normalt flaskehalsen i hastigheten på MD -simuleringer. For å senke beregningskostnaden bruker kraftfelt numeriske tilnærminger som forskyvede avskjæringsradier, reaksjonsfeltalgoritmer , partikkelmaske Ewald-summering eller den nyere partikkel-partikkel-partikkel-masken ( P3M ).
Kjemikraftfelt bruker vanligvis forhåndsinnstilte bindingsordninger (et unntak er ab initio dynamics), og er derfor ikke i stand til å modellere prosessen med kjemisk binding og reaksjoner eksplisitt. På den annen side kan mange av potensialene som brukes i fysikk, for eksempel de som er basert på bindingsordensformalismen, beskrive flere forskjellige koordinasjoner av et system og bindingsbrudd. Eksempler på slike potensialer inkluderer Brenner-potensialet for hydrokarboner og dens videre utvikling for C-Si-H og COH-systemene. Den ReaxFF potensialet kan betraktes som en fullstendig reaktiv hybrid mellom bindingen ordre potensialer og kjemi kraftfelt.
Par potensialer mot mange kroppspotensialer
De potensielle funksjonene som representerer den ikke-bundne energien er formulert som en sum over interaksjoner mellom partiklene i systemet. Det enkleste valget, brukt i mange populære kraftfelt , er "parpotensialet", der den totale potensielle energien kan beregnes ut fra summen av energibidrag mellom par atomer. Derfor kalles disse kraftfeltene også "additive kraftfelt". Et eksempel på et slikt parpotensial er det ikke-bundne Lennard-Jones-potensialet (også kalt 6–12 potensialet), brukt for å beregne van der Waals-krefter.
Et annet eksempel er Born (ionisk) modell av det ioniske gitteret. Den første termen i den neste ligningen er Coulombs lov for et par ioner, den andre termen er den korte avstøtingen som forklares av Paulis eksklusjonsprinsipp, og den siste termen er dispersjon interaksjon. Vanligvis inkluderer en simulering bare det dipolare uttrykket, selv om det noen ganger også er en firepolar -term. Når n l = 6, kalles dette potensialet også Coulomb - Buckingham -potensialet .
I mange kroppspotensialer inkluderer den potensielle energien effekten av tre eller flere partikler som interagerer med hverandre. I simuleringer med parvise potensialer eksisterer det også globale interaksjoner i systemet, men de forekommer bare gjennom parvise termer. I mange kroppspotensialer kan den potensielle energien ikke bli funnet med en sum over atomer, ettersom disse interaksjonene er eksplisitt beregnet som en kombinasjon av overordnede vilkår. I det statistiske synet kan avhengigheten mellom variablene generelt ikke uttrykkes ved bruk av bare parvise produkter av frihetsgrader. For eksempel innebærer Tersoff -potensialet , som opprinnelig ble brukt for å simulere karbon , silisium og germanium , og som siden har blitt brukt til en lang rekke andre materialer, en sum over grupper på tre atomer, med vinklene mellom atomene viktig faktor i potensialet. Andre eksempler er embedded-atom-metoden (EAM), EDIP og TBSMA-potensialene (Tight-Binding Second Moment Approximation), der elektrontettheten til tilstander i et atoms område er beregnet ut fra en sum av bidrag fra omkringliggende atomer , og det potensielle energibidraget er da en funksjon av denne summen.
Semi-empiriske potensialer
Semi-empiriske potensialer benytter matrisepresentasjonen fra kvantemekanikk. Verdiene til matriseelementene finnes imidlertid gjennom empiriske formler som anslår graden av overlapping av spesifikke atomorbitaler. Matrisen blir deretter diagonalisert for å bestemme okkupasjonen av de forskjellige atomorbitalene, og empiriske formler brukes igjen for å bestemme energibidragene til orbitalene.
Det er et bredt utvalg av semi-empiriske potensialer, betegnet tettbindende potensialer, som varierer avhengig av atomer som blir modellert.
Polariserbare potensialer
De fleste klassiske kraftfelt inkluderer implisitt effekten av polariserbarhet , f.eks. Ved å skalere opp de delvise ladningene hentet fra kvantekjemiske beregninger. Disse delladningene er stasjonære med hensyn til atomets masse. Men molekylær dynamikk simuleringer kan eksplisitt modellere polariserbarhet med introduksjon av induserte dipoler gjennom forskjellige metoder, for eksempel Drude -partikler eller svingende ladninger. Dette gir mulighet for en dynamisk omfordeling av ladning mellom atomer som reagerer på det lokale kjemiske miljøet.
I mange år har polariserbare MD -simuleringer blitt spioneringen som neste generasjon. For homogene væsker som vann er det oppnådd økt nøyaktighet gjennom inkludering av polariserbarhet. Noen lovende resultater er også oppnådd for proteiner. Imidlertid er det fortsatt usikkert hvordan man best tilnærmet polariserbarhet i en simulering.
Potensialer i ab initio -metoder
I klassisk molekylær dynamikk er en potensiell energioverflate (vanligvis grunntilstanden) representert i kraftfeltet. Dette er en konsekvens av tilnærmingen Born – Oppenheimer . I eksiterte tilstander, kjemiske reaksjoner eller når det er nødvendig med en mer nøyaktig fremstilling, kan elektronisk oppførsel hentes fra de første prinsippene ved å bruke en kvantemekanisk metode, for eksempel funksjonell teori om tetthet . Dette heter Ab Initio Molecular Dynamics (AIMD). På grunn av kostnaden for å behandle de elektroniske frihetsgrader, er beregningskostnadene for disse simuleringene langt høyere enn klassisk molekylær dynamikk. Dette innebærer at AIMD er begrenset til mindre systemer og kortere tider.
Ab initio kvantemekaniske og kjemiske metoder kan brukes til å beregne den potensielle energien til et system i farten, etter behov for konformasjoner i en bane. Denne beregningen gjøres vanligvis i nærheten av reaksjonskoordinaten . Selv om forskjellige tilnærminger kan brukes, er disse basert på teoretiske hensyn, ikke på empirisk tilpasning. Ab initio -beregninger gir en enorm mengde informasjon som ikke er tilgjengelig fra empiriske metoder, for eksempel tetthet av elektroniske tilstander eller andre elektroniske egenskaper. En betydelig fordel ved å bruke ab initio -metoder er muligheten til å studere reaksjoner som involverer brudd eller dannelse av kovalente bindinger, som tilsvarer flere elektroniske tilstander. Videretillater ab initio- metoder også å gjenopprette effekter utover Born-Oppenheimer-tilnærmingen ved å bruke tilnærminger som blandet kvanteklassisk dynamikk .
Hybrid QM/MM
QM (kvantemekaniske) metoder er veldig kraftige. Imidlertid er de beregningsmessig dyre, mens MM -metodene (klassisk eller molekylær mekanikk) er raske, men lider av flere grenser (krever omfattende parameterisering; oppnådde energianslag er ikke veldig nøyaktige; kan ikke brukes til å simulere reaksjoner der kovalente bindinger brytes/dannes ; og er begrenset i sine evner for å gi nøyaktige detaljer om det kjemiske miljøet). En ny metodeklasse har dukket opp som kombinerer gode poeng med QM (nøyaktighet) og MM (hastighet) beregninger. Disse metodene kalles blandede eller hybrid kvantemekaniske og molekylære mekaniske metoder (hybrid QM/MM).
Den viktigste fordelen med hybrid QM/MM -metode er hastigheten. Kostnaden for å gjøre klassisk molekylær dynamikk (MM) i de mest enkle sakene skalerer O (n 2 ), hvor n er antall atomer i systemet. Dette skyldes hovedsakelig termen for elektrostatiske interaksjoner (hver partikkel interagerer med hver annen partikkel). Imidlertid har bruk av avskjæringsradius, periodiske oppdateringer av parlister og mer nylig variasjonene av partikkelmasket Ewalds (PME) metode redusert dette til mellom O (n) til O (n 2 ). Med andre ord, hvis et system med dobbelt så mange atomer blir simulert, vil det ta mellom to og fire ganger så mye datakraft. På den annen side er de enkleste ab initio -beregningene vanligvis skala O (n 3 ) eller verre (begrensede Hartree - Fock -beregninger har blitt foreslått å skalere ~ O (n 2.7 )). For å overvinne grensen blir en liten del av systemet behandlet kvantemekanisk (typisk aktiv sted for et enzym) og det gjenværende systemet behandles klassisk.
I mer sofistikerte implementeringer eksisterer QM/MM -metoder for å behandle både lette kjerner som er utsatt for kvanteeffekter (for eksempel hydrogen) og elektroniske tilstander. Dette gjør det mulig å generere hydrogenbølgefunksjoner (lik elektroniske bølgefunksjoner). Denne metodikken har vært nyttig for å undersøke fenomener som hydrogentunnel. Et eksempel der QM/MM -metoder har gitt nye funn, er beregning av hydridoverføring i enzymet leveralkoholdehydrogenase . I dette tilfellet er kvantetunneling viktig for hydrogenet, da det bestemmer reaksjonshastigheten.
Grovkornet og reduserte representasjoner
I den andre enden av detaljskalaen er det grovkornede og gittermodeller. I stedet for eksplisitt å representere hvert atom i systemet, bruker man "pseudo-atomer" for å representere grupper av atomer. MD-simuleringer på veldig store systemer kan kreve så store datamaskinressurser at de ikke lett kan studeres med tradisjonelle all-atom-metoder. På samme måte er simuleringer av prosesser på lange tidsskalaer (utover omtrent 1 mikrosekund) uoverkommelig dyre, fordi de krever så mange tidstrinn. I disse tilfellene kan man noen ganger takle problemet ved å bruke reduserte representasjoner, som også kalles grovkornede modeller .
Eksempler på grovkorning (CG) -metoder er diskontinuerlig molekylær dynamikk (CG-DMD) og Go-modeller. Grovkorning gjøres noen ganger ved å ta større pseudo-atomer. Slike forenede atomtilnærminger har blitt brukt i MD -simuleringer av biologiske membraner. Implementering av en slik tilnærming på systemer der elektriske egenskaper er av interesse kan være utfordrende på grunn av vanskeligheten med å bruke en riktig ladningsfordeling på pseudoatomene. De alifatiske halene til lipider representeres av noen få pseudo-atomer ved å samle 2 til 4 metylengrupper i hvert pseudoatom.
Parameteriseringen av disse veldig grovkornede modellene må gjøres empirisk, ved å matche oppførselen til modellen til passende eksperimentelle data eller all-atom-simuleringer. Ideelt sett bør disse parametrene stå for både entalpiske og entropiske bidrag til fri energi på en implisitt måte. Når grovkorning utføres på høyere nivåer, kan nøyaktigheten av den dynamiske beskrivelsen være mindre pålitelig. Men svært grovkornede modeller har blitt brukt med hell for å undersøke et bredt spekter av spørsmål innen strukturbiologi, flytende krystallorganisasjon og polymerglass.
Eksempler på anvendelser av grovkorning:
- proteinfolding og prediksjonsstudier av proteinstruktur utføres ofte ved bruk av ett eller noen få, pseudo-atomer per aminosyre;
- flytende krystallfaseoverganger har blitt undersøkt i begrensede geometrier og/eller under strømning ved bruk av Gay-Berne-potensialet , som beskriver anisotropiske arter;
- Polymerglass under deformasjon har blitt studert ved bruk av enkle harmoniske eller FENE- fjærer for å koble sammen sfærer beskrevet av Lennard-Jones-potensialet ;
- DNA-supercoiling har blitt undersøkt ved hjelp av 1-3 pseudo-atomer per basepar, og med enda lavere oppløsning;
- Emballasje av dobbelt-spiralformet DNA i bakteriofag har blitt undersøkt med modeller der ett pseudoatom representerer en sving (ca. 10 basepar) av den dobbelte spiralen;
- RNA-strukturen i ribosomet og andre store systemer er modellert med ett pseudoatom per nukleotid.
- Virtuell cellesimulering for å studere samspillet mellom celler og forskjellige underlag.
Den enkleste formen for grovkorning er det forenede atomet (noen ganger kalt utvidet atom ) og ble brukt i de fleste tidlige MD-simuleringene av proteiner, lipider og nukleinsyrer. For eksempel, i stedet for å behandle alle fire atomer av en CH- 3- metylgruppe eksplisitt (eller alle tre atomer CH 2 metylengruppe), representerer ett hele gruppen med en pseudo-atom. Den må selvfølgelig parametriseres på riktig måte slik at van der Waals interaksjoner med andre grupper har den riktige avstandsavhengigheten. Lignende hensyn gjelder bindinger, vinkler og vridninger som pseudoatomet deltar i. I denne typen forent atomrepresentasjon eliminerer man vanligvis alle eksplisitte hydrogenatomer bortsett fra de som har evnen til å delta i hydrogenbindinger ( polare hydrogener ). Et eksempel på dette er kraftfeltet CHARMM 19.
De polare hydrogenene beholdes vanligvis i modellen, fordi riktig behandling av hydrogenbindinger krever en rimelig nøyaktig beskrivelse av retningen og de elektrostatiske interaksjonene mellom donor- og akseptorgruppene. En hydroksylgruppe kan for eksempel både være en hydrogenbindingsdonor og en hydrogenbindingsakseptor, og det ville være umulig å behandle dette med ett OH-pseudoatom. Omtrent halvparten av atomene i et protein eller en nukleinsyre er upolare hydrogener, så bruk av forenede atomer kan gi betydelige besparelser i datatiden.
Inkluderer løsningsmiddeleffekter
I mange simuleringer av et løsningsmiddel-løsningsmiddelsystem er hovedfokuset på oppløsningen til løsemiddelet med liten interesse for løsningsmiddelatferden, spesielt i de løsningsmiddelmolekylene som er bosatt i regioner langt fra det oppløste molekylet. Løsningsmidler kan påvirke den dynamiske oppførselen til oppløste stoffer ved tilfeldige kollisjoner og ved å påføre et friksjonsmotstand på oppløsningenes oppløsning gjennom løsningsmidlet. Bruken av ikke-rektangulære periodiske grensebetingelser, stokastiske grenser og løsemiddelskall kan alle bidra til å redusere antall løsemiddelmolekyler som kreves og muliggjøre at en større andel av datatiden brukes i stedet på å simulere oppløsningen. Det er også mulig å inkorporere virkningene av et løsningsmiddel uten å ha noen eksplisitte løsningsmiddelmolekyler til stede. Et eksempel på denne tilnærmingen er å bruke en potensiell middelkraft (PMF) som beskriver hvordan den frie energien endres når en bestemt koordinat varieres. Den frie energiforandringen beskrevet av PMF inneholder gjennomsnittlige effekter av løsningsmidlet.
Langdistanse krefter
En langdistanseinteraksjon er en interaksjon der den romlige interaksjonen ikke faller raskere enn hvor dimensjonaliteten til systemet er. Eksempler inkluderer ladning-ladning-interaksjoner mellom ioner og dipol-dipol-interaksjoner mellom molekyler. Å modellere disse kreftene gir en ganske utfordring, ettersom de er betydelige over en avstand som kan være større enn halve bokslengden med simuleringer av mange tusen partikler. Selv om en løsning ville være å øke størrelsen på bokslengden betydelig, er denne brute force -tilnærmingen mindre enn ideell, ettersom simuleringen vil bli beregningsmessig veldig dyr. Sfærisk avkorting av potensialet er også uaktuelt, da urealistisk oppførsel kan observeres når avstanden er nær avskjæringsavstanden.
Styret molekylær dynamikk (SMD)
Styrte molekylær dynamikk (SMD) simuleringer, eller kraftprobesimuleringer, bruker krefter på et protein for å manipulere strukturen ved å trekke det langs ønskede frihetsgrader. Disse eksperimentene kan brukes til å avsløre strukturelle endringer i et protein på atomnivå. SMD brukes ofte til å simulere hendelser som mekanisk utfoldelse eller strekking.
Det er to typiske protokoller for SMD: en der trekkhastigheten holdes konstant, og en der påført kraft er konstant. Vanligvis er en del av det studerte systemet (f.eks. Et atom i et protein) begrenset av et harmonisk potensial. Krefter påføres deretter spesifikke atomer med enten en konstant hastighet eller en konstant kraft. Paraplyprøvetaking brukes til å flytte systemet langs den ønskede reaksjonskoordinaten ved for eksempel å variere kreftene, avstandene og vinklene som er manipulert i simuleringen. Gjennom paraplyprøvetaking samles alle systemets konfigurasjoner-både høyenergi og lavenergi-tilstrekkelig. Deretter kan hver konfigurasjons endring i fri energi beregnes som potensialet for gjennomsnittlig kraft . En populær metode for å beregne PMF er gjennom den vektede histogramanalysemetoden (WHAM), som analyserer en rekke paraplyprøvesimuleringer.
Mange viktige anvendelser av SMD er innen medisinfunn og biomolekylær vitenskap. For eksempel ble SMD brukt til å undersøke stabiliteten til Alzheimers protofibriller, for å studere proteinligandinteraksjonen i syklinavhengig kinase 5 og til og med for å vise effekten av elektrisk felt på trombin (protein) og aptamer (nukleotid) kompleks blant mange andre interessante studier .
Eksempler på applikasjoner

Molekylær dynamikk brukes på mange vitenskapsområder.
- Den første MD-simuleringen av en forenklet biologisk bretteprosess ble publisert i 1975. Simuleringen som ble publisert i Nature banet vei for det store området med moderne beregningsmessig proteinfolding.
- Den første MD -simuleringen av en biologisk prosess ble publisert i 1976. Simuleringen publisert i Nature banet vei for å forstå proteinbevegelser som viktige i funksjon og ikke bare tilbehør.
- MD er standardmetoden for å behandle kollisjonskaskader i varmespike -regimet, dvs. virkningene som energisk nøytron og ionestråling har på faste stoffer og faste overflater.
Følgende biofysiske eksempler illustrerer bemerkelsesverdig innsats for å produsere simuleringer av systemer av veldig stor størrelse (et komplett virus) eller veldig lange simuleringstider (opptil 1.112 millisekunder):
- MD -simulering av hele satellitt -tobakkmosaikkviruset (STMV) (2006, størrelse: 1 million atomer, simuleringstid: 50 ns, program: NAMD ) Dette viruset er et lite, ikosahedral plantevirus som forverrer symptomene på infeksjon av Tobacco Mosaic Virus (TMV). Molekylær dynamikk simuleringer ble brukt til å undersøke mekanismene for viral samling . Hele STMV -partikkelen består av 60 identiske kopier av ett protein som utgjør det virale kapsidet (belegget), og et 1063 nukleotid enkeltstrenget RNA -genom . Et sentralt funn er at kapsiden er veldig ustabil når det ikke er RNA inne. Simuleringen vil ta en stasjonær datamaskin fra 2006 rundt 35 år å fullføre. Det ble dermed gjort i mange prosessorer parallelt med kontinuerlig kommunikasjon mellom dem.
- Foldingsimuleringer av Villin Headpiece i alle atomdetaljer (2006, størrelse: 20 000 atomer; Simuleringstid: 500 μs = 500 000 ns, Program: Folding@home ) Denne simuleringen ble kjørt i 200 000 CPU-er av deltakende personlige datamaskiner rundt om i verden. Disse datamaskinene hadde Folding@home-programmet installert, en storstilt distribuert databehandlingsinnsats koordinert av Vijay Pande ved Stanford University. De kinetiske egenskapene til Villin Headpiece-proteinet ble undersøkt ved å bruke mange uavhengige, korte baner som ble kjørt av CPU-er uten kontinuerlig sanntidskommunikasjon. En metode som ble brukt var Pfold -verdianalysen, som måler sannsynligheten for folding før utfoldelse av en bestemt startkonformasjon. Pfold gir informasjon om overgangstilstand strukturer og en ordning av konformasjoner langs bretteveien . Hver bane i en Pfold -beregning kan være relativt kort, men mange uavhengige baner er nødvendige.
- Det har blitt utført lange kontinuerlige banesimuleringer på Anton , en massivt parallell superdatamaskin designet og bygget rundt tilpassede applikasjonsspesifikke integrerte kretser (ASIC) og sammenkoblinger av DE Shaw Research . Det lengste publiserte resultatet av en simulering utført ved hjelp av Anton er en 1.112 millisekundersimulering av NTL9 ved 355 K; en andre, uavhengig 1.073 millisekundersimulering av denne konfigurasjonen ble også utført (og mange andre simuleringer av over 250 μs kontinuerlig kjemisk tid). I How Fast-Folding Proteins Fold diskuterer forskerne Kresten Lindorff-Larsen, Stefano Piana, Ron O. Dror og David E. Shaw "resultatene av simuleringer på molekylær dynamikk på atomnivå over perioder på mellom 100 μs og 1 ms, at avsløre et sett med felles prinsipper som ligger til grunn for foldingen av 12 strukturelt forskjellige proteiner. " Undersøkelse av disse mangfoldige lange banene, muliggjort av spesialisert, tilpasset maskinvare, lar dem konkludere med at "I de fleste tilfeller følger folding en enkelt dominerende rute der elementer av den opprinnelige strukturen vises i en rekkefølge som er sterkt korrelert med deres tilbøyelighet til å danne seg i utfoldet tilstand. " I en egen studie ble Anton brukt til å utføre en 1.013 millisekundersimulering av dynamikken i innfødt tilstand av trypsininhibitorer i bukspyttkjertelen (BPTI) ved 300 K.
En annen viktig anvendelse av MD-metoden drar fordel av dens evne til tredimensjonal karakterisering og analyse av mikrostrukturell evolusjon i atomskala.
- MD -simuleringer brukes til å karakterisere kornstørrelsesutviklingen, for eksempel når man beskriver slitasje og friksjon av nanokrystallinske Al- og Al (Zr) materialer. Dislokasjoner evolusjon og kornstørrelse evolusjon analyseres under friksjonsprosessen i denne simuleringen. Siden MD -metoden ga fullstendig informasjon om mikrostrukturen, ble kornstørrelsesutviklingen beregnet i 3D ved bruk av metoden Polyhedral Template Matching, Grain Segmentation og Graph. I en slik simulering ga MD -metoden en nøyaktig måling av kornstørrelse. Ved å bruke denne informasjonen ble de faktiske kornstrukturene ekstrahert, målt og presentert. Sammenlignet med den tradisjonelle metoden for bruk av SEM med en enkelt todimensjonal skive av materialet, gir MD en tredimensjonal og nøyaktig måte å karakterisere den mikrostrukturelle utviklingen på atomskala.
Molekylær dynamikk algoritmer
Integratorer
- Symplektisk integrator
- Verlet - Stoermer integrasjon
- Runge - Kutta integrasjon
- Beemans algoritme
- Begrensningsalgoritmer (for begrensede systemer)
Kortdistanse interaksjonsalgoritmer
- Cellelister
- Verlet liste
- Forbundne interaksjoner
Langdistanse interaksjonsalgoritmer
- Ewald summering
- Partikkelmesh Ewald summasjon (PME)
- Partikkel-partikkel-partikkel-mesh ( P3M )
- Skiftet kraftmetode
Paralleliseringsstrategier
- Nedbrytningsmetode for domener (Distribusjon av systemdata for parallell databehandling )
Ab-initio molekylær dynamikk
Spesialisert maskinvare for MD -simuleringer
- Anton - En spesialisert, massivt parallell superdatamaskin designet for å utføre MD -simuleringer
- MDGRAPE - Et spesialtilpasset system bygget for molekylær dynamikk simuleringer, spesielt forutsigelse av proteinstruktur
Grafikkort som maskinvare for MD -simuleringer
Se også
- Molekylær modellering
- Beregningskjemi
- Kraftfelt (kjemi)
- Sammenligning av kraftfeltimplementeringer
- Monte Carlo -metoden
- Molekylær designprogramvare
- Molekylær mekanikk
- Multiscale Green sin funksjon
- Car – Parrinello -metoden
- Sammenligning av programvare for molekylær mekanikk modellering
- Kvantekjemi
- Diskret elementmetode
- Sammenligning av nukleinsyresimuleringsprogramvare
- Molekylredaktør
- Blandet kvanteklassisk dynamikk
Referanser
Generelle referanser
- MP Allen, DJ Tildesley (1989) Datasimulering av væsker . Oxford University Press. ISBN 0-19-855645-4 .
- JA McCammon, SC Harvey (1987) Dynamics of Proteins and Nucleic Acids . Cambridge University Press. ISBN 0-521-30750-3 (innbundet).
- DC Rapaport (1996) The Art of Molecular Dynamics Simulation . ISBN 0-521-44561-2 .
- M. Griebel ; S. Knapek; G. Zumbusch (2007). Numerisk simulering i molekylær dynamikk . Berlin, Heidelberg: Springer. ISBN 978-3-540-68094-9.
- Frenkel, Daan ; Smit, Berend (2002) [2001]. Forstå molekylær simulering: fra algoritmer til applikasjoner . San Diego: Academic Press. ISBN 978-0-12-267351-1.
- JM Haile (2001) Molecular Dynamics Simulation: Elementary Methods . ISBN 0-471-18439-X
- RJ Sadus, Molecular Simulation of Fluids: Theory, Algorithms and Object-Orientation , 2002, ISBN 0-444-51082-6
- Oren M. Becker, Alexander D. Mackerell, Jr., Benoît Roux, Masakatsu Watanabe (2001) Computational Biochemistry and Biophysics . Marcel Dekker. ISBN 0-8247-0455-X .
- Andrew Leach (2001) Molecular Modeling: Principles and Applications . (2. utgave) Prentice Hall. ISBN 978-0-582-38210-7 .
- Tamar Schlick (2002) Molekylær modellering og simulering . Springer. ISBN 0-387-95404-X .
- William Graham Hoover (1991) Computational Statistical Mechanics , Elsevier, ISBN 0-444-88192-1 .
- DJ Evans og GP Morriss (2008) Statistical Mechanics of Nonequilibrium Liquids , andre utgave, Cambridge University Press, ISBN 978-0-521-85791-8 .
















![U (r) = 4 \ varepsilon \ venstre [\ venstre (\ frac {\ sigma} {r} \ høyre)^{12} - \ venstre (\ frac {\ sigma} {r} \ høyre)^{6} \Ikke sant]](https://wikimedia.org/api/rest_v1/media/math/render/svg/374024e23ac5eb77e91b68ad9ba86ad3bbf5f113)


