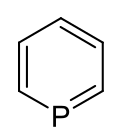
Fosfor - Phosphorine
|
|
|||
| Navn | |||
|---|---|---|---|
|
Foretrukket IUPAC -navn
Fosfinin |
|||
| Andre navn
Fosfabensen
|
|||
| Identifikatorer | |||
|
3D -modell ( JSmol )
|
|||
| ChemSpider | |||
| MeSH | Fosfinin | ||
|
PubChem CID
|
|||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| C 5 H 5 P | |||
| Molar masse | 96,069 g · mol −1 | ||
| Relaterte forbindelser | |||
|
Relaterte -ines
|
Arsabensen |
||
|
Relaterte forbindelser
|
Fosfol | ||
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infobox -referanser | |||
Fosforin ( IUPAC navn: phosphinine ) er en tyngre element analog av pyridin , inneholdende et fosforatom i stedet for en aza- del. Det kalles også fosfabensen og tilhører fosfaalkene -klassen. Det er en fargeløs væske som hovedsakelig er av interesse for forskning.
Fosfor er en luftfølsom olje, men er ellers stabil når den håndteres ved hjelp av luftfrie teknikker (substituerte derivater kan imidlertid ofte håndteres under luft uten risiko for nedbrytning). I kontrast er silabensen , en beslektet tungelementanalog av benzen, ikke bare luft- og fuktighetsfølsom, men også termisk ustabil uten omfattende sterisk beskyttelse.
Historie
Det første fosforet som skal isoleres er 2,4,6-trifenylfosfor. Det ble syntetisert ved Gottfried Märkl i 1966 ved kondensasjon av det tilsvarende pyrylium salt og fosfin eller tilsvarende (P (CH, 2 OH) 3 og P (SiMe 3 ) 3 ).
Det (usubstituerte) foreldrefosforet ble rapportert av Arthur J. Ashe III i 1971. Tilnærminger til ringåpning er utviklet fra fosfoler .
Struktur, binding og egenskaper
Strukturelle studier av elektrondiffraksjon avslører at fosfor er en plan aromatisk forbindelse med 88% av aromatikken til benzen . Potensielt relevant for den høye aromatikken er de godt tilpassede elektronegativitetene til fosfor (2.1) og karbon (2.5). PC -bindingslengden er 173 pm, og CC -bindingslengdene er rundt 140 pm og viser liten variasjon.
Selv om fosfor og pyridin er strukturelt like, er fosforer langt mindre grunnleggende. PKa en 's C 5 H 5 PH + og C 5 H 5 NH + er henholdsvis -16,1 og 5,2. Metyl litium tilfører fosfor i fosfor mens det øker pyridins 2-posisjon.
Fosfor gjennomgår elektrofile substitusjonsreaksjoner som vanlige aromatiske forbindelser: brominering , acylering og så videre.
Koordineringskjemi
Koordineringskomplekser som bærer fosfor som en [ligand] er kjent. Fosforiner kan binde seg til metaller gjennom fosforsenter. Komplekser av diphospha-analogen av 2,2'-bipyridin er kjent. Fosforiner danner også pi -komplekser, illustrert av V (η 6 -C 5 H 5 P) 2 .
Se også
- 6-ledd aromatiske ringer med ett karbon erstattet av en annen gruppe: borabensen , silabensen , germabensen , stannabensen , pyridin , fosfor, arsabensen , stibabensen , bismabensen , pyrylium , tiopyrylium , selenopyrylium , telluropyrylium
Referanser
- Quin, LD (2000). En guide til organofosforkjemi . Wiley-Interscience. ISBN 978-0-471-31824-8.