Proteopati - Proteopathy
| Proteopati | |
|---|---|
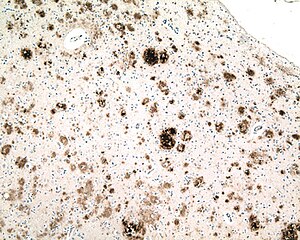 | |
| Mikrograf av en del av hjernebarken fra en person med Alzheimers sykdom , immunfarget med et antistoff mot amyloid beta (brun), et proteinfragment som akkumuleres i senile plakk og cerebral amyloid angiopati . 10X mikroskopobjektiv. |
I medisin , proteopati ( / p r oʊ t jeg ɒ p ə é jeg / ; fra proteo- [ pref . Protein]; -pathy [ suff . Sykdom]; proteopathies pl ;. Proteopathic adj ) refererer til en klasse av sykdommer i som visse proteiner blir strukturelt unormale, og derved forstyrrer funksjonen til celler , vev og organer i kroppen. Ofte klarer ikke proteinene å brette seg inn i sin normale konfigurasjon ; i denne feilfoldede tilstanden kan proteinene bli giftige på en eller annen måte (en giftig funksjonsøkning ) eller de kan miste sin normale funksjon. Proteopatiene (også kjent som proteinopatier , proteinkonformasjonsforstyrrelser eller sykdommer i proteinfeilfolding ) inkluderer sykdommer som Creutzfeldt -Jakobs sykdom og andre prionsykdommer , Alzheimers sykdom , Parkinsons sykdom , amyloidose , multiple systematrofi og et bredt spekter av andre lidelser. Begrepet proteopati ble først foreslått i 2000 av Lary Walker og Harry LeVine.
Begrepet proteopati kan spore sin opprinnelse til midten av 1800-tallet, da Rudolf Virchow i 1854 laget begrepet amyloid ("stivelseslignende") for å beskrive et stoff i cerebral corpora amylacea som utviste en kjemisk reaksjon som lignet på cellulose . I 1859 demonstrerte Friedreich og Kekulé at "amyloid" faktisk er rik på proteiner i stedet for å bestå av cellulose. Senere forskning har vist at mange forskjellige proteiner kan danne amyloid, og at alle amyloider viser dobbeltbrytning i krysspolarisert lys etter farging med fargestoffet Kongorødt , samt en fibrillær ultrastruktur sett med et elektronmikroskop . Noen proteinholdige lesjoner mangler imidlertid dobbeltbrytning og inneholder få eller ingen klassiske amyloidfibriller, for eksempel de diffuse avsetningene av amyloid beta (Aβ) protein i hjernen til mennesker med Alzheimers. Videre har det kommet bevis for at små, ikke-fibrillære proteinaggregater kjent som oligomerer er giftige for cellene i et berørt organ, og at amyloidogene proteiner i deres fibrillære form kan være relativt godartede.
Patofysiologi
I de fleste, om ikke alle proteopatier, øker en endring i tredimensjonal folding (konformasjon) tendensen til et spesifikt protein til å binde seg selv. I denne aggregerte formen er proteinet motstandsdyktig mot klaring og kan forstyrre den normale kapasiteten til de berørte organene. I noen tilfeller resulterer feilfolding av proteinet i tap av sin vanlige funksjon. For eksempel er cystisk fibrose forårsaket av et defekt cystisk fibrose transmembran konduktansregulator (CFTR) protein, og ved amyotrofisk lateral sklerose / frontotemporal lobar degenerasjon (FTLD), samler visse genregulerende proteiner seg uhensiktsmessig i cytoplasmaet, og kan derfor ikke utføre deres normale oppgaver i kjernen. Fordi proteiner deler en felles strukturell egenskap kjent som polypeptid -ryggraden, har alle proteiner potensial til å falle feil under noen omstendigheter. Imidlertid er bare et relativt lite antall proteiner knyttet til proteopatiske lidelser, muligens på grunn av strukturelle særegenheter hos de sårbare proteinene. For eksempel er det mer sannsynlig at proteiner som normalt er utbrettet eller relativt ustabile som monomerer (det vil si som enkle, ubundne proteinmolekyler), vil falle sammen til en unormal konformasjon. I nesten alle tilfeller innebærer den sykdomsfremkallende molekylære konfigurasjonen en økning i beta-arkets sekundære struktur av proteinet. De unormale proteinene i noen proteopatier har vist seg å brette seg inn i flere tredimensjonale former; disse variantene, proteinholdige strukturer er definert av deres forskjellige patogene, biokjemiske og konformasjonelle egenskaper. De har vært mest grundig studert med hensyn til prionsykdom , og blir referert til som protein -stammer .

Sannsynligheten for at proteopati vil utvikle seg er økt med visse risikofaktorer som fremmer selvmontering av et protein. Disse inkluderer destabiliserende endringer i proteinets primære aminosyresekvens, posttranslasjonelle modifikasjoner (for eksempel hyperfosforylering ), endringer i temperatur eller pH , en økning i produksjonen av et protein eller en reduksjon i clearance. Å øke alder er en sterk risikofaktor, det samme er traumatisk hjerneskade. I den aldrende hjernen kan flere proteopatier overlappe hverandre. For eksempel, i tillegg til tauopati og Aβ-amyloidose (som sameksisterer som viktige patologiske trekk ved Alzheimers sykdom), har mange Alzheimer-pasienter samtidig synukleinopati ( Lewy-kropper ) i hjernen.
Det antas at chaperoner og co-chaperones (proteiner som hjelper proteinfolding ) kan motvirke proteotoksisitet under aldring og ved proteinfalsingssykdommer for å opprettholde proteostase .
Frøinduksjon
Noen proteiner kan bli indusert til å danne unormale sammensetninger ved eksponering for det samme (eller lignende) proteinet som har brettet seg til en sykdomsfremkallende konformasjon, en prosess som kalles 'såing' eller 'permissiv templating'. På denne måten kan sykdomstilstanden oppstå i en mottagelig vert ved introduksjon av sykt vevsekstrakt fra en rammet donor. De mest kjente former for induserbar proteopati er prionsykdommer , som kan overføres ved eksponering av en vertsorganisme for renset prionprotein i en sykdomsfremkallende konformasjon. Det er nå bevis på at andre proteopatier kan induseres av en lignende mekanisme, inkludert Aβ -amyloidose, amyloid A (AA) amyloidose og apolipoprotein AII -amyloidose, tauopati, synukleinopati og aggregering av superoksiddismutase -1 (SOD1), polyglutamin og TAR DNA-bindende protein-43 ( TDP-43 ).
I alle disse tilfellene ser det ut til at en avvikende form av selve proteinet er det patogene middelet. I noen tilfeller kan avsetningen av en type proteiner induseres eksperimentelt av aggregerte samlinger av andre proteiner som er rike på β-arkstruktur, muligens på grunn av strukturell komplementaritet av proteinmolekylene. For eksempel kan AA amyloidose bli stimulert på mus av så forskjellige makromolekyler som silke, gjær amyloid Sup35, og curli fibriller fra bakterien Escherichia coli . AII-amyloid kan induseres hos mus av en rekke β-arkrike amyloidfibriller, og cerebral tauopati kan induseres av hjerneekstrakter som er rike på aggregerte Aβ. Det er også eksperimentelle bevis for krysssåing mellom prionprotein og Aβ. Generelt er slik heterolog såing mindre effektiv enn såing med en ødelagt form av det samme proteinet.
Liste over proteopatier
Ledelse
Utviklingen av effektive behandlinger for mange proteopatier har vært utfordrende. Fordi proteopatiene ofte involverer forskjellige proteiner som stammer fra forskjellige kilder, må behandlingsstrategier tilpasses hver lidelse; Imidlertid inkluderer generelle terapeutiske tilnærminger å opprettholde funksjonen til berørte organer, redusere dannelsen av de sykdomsfremkallende proteiner, forhindre at proteinene folder seg sammen og/eller aggregerer, eller fremmer fjerning av dem. For eksempel, ved Alzheimers sykdom, søker forskere etter måter å redusere produksjonen av det sykdomsassosierte proteinet Aβ ved å hemme enzymene som frigjør det fra det opprinnelige proteinet. En annen strategi er å bruke antistoffer for å nøytralisere spesifikke proteiner ved aktiv eller passiv immunisering . I noen proteopatier kan det være gunstig å hemme de toksiske effektene av proteinoligomerer. Amyloid A (AA) amyloidose kan reduseres ved å behandle den inflammatoriske tilstanden som øker mengden av proteinet i blodet (referert til som serumamyloid A eller SAA). Ved immunglobulin lett kjede amyloidose (AL amyloidose) kan cellegift brukes til å senke antallet blodceller som lager det lette kjedeproteinet som danner amyloid i forskjellige kroppsorganer. Transthyretin (TTR) amyloidose (ATTR) skyldes avsetning av feilfoldet TTR i flere organer. Fordi TTR hovedsakelig produseres i leveren , kan TTR -amyloidose bremses i noen arvelige tilfeller ved levertransplantasjon . TTR -amyloidose kan også behandles ved å stabilisere de normale sammensetningene av proteinet (kalt tetramerer fordi de består av fire TTR -molekyler bundet sammen). Stabilisering forhindrer at individuelle TTR -molekyler rømmer, folder seg sammen og samler seg til amyloid.
Flere andre behandlingsstrategier for proteopatier blir undersøkt, inkludert små molekyler og biologiske medisiner som små interfererende RNA , antisense oligonukleotider , peptider og konstruerte immunceller . I noen tilfeller kan flere terapeutiske midler kombineres for å forbedre effektiviteten.

