Rotavirus -Rotavirus
| Rotavirus | |
|---|---|
|
|
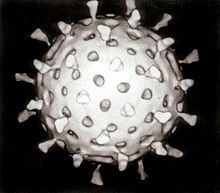
| Dataassistert rekonstruksjon av et rotavirus basert på flere elektronmikrografer | |
|
Virusklassifisering |
|
| (urangert): | Virus |
| Rike : | Riboviria |
| Kongedømme: | Orthornavirae |
| Phylum: | Duplornaviricota |
| Klasse: | Resentoviricetes |
| Rekkefølge: | Reovirales |
| Familie: | Reoviridae |
| Underfamilie: | Sedoreovirinae |
| Slekt: | Rotavirus |
| Arter | |
|
|
Rotavirus er en slekt av dobbelttrådet RNA-virus i familien Reoviridae . Rotavirus er den vanligste årsaken til diarésykdom blant spedbarn og små barn. Nesten hvert eneste barn i verden er smittet med et rotavirus minst én gang i en alder av fem. Immunitet utvikler seg med hver infeksjon, så påfølgende infeksjoner er mindre alvorlige. Voksne rammes sjelden. Det er ni arter av slekten, referert til som A, B, C, D, F, G, H, I og J. Rotavirus A , den vanligste arten, forårsaker mer enn 90 % av rotavirusinfeksjonene hos mennesker.
Viruset overføres via fekal-oral vei . Det infiserer og skader cellene i tynntarmen og forårsaker gastroenteritt (som ofte kalles "mageinfluensa" til tross for at det ikke har noe forhold til influensa ). Selv om rotavirus ble oppdaget i 1973 av Ruth Bishop og hennes kolleger ved hjelp av elektronmikrofotografier og står for omtrent en tredjedel av sykehusinnleggelsene for alvorlig diaré hos spedbarn og barn, har dets betydning historisk blitt undervurdert i folkehelsesamfunnet , spesielt i utviklingsland . I tillegg til innvirkningen på menneskers helse, infiserer rotavirus også andre dyr, og er et patogen for husdyr.
Rotaviral enteritt er vanligvis en lettbehandlet barnesykdom, men blant barn under 5 år forårsaket rotavirus anslagsvis 151 714 dødsfall fra diaré i 2019. I USA, før oppstart av rotavirusvaksinasjonsprogrammet på 2000-tallet, forårsaket rotavirus ca. 2,7 millioner tilfeller av alvorlig gastroenteritt hos barn, nesten 60 000 sykehusinnleggelser og rundt 37 dødsfall hvert år. Etter introduksjon av rotavirusvaksine i USA, har sykehusinnleggelsesratene falt betydelig. Folkehelsekampanjer for å bekjempe rotavirus fokuserer på å gi oral rehydreringsterapi til infiserte barn og vaksinasjon for å forhindre sykdommen. Forekomsten og alvorlighetsgraden av rotavirusinfeksjoner har gått betydelig ned i land som har lagt til rotavirusvaksine i deres rutinemessige barnevaksinasjonspolitikk .
Virologi
Typer rotavirus
Det er ni arter av rotavirus, referert til som A, B, C, D, F, G, H, I og J. Mennesker er primært infisert av arten rotavirus A . A–I arter forårsaker sykdom hos andre dyr, art H hos griser, D, F og G hos fugler, I hos katter og J hos flaggermus.
Innen rotavirus A er det forskjellige stammer, kalt serotyper . Som med influensavirus , brukes et dobbelt klassifiseringssystem basert på to proteiner på overflaten av viruset. Glykoproteinet VP7 definerer G-serotypene og det proteasesensitive proteinet VP4 definerer P-serotyper. Fordi de to genene som bestemmer G-typer og P-typer kan overføres separat til avkomsvirus, finner man forskjellige kombinasjoner. Det er etablert et helt genom-genotypingssystem for rotavirus A , som har blitt brukt til å bestemme opprinnelsen til atypiske stammer. Prevalensen av de enkelte G-typene og P-typene varierer mellom, og innenfor, land og år. Det er minst 36 G-typer og 51 P-typer, men ved infeksjoner hos mennesker er det bare noen få kombinasjoner av G- og P-typer som dominerer. De er G1P[8], G2P[4], G3P[8], G4P[8], G9P[8] og G12P[8].
Struktur
Genomet til rotavirus består av 11 unike doble helix-molekyler av RNA ( dsRNA) som er 18 555 nukleotider totalt. Hver helix, eller segment, er et gen , nummerert 1 til 11 ved avtagende størrelse. Hvert gen koder for ett protein , bortsett fra gener 9, som koder for to. RNA er omgitt av en tre- lags ikosaedrisk proteinkapsid . Virale partikler er opptil 76,5 nm i diameter og er ikke innhyllet .
Proteiner
Det er seks virale proteiner (VP-er) som danner viruspartikkelen ( virion ). Disse strukturelle proteinene kalles VP1, VP2, VP3, VP4, VP6 og VP7. I tillegg til VP-ene er det seks ikke-strukturelle proteiner ( NSPs ), som bare produseres i celler infisert av rotavirus. Disse kalles NSP1 , NSP2 , NSP3 , NSP4 , NSP5 og NSP6 .
Minst seks av de tolv proteinene som er kodet av rotavirusgenomet, binder RNA . Rollen til disse proteinene i rotavirusreplikasjon er ikke helt forstått; deres funksjoner antas å være relatert til RNA-syntese og pakking i virion, mRNA-transport til stedet for genomreplikasjon og mRNA -translasjon og regulering av genuttrykk.
Strukturelle proteiner
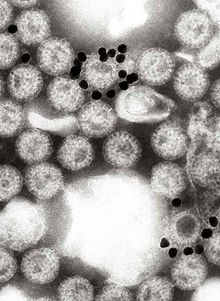
VP1 er lokalisert i kjernen av viruspartikkelen og er et RNA-avhengig RNA- polymeraseenzym . I en infisert celle produserer dette enzymet mRNA-transkripter for syntese av virale proteiner og produserer kopier av rotavirusgenomets RNA-segmenter for nyproduserte viruspartikler.
VP2 danner kjernelaget til virionet og binder RNA-genomet.
VP3 er en del av den indre kjernen av virion og er et enzym som kalles guanylyltransferase . Dette er et avdekningsenzym som katalyserer dannelsen av 5' -hetten i den post-transkripsjonelle modifikasjonen av mRNA. Hetten stabiliserer viralt mRNA ved å beskytte det mot nukleinsyrenedbrytende enzymer kalt nukleaser .
VP4 er på overflaten av virionet som stikker ut som en pigg. Det binder seg til molekyler på overflaten av celler som kalles reseptorer og driver virusets inntreden i cellen. VP4 må modifiseres av proteaseenzymet trypsin , som finnes i tarmen, til VP5* og VP8* før viruset er smittsomt. VP4 bestemmer hvor virulent viruset er, og det bestemmer P-typen til viruset. Hos mennesker er det en assosiasjon mellom blodgruppen ( Lewis antigensystem , ABO blodgruppesystem og sekretorstatus ) og mottakelighet for infeksjon. Ikke-sekretorer virker resistente mot infeksjon av typene P[4] og P[8], noe som indikerer at blodgruppeantigener er reseptorene for disse genotypene. Denne resistensen er avhengig av rotavirusgenotypen.
VP6 utgjør hoveddelen av kapsiden. Det er svært antigent og kan brukes til å identifisere rotavirusarter. Dette proteinet brukes i laboratorietester for rotavirus A-infeksjoner.
VP7 er et glykoprotein som danner den ytre overflaten av virion. Bortsett fra dens strukturelle funksjoner, bestemmer den G-typen til stammen og er sammen med VP4 involvert i immunitet mot infeksjon.
Ikke-strukturelle virale proteiner
NSP1, produktet av gen 5, er et ikke- strukturelt RNA-bindende protein. NSP1 blokkerer også interferonresponsen , den delen av det medfødte immunsystemet som beskytter cellene mot virusinfeksjon. NSP1 får proteosomet til å bryte ned nøkkelsignalkomponenter som kreves for å stimulere produksjonen av interferon i en infisert celle og reagere på interferon som skilles ut av tilstøtende celler.
Mål for nedbrytning inkluderer flere IRF -transkripsjonsfaktorer som kreves for interferon-gentranskripsjon.
NSP2 er et RNA-bindende protein som akkumuleres i cytoplasmatiske inneslutninger ( viroplasmer ) og er nødvendig for genomreplikasjon.
NSP3 er bundet til virale mRNA-er i infiserte celler og er ansvarlig for nedstengning av cellulær proteinsyntese. NSP3 inaktiverer to translasjonsinitieringsfaktorer som er essensielle for syntese av proteiner fra verts-mRNA.
Først sender NSP3 ut poly(A)-bindende protein (PABP) fra translasjonsinitieringsfaktoren eIF4F . PABP er nødvendig for effektiv oversettelse av transkripsjoner med en 3' poly(A) hale , som finnes på de fleste vertscelletranskripsjoner. For det andre inaktiverer NSP3 eIF2 ved å stimulere fosforyleringen. Effektiv translasjon av rotavirus-mRNA, som mangler 3'-poly(A)-halen, krever ingen av disse faktorene.
NSP4 er et viralt enterotoksin som induserer diaré og var det første virale enterotoksinet som ble oppdaget. Det er et viroporin som øker cytosolisk Ca2+ i pattedyrceller.
NSP5 er kodet av genomsegment 11 av rotavirus A. I virusinfiserte celler akkumuleres NSP5 i viroplasmaet.
NSP6 er et nukleinsyrebindende protein og er kodet av gen 11 fra en åpen leseramme som ikke er i fase .
| RNA-segment (gen) | Størrelse ( basepar ) | Protein | UniProt | Molekylvekt kDa | plassering | Kopier per partikkel | Funksjon |
|---|---|---|---|---|---|---|---|
| 1 | 3302 | VP1 | P22678 | 125 | Ved hjørnene av kjernen | 12 | RNA-avhengig RNA-polymerase |
| 2 | 2690 | VP2 | A2T3R5 | 102 | Danner indre skall av kjernen | 120 | RNA-binding |
| 3 | 2591 | VP3 | A2T3S5 | 88 | Ved hjørnene av kjernen | 12 | metyltransferase-mRNA-avgrensningsenzym |
| 4 | 2362 | VP4 | A2T3T2 | 87 | Overflatepigg | 180 | Cellefeste, virulens |
| 5 | 1611 | NSP1 | Q99FX5 | 59 | Ikke-strukturelt | 0 | 5'RNA-binding, interferonantagonist |
| 6 | 1356 | VP6 | Q6LE89 | 45 | Indre kapsid | 780 | Strukturelt og artsspesifikt antigen |
| 7 | 1104 | NSP3 | P03536 | 37 | Ikke-strukturelt | 0 | Forbedrer viral mRNA-aktivitet og stenger cellulær proteinsyntese |
| 8 | 1059 | NSP2 | A2T3P0 | 35 | Ikke-strukturelt | 0 | NTPase involvert i RNA-emballasje |
| 9 | 1062 | VP7 1 VP7 2 | P03533 | 38 og 34 | Flate | 780 | Strukturelt og nøytraliserende antigen |
| 10 | 751 | NSP4 | P04512 | 20 | Ikke-strukturelt | 0 | Viroporin ( enterotoksin ) |
| 11 | 667 | NSP5 NSP6 | A2T3Q9 P11203 | 22 | Ikke-strukturelt | 0 | ssRNA og dsRNA bindingsmodulator av NSP2 , fosfoprotein |
Denne tabellen er basert på simian rotavirus-stammen SA11. RNA-proteinkodingsoppgaver er forskjellige i noen stammer.
Replikering

- Festing av viruset til vertscellene, som formidles av VP4 og VP7
- Penetrering av cellen av viruset og avbelegg av viruskapsid
- Syntese av plusstråd ssRNA (dette fungerer som mRNA) syntese, som formidles av VP1, VP3 og VP2
- Dannelse av viroplasma, viral RNA-emballasje og minusstreng RNA-syntese og dannelse av dobbeltlags viruspartikler
- Viruspartikkelmodning og frigjøring av avkomsvirioner
Tilknytningen av viruset til vertscellen initieres av VP4, som fester seg til molekyler, kalt glykaner , på overflaten av cellen. Viruset kommer inn i cellene ved reseptormediert endocytose og danner en vesikkel kjent som et endosom . Proteiner i det tredje laget (VP7 og VP4 spike) forstyrrer membranen til endosomet, og skaper en forskjell i kalsiumkonsentrasjonen . Dette forårsaker nedbrytning av VP7 - trimerer til enkeltproteinunderenheter, og etterlater VP2- og VP6-proteinkappene rundt det virale dsRNA-et, og danner en dobbeltlagspartikkel (DLP).
De elleve dsRNA-trådene forblir innenfor beskyttelsen av de to proteinskallene, og den virale RNA-avhengige RNA-polymerasen skaper mRNA-transkripter av det dobbelttrådete virale genomet. Ved å forbli i kjernen, unngår det virale RNA medfødt vertsimmunrespons inkludert RNA-interferens som utløses av tilstedeværelsen av dobbelttrådet RNA.
Under infeksjonen produserer rotavirus mRNA for både proteinbiosyntese og genreplikasjon. De fleste av rotavirusproteinene akkumuleres i viroplasma, der RNA replikeres og DLP-ene settes sammen. I viroplasmaet er de positive sens virale RNA-ene som brukes som maler for syntesen av viralt genomisk dsRNA, beskyttet mot siRNA -indusert RNase-nedbrytning. Viroplasma dannes rundt cellekjernen så tidlig som to timer etter virusinfeksjon, og består av virale fabrikker som antas å være laget av to virale ikke-strukturelle proteiner: NSP5 og NSP2. Hemming av NSP5 ved RNA-interferens in vitro resulterer i en kraftig reduksjon i rotavirusreplikasjon. DLP-ene migrerer til det endoplasmatiske retikulum hvor de får sitt tredje ytre lag (dannet av VP7 og VP4). Avkomsvirusene frigjøres fra cellen ved lysis .
Overføring

Rotavirus overføres via fekal-oral vei , via kontakt med kontaminerte hender, overflater og gjenstander, og muligens via luftveiene. Viral diaré er svært smittsomt. Avføringen til en smittet person kan inneholde mer enn 10 billioner smittsomme partikler per gram; færre enn 100 av disse er nødvendige for å overføre smitte til en annen person.
Rotavirus er stabile i miljøet og har blitt funnet i elvemunningsprøver i nivåer opp til 1–5 smittsomme partikler per US gallon. Virusene overlever mellom 9 og 19 dager. Sanitære tiltak som er tilstrekkelige for å eliminere bakterier og parasitter ser ut til å være ineffektive i kontroll av rotavirus, ettersom forekomsten av rotavirusinfeksjon i land med høye og lave helsestandarder er lik.
Tegn og symptomer
Rotaviral enteritt er en mild til alvorlig sykdom preget av kvalme , oppkast , vannaktig diaré og lavgradig feber . Når et barn er infisert av viruset, er det en inkubasjonsperiode på omtrent to dager før symptomene vises. Sykdomsperioden er akutt. Symptomer starter ofte med oppkast etterfulgt av fire til åtte dager med kraftig diaré. Dehydrering er mer vanlig ved rotavirusinfeksjon enn hos de fleste forårsaket av bakterielle patogener, og er den vanligste dødsårsaken relatert til rotavirusinfeksjon.
Rotavirus A -infeksjoner kan forekomme gjennom hele livet: den første gir vanligvis symptomer , men påfølgende infeksjoner er vanligvis milde eller asymptomatiske , da immunsystemet gir en viss beskyttelse. Følgelig er symptomatiske infeksjonsrater høyest hos barn under to år og avtar gradvis mot 45 år. De mest alvorlige symptomene har en tendens til å oppstå hos barn i alderen seks måneder til to år, eldre og de med immunsvikt . På grunn av immunitet oppnådd i barndommen, er de fleste voksne ikke mottakelige for rotavirus; gastroenteritt hos voksne har vanligvis en annen årsak enn rotavirus, men asymptomatiske infeksjoner hos voksne kan opprettholde overføring av infeksjon i samfunnet. Det er noen bevis som tyder på at blodgruppe kan påvirke følsomheten for infeksjon med rotavirus.
Sykdomsmekanismer
Rotavirus replikerer hovedsakelig i tarmen , og infiserer enterocytter i villi i tynntarmen , noe som fører til strukturelle og funksjonelle endringer av epitelet . Det er bevis hos mennesker, og spesielt i dyremodeller, for ekstraintestinal spredning av smittsomt virus til andre organer og makrofager.
Diaréen er forårsaket av flere aktiviteter av viruset. Malabsorpsjon oppstår på grunn av ødeleggelse av tarmceller kalt enterocytter . Det toksiske rotavirusproteinet NSP4 induserer alders- og kalsiumioneavhengig kloridsekresjon , forstyrrer SGLT1 (natrium/glukose cotransporter 2) transportør - mediert reabsorpsjon av vann, reduserer tilsynelatende aktiviteten til børstegrense membran disakkaridaser , og aktiverer den kalsiumionavhengige sekretoren . reflekser i det enteriske nervesystemet . De forhøyede konsentrasjonene av kalsiumioner i cytosolen (som er nødvendig for sammensetningen av avkomsvirusene) oppnås ved at NSP4 fungerer som et viroporin . Denne økningen i kalsiumioner fører til autofagi (selvdestruksjon) av de infiserte enterocyttene.
NSP4 utskilles også. Denne ekstracellulære formen, som er modifisert av proteaseenzymer i tarmen, er et enterotoksin som virker på uinfiserte celler via integrinreseptorer , som igjen forårsaker og øker intracellulære kalsiumionkonsentrasjoner, sekretorisk diaré og autofagi.
Oppkastet, som er karakteristisk for rotaviral enteritt, er forårsaket av viruset som infiserer enterokromaffincellene på slimhinnen i fordøyelseskanalen. Infeksjonen stimulerer produksjonen av 5'-hydroksytryptamin ( serotonin ). Dette aktiverer vagale afferente nerver, som igjen aktiverer cellene i hjernestammen som styrer brekningsrefleksen.
Friske enterocytter skiller ut laktase i tynntarmen; melkintoleranse på grunn av laktasemangel er et symptom på rotavirusinfeksjon, som kan vedvare i flere uker. En tilbakefall av mild diaré følger ofte gjeninnføring av melk i barnets kosthold, på grunn av bakteriell fermentering av disakkaridet laktose i tarmen.
Immunresponser
Spesifikke svar
Rotavirus fremkaller både B- og T-celle-immunresponser. Antistoffer mot rotavirus-VP4- og VP7-proteinene nøytraliserer viral smitteevne in vitro og in vivo . Det produseres spesifikke antistoffer av klassene IgM, IgA og IgG, som har vist seg å beskytte mot rotavirusinfeksjon ved passiv overføring av antistoffene i andre dyr. Mors trans-placentalt IgG kan spille en rolle i beskyttelsen av nyfødte mot rotavirusinfeksjoner, men kan på den annen side redusere vaksinens effekt.
Medfødte svar
Etter infeksjon med rotavirus er det en rask medfødt immunrespons som involverer type I og III interferoner og andre cytokiner (spesielt Th1 og Th2) som hemmer replikasjonen av viruset og rekrutterer makrofager og naturlige dreperceller til de rotavirusinfiserte cellene. Rotavirus- dsRNA aktiverer mønstergjenkjenningsreseptorer som tolllignende reseptorer som stimulerer produksjonen av interferoner. Rotavirusproteinet NSP1 motvirker effekten av type 1 interferoner ved å undertrykke aktiviteten til de interferonregulerende proteinene IRF3, IRF5 og IRF7.
Markører for beskyttelse
Nivåene av IgG og IgA i blodet og IgA i tarmen korrelerer med beskyttelse mot infeksjon. Rotavirusspesifikt serum IgG og IgA ved høye titre (f.eks. >1:200) har blitt hevdet å være beskyttende og det er en signifikant korrelasjon mellom IgA-titere og rotavirusvaksineeffektivitet.
Diagnose og påvisning
Diagnose av infeksjon med rotavirus følger normalt diagnosen gastroenteritt som årsak til alvorlig diaré. De fleste barn som legges inn på sykehus med gastroenteritt blir testet for rotavirus A.
Spesifikk diagnose av infeksjon med rotavirus A stilles ved å finne viruset i barnets avføring ved enzymimmunoassay . Det finnes flere lisensierte testsett på markedet som er sensitive, spesifikke og oppdager alle serotyper av rotavirus A . Andre metoder, som elektronmikroskopi og PCR (polymerasekjedereaksjon), brukes i forskningslaboratorier. Omvendt transkripsjon-polymerasekjedereaksjon ( RT-PCR ) kan oppdage og identifisere alle arter og serotyper av humane rotavirus.
Behandling og prognose
Behandling av akutt rotavirusinfeksjon er uspesifikk og involverer håndtering av symptomer og, viktigst av alt, håndtering av dehydrering . Hvis ubehandlet, kan barn dø av den resulterende alvorlige dehydreringen. Avhengig av alvorlighetsgraden av diaréen, består behandlingen av oral rehydreringsterapi , hvor barnet får ekstra vann å drikke som inneholder spesifikke mengder salt og sukker. I 2004 anbefalte Verdens helseorganisasjon (WHO) og UNICEF bruk av oral rehydreringsløsning med lav osmolaritet og sinktilskudd som en todelt behandling av akutt diaré. Noen infeksjoner er alvorlige nok til å rettferdiggjøre sykehusinnleggelse der væske gis ved intravenøs terapi eller nasogastrisk intubasjon , og barnets elektrolytter og blodsukker overvåkes. Rotavirusinfeksjoner forårsaker sjelden andre komplikasjoner, og for et godt administrert barn er prognosen utmerket. Probiotika har vist seg å redusere varigheten av rotavirusdiaré, og ifølge European Society for Pediatric Gastroenterology inkluderer "effektive intervensjoner administrering av spesifikke probiotika som Lactobacillus rhamnosus eller Saccharomyces boulardii , diosmektitt eller racecadotril ."
Forebygging
Rotavirus er svært smittsomt og kan ikke behandles med antibiotika eller andre legemidler. Fordi forbedrede sanitærforhold ikke reduserer forekomsten av rotaviral sykdom, og antallet sykehusinnleggelser forblir høy til tross for bruk av orale rehydrerende medisiner, er den primære folkehelseintervensjonen vaksinasjon. I 1998 ble en rotavirusvaksine lisensiert for bruk i USA. Kliniske studier i USA, Finland og Venezuela hadde funnet at det var 80 til 100 % effektivt for å forhindre alvorlig diaré forårsaket av rotavirus A , og forskere hadde ikke oppdaget noen statistisk signifikante alvorlige bivirkninger . Produsenten trakk den imidlertid fra markedet i 1999, etter at det ble oppdaget at vaksinen kan ha bidratt til en økt risiko for tarm , en type tarmobstruksjon , hos ett av hver 12.000 vaksinerte spedbarn. Erfaringen provoserte intens debatt om de relative risikoene og fordelene med en rotavirusvaksine.
I 2006 ble to nye vaksiner mot rotavirus A- infeksjon vist å være trygge og effektive hos barn, og i 2009 anbefalte WHO at rotavirusvaksine inkluderes i alle nasjonale vaksinasjonsprogrammer.
Forekomsten og alvorlighetsgraden av rotavirusinfeksjoner har gått betydelig ned i land som har fulgt denne anbefalingen. En gjennomgang fra 2014 av tilgjengelige kliniske forsøksdata fra land som rutinemessig bruker rotavirusvaksiner i sine nasjonale immuniseringsprogrammer fant at rotavirusvaksiner har redusert rotavirussykehusinnleggelser med 49–92 prosent og alle forårsaker diarésykehusinnleggelser med 17–55 prosent. I Mexico, som i 2006 var blant de første landene i verden som introduserte rotavirusvaksine, falt dødsratene ved diarésykdom i løpet av rotavirussesongen 2009 med mer enn 65 prosent blant barn i alderen to og under. I Nicaragua, som i 2006 ble det første utviklingsland som innførte en rotavirusvaksine, ble alvorlige rotavirusinfeksjoner redusert med 40 prosent og legevaktbesøk med det halve. I USA har rotavirusvaksinasjon siden 2006 ført til fall i rotavirusrelaterte sykehusinnleggelser med så mye som 86 prosent. Vaksinene kan også ha forhindret sykdom hos ikke-vaksinerte barn ved å begrense antallet sirkulerende infeksjoner. I utviklingsland i Afrika og Asia, hvor flertallet av rotavirusdødsfall forekommer, har et stort antall sikkerhets- og effektstudier samt nylige effekt- og effektivitetsstudier etter introduksjon av Rotarix og RotaTeq funnet at vaksiner dramatisk reduserte alvorlig sykdom blant spedbarn. I september 2013 ble vaksinen tilbudt alle barn i Storbritannia, i alderen mellom to og tre måneder, og den forventes å halvere tilfellene av alvorlig infeksjon og redusere antall barn innlagt på sykehus på grunn av infeksjonen med 70 prosent. I Europa har sykehusinnleggelsesraten etter infeksjon med rotavirus gått ned med 65 % til 84 % etter introduksjonen av vaksinen. Globalt har vaksinasjon redusert sykehusinnleggelser og akuttmottaksbesøk med en median på 67 %.
Rotavirusvaksiner er lisensiert i over 100 land, og mer enn 80 land har innført rutinemessig rotavirusvaksinasjon, nesten halvparten med støtte fra GAVI - vaksinealliansen. For å gjøre rotavirusvaksiner tilgjengelige, tilgjengelige og rimelige i alle land – spesielt lav- og mellominntektsland i Afrika og Asia hvor flertallet av rotavirusdødsfall forekommer, PATH (tidligere Program for Appropriate Technology in Health), WHO, USA Centers for Disease Control and Prevention og GAVI har inngått samarbeid med forskningsinstitusjoner og myndigheter for å generere og spre bevis, senke priser og fremskynde introduksjonen.
Vaksinen kan forebygge type 1 diabetes .
Epidemiologi
Rotavirus A , som utgjør mer enn 90 % av rotavirus-gastroenteritt hos mennesker, er endemisk over hele verden. Hvert år forårsaker rotavirus millioner av tilfeller av diaré i utviklingsland, hvorav nesten 2 millioner fører til sykehusinnleggelse. I 2019 døde anslagsvis 151 714 barn yngre enn fem av rotavirusinfeksjoner, hvorav 90 prosent var i utviklingsland. Nesten hvert barn har blitt smittet med rotavirus ved fem års alder. Rotavirus er den ledende enkeltårsaken til alvorlig diaré blant spedbarn og barn, er ansvarlig for omtrent en tredjedel av tilfellene som krever sykehusinnleggelse, og forårsaker 37 % av dødsfallene som kan tilskrives diaré og 5 % av alle dødsfall hos barn under fem år. Det er dobbelt så stor sannsynlighet for at gutter som jenter blir innlagt på sykehus for rotavirusinfeksjoner. I førvaksinasjonstiden forekom rotavirusinfeksjoner primært i kjølige, tørre årstider. Antallet som kan tilskrives matforurensning er ukjent.
Utbrudd av rotavirus A diaré er vanlig blant innlagte spedbarn, små barn som går i barnehager og eldre på sykehjem. Et utbrudd forårsaket av forurenset kommunalt vann skjedde i Colorado i 1981. I løpet av 2005 skjedde den største registrerte epidemien av diaré i Nicaragua. Dette uvanlig store og alvorlige utbruddet var assosiert med mutasjoner i rotavirus A -genomet, noe som muligens hjalp viruset med å unnslippe den utbredte immuniteten i befolkningen. Et lignende stort utbrudd skjedde i Brasil i 1977.
Rotavirus B , også kalt voksendiaré rotavirus eller ADRV, har forårsaket store epidemier med alvorlig diaré som rammer tusenvis av mennesker i alle aldre i Kina. Disse epidemiene oppsto som et resultat av kloakkforurensning av drikkevann. Rotavirus B- infeksjoner forekom også i India i 1998; den forårsakende stammen ble kalt CAL. I motsetning til ADRV er CAL-stammen endemisk. Til dags dato har epidemier forårsaket av rotavirus B vært begrenset til fastlands-Kina , og undersøkelser indikerer mangel på immunitet mot denne arten i USA. Rotavirus C har vært assosiert med sjeldne og sporadiske tilfeller av diaré hos barn, og små utbrudd har forekommet i familier.
Andre dyr
Rotavirus infiserer ungene til mange dyrearter, og de er en viktig årsak til diaré hos ville og oppdrettede dyr over hele verden. Som et patogen for husdyr, spesielt hos unge kalver og smågriser, forårsaker rotavirus økonomisk tap for bøndene på grunn av behandlingskostnader forbundet med høy sykelighet og dødelighet. Disse rotavirusene er et potensielt reservoar for genetisk utveksling med humane rotavirus. Det er bevis på at animalske rotavirus kan infisere mennesker, enten ved direkte overføring av viruset eller ved å bidra med ett eller flere RNA-segmenter til reassortanter med menneskelige stammer.
Historie
I 1943 beviste Jacob Light og Horace Hodes at et filtrerbart middel i avføringen til barn med smittsom diaré også forårsaket skuring (husdyrdiaré) hos storfe. Tre tiår senere ble bevarte prøver av midlet vist å være rotavirus. I de mellomliggende årene ble et virus hos mus vist å være relatert til viruset som forårsaker skuring. I 1973 beskrev Ruth Bishop og kolleger relaterte virus funnet hos barn med gastroenteritt.
I 1974 foreslo Thomas Henry Flewett navnet rotavirus etter å ha observert at når den sees gjennom et elektronmikroskop , ser en rotaviruspartikkel ut som et hjul ( rota på latin), navnet ble offisielt anerkjent av International Committee on Taxonomy of Viruses fire år senere. I 1976 ble relaterte virus beskrevet i flere andre dyrearter. Disse virusene, som alle forårsaker akutt gastroenteritt, ble anerkjent som et kollektivt patogen som påvirker mennesker og andre dyr over hele verden. Rotavirus serotyper ble først beskrevet i 1980, og året etter ble rotavirus fra mennesker først dyrket i cellekulturer avledet fra apenyrer, ved å tilsette trypsin (et enzym som finnes i tolvfingertarmen hos pattedyr og nå kjent for å være essensielt for at rotavirus skal replikeres ) til kulturmediet. Evnen til å dyrke rotavirus i kultur satte fart i forskningen, og på midten av 1980-tallet ble de første kandidatvaksinene evaluert.
Referanser
Eksterne linker
-
 Medisinportal
Medisinportal
-
 Virusportal
Virusportal
-
 Media relatert til Rotavirus på Wikimedia Commons
Media relatert til Rotavirus på Wikimedia Commons


![Sesongvariasjonen av rotavirus A-infeksjoner i England: infeksjonsrater topper i vintermånedene. [141]](https://upload.wikimedia.org/wikipedia/commons/thumb/4/4e/Rotavirus_seasonal_distribution.png/650px-Rotavirus_seasonal_distribution.png)
![Forebyggbare barnedødsfall fra rotavirusvaksinasjon, 2016. Årlig antall forebyggbare dødsfall hos barn under fem år fra rotavirus dersom full dekning av rotavirusvaksinen ble oppnådd. [142]](https://upload.wikimedia.org/wikipedia/commons/thumb/8/81/Avertable-deaths-from-rotavirus-with-full-vaccine-coverage.png/650px-Avertable-deaths-from-rotavirus-with-full-vaccine-coverage.png)
