Epstein -Barr -virus - Epstein–Barr virus
| Menneskelig gammaherpesvirus 4 | |
|---|---|

|
|
| Elektronmikrograf av to Epstein-Barr-viruspartikler (viruspartikler) som viser firkant kapsider løst omgitt av membranen konvolutten | |
|
Virusklassifisering |
|
| (uten rangering): | Virus |
| Rike : | Duplodnaviria |
| Kongedømme: | Heunggongvirae |
| Filum: | Peploviricota |
| Klasse: | Herviviricetes |
| Rekkefølge: | Herpesvirales |
| Familie: | Herpesviridae |
| Slekt: | Lymfokryptovirus |
| Arter: |
Menneskelig gammaherpesvirus 4
|
| Synonymer | |
|
|
Den Epstein-Barr-virus ( EBV ), formelt kalt Menneskelig gammaherpesvirus 4 , er en av de ni kjente menneskelige herpestyper i herpes familien , og er en av de mest vanlige virus hos mennesker. EBV er et dobbeltstrenget DNA-virus .
Det er best kjent som årsaken til smittsom mononukleose ("mono" eller "kjertelfeber"). Det er også assosiert med forskjellige ikke-ondartede, premaligne og ondartede Epstein-Barr-virusassosierte lymfoproliferative sykdommer som Burkitt lymfom , hemofagocytisk lymfohistiocytose og Hodgkins lymfom ; ikke-lymfoide maligniteter som magekreft og nasofaryngeal karsinom ; og tilstander assosiert med humant immunsviktvirus som hårete leukoplaki og lymfomer i sentralnervesystemet . Viruset er også assosiert med barndomsforstyrrelsene i Alice in Wonderland syndrom og akutt cerebellar ataksi og, basert på noen bevis, høyere risiko for å utvikle visse autoimmune sykdommer , spesielt dermatomyositis , systemisk lupus erythematosus , revmatoid artritt , Sjögrens syndrom og multippel sklerose . Omtrent 200 000 krefttilfeller per år antas å skyldes EBV.
Infeksjon med EBV skjer ved oral overføring av spytt og kjønnssekresjoner. De fleste blir smittet med EBV og får adaptiv immunitet . I USA har omtrent halvparten av alle fem år gamle barn og omtrent 90% av voksne tegn på tidligere infeksjon. Spedbarn blir utsatt for EBV så snart mors antistoffbeskyttelse forsvinner. Mange barn blir smittet med EBV, og disse infeksjonene forårsaker vanligvis ingen symptomer eller kan ikke skilles fra de andre milde, korte sykdommene i barndommen. I USA og andre utviklede land er mange mennesker ikke smittet med EBV i barndommen. Når infeksjon med EBV oppstår i ungdomsårene, forårsaker det smittsom mononukleose 35 til 50% av tiden.
EBV infiserer B -celler i immunsystemet og epitelceller . Når EBVs første lytiske infeksjon er brakt under kontroll, vedvarer EBV -latens i individets B -celler resten av livet.
Virologi
Struktur og genom
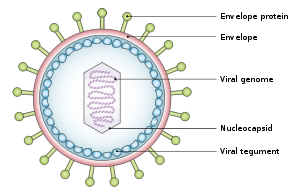
Den Viruset er omtrent 122 til 180 nm i diameter, og består av en dobbeltspiralen av deoksyribonukleinsyre (DNA), som inneholder omtrent 172.000 basepar og 85 gener . DNA blir omgitt av en protein nukleokapsid , som er omgitt av en tegument laget av protein, som i sin tur er omgitt av en konvolutt som inneholder både fett og overflate projeksjoner av glykoproteiner , som er avgjørende for infeksjon av vertscellen . I juli 2020 rapporterte et team av forskere den første komplette atommodellen for nukleokapsidet til viruset. Denne "første komplette atommodellen [inkluderer] det icosahedral capsid, det capsid-assosierte tegumentkomplekset (CATC) og dodecameric-portalen-det virale genom-translokasjonsapparatet."
Tropisme
Begrepet viral tropisme refererer til hvilke celletyper som EBV infiserer. EBV kan infisere forskjellige celletyper, inkludert B -celler og epitelceller .
De virale tredelte glykoproteinkompleksene av gHgL gp42 formidler B-cellemembranfusjon; selv om todelte komplekser av gHgL formidler fusjon av epitelcellemembraner. EBV som er laget i B-cellene har et lavt antall gHgLgp42-komplekser, fordi disse tredelte kompleksene interagerer med human-leukocytt-antigen klasse II- molekyler som er tilstede i B-celler i det endoplasmatiske retikulum og nedbrytes. I kontrast er EBV fra epitelceller rikt på de tredelte kompleksene fordi disse cellene normalt ikke inneholder HLA klasse II-molekyler. Som en konsekvens er EBV laget av B -celler mer smittsom for epitelceller, og EBV laget av epitelceller er mer smittsom for B -celler. Virus som mangler gp42 -delen er i stand til å binde seg til humane B -celler, men klarer ikke å infisere.
Replikasjonssyklus
Inngang til cellen
EBV kan infisere både B -celler og epitelceller. Mekanismene for å komme inn i disse to cellene er forskjellige.
For å komme inn i B -celler, binder viralt glykoprotein gp350 seg til mobilreseptoren CD21 (også kjent som CR2). Deretter interagerer viralt glykoprotein gp42 med cellulære MHC klasse II -molekyler. Dette utløser fusjon av virushylsteret med cellemembranen, slik at EBV kan komme inn i B -cellen. Human CD35, også kjent som komplementreseptor 1 (CR1), er en ekstra festefaktor for gp350/220, og kan gi en rute for inntreden av EBV i CD21-negative celler, inkludert umodne B-celler. EBV -infeksjon nedregulerer uttrykk for CD35.
For å komme inn i epitelceller interagerer viralt protein BMRF-2 med cellulære β1- integriner . Deretter samhandler viralt protein gH / gL med cellulære αvβ6 / αvβ8 integriner. Dette utløser fusjon av virushylsteret med epitelcellemembranen, slik at EBV kan komme inn i epitelcellen. I motsetning til B-celleoppføring, er epitelcelleoppføring faktisk hindret av viralt glykoprotein gp42.
Når EBV kommer inn i cellen, oppløses det virale kapsidet og det virale genomet transporteres til cellekjernen .
Lytisk replikasjon
Den lytiske syklusen , eller produktiv infeksjon, resulterer i produksjon av smittsomme virioner . EBV kan gjennomgå lytisk replikasjon i både B -celler og epitelceller. I B -celler skjer lytisk replikasjon normalt bare etter reaktivering fra latens . I epitelceller følger lytisk replikasjon ofte direkte etter virusinngang .
For at lytisk replikasjon skal skje, må det virale genomet være lineært. Det latente EBV -genomet er sirkulært, så det må linearisere i prosessen med lytisk reaktivering. Under lytisk replikasjon er viral DNA -polymerase ansvarlig for kopiering av virusgenomet. Dette står i kontrast med latens, der vertscelle-DNA-polymerase kopierer det virale genomet.
Lytiske genprodukter produseres i tre påfølgende stadier: umiddelbart-tidlig, tidlig og sent. Umiddelbart tidlig lytiske genprodukter fungerer som transaktivatorer , noe som forbedrer uttrykket for senere lytiske gener. Umiddelbart tidlig lytiske genprodukter inkluderer BZLF1 (også kjent som Zta, EB1, assosiert med produktgenet ZEBRA ) og BRLF1 (assosiert med produktgenet Rta ). Tidlige lytiske genprodukter har mange flere funksjoner, for eksempel replikasjon, metabolisme og blokkering av antigenbehandling . Tidlige lytiske genprodukter inkluderer BNLF2 . Til slutt har late lytiske genprodukter en tendens til å være proteiner med strukturelle roller, for eksempel VCA , som danner det virale kapsidet . Andre sent lytiske genprodukter, som BCRF1, hjelper EBV med å unngå immunsystemet.
EGCG , en polyfenol i grønn te , har vist i en studie å hemme EBV spontan lytisk infeksjon ved DNA, gentranskripsjon og proteinnivåer på en tids- og doseavhengig måte; uttrykket av EBV lytiske gener Zta, Rta og tidlig antigenkompleks EA-D (indusert av Rta ), men det meget stabile EBNA-1- genet som er funnet på alle stadier av EBV-infeksjon, er upåvirket. Spesifikke hemmere (til veiene) antyder at Ras/MEK/MAPK-banen bidrar til EBV lytisk infeksjon selv om BZLF1 og PI3-K- banen gjennom BRLF1, sistnevnte opphever fullstendig evnen til en BRLF1 adenovirusvektor til å indusere den lytiske formen for EBV-infeksjon. I tillegg studeres aktiveringen av noen gener, men ikke andre, for å bestemme hvordan man kan indusere immunødeleggelse av latent infiserte B-celler ved bruk av enten TPA eller natriumbutyrat .
Ventetid
I motsetning til lytisk replikasjon, resulterer ikke ventetid i produksjon av virioner. I stedet ligger EBV -genomets sirkulære DNA i cellekjernen som et episom og kopieres av cellulær DNA -polymerase . I latens uttrykkes bare en del av EBVs gener . Latent EBV uttrykker sine gener i ett av tre mønstre, kjent som latensprogrammer. EBV kan latent vedvare i B -celler og epitelceller , men forskjellige latensprogrammer er mulige i de to celletyper.
EBV kan vise et av tre latensprogrammer: Latency I, Latency II eller Latency III. Hvert latensprogram fører til produksjon av et begrenset, distinkt sett med virale proteiner og virale RNA .
| Gene uttrykt | EBNA-1 | EBNA-2 | EBNA-3 A | EBNA-3 B | EBNA-3 C | EBNA-LP | LMP-1 | LMP-2 A | LMP-2 B | EBER |
|---|---|---|---|---|---|---|---|---|---|---|
| Produkt | Protein | Protein | Protein | Protein | Protein | Protein | Protein | Protein | Protein | ncRNA |
| Forsinkelse I | + | - | - | - | - | - | - | - | - | + |
| Latens II | + | - | - | - | - | + | + | + | + | + |
| Latens III | + | + | + | + | + | + | + | + | + | + |
Det postuleres også et program der alt viralt proteinuttrykk blir slått av (latens 0).
Innen B -celler er alle tre latensprogrammene mulige. EBV -latenstid i B -celler utvikler seg vanligvis fra latens III til latens II til latens I. Hvert stadium av latens påvirker B -cellens oppførsel unikt. Ved infeksjon av en hvilende naiv B -celle , går EBV inn i Latency III. Settet med proteiner og RNA produsert i latens III forvandler B -cellen til en spredende eksplosjon (også kjent som B -celleaktivering). Senere begrenser viruset genuttrykket og går inn i latens II. Det mer begrensede settet med proteiner og RNA produsert i latens II får B -cellen til å differensiere til en minne -B -celle . Til slutt begrenser EBV genuttrykket ytterligere og går inn i latens I. Uttrykk av EBNA-1 lar EBV-genomet replikere når B-cellehukommelsen deler seg.
Innen epitelceller er bare Latency II mulig.
Ved primær infeksjon replikerer EBV seg i orofaryngeale epitelceller og etablerer Latency III, II og I infeksjoner i B-lymfocytter. EBV latent infeksjon av B-lymfocytter er nødvendig for virusbestandighet, påfølgende replikasjon i epitelceller og frigjøring av smittsomt virus i spytt. EBV Latency III og II infeksjoner av B-lymfocytter, Latency II infeksjon av orale epitelceller og Latency II infeksjon av NK- eller T-celle kan resultere i maligniteter, preget av jevn EBV-genomtilstedeværelse og genuttrykk.
Reaktivering
Latent EBV i B -celler kan reaktiveres for å bytte til lytisk replikasjon . Dette er kjent for å skje in vivo , men hva som utløser det er ikke kjent nøyaktig. In vitro kan latent EBV i B -celler reaktiveres ved å stimulere B -celle reseptoren, så reaktivering in vivo skjer sannsynligvis når latent infiserte B -celler reagerer på ikke -relaterte infeksjoner. In vitro kan latent EBV i B-celler også reaktiveres ved å behandle cellene med natriumbutyrat eller 12-O-Tetradecanoylphorbol-13-acetat .
Transformasjon av B-lymfocytter
Når EBV infiserer B -celler in vitro , dukker det etter hvert opp lymfoblastoide cellelinjer som er i stand til ubestemt vekst. Veksttransformasjonen av disse cellelinjene er konsekvensen av viralt proteinuttrykk.
EBNA-2, EBNA-3C og LMP-1 er avgjørende for transformasjon, mens EBNA-LP og EBER ikke er det.
Etter naturlig infeksjon med EBV, antas viruset å utføre noen eller alle av sitt repertoar av genuttrykksprogrammer for å etablere en vedvarende infeksjon. Gitt det opprinnelige fraværet av vertsimmunitet , produserer den lytiske syklusen et stort antall virioner for å infisere andre (antagelig) B-lymfocytter i verten.
De latente programmene omprogrammerer og undergraver infiserte B-lymfocytter for å spre seg og bringe infiserte celler til stedene hvor viruset antagelig vedvarer. Til slutt, når vertsimmuniteten utvikler seg, vedvarer viruset ved å slå av de fleste (eller muligens alle) genene, og reaktiverer bare av og til for å produsere friske virioner. Til slutt blir det en balanse mellom sporadisk viral reaktivering og vertsimmunovervåking som fjerner celler som aktiverer viralt genuttrykk.
Stedet for persistens av EBV kan være beinmarg . EBV-positive pasienter som har fått sitt eget benmarg erstattet med benmarg fra en EBV-negativ donor, er funnet å være EBV-negative etter transplantasjon .
Latente antigener
Alle EBV -kjerneproteiner produseres ved alternativ spleising av et transkript som starter ved enten Cp- eller Wp -promotorene i venstre ende av genomet (i den konvensjonelle nomenklaturen). Genene er ordnet EBNA-LP/EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 i genomet.
Initieringen kodon av EBNA-LP-kodende område blir skapt av en alternativ spleise av kjerneproteinet transkripsjon. I fravær av denne initieringskodon vil EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 bli uttrykt avhengig av hvilke av disse genene som alternativt er spleiset inn i transkripsjonen.
Protein/gener
| Protein/gen/antigen | Scene | Beskrivelse |
|---|---|---|
| EBNA-1 | latent+lytisk | EBNA-1-protein binder seg til en replikasjonsorigin (oriP) i virusgenomet og formidler replikasjon og partisjonering av episomet under deling av vertscellen. Det er det eneste virale proteinet uttrykt under gruppe I latens. |
| EBNA-2 | latent+lytisk | EBNA-2 er den viktigste virale transaktivator . |
| EBNA-3 | latent+lytisk | Disse genene binder også verten RBP-Jκ- protein. |
| LMP-1 | latent | LMP-1 er et seks-spenn transmembranprotein som også er avgjørende for EBV-mediert veksttransformasjon. |
| LMP-2 | latent | LMP-2A/LMP-2B er transmembrane proteiner som virker for å blokkere tyrosinkinasesignalering . |
| EBER | latent | EBER-1/EBER-2 er små kjernefysiske RNAer, som binder seg til visse nukleoproteinpartikler, noe som muliggjør binding til PKR (dsRNA-avhengig serin/treoninproteinkinase), og dermed hemmer dets funksjon. EBER er de desidert vanligste EBV -produktene som er transkribert i EBV -infiserte celler. De brukes ofte som mål for påvisning av EBV i histologiske vev. ER-partikler induserer også produksjon av IL-10, som øker veksten og hemmer cytotoksiske T-celler. |
| v-snoRNA1 | latent | Epstein-Barr-virus snoRNA1 er en eske-CD-snoRNA generert av viruset under ventetid. V-snoRNA1 kan fungere som en miRNA-lignende forløper som behandles til 24 RNA-fragmenter av nukleotidstørrelse som målretter mot 3'UTR av viralt DNA-polymerase-mRNA. |
| ebv-sisRNA | latent | Ebv-sisRNA-1 er en stabil intronisk sekvens-RNA generert under latensprogram III. Etter EBER-tallet er det det tredje forekomsten av små RNA som viruset produserer under dette programmet. |
| miRNA | latent | EBV -mikroRNA er kodet av to transkripsjoner, ett sett i BART -genet og ett sett nær BHRF1 -klyngen . De tre BHRF1 pri-miRNAS (som genererer fire miRNA) uttrykkes under type III latens, mens den store klyngen av BART miRNA (opptil 20 miRNA) uttrykkes under type II latens. Funksjonene til disse miRNA -ene er for tiden ukjente. |
| EBV-EA | lytisk | tidlig antigen |
| EBV-MA | lytisk | membranantigen |
| EBV-VCA | lytisk | viralt kapsidantigen |
| EBV-AN | lytisk | alkalisk nuklease |
Undertyper av EBV
EBV kan deles inn i to hovedtyper, EBV type 1 og EBV type 2. Disse to undertyper har forskjellige EBNA-3- gener. Som et resultat er de to undertyper forskjellige i deres transformerende evner og reaktiveringsevne. Type 1 er dominerende i det meste av verden, men de to typene er like utbredt i Afrika . Man kan skille EBV type 1 fra EBV type 2 ved å kutte virusgenomet med et restriksjonsenzym og sammenligne de resulterende fordøyelsesmønstrene ved gelelektroforese .
Rolle i sykdom
EBV forårsaker smittsom mononukleose . Barn smittet med EBV har få symptomer eller kan virke asymptomatiske, men når infeksjon forsinkes til ungdomsårene eller voksenlivet, kan det forårsake tretthet , feber , betent hals , hovne lymfeknuter i nakken, forstørret milt , hovent lever eller utslett. Post-smittsomt kronisk utmattelsessyndrom har også vært assosiert med EBV-infeksjon.
EBV har også blitt implisert i flere andre sykdommer, inkludert Burkitts lymfom , hemofagocytisk lymfohistiocytose , Hodgkins lymfom , magekreft , nasofaryngeal karsinom , multippel sklerose og lymfomatoid granulomatose . Spesielt har EBV-infiserte B-celler vist seg å befinne seg i hjerneskader hos pasienter med multippel sklerose . Ytterligere sykdommer som har vært knyttet til EBV inkluderer Gianotti - Crosti syndrom , erythema multiforme , akutte kjønnsår, oral hårete leukoplaki . Den virale infeksjon er også forbundet med, og ofte bidrar til utvikling av et bredt spekter av ikke-ondartede lymfoproliferative sykdommer så som alvorlig hypersensitivitets myggstikk allergireaksjoner, Epstein-Barr virus-positive mukokutane magesår , og hydroa vacciniforme så vel som ondartet lymfoproliferative sykdommer som Epstein-Barr virus-positivt Burkitt lymfom , Epstein-Barr virus-positivt Hodgkin lymfom og primær effusjon lymfom .
Epstein-Barr-viruset har vært involvert i lidelser relatert til aggregering av alfa-synuklein (f.eks. Parkinsons sykdom , demens med Lewy-kropper og atrofi av flere systemer ).
Historie
Epstein - Barr -viruset ble oppkalt etter Michael Anthony Epstein og Yvonne Barr , som oppdaget viruset sammen med Bert Achong . I 1961 deltok Epstein, en patolog og en ekspert elektronmikroskop , på et foredrag om "The Commonest Children's Cancer in Tropical Africa — A Hitherto Unrecognized Syndrome" av Denis Parsons Burkitt , en kirurg som praktiserte i Uganda , der Burkitt beskrev den "endemiske varianten" (pediatrisk form) av sykdommen som bærer navnet hans . I 1963 ble et eksemplar sendt fra Uganda til Middlesex Hospital for å dyrkes. Viruspartikler ble identifisert i de dyrkede cellene, og resultatene ble publisert i The Lancet i 1964 av Epstein, Achong og Barr. Cellelinjer ble sendt til Werner og Gertrude Henle ved Children's Hospital i Philadelphia som utviklet serologiske markører. I 1967 utviklet en tekniker i laboratoriet deres mononukleose, og de var i stand til å sammenligne en lagret serumprøve, som viste at antistoffer mot viruset utviklet seg. I 1968 oppdaget de at EBV direkte kan udødeliggjøre B-celler etter infeksjon, etterligne noen former for EBV-relaterte infeksjoner, og bekreftet koblingen mellom viruset og smittsom mononukleose.
Forskning
Som et relativt komplekst virus er EBV ennå ikke fullt ut forstått. Laboratorier rundt om i verden fortsetter å studere viruset og utvikler nye måter å behandle sykdommene det forårsaker. En populær måte å studere EBV in vitro er å bruke bakterielle kunstige kromosomer . Epstein-Barr-virus kan opprettholdes og manipuleres i laboratoriet i kontinuerlig latens (en egenskap som deles med Kaposis sarkomassosierte herpesvirus , et annet av de åtte humane herpesvirusene). Selv om mange virus antas å ha denne egenskapen under infeksjon av deres naturlige verter, er det ikke et lett administrert system for å studere denne delen av den virale livssyklusen. Genomiske studier av EBV har vært i stand til å utforske lytisk reaktivering og regulering av det latente virale episomet.
Selv om det er aktiv forskning, er det ikke en Epstein -Barr -virusvaksine tilgjengelig ennå. Utviklingen av en effektiv vaksine kan forhindre opptil 200 000 kreftformer globalt per år. I likhet med andre menneskelige herpesvirus kan Epstein-Barr tillate utryddelse via et forløp av pro-drug valaciclovir , men ytterligere forskning er nødvendig for å avgjøre om utryddelse faktisk er mulig. Antivirale midler virker ved å hemme viral DNA -replikasjon, men det er lite bevis på at de er effektive mot Epstein -Barr -virus. Videre er de dyre, risikerer å forårsake resistens mot antivirale midler, og (i 1% til 10% av tilfellene) kan forårsake ubehagelige bivirkninger .
Se også
- Epstein -Barr -virusinfeksjon
- Epstein-Barr-virusassosierte lymfoproliferative sykdommer
- James Corson Niederman , legen som beviste hvordan Epstein - Barr -viruset overføres ved smittsom mononukleose
Referanser
Eksterne linker
-
 Medier relatert til Epstein-Barr-viruset på Wikimedia Commons
Medier relatert til Epstein-Barr-viruset på Wikimedia Commons -
 Data relatert til Epstein - Barr -viruset på Wikispecies
Data relatert til Epstein - Barr -viruset på Wikispecies - Wikidata : emne ( Scholia )
- Transkriptom og epigenom av EBV