Avvisning av transplantasjon - Transplant rejection
| Avvisning av transplantasjon | |
|---|---|
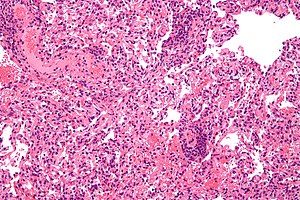 | |
| Mikrograf som viser avvisning av lungetransplantasjon . Lunge biopsi . H & E flekk . | |
| Spesialitet | Immunologi |
| Behandling | Immunsuppressive legemidler |
Transplantasjonsavvisning oppstår når transplantert vev blir avvist av mottakerens immunsystem , noe som ødelegger det transplanterte vevet. Avvisning av transplantasjon kan reduseres ved å bestemme den molekylære likheten mellom donor og mottaker og ved bruk av immunsuppressive legemidler etter transplantasjon.
Forebygging av avvisning av forplantning
Den første vellykkede organtransplantasjonen, utført i 1954 av Joseph Murray , involverte identiske tvillinger, og det ble derfor ikke observert avvisning. Ellers korrelerer antallet ikke -matchede genvarianter, nemlig alleler , kodende celleoverflatemolekyler som kalles hovedhistokompatibilitetskompleks (MHC), klasse I og II, med hastigheten og alvorlighetsgraden av transplantatavvisning. Hos mennesker kalles MHC også humant leukocyttantigen (HLA).
Selv om cytotoksisk crossmatch-analyse kan forutsi avvisning som er formidlet av cellulær immunitet , har genetiske ekspresjonstester som er spesifikke for organtypen som skal transplanteres, for eksempel AlloMap Molecular Expression Testing , en høy negativ prediktiv verdi. Å transplantere kun ABO -kompatible transplantater (matchende blodgrupper mellom donor og mottaker) bidrar til å forhindre avvisning mediert av humoral immunitet .
ABO-inkompatible transplantasjoner
Fordi svært små barn (vanligvis under 12 måneder, men ofte så gamle som 24 måneder) ikke har et godt utviklet immunsystem , er det mulig for dem å motta organer fra ellers inkompatible givere. Dette er kjent som ABO-inkompatibel (ABOi) transplantasjon. Graftoverlevelse og pasientdødelighet er omtrent det samme mellom ABOi og ABO-kompatible (ABOc) mottakere. Selv om fokus har vært på hjertetransplantasjoner hos spedbarn, gjelder prinsippene generelt for andre former for solid organtransplantasjon.
De viktigste faktorene er at mottakeren ikke har produsert isohemagglutininer , og at de har lave nivåer av T- celleuavhengige antigener . UNOS -forskrifter tillater ABOi -transplantasjon hos barn under to år hvis isohemagglutinin -titre er 1: 4 eller lavere, og hvis det ikke finnes en matchende ABOc -mottaker. Studier har vist at perioden en mottaker kan gjennomgå ABOi -transplantasjon, kan forlenges ved eksponering for ikke -selv A- og B -antigener. Hvis mottakeren (for eksempel type B-positiv med type AB-positiv transplantat) krever ytterligere transplantasjon, kan mottakeren motta et nytt organ av enten blodtype.
Begrenset suksess er oppnådd ved ABO-inkompatible hjertetransplantasjoner hos voksne, selv om dette krever at de voksne mottakerne har lave nivåer av anti-A eller anti-B antistoffer. Nyretransplantasjon er mer vellykket, med lignende langsiktige transplantatoverlevelsesrater som ABOc-transplantasjoner.
Immunologiske mekanismer for avvisning
Avvisning er en adaptiv immunrespons via cellulær immunitet (mediert av drepende T -celler som induserer apoptose av målceller) samt humoral immunitet (mediert av aktiverte B -celler som utskiller antistoffmolekyler ), selv om handlingen er forbundet med komponenter i medfødt immunrespons ( fagocytter) og oppløselige immunproteiner). Ulike typer transplanterte vev har en tendens til å favorisere forskjellige balanser av avvisningsmekanismer.
Immunisering
Et dyrs eksponering for antigenene til et annet medlem av samme eller lignende art er allostimulering , og vevet er allogent . Transplanterte organer blir ofte hentet fra en kadaver (vanligvis en vert som hadde bukket under for traumer), hvis vev allerede hadde påført iskemi eller betennelse .
Dendrittceller (DCS), som er den primære antigen-presenterende celler (APC), av donorvevet migrere til mottakerens perifere lymfoide vev ( lymfoide follikler og lymfeknuter ) og aktuelle giverens selv peptider til mottakerens lymfocytter (immuncellene bosatt i lymfoide vev). Lymfocytter inkluderer to klasser som vedtar adaptiv immunitet , også kalt spesifikk immunitet. Lymfocytter av spesifikke immunitet T -celler - inkludert underklassene hjelper T -celler og drepende T -celler - og B -celler .
Mottakerens hjelper-T-celler koordinat spesifikk immunitet rettet mot giverens selv peptider eller på donorens hovedhistokompatibilitetskomplekset molekyler, eller på begge.
Immunminne
Når T4 -reseptorene til minnehjelper T -celler binder seg til MHC -klasse II -molekylene som uttrykkes på overflatene til målcellene i transplantatvevet, kan T -cellers T -reseptorer (TCRer) gjenkjenne målantigenet som presenteres av MHC klasse II molekyler. T -cellen for hukommelseshjelper produserer deretter kloner som, som effektorceller, utskiller immunsignalmolekyler ( cytokiner ) i omtrent cytokinbalansen som hadde hersket ved T -cellens minnehjelper for å memorere antigenet. Siden priminghendelsen i dette tilfellet skjedde midt i betennelse, er immunminnet proinflammatorisk.
Cellulær immunitet
Transplantasjonsavvisning er en type IV ("forsinket") overfølsomhetsreaksjon mediert av T -celler der transplantatmottakerens T -celler blir alloreaktive, gjenkjenner store histokompatibilitetskompleks (MHC) antigener på donert organ, og fremmer lokale immun- og inflammatoriske reaksjoner for å forsvare seg mot den oppfattede trusselen. T-cellene kan gjenkjenne det donerte organets MHC-antigener gjennom en av to ruter: en direkte vei, der det transplanterte organs antigenpresenterende celler (for eksempel dendritiske celler som inneholder MHC klasse I-molekyler) migrerer til mottakerens lymfeknuter og aktiverer T-celler som bor der; eller en indirekte vei, der mottakerens dendritiske celler kan endocytose donorproteiner som donor MHC -proteiner og aktivere T -celler i sekundære lymfoide vev. Alloreaktive killer T -celler, også kalt cytotoksiske T -lymfocytter (CTL), har CD8 -reseptorer som legger til det transplanterte vevets MHC klasse I -molekyler, som viser donorens selvpeptider. (I den levende donoren bidro slik presentasjon av selvantigener til å opprettholde selvtoleranse.) Deretter gjenkjenner T -cellereseptorene (TCR) til de drepende T -cellene deres matchende epitop, og utløser målcellens programmerte celledød ved apoptose.
Humoral immunitet
Utviklet gjennom en tidligere primær eksponering som grunnet spesifikk immunitet mot ikke -selvantigenet , kan en transplantasjonsmottaker ha spesifikt antistoff som kryssreagerer med donorvevet ved transplantasjonshendelsen, en sekundær eksponering . Dette er typisk for mindre eksponering for blodgrupper (f.eks. Kell) etter allogen blodoverføring eller traumer under graviditet. Ved sekundær eksponering interagerer disse kryssreaktive antistoffmolekylene med aspekter ved medfødt immunitet - oppløselige immunproteiner som kalles komplement og medfødte immunceller som kalles fagocytter - som brenner og ødelegger det transplanterte vevet.
Antistoff
Utskilt av en aktivert B -celle, deretter kalt plasmacelle , er et antistoffmolekyl et løselig immunglobulin (Ig) hvis grunnenhet er formet som bokstaven Y : de to armene er Fab -regionene , mens den enkelte stilken er Fc -regionen . Hver av de to spissene i Fab -regionen er paratopen , som binder en matchende molekylær sekvens og dens 3D -form (konformasjon), totalt kalt epitop , i målantigenet.
Opsonisering
IgGs Fc -region muliggjør også opsonisering av en fagocytt , en prosess der Fc -reseptoren på fagocytt - for eksempel nøytrofiler i blod og makrofager i vev - binder antistoffmolekylets FC -stilk, og fagocytten viser forbedret opptak av antigenet, festet til antistoffmolekylets Fab -region.
Komplement kaskade
Når paratopen av Ig -klasse gamma (IgG) binder dets matchende epitop, skifter IgGs Fc -region konformasjonelt og kan være vert for et komplementprotein, og initierer komplementkaskaden som avsluttes ved å slå et hull i en cellemembran. Med mange hull så hullet, siver væske inn i cellen og sprekker den.
Celleavfall kan gjenkjennes som skaderelaterte molekylære mønstre (DAMP) ved mønstergjenkjenningsreseptorer (PRR), for eksempel tolllignende reseptorer (TLR), på membraner av fagocytter , som deretter utskiller proinflammatoriske cytokiner , og rekrutterer flere fagocytter til trafikk til området ved å kjenne konsentrasjonsgradienten til de utskilte cytokinene ( kjemotaksi ).
| Vev | Mekanisme |
|---|---|
| Blod | Antistoffer (isohaemagglutininer) |
| Nyre | Antistoffer, cellemediert immunitet (CMI) |
| Hjerte | Antistoffer, CMI |
| Hud | CMI |
| Bonemarrow | CMI |
| Hornhinnen | Vanligvis akseptert med mindre det vaskulariseres: CMI |
Medisinske kategorier
Hyperakutt avvisning
Startet av eksisterende humoral immunitet , manifesterer hyperakutt avstøtning seg i løpet av minutter etter transplantasjon, og hvis vev blir igjen implantert bringer systemisk inflammatorisk respons syndrom . Av høy risiko i nyretransplantasjoner er hurtig sammenklumpingen, nemlig agglutinering , av røde blodceller (RBC eller erythrocytter), som et antistoffmolekyl som binder flere mål-celler på en gang.
Selv om nyrer rutinemessig kan hentes fra menneskelige givere, er det mangel på de fleste organer, noe som fører til vurdering av xenotransplantasjoner fra andre arter. Gris er spesielt sannsynlige kilder til xenotransplantasjoner, valgt for de anatomiske og fysiologiske egenskapene de deler med mennesker. Imidlertid har sukker galaktose-alfa-1,3-galaktose (αGal) blitt implisert som en hovedfaktor for hyperakutt avvisning ved xenotransplantasjon . I motsetning til praktisk talt alle andre pattedyr lager ikke mennesker og andre primater αGal, og gjenkjenner det faktisk som et antigen. Under transplantasjon gjenkjenner xenoreaktive naturlige antistoffer αGal på transplantatendotelet som et antigen, og den resulterende komplementmedierte immunresponsen fører til en avvisning av transplantasjonen.
Akutt avvisning
Utvikling med dannelse av cellulær immunitet , akutt avvisning finner sted i noen grad i alle transplantasjoner, unntatt mellom identiske tvillinger, med mindre immunsuppresjon er oppnådd (vanligvis gjennom medikamenter). Akutt avvisning begynner så tidlig som en uke etter transplantasjon, risikoen er høyest de første tre månedene, selv om den kan forekomme måneder til år senere. Svært vaskulære vev som nyre eller lever er ofte de tidligste tegnene - spesielt på endotelceller som omgir blodårene - selv om det til slutt forekommer i omtrent 10 til 30% av levertransplantasjoner og 10 til 20% av nyretransplantasjoner. En enkelt episode med akutt avvisning kan gjenkjennes og behandles raskt, vanligvis forhindrer organsvikt, men tilbakevendende episoder fører til kronisk avvisning . Det antas at prosessen med akutt avstøtning medieres av den cellemedierte banen, spesielt av mononukleære makrofager og T-lymfocytter. Histologi for akutt avvisning er definert av tett lymfocytisk cellulært infiltrat samt vaskulitt i organdonorkar.
Kronisk avvisning
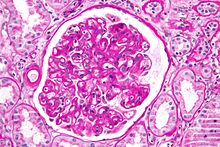
Begrepet kronisk avvisning beskrev opprinnelig langsiktig funksjonstap i transplanterte organer via fibrose i det transplanterte vevets blodkar. Dette er nå kronisk allograft vaskulopati , men kronisk avvisning etterlater avvisning på grunn av flere patentaspekter ved immunitet.
Kronisk avvisning forklarer langvarig sykelighet hos de fleste lungetransplanterte, medianoverlevelsen omtrent 4,7 år, omtrent halvparten av spennet i forhold til andre større organtransplantasjoner. I histopatologi er tilstanden bronkiolitt obliterans , som klinisk presenteres som progressiv luftstrømobstruksjon, ofte med dyspné og hoste , og pasienten bukker til slutt under for lungesvikt eller sekundær akutt infeksjon.
Luftstrømobstruksjon som ikke kan tilskrives andre årsaker er merket med bronkiolitt obliterans syndrom (BOS), bekreftet av et vedvarende fall - tre eller flere uker - i tvunget ekspiratorisk volum (FEV 1 ) med minst 20%. BOS er sett hos over 50% av lungetransplanterte etter 5 år, og hos over 80% med ti år. Først bemerket er infiltrasjon av lymfocytter , etterfulgt av epitelcelleskade , deretter inflammatoriske lesjoner og rekruttering av fibroblaster og myofibroblaster , som formerer seg og utskiller proteiner som danner arrvev. Generelt antatt uforutsigbar, varierer BOS -progresjonen mye: lungefunksjonen kan plutselig falle, men stabilisere seg i årevis eller raskt utvikle seg til døden i løpet av få måneder. Risikofaktorer inkluderer tidligere akutte avstøtningsepisoder, gastroøsofageal reflukssykdom , akutte infeksjoner, bestemte aldersgrupper, HLA-feilmatching, lymfocytisk bronkiolitt og transplantatdysfunksjon (f.eks. Iskemi i luftveiene).
Avvisning på grunn av manglende overholdelse
En hovedårsak til avvisning av transplantasjon er manglende overholdelse av foreskrevne immunsuppressive midler. Dette er spesielt tilfellet for ungdomsmottakere, med ikke-adherensrater nær 50% i noen tilfeller.
Avvisning av avvisning
Diagnose av akutt avvisning er avhengig av kliniske data - pasientens tegn og symptomer, men krever også laboratoriedata som blod eller til og med vevsbiopsi . Laboratoriet patolog generelt søker tre hoved histologiske tegn: (1) infiltrerende T-celler , muligens ledsaget av infiltrering av eosinofiler , plasmaceller og neutrofiler , særlig i avslørende-forhold, (2) strukturelle kompromiss av vev anatomi, varierende etter vevstype transplantert, og (3) skade på blodkar. Vevsbiopsi er imidlertid begrenset av prøvetakingsbegrensninger og risiko/komplikasjoner ved den invasive prosedyren. Cellulær magnetisk resonansavbildning (MR) av immunceller som er radiomerket i vivo, kan - på samme måte som Gene Expression Profiling (GEP) - tilby ikke -invasiv testing.
Avvisning behandling
Hyperakutt avvisning manifesterer seg alvorlig og i løpet av minutter, og derfor er behandlingen umiddelbar: fjerning av vevet. Kronisk avvisning anses generelt som irreversibel og dårlig egnet til behandling - bare omplanting generelt angitt hvis mulig - selv om inhalert ciklosporin blir undersøkt for å forsinke eller forhindre kronisk avvisning av lungetransplantasjoner. Akutt avvisning behandles med en eller flere av noen få strategier. Til tross for behandling er avvisning fortsatt en viktig årsak til transplantasjonssvikt.
Immunsuppressiv terapi
En kort kur med høydose kortikosteroider kan påføres og gjentas. Trippel terapi legger til en kalsineurinhemmer og et antiproliferativt middel . Når kalsineurinhemmere eller steroider er kontraindisert, brukes mTOR -hemmere .
Immunsuppressive legemidler :
- Kortikosteroider
- Calcineurin -hemmere
- Anti-proliferativer
- mTOR -hemmere
Antistoffbaserte behandlinger
Antistoff som er spesifikt for å velge immunkomponenter, kan legges til immunsuppressiv terapi. Det monoklonale anti-T-celle-antistoffet OKT3 , som en gang ble brukt for å forhindre avstøtning, og fremdeles noen ganger brukes til å behandle alvorlig akutt avstøting, har falt i ugunst, ettersom det vanligvis medfører alvorlig cytokinfrigivelsessyndrom og sen post-transplantasjon lymfoproliferativ lidelse . (OKT3 er bare tilgjengelig i Storbritannia for bruk med pasientnavn.)
Antistoffmedisiner :
- Monoklonale anti-IL-2Rα-reseptorantistoffer
- Monoklonale anti-IL-6R-reseptorantistoffer
- Polyklonale anti-T-celle antistoffer
- Anti-tymocytt globulin (ATG)
- Anti-lymfocytt globulin (ALG)
- Monoklonale anti-CD20 antistoffer
Blodoverføring
Tilfeller som er ildfaste for immunsuppressiv behandling eller antistoffbehandling, blir noen ganger behandlet med fotoferese eller ekstrakorporeal fotoimmun terapi (ECP) for å fjerne antistoffmolekyler som er spesifikke for det transplanterte vevet.
Margtransplantasjon
Benmargstransplantasjon kan erstatte transplantatmottakerens immunsystem med donor, og mottakeren godtar det nye organet uten avvisning. Margens hematopoietiske stamceller - reservoaret av stamceller som fyller ut utmattede blodceller inkludert hvite blodlegemer som danner immunsystemet - må være av personen som donerte organet eller av en identisk tvilling eller en klon . Det er imidlertid en risiko for transplantat-mot-vert-sykdom (GVHD), slik at modne lymfocytter som kommer inn med marg gjenkjenner det nye vertsvevet som fremmed og ødelegger dem.
Genterapi
Genterapi er en annen metode som kan brukes. I denne metoden vil genene som får kroppen til å avvise transplantasjoner bli deaktivert. Det forskes fortsatt, og ingen genterapier brukes hittil for å behandle pasienter. Nåværende forskning har en tendens til å fokusere på Th1 og Th17 som formidler allograftavvisning via CD4 og CD8 T -cellene .
Se også
Referanser
Eksterne linker
| Klassifisering | |
|---|---|
| Eksterne ressurser |
