H -teorem - H-theorem
I klassisk statistisk mekanikk beskriver H -teoremet , introdusert av Ludwig Boltzmann i 1872, tendensen til å redusere mengden H (definert nedenfor) i en nesten ideell gass av molekyler. Som denne mengden H var ment å representere entropi av termodynamikk, den H -theorem var en tidlig demonstrasjon av kraften i statistisk mekanikk som det hevdes å utlede termodynamikkens andre lov -a uttalelse om fundamentalt irreversible prosesser -Fra reversible mikroskopiske mekanikk. Det antas å bevise den andre loven for termodynamikk , om enn under antagelse av laventropiske innledende forhold.
Den H -theorem er en naturlig konsekvens av den kinetiske ligning utledet av Boltzmann som har blitt kjent som Boltzmanns ligning . The H -theorem har ført til betydelig diskusjon om dens faktiske konsekvenser, med store temaer er:
- Hva er entropi? På hvilken måte tilsvarer Boltzmanns mengde H den termodynamiske entropien?
- Er antagelsene (spesielt antagelsen om molekylært kaos ) bak Boltzmanns ligning for sterke? Når blir disse forutsetningene brutt?
Navn og uttale
Boltzmann i sin originale publikasjon skriver symbolet E (som i entropi ) for sin statistiske funksjon . År senere skrev Samuel Hawksley Burbury , en av kritikerne av teoremet, funksjonen med symbolet H, en notasjon som senere ble vedtatt av Boltzmann når han refererte til hans "H- teorem". Notasjonen har ført til en viss forvirring angående navnet på teoremet. Selv om uttalelsen er vanligvis referert til som " Aitch teorem " , noen ganger er det i stedet kalt " Eta teorem", som hovedstad greske bokstaven Eta ( Η ) er undistinguishable fra hovedstaden versjonen av Latin brev h ( H ) . Det er reist diskusjoner om hvordan symbolet skal forstås, men det er fortsatt uklart på grunn av mangel på skriftlige kilder fra teoremets tid. Studier av typografien og arbeidet til JW Gibbs ser ut til å favorisere tolkningen av H som Eta .
Definisjon og mening av Boltzmann's H
Den H- verdien bestemmes fra funksjonen f ( E , t ) dE , som er energifordelingen funksjon av molekyler ved tiden t . Verdien f ( E , t ) dE er antallet molekyler som har kinetisk energi mellom E og E + dE . H selv er definert som
For en isolert ideell gass (med fast total energi og fast totalt antall partikler) er funksjonen H på et minimum når partiklene har en Maxwell – Boltzmann -fordeling ; hvis molekylene i den ideelle gassen fordeles på annen måte (si at alle har samme kinetiske energi), vil verdien av H være høyere. Boltzmanns H -teorem, beskrevet i neste avsnitt, viser at når kollisjoner mellom molekyler er tillatt, er slike fordelinger ustabile og har en tendens til irreversibelt å søke mot minimumsverdien av H (mot Maxwell -Boltzmann -fordelingen).
(Merknad om notasjon: Boltzmann brukte opprinnelig bokstaven E for mengde H ; det meste av litteraturen etter Boltzmann bruker bokstaven H som her. Boltzmann brukte også symbolet x for å referere til kinetisk energi til en partikkel.)
Boltzmanns H -teorem

Boltzmann vurderte hva som skjer under kollisjonen mellom to partikler. Det er et grunnleggende faktum i mekanikken at i den elastiske kollisjonen mellom to partikler (for eksempel harde kuler) varierer energien som overføres mellom partiklene avhengig av de første forholdene (kollisjonsvinkel, etc.).
Boltzmann gjorde en sentral antagelse kjent som Stosszahlansatz ( antagelse om molekylært kaos ), at under alle kollisjonshendelser i gassen har de to partiklene som deltar i kollisjonen 1) uavhengig valgte kinetiske energier fra fordelingen, 2) uavhengige hastighetsretninger, 3) uavhengige utgangspunkt. Under disse forutsetningene, og gitt mekanikken for energioverføring, vil energiene til partiklene etter kollisjonen følge en viss ny tilfeldig fordeling som kan beregnes.
Med tanke på gjentatte, ikke -korrelerte kollisjoner, mellom alle molekylene i gassen, konstruerte Boltzmann sin kinetiske ligning ( Boltzmanns ligning ). Fra denne kinetiske ligningen er et naturlig resultat at den kontinuerlige kollisjonsprosessen får mengden H til å falle til den har nådd et minimum.
innvirkning
Selv om Boltzmanns H -teorem viste seg ikke å være det absolutte beviset på termodynamikkens andre lov som opprinnelig hevdet (se kritikk nedenfor), førte H -teoremet Boltzmann i de siste årene av 1800 -tallet til flere og flere sannsynlighetsargumenter om termodynamikkens natur. Det sannsynlige synet på termodynamikk kulminerte i 1902 med Josiah Willard Gibbs 'statistiske mekanikk for fullt generelle systemer (ikke bare gasser), og introduksjonen av generaliserte statistiske ensembler .
Den kinetiske ligningen og spesielt Boltzmanns molekylære kaosantagelse inspirerte en hel familie av Boltzmann -ligninger som fremdeles brukes i dag for å modellere bevegelsene til partikler, for eksempel elektronene i en halvleder. I mange tilfeller er antagelsen om molekylært kaos svært nøyaktig, og muligheten til å forkaste komplekse korrelasjoner mellom partikler gjør beregninger mye enklere.
Prosessen med thermalisation kan beskrives ved hjelp av H-teoremet eller avslapping teorem .
Kritikk og unntak
Det er flere bemerkelsesverdige årsaker beskrevet nedenfor til hvorfor H -teoremet, i det minste i sin opprinnelige form fra 1871, ikke er helt streng. Som Boltzmann til slutt ville innrømme, er tidspilen i H -teoremet faktisk ikke rent mekanisk, men egentlig en konsekvens av antagelser om innledende forhold.
Loschmidts paradoks
Rett etter at Boltzmann publiserte sitt H- teorem, innvendte Johann Josef Loschmidt at det ikke burde være mulig å utlede en irreversibel prosess fra tidssymmetrisk dynamikk og en tidssymmetrisk formalisme. Hvis H synker over tid i en tilstand, må det være en matchende reversert tilstand der H øker over tid ( Loschmidts paradoks ). Forklaringen er at Boltzmanns ligning er basert på antagelsen om " molekylært kaos ", det vil si at det følger av, eller i det minste er i samsvar med, den underliggende kinetiske modellen at partiklene anses som uavhengige og ukorrelerte. Det viser seg at denne antagelsen bryter tids reverseringssymmetri i en subtil forstand, og stiller derfor spørsmålet . Når partiklene fikk anledning til å kollidere, deres hastighets retninger og stillinger i faktisk har blitt korrelert (imidlertid tas disse korrelasjoner kodet i en ekstremt komplisert måte). Dette viser at en (pågående) antagelse om uavhengighet ikke er i samsvar med den underliggende partikkelmodellen.
Boltzmanns svar til Loschmidt var å innrømme muligheten for disse statene, men bemerket at slike stater var så sjeldne og uvanlige at det var umulig i praksis. Boltzmann ville videre skjerpe denne oppfatningen om staters "sjeldenhet", noe som resulterte i hans berømte ligning, hans entropiformel fra 1877 (se Boltzmanns entropiformel ).
Spinn ekko
Som en demonstrasjon av Loschmidt paradoks, en berømt moderne teller eksempel (for ikke å Boltzmann opprinnelige gassrelatert H -theorem, men til en nært beslektet analog) er fenomenet spin ekko . I spin -ekko -effekten er det fysisk mulig å indusere tidsomvendelse i et interaktivt spinnsystem.
En analog til Boltzmanns H for spinnsystemet kan defineres når det gjelder fordelingen av spinntilstander i systemet. I eksperimentet forstyrres spinnsystemet i utgangspunktet til en ikke-likevektstilstand (høy H ), og som forutsagt av H- setningen reduseres mengden H snart til likevektsverdien. På et tidspunkt påføres en nøye konstruert elektromagnetisk puls som reverserer bevegelsene til alle spinnene. Spinnene da angre tidsutviklingen fra før pulsen, og etter en tid H faktisk øker vekk fra likevekt (etter at utviklingen har fullstendig avspolet, den H atter reduseres til minimumsverdien). På en eller annen måte viste tiden som omvendte tilstander Loschmidt bemerket seg ikke å være helt upraktisk.
Poincaré -gjentakelse
I 1896 bemerket Ernst Zermelo et ytterligere problem med H- teoremet, som var at hvis systemets H til enhver tid ikke er et minimum, så må det ikke-minimale H gjentas etter at Poincaré gjentar seg (men etter ekstremt lang tid). Boltzmann innrømmet at disse tilbakevendende stigningene i H teknisk sett ville forekomme, men påpekte at systemet over lange tider bare bruker en liten brøkdel av tiden sin i en av disse tilbakevendende tilstandene.
Den termodynamikkens andre lov sier at entropien til et isolert system øker alltid til en maksimal likevektsverdi. Dette gjelder strengt tatt bare i den termodynamiske grensen for et uendelig antall partikler. For et begrenset antall partikler vil det alltid være entropisvingninger. For eksempel, i det faste volumet i det isolerte systemet, oppnås maksimal entropi når halvpartiklene er i den ene halvdelen av volumet, halvparten i den andre, men noen ganger vil det midlertidig være noen flere partikler på den ene siden enn den andre , og dette vil utgjøre en svært liten reduksjon i entropi. Disse svingningene i entropi er slik at jo lenger man venter, desto større vil en antropifluktuasjon sannsynligvis se i løpet av den tiden, og tiden man må vente på en gitt entropisvingning er alltid begrenset, selv for en svingning til den minste mulige verdien. For eksempel kan man ha en ekstremt lav entropytilstand for at alle partikler er i den ene halvdelen av beholderen. Gassen vil raskt oppnå likevektsverdien av entropi, men gitt nok tid vil den samme situasjonen skje igjen. For praktiske systemer, f.eks. En gass i en 1-liters beholder ved romtemperatur og atmosfærisk trykk, er denne tiden virkelig enorm, mange multipler av universets alder, og praktisk talt kan man se bort fra muligheten.
Svingninger av H i små systemer
Siden H er en mekanisk definert variabel som ikke er konservert, vil den som alle andre slike variabler (trykk, etc.) vise termiske svingninger . Dette betyr at H regelmessig viser spontane økninger fra minimumsverdien. Teknisk sett er dette ikke et unntak fra H -setningen, siden H -setningen bare var ment å gjelde en gass med et veldig stort antall partikler. Disse svingningene er bare merkbare når systemet er lite og tidsintervallet det observeres over ikke er enormt stort.
Hvis H tolkes som entropi som Boltzmann hadde til hensikt, kan dette ses på som en manifestasjon av svingningssetningen .
Tilkobling til informasjonsteori
H er en forløper for Shannons informasjonsentropi . Claude Shannon angav sitt mål på informasjonsentropi H etter H-teoremet. Artikkelen om Shannons informasjonsentropi inneholder en forklaring på den diskrete motparten til mengden H , kjent som informasjonsentropien eller informasjonsusikkerhet (med et minustegn). Ved å utvide den diskrete informasjonen entropi til den kontinuerlige informasjonen entropi , også kalt differensial entropi , oppnår man uttrykket i ligningen fra avsnittet ovenfor, Definisjon og Betydning av Boltzmanns H , og dermed et bedre inntrykk av betydningen av H .
The H -theorem tilknytning mellom informasjon og entropi spiller en sentral rolle i en siste striden kalt Black hole informasjon paradoks .
Tolmans H -teorem
Richard C. Tolmans bok The Principles of Statistical Mechanics fra 1938 dedikerer et helt kapittel til studiet av Boltzmanns H -teorem og dens utvidelse i den generaliserte klassiske statistiske mekanikken til Gibbs . Et ytterligere kapittel er viet til den kvantemekaniske versjonen av H -teoremet.
Klassisk mekanisk
Vi lar og er våre generaliserte koordinater for et sett med partikler. Deretter vurderer vi en funksjon som returnerer sannsynlighetstettheten til partikler, over tilstandene i faserommet . Legg merke til hvordan dette kan multipliseres med en liten region i faserommet, angitt med , for å gi (gjennomsnittlig) forventet antall partikler i den regionen.
Tolman tilbyr følgende ligninger for definisjonen av mengden H i Boltzmanns originale H -setning.
Her summerer vi regionene som faseområdet er delt inn i, indeksert av . Og i grensen for et uendelig lite faseromsvolum kan vi skrive summen som en integral.
H kan også skrives i form av antall molekyler som er tilstede i hver av cellene.
En ekstra måte å beregne mengden H på er:
hvor P er sannsynligheten for å finne et system valgt tilfeldig fra det spesifiserte mikrokanoniske ensemblet . Det kan endelig skrives slik:
hvor G er antallet klassiske tilstander.
Mengden H kan også defineres som integralen over hastighetsrom:
(1)
hvor P ( v ) er sannsynlighetsfordelingen.
Ved å bruke Boltzmann -ligningen kan man bevise at H bare kan redusere.
For et system med N statistisk uavhengige partikler er H relatert til den termodynamiske entropien S gjennom:
Så ifølge H -teoremet kan S bare øke.
Kvantemekanisk
I kvantestatistisk mekanikk (som er kvanteversjonen av klassisk statistisk mekanikk), er H-funksjonen funksjonen:
hvor summering går over alle mulige forskjellige tilstander i systemet, og p i er sannsynligheten for at systemet kan bli funnet i den i -tilstanden.
Dette er nært beslektet med entropiformelen til Gibbs ,
og vi skal (etter f.eks Waldram (1985), s. 39) finner sted ved hjelp av S i stedet for H .
For det første gir differensiering med hensyn til tid
(ved å bruke det faktum at Σ dp i / dt = 0, siden Σ p i = 1, så forsvinner det andre begrepet. Vi får se senere at det vil være nyttig å dele dette i to summer.)
Nå gir Fermis gylne regel en masterligning for gjennomsnittshastigheten for kvantehopp fra tilstand α til β; og fra tilstand β til α. (Selvfølgelig gjør Fermis gylne regel selv visse tilnærminger, og innføringen av denne regelen er det som introduserer irreversibilitet. Det er i hovedsak kvanteversjonen av Boltzmanns Stosszahlansatz .) For et isolert system vil hoppene gi bidrag
hvor reversibiliteten til dynamikken sikrer at den samme overgangskonstanten ν αβ vises i begge uttrykkene.
Så
De to forskjellstermene i summeringen har alltid det samme tegnet. For eksempel:
deretter
så totalt sett vil de to negative tegnene avbrytes.
Derfor,
for et isolert system.
Den samme matematikken brukes noen ganger for å vise at relativ entropi er en Lyapunov -funksjon av en Markov -prosess i detaljert balanse og andre kjemiske sammenhenger.
Gibbs ' H -teorem
Josiah Willard Gibbs beskrev en annen måte som entropien til et mikroskopisk system vil ha en tendens til å øke over tid. Senere forfattere har kalt dette "Gibbs ' H -teorem" ettersom konklusjonen ligner på Boltzmanns. Gibbs selv kalte det aldri et H -teorem, og faktisk er hans definisjon av entropi -og økningsmekanisme -veldig forskjellig fra Boltzmanns. Denne delen er inkludert for historisk fullstendighet.
Innstillingen av Gibbs 'entropiproduksjonsteorem er i ensemble statistisk mekanikk, og entropimengden er Gibbs -entropien (informasjonsentropi) definert i form av sannsynlighetsfordelingen for hele systemets tilstand. Dette er i motsetning til Boltzmanns H definert når det gjelder fordelingen av tilstander for individuelle molekyler, innenfor en bestemt tilstand i systemet.
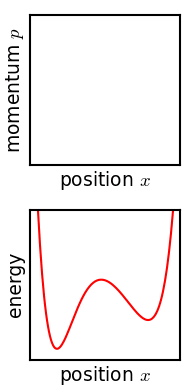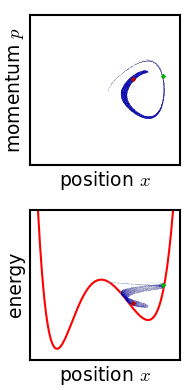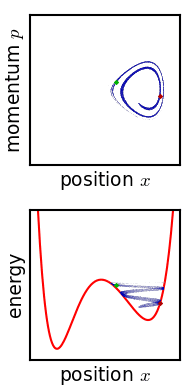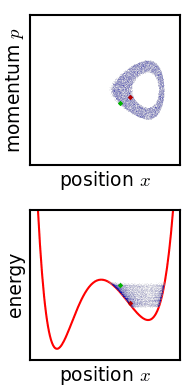
Gibbs vurderte bevegelsen til et ensemble som opprinnelig starter begrenset til et lite område med faserom, noe som betyr at systemets tilstand er kjent med rimelig presisjon, men ikke helt nøyaktig (lav Gibbs -entropi). Utviklingen av dette ensemblet over tid fortsetter i henhold til Liouvilles ligning . For nesten alle slags realistiske systemer har Liouville -evolusjonen en tendens til å "røre" ensemblet over faserommet, en prosess analog med blanding av et fargestoff i en inkomprimerbar væske. Etter en stund ser det ut til at ensemblet er spredt ut over faserom, selv om det faktisk er et fint stripet mønster, med det totale volumet til ensemblet (og dets Gibbs -entropi) bevart. Liouvilles ligning vil garantert bevare Gibbs entropi siden det ikke er noen tilfeldig prosess som virker på systemet; i prinsippet kan det originale ensemblet gjenopprettes når som helst ved å snu bevegelsen.
Teoremets kritiske punkt er således: Hvis den fine strukturen i det opphissede ensemblet er veldig svakt av en eller annen grunn, så øker Gibbs-entropien, og ensemblet blir et likevektsensemble. Hvorfor denne uskarpheten skal skje i virkeligheten, er det en rekke foreslåtte mekanismer. For eksempel er en foreslått mekanisme at faserommet er grovkornet av en eller annen grunn (analogt med pikseliseringen i simuleringen av faserommet vist på figuren). For enhver påkrevd endelig finhetsgrad blir ensemblet "fornuftig ensartet" etter en endelig tid. Eller, hvis systemet opplever et lite ukontrollert samspill med omgivelsene, vil ensartets skarpe sammenheng gå tapt. Edwin Thompson Jaynes argumenterte for at uskarpheten er subjektiv, og tilsvarer ganske enkelt tap av kunnskap om systemets tilstand. Uansett, uansett hvor det skjer, er Gibbs entropiøkning irreversibel forutsatt at uskarpheten ikke kan reverseres.
Den nøyaktig utviklende entropien, som ikke øker, er kjent som finkornet entropi . Den uskarpe entropien er kjent som grovkornet entropi . Leonard Susskind analogiserer dette skillet med forestillingen om volumet av en fiberkule av bomull: På den ene siden er volumet av fibrene selv konstant, men på en annen måte er det et større grovkornet volum, som tilsvarer ballens omriss .
Gibbs entropi -økningsmekanisme løser noen av de tekniske vanskelighetene som finnes i Boltzmanns H -teorem: Gibbs -entropien svinger ikke, og den viser heller ikke Poincare -tilbakefall, og derfor er økningen i Gibbs -entropi, når den oppstår, derfor irreversibel som forventet av termodynamikk . Gibbs-mekanismen gjelder også like godt for systemer med svært få frihetsgrader, for eksempel enkeltpartikkelsystemet vist på figuren. I den grad man godtar at ensemblet blir uskarpt, er Gibbs tilnærming et renere bevis på termodynamikkens andre lov .
Dessverre, som påpekt tidlig i utviklingen av kvantestatistisk mekanikk av John von Neumann og andre, overfører ikke denne typen argument til kvantemekanikk. I kvantemekanikk kan ikke ensemblet støtte en stadig finere blandingsprosess, på grunn av den endelige dimensjonaliteten til den relevante delen av Hilbert-rommet. I stedet for å konvergere nærmere og nærmere likevektsensemblet (tidsgjennomsnittlig ensemble) som i det klassiske tilfellet, vil tetthetsmatrisen til kvantesystemet stadig vise evolusjon, til og med vise tilbakefall. Å utvikle en kvanteversjon av H -teoremet uten appell til Stosszahlansatz er dermed betydelig mer komplisert.
Se også
Merknader
Referanser
- Lifshitz, EM; Pitaevskii, LP (1981). Fysisk kinetikk . Kurs i teoretisk fysikk . 10 (3. utg.). Pergamon . ISBN 978-0-08-026480-6.
- Waldram, JR (1985). Teorien om termodynamikk . Cambridge University Press . ISBN 978-0-521-28796-8.
- Tolman, RC (1938). Prinsippene for statistisk mekanikk . Oxford University Press .
- Gull, SF (1989). "Noen misforståelser om entropi" . I Buck, B .; Macaulay, V. A (red.). Maksimal entropi i bruk . Oxford University Press (utgitt 1991). ISBN 978-0-19-853963-6. Arkivert fra originalen 2012-02-04.
- Reif, F. (1965). Grunnleggende om statistisk og termisk fysikk . McGraw-Hill . ISBN 978-0-07-051800-1.
- Gleick, J. (2011). Informasjonen: En historie, en teori, en flom . Random House Digital . ISBN 978-0-375-42372-7.
- Huang, Kerson (1987). Statistical Mechanics, 2ed . Random House Digital . ISBN 978-0-471-81518-1.
- Badino, M. (2011). "Mechanistic Slumber vs. Statistical Insomnia: The early history of Boltzmann's H-theorem (1868–1877)". European Physical Journal H . 36 (3): 353–378. Bibcode : 2011EPJH ... 36..353B . doi : 10.1140/epjh/e2011-10048-5 . S2CID 120302680 .


























