Pentacene - Pentacene
|
|
|
|
|
| Navn | |
|---|---|
|
Foretrukket IUPAC -navn
Pentacene |
|
| Andre navn
2,3: 6,7-Dibenzanthracene
Benzo [b] naftacen Dibenz [b, i] antracen NSC 90784 lin-Dibenzanthracene lin-Naphthoanthracene |
|
| Identifikatorer | |
|
3D -modell ( JSmol )
|
|
| 1912418 | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.004.722 |
| EC -nummer | |
| 733903 | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C 22 H 14 | |
| Molar masse | 278,354 g · mol −1 |
| Utseende | Mørkeblått pulver |
| Tetthet | 1,3 g cm −3 |
| Smeltepunkt | > 300 ° C (572 ° F; 573 K) sublimerer ved 372 ° C |
| Kokepunkt | 40–43 ° C (104–109 ° F; 313–316 K) ved 0,15 torr |
| -205,4 × 10 −6 cm 3 mol −1 | |
| Struktur | |
| Triclinic | |
| P-1 | |
|
Med mindre annet er angitt, gis data for materialer i standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox -referanser | |
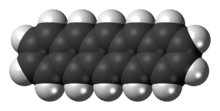
Pentacene er et polysyklisk aromatisk hydrokarbon som består av fem lineært smeltede benzenringer . Denne sterkt konjugerte forbindelsen er en organisk halvleder . Forbindelsen genererer eksitoner ved absorpsjon av ultrafiolett ( UV ) eller synlig lys ; dette gjør den veldig følsom for oksidasjon. Av denne grunn nedbrytes denne forbindelsen, som er et lilla pulver, sakte ved eksponering for luft og lys.
Strukturelt er pentacen en av de lineære acenene , den forrige var tetracen (fire smeltede benzenringer) og den neste var heksasen (seks smeltede benzenringer). I august 2009 ble en gruppe forskere fra IBM publiserte eksperimentelle resultatene av imaging en eneste molekyl av pentacen ved hjelp av en atommikroskop . I juli 2011 brukte de en modifikasjon av skanningstunnelmikroskopi for å eksperimentelt bestemme formene til de høyest okkuperte og laveste ubesatte molekylære orbitalene .
I 2012, pentacen dopet p -terphenyl ble vist å være effektive som forsterkeren medium for et rom-temperatur maser .
Syntese

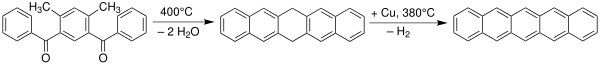
Pentacene ble først syntetisert i 1912 av britiske kjemikere William Hobson Mills og Mildred May Gostling . En klassisk metode for pentacensyntese er ved Elbs -reaksjonen .
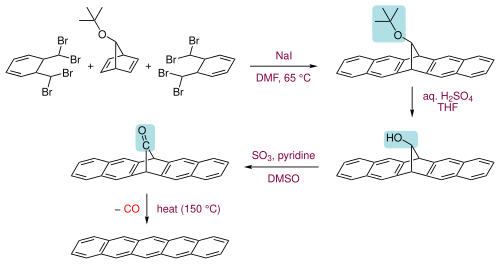
Pentacener kan også fremstilles ved ekstrudering av en liten flyktig komponent ( karbonmonoksid ) fra en passende forløper ved 150 ° C.
Selve forløperen fremstilles i tre trinn fra to molekyler av α, α, α ', α'-tetrabromo- o- xylen med en 7- tert- butoksybicyklo [2.2.1] hepta-2,5-dien ved første oppvarming med natriumjodid i dimetylformamid for å gjennomgå en rekke eliminasjons- og Diels – Alder -reaksjoner for å danne ringsystemet, deretter hydrolysere tert -butoksygruppen til en alkohol og etterfulgt av dens oksidasjon til ketonet .
Produktet er rapportert å ha en oppløselighet i kloroform og er derfor utsatt for spinnbelegg . Pentacen er løselig i varme klorerte benzener, slik som 1,2,4-triklorbenzen , hvorfra det kan omkrystalliseres for å danne blodplater.
Pentacenderivater
Monomeriske pentacenderivater
6,13-substituerte pentacener er tilgjengelige gjennom pentacenkinon ved reaksjon med en aryl- eller alkynylnukleofil (for eksempel Grignard eller organolitiumreagenser) etterfulgt av reduktiv aromatisering. En annen metode er basert på homologisering av diyner med overgangsmetaller (gjennom zirconacyclopentadienes) Funksjonalisering av pentacen har gjort det mulig å kontrollere solid-state-pakningen av denne kromoforen. Valget av substituentene (både størrelse og plassering av substitusjon på pentacen) påvirker solid-state-pakningen og kan brukes til å kontrollere om forbindelsen vedtar 1-dimensjonal eller 2-dimensjonal kofacial pi-stabling i solid-state, som i motsetning til sildebeinpakningen observert for pentacen.
Selv om pentacens struktur ligner strukturen til andre aromatiske forbindelser som antracen , er dens aromatiske egenskaper dårlig definert; som sådan er pentacen og dets derivater gjenstand for mye forskning.
Det er en tautomer kjemisk likevekt mellom 6-metylen-6,13-dihydropentacen og 6-metylpentacen.
Denne likevekten er helt til fordel for metylenforbindelsen. Bare ved oppvarming av en løsning av forbindelsen til 200 ° C utvikler en liten mengde pentacen seg, noe som fremgår av fremveksten av en rødfiolett farge. I følge en studie er reaksjonsmekanismen for denne likevekten ikke basert på et intramolekylært 1,5-hydridskift , men på en bimolekylær hydrogenering av frie radikaler . I kontrast aromatiseres lett isotoluener med det samme sentrale kjemiske motivet.
Pentacen reagerer med elementært svovel i 1,2,4-triklorbenzen til forbindelsen hexathiapentacene . Røntgenkrystallografi viste at alt karbon-til-svovel bindingslengder er omtrent like (170 pm ); av dette følger det at resonansstrukturene B og C med fullstendig ladningsseparasjon er mer signifikante enn struktur A.
I krystallfasen viser molekylene aromatiske stablingsinteraksjoner , hvorved avstanden mellom noen svovelatomer på nabomolekyler kan bli mindre (337 pm) enn summen av to Van der Waals radier (180 pm)
Som den beslektede tetrathiafulvalene , studeres denne forbindelsen innen organiske halvledere .
Akene kan fremstå som plane og stive molekyler, men faktisk kan de være veldig forvrengt. Pentacenen avbildet nedenfor:
har en ende-til-ende-vri på 144 ° og er sterisk stabilisert av de seks fenylgruppene . Forbindelsen kan oppløses i sine to enantiomerer med en uvanlig høy rapportert optisk rotasjon på 7400 ° selv om racemisering skjer med en kjemisk halveringstid på 9 timer.
Oligomerer og polymerer av pentacen
Oligomerer og polymerer basert på pentacen har blitt undersøkt både syntetisk og i enhetsapplikasjonsinnstillinger. Polymerlysemitterende dioder ( PLED ) er konstruert ved bruk av konjugerte kopolymerer ( 1a – b ) som inneholder fluoren og pentacen. Noen få andre konjugerte pentacenpolymerer ( 2a – b og 3 ) har blitt realisert basert på Sonogashira og Suzuki koblingsreaksjoner av en dibromopentacenmonomer. Ikke-konjugerte pentacenbaserte polymerer har blitt syntetisert via forestring av en pentacendiolmonomer med bis-syreklorider for å danne polymerer 4a – b .

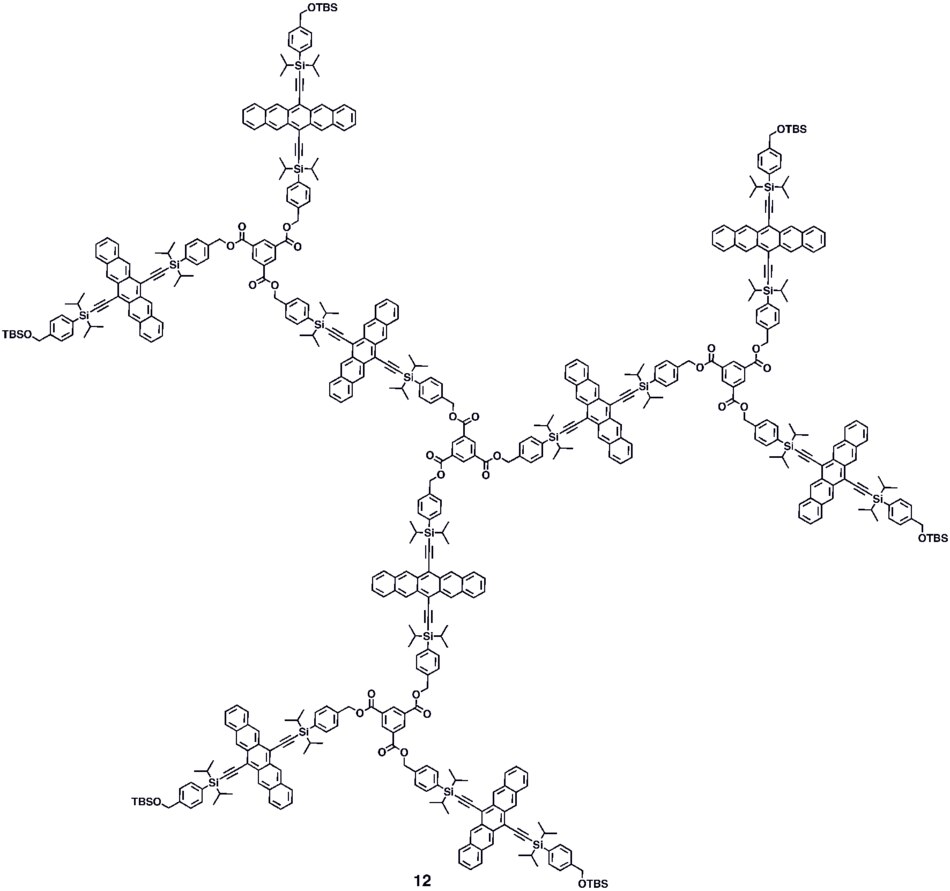
Ulike syntetiske strategier har blitt brukt for å danne konjugerte oligomerer av pentacen 5a – c, inkludert en en-gryte-fire-bindingsdannende prosedyre som ga en løsning-behandlingsbar konjugert pentacen-dimer ( 5c ) som viste fotokonduktiv forsterkning> 10, og plasserte ytelsen innenfor samme størrelsesorden som termisk fordampede filmer av ikke-funksjonalisert pentacen som viste fotoledende forsterkning> 16 ved bruk av analoge måleteknikker. Det er rapportert en modulær syntetisk metode for konjugerte pentacene di-, tri- og tetramerer ( 6–8 ) som er basert på homo- og krysskoblingsreaksjoner av robuste dehydropentacen-mellomprodukter. Ikke-konjugerte oligomerer 9–10 basert på pentacen har blitt syntetisert, inkludert dendrimerer 9–10 med opptil 9 pentacenenheter per molekyl med molar absorpsjon for den mest intense absorpsjonen> 2 000 000 M −1 • cm −1 . Dendrimere 11–12 ble vist å ha forbedret ytelse i enheter sammenlignet med analoge pentacenbaserte polymerer 4a – b i sammenheng med fotodetektorer.
Materialforskning
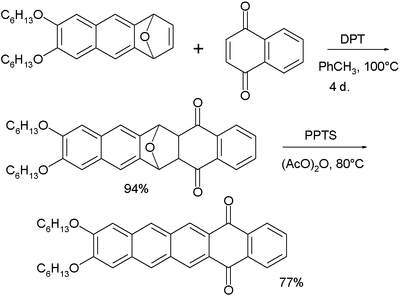
Pentacener har blitt undersøkt som potensielle dikroiske fargestoffer . Pentacenokinonen vist nedenfor er fluorescerende, og når den blandes med flytende krystall E7 -blanding, oppnås et dikroisk forhold på 8. Lengre acener justerer seg bedre i den nematiske flytende krystallfasen .
Kombinert med buckminsterfullerene , brukes pentacene i utviklingen av organiske solcelleprototyper. Organiske solceller er billigere og mer fleksible enn tradisjonelle uorganiske celler, som potensielt kan åpne dører til solceller i nye markeder.
Pentacene er et populært valg for forskning på organiske tynnfilmstransistorer og OFET , og er et av de mest grundig undersøkte konjugerte organiske molekylene med et høyt applikasjonspotensial på grunn av en hullmobilitet i OFETs på opptil 5,5 cm 2 /(V · s) , som overstiger det for amorft silisium.
Pentacen, så vel som andre organiske ledere, utsettes for rask oksidasjon i luft, noe som utelukker kommersialisering. Hvis pentacenen er preoksydert, er pentacen-kinon en potensiell gateisolator, da kan mobiliteten nærme seg rubren -den organiske halvlederen med høyest mobilitet-nemlig 40 cm 2 /(V · s). Denne pentacen -oksidasjonsteknikken er lik silisiumoksidasjonen som brukes i silisiumelektronikken.
Se også
Referanser
Eksterne linker
- fakta om pentacen , hentet 17. april 2006
- Organisk transistor forbedres med alderen , New Scientist, 2. desember 2007
- Pentacene Imaged , IBM -bilder Pentacene, det første molekylet som ble avbildet i detalj 29. august 2009