Embryooverføring - Embryo transfer
| Embryooverføring 123 | |
|---|---|
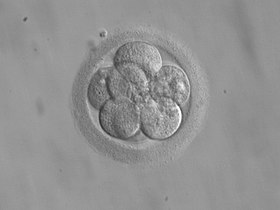 8-cellers embryo for overføring 3 dager etter befruktning
| |
| MeSH | D004624 |
Embryooverføring refererer til et trinn i prosessen med assistert reproduksjon der embryoer plasseres i livmoren til en hunn med den hensikt å etablere en graviditet . Denne teknikken (som ofte brukes i forbindelse med in vitro -fertilisering (IVF)), kan brukes hos mennesker eller hos dyr, i hvilke situasjoner målene kan variere.
Embryooverføring kan utføres på dag to eller dag tre, eller senere i blastocyststadiet , som først ble utført i 1984.
Faktorer som kan påvirke suksessen til embryooverføring inkluderer endometriemottaklighet, embryokvalitet og embryooverføringsteknikk.
Frisk kontra frossen
Embryoer kan enten være "ferske" fra befruktede eggceller i samme menstruasjonssyklus , eller "frosset", det vil si at de har blitt generert i en foregående syklus og gjennomgått embryokryokonservering , og tines opp like før overføringen, som deretter kalles "frossen embryooverføring" (FET). Resultatet av bruk av kryokonserverte embryoer har jevnt vært positivt uten økning i fødselsskader eller utviklingsavvik, også mellom ferske versus frosne egg som brukes til intracytoplasmatisk sædinjeksjon (ICSI). Faktisk øker graviditetsraten etter FET, og perinatale utfall påvirkes mindre, sammenlignet med embryooverføring i samme syklus som ovarial hyperstimulering ble utført. Den endometrium er antatt å ikke være optimalt forberedt for implantering etter ovarial hyperstimulering, og derfor frosne embryo transfer tilgjengelige ressurser for en separat syklus for å fokusere på å optimalisere sjansene for vellykket implantasjon. Barn født av forglassede blastocyster har betydelig høyere fødselsvekt enn de som er født fra ikke-frosne blastocyster. Ved overføring av en frossen-tint oocytt er sjansen for graviditet i hovedsak den samme, enten den overføres i en naturlig syklus eller en med eggløsning .
Det er sannsynligvis liten eller ingen forskjell mellom FET og ferske embryooverføringer når det gjelder livsfødselsrate og pågående graviditetsrate, og risikoen for ovarial hyperstimuleringssyndrom kan være mindre ved å bruke "fryse alt" -strategien. Risikoen for å få en baby i svangerskapsalderen og høyere fødselsrate, i tillegg til mors hypertensive forstyrrelser i svangerskapet, kan økes ved hjelp av en "fryse alt" -strategi.
Uterin forberedelse
Hos mennesker må livmorslimhinnen ( endometrium ) forberedes på riktig måte slik at embryoet kan implanteres. I en naturlig syklus foregår embryooverføringen i lutealfasen på et tidspunkt hvor foringen er passende uutviklet i forhold til statusen til det nåværende luteiniserende hormonet. I en stimulert eller syklus hvor et "frosset" embryo overføres, kan mottakerkvinnen gis først østrogenpreparater (ca. 2 uker), deretter en kombinasjon av østrogen og progesteron slik at foringen blir mottakelig for embryoet. Tid for mottakelighet er implantasjonsvinduet . En vitenskapelig gjennomgang i 2013 kom til den konklusjon at det ikke er mulig å identifisere en metode for forberedelse av endometrium ved frossen embryooverføring som mer effektiv enn en annen.
Begrenset bevis støtter også fjerning av livmorhalsslim før overføring.
Timing
Embryo kan utføres etter ulike varigheter av embryo kultur , overdragelse forskjellige stadier i embryogenese . Hovedstadiene der embryooverføring utføres er spaltningsstadium (dag 2 til 4 etter koinkubasjon ) eller blastocyststadiet (dag 5 eller 6 etter koinkubasjon ).
Fordi in vivo fortsatt befinner seg et spaltningsstadium i egglederen og det er kjent at livmorens ernæringsmiljø er forskjellig fra rørets, det antas at dette kan forårsake stress på embryoet hvis det overføres på dag 3. i redusert implantasjonspotensial. Et blastocyststadiumembryo har ikke dette problemet, da det er best egnet for livmormiljøet [1]
Embryoer som når cellefasen på dag 3 kan testes for kromosomale eller spesifikke genetiske defekter før mulig overføring ved preimplantasjonsgenetisk diagnose (PGD). Overføring på blastocyststadiet gir en betydelig økning i levende fødselsrate per overføring, men gir også et redusert antall embryoer tilgjengelig for overføring og embryokryokonservering , så de kumulative kliniske graviditetsratene økes med spaltningsstadiet. Det er usikkert om det er noen forskjell i levende fødselsrate mellom overføring på dag to eller dag tre etter befruktning.
Monozygotisk tvilling blir ikke økt etter overføring av blastocyst sammenlignet med embryooverføring i spaltningsstadium .
Det er en betydelig høyere sjanse for prematur fødsel ( oddsforhold 1.3) og medfødte anomalier ( oddsforhold 1.3) blant fødsler som har nådd blastocyststadiet sammenlignet med spaltningsstadium. På grunn av økt embryodødelighet hos kvinner på grunn av epigenetiske modifikasjoner forårsaket av utvidet kultur, fører blastocystoverføring til flere mannlige fødsler (56,1% hann) mot 2 eller 3 dagers overføring (et normalt kjønnsforhold på 51,5% mann).
Valg av embryo
Laboratorier har utviklet graderingsmetoder for å bedømme eggløsning og embryokvalitet . For å optimalisere graviditetsraten er det betydelige bevis på at et morfologisk scoringssystem er den beste strategien for valg av embryoer. Siden 2009 hvor det første time-lapse-mikroskopisystemet for IVF ble godkjent for klinisk bruk, har morfokinetiske scoringssystemer vist seg å forbedre seg til graviditetsfrekvensen ytterligere. Imidlertid, når alle forskjellige typer tidsforløpende embryoavbildningsenheter, med eller uten morfokinetiske scoringssystemer, sammenlignes med konvensjonell embryovurdering for IVF, er det utilstrekkelig bevis på en forskjell i levende fødsel, graviditet, dødfødsel eller spontanabort for å velge mellom dem. En liten prospektivt randomisert studie i 2016 rapporterte dårligere embryokvalitet og mer personaltid i en automatisk time-lapse embryo imaging enhet sammenlignet med konvensjonell embryologi. En aktiv innsats for å utvikle en mer nøyaktig analyse av embryoseleksjon basert på kunstig intelligens og dyp læring pågår. Embryo Ranking Intelligent Classification Algorithm (ERICA), er et tydelig eksempel. Denne Deep Learning-programvaren erstatter manuelle klassifiseringer med et rangeringssystem basert på et individuelt embryos forutsagte genetiske status på en ikke-invasiv måte. Studier på dette området venter fortsatt, og gjeldende mulighetsstudier støtter potensialet.
Fremgangsmåte
Embryooverføringsprosedyren starter med å plassere et spekulum i skjeden for å visualisere livmorhalsen, som renses med saltoppløsning eller kulturmedier. Et mykt overføringskateter lastes med embryoene og overleveres til klinikeren etter bekreftelse av pasientens identitet. Kateteret settes inn gjennom livmorhalskanalen og føres inn i livmorhulen.
Det er gode og konsekvente bevis på fordeler ved ultralydveiledning , det vil si å lage en abdominal ultralyd for å sikre riktig plassering, som er 1-2 cm fra livmorfonden. Det er tegn på en signifikant økning i klinisk graviditet ved bruk av ultralydveiledning sammenlignet med bare "klinisk berøring". Anestesi er vanligvis ikke nødvendig. Spesielt enkle embryooverføringer krever nøyaktighet og presisjon i plassering i livmorhulen. Det optimale målet for embryo plassering, kjent som maksimal implantasjon potensial (MIP) punkt, er identifisert ved hjelp av 3D/4D ultralyd. Imidlertid er det begrenset bevis som støtter avsetning av embryoer i livmors midtdel.
Etter innføring av kateteret blir innholdet utvist og embryoene deponert. Begrenset bevis støtter prøveoverføringer før du utfører prosedyren med embryoer. Etter utvisning har varigheten som kateteret forblir inne i livmoren ingen effekt på graviditetsfrekvensen. Begrenset bevis tyder på at man unngår negativt trykk fra kateteret etter utvisning. Etter tilbaketrekning blir kateteret overlevert til embryologen, som inspiserer det for beholdte embryoer.
I prosessen med zygote intrafallopian transfer (ZIFT), blir egg fjernet fra kvinnen, befruktet og deretter plassert i kvinnens eggleder i stedet for livmoren.
Embryonummer
Et stort problem er hvor mange embryoer som skal overføres, siden plassering av flere embryoer medfører risiko for multippel graviditet. Mens tidligere leger plasserte flere embryoer for å øke sjansen for graviditet, har denne tilnærmingen falt i unåde. Profesjonssamfunn og lovgivere i mange land har gitt retningslinjer eller lover for å begrense praksisen. Det er lave til moderate bevis for at en dobbel embryooverføring i løpet av en syklus oppnår en høyere levende fødselsrate enn en enkelt embryooverføring; men å gjøre to enkle embryooverføringer i to sykluser har samme levende fødselsrate og ville unngå flere graviditeter.
Det riktige antallet embryoer som skal overføres, avhenger av kvinnenes alder, om det er første, andre eller tredje hele IVF-syklusforsøk og om det er embryoer av topp kvalitet tilgjengelig. I henhold til en retningslinje fra National Institute for Health and Care Excellence (NICE) i 2013, bør antall embryoer som overføres i en syklus velges som i følgende tabell:
| Alder | Forsøk nr. | Embryoer overført |
|---|---|---|
| <37 år | 1. | 1 |
| 2. | 1 hvis topp kvalitet | |
| 3. | Ikke mer enn 2 | |
| 37–39 år | 1. og 2. | 1 hvis topp kvalitet |
| 2 hvis ingen topp kvalitet | ||
| 3. | Ikke mer enn 2 | |
| 40–42 år | 2 |
e-SET
Teknikken med å velge bare ett embryo for å overføre til kvinnen kalles elektiv-enkelt embryooverføring ( e-SET ), eller når embryoer er på blastocyststadiet, kan det også kalles elektiv enkeltblastocystoverføring (eSBT) . Det reduserer risikoen for flere graviditeter betydelig, sammenlignet med f.eks. Double Embryo Transfer (DET) eller double blastocyst transfer (2BT), med en vennskapshastighet på omtrent 3,5% i sET sammenlignet med omtrent 38% i DET, eller 2% i eSBT sammenlignet med omtrent 25% i 2BT. Samtidig er graviditetsraten ikke signifikant lavere med eSBT enn med 2BT. Det vil si at den kumulative levende fødselsraten forbundet med enkelt fersk embryooverføring etterfulgt av en enkelt frosset og tint embryooverføring er sammenlignbar med den etter en syklus med dobbel fersk embryooverføring. Videre har SET bedre resultater når det gjelder gjennomsnittlig svangerskapsalder ved fødsel, leveringsmåte, fødselsvekt og risiko for neonatal intensivavdeling enn DET. e-SET av embryoer på spaltningsstadiet reduserer sannsynligheten for levende fødsel med 38% og flerfødsel med 94%. Bevis fra randomiserte, kontrollerte studier tyder på at økning av antall e-SET-forsøk (ferske og/eller frosne) resulterer i en kumulativ levende fødselsrate som ligner på DET.
Bruken av enkelt embryooverføring er høyest i Sverige (69,4%), men så lavt som 2,8% i USA. Tilgang til offentlig finansiering av ART, tilgjengelighet av gode kryokonserveringsfasiliteter , effektiv utdannelse om risikoen ved multippel graviditet og lovgivning ser ut til å være de viktigste faktorene for regional bruk av enkelt embryooverføring. Personlig valg spiller også en viktig rolle ettersom mange subfertile par har en sterk preferanse for tvillinger.
Tilleggsprosedyrer
Det er usikkert om bruk av mekanisk lukking av livmorhalskanalen etter embryooverføring har noen effekt.
Hvorvidt kvinner blir liggende i en viss tid etter embryooverføring, kan gjøre liten eller ingen forskjell.
Bruk av hyaluronsyre som et adherensmedium for embryoet kan øke fødselsraten. Det kan være liten eller fordel med full blære, fjerning av livmorhalsslim eller spyling av endometrial eller endocervikal hulrom på tidspunktet for embryooverføring. Tilskuddsantibiotika i form av amoksicillin pluss klavulansyre øker sannsynligvis ikke den kliniske graviditetsraten sammenlignet med ingen antibiotika.
For frossen-tint embryooverføring eller overføring av embryo fra eggdonasjon , er det ikke nødvendig med tidligere ovarial hyperstimulering for mottakeren før overføring, som kan utføres i spontane eggløsningssykluser. Likevel finnes det forskjellige protokoller for frossen-tint embryooverføring også, for eksempel protokoller med hyperstimulering av eggstokkene , protokoller der endometrium kunstig fremstilles av østrogen og/eller progesteron . Det er noen bevis for at i sykluser der endometrium kunstig fremstilles av østrogen eller progesteron, kan det være gunstig å administrere et ekstra legemiddel som undertrykker hormonproduksjonen fra eggstokkene, for eksempel kontinuerlig administrering av en gonadotropinfrigivende hormonagonist (GnRHa). For eggdonasjon , det er tegn på en lavere graviditetsfrekvens og høyere syklus avbestillings hastighet når progesteron tilskudd i resipienten er påbegynt før til eggcelle henting fra donor, sammenlignet med påbegynt dag av egg henting eller dagen etter.
Sædvæske inneholder flere proteiner som interagerer med epitelceller i livmorhalsen og livmoren , noe som induserer aktiv svangerskapstemperatur . Det er signifikant forbedrede resultater når kvinner utsettes for sædplasma rundt embryooverføringstidspunktet, med statistisk signifikans for klinisk graviditet , men ikke for pågående graviditet eller levende fødselsrater med de begrensede tilgjengelige dataene.
Følge opp
Pasienter starter vanligvis progesteronmedisinering etter egg (også kalt oocytt). Mens daglige intramuskulære injeksjoner av progesteron-i-olje (PIO) har vært standard administrasjonsvei, er PIO-injeksjoner ikke FDA-godkjent for bruk under graviditet. En nylig metaanalyse viste at den intravaginale ruten med en passende dose og doseringsfrekvens tilsvarer daglige intramuskulære injeksjoner. I tillegg viste en nylig case-matchet studie som sammenlignet vaginalt progesteron med PIO-injeksjoner at levende fødselsrater var nesten identiske med begge metodene. En varighet av progesteronadministrasjon på 11 dager resulterer i nesten samme fødselsrate som lengre varighet.
Pasienter får også østrogenmedisin i noen tilfeller etter embryooverføringen. Graviditetstesting utføres vanligvis to uker etter egguttak.
Tredjeparts reproduksjon
Det er ikke nødvendig at embryooverføringen utføres på hunnen som ga eggene. Dermed kan en annen kvinne hvis livmor er riktig forberedt, motta embryoet og bli gravid. Embryooverføring kan brukes der en kvinne som har egg men ikke har livmor og ønsker å få en biologisk baby; hun ville kreve hjelp av en svangerskapsbærer eller surrogat for å bære graviditeten. Også en kvinne som ikke har egg, men en livmor, kan bruke eggdonor IVF, i så fall vil en annen kvinne gi egg til befruktning og de resulterende embryoene plasseres i livmoren til pasienten. Befruktning kan utføres ved bruk av kvinnens partners sædceller eller ved bruk av donorsæd. "Ekstra" embryoer som er opprettet for et annet par som gjennomgår IVF -behandling, men som deretter er overskudd til parets behov, kan også overføres (kalt embryodonasjon ). Embryoer kan opprettes spesielt ved bruk av egg og sæd fra donorer, og disse kan deretter overføres til livmoren til en annen kvinne. En surrogat kan bære en baby som er produsert ved embryooverføring for et annet par, selv om verken hun eller 'bestillingsparet' er biologisk knyttet til barnet. Tredjeparts reproduksjon er kontroversiell og regulert i mange land. Personer som går inn i svangerskaps -surrogati -ordninger må forstå en helt ny type forhold som ikke passer til noen av de tradisjonelle manusene vi bruker for å kategorisere forhold som slektskap, vennskap, romantisk partnerskap eller markedsforhold. Surrogater har opplevelsen av å bære en baby som de forestiller seg som ikke av sin egen slektning, mens tiltenkte mødre har opplevelsen av å vente gjennom ni måneders graviditet og overgå til morskap utenfra den gravide kroppen. Dette kan føre til nye konseptualiseringer av kropp og selv.
Historie
Den første overføringen av et embryo fra et menneske til et annet som resulterte i graviditet ble rapportert i juli 1983 og førte deretter til kunngjøringen av den første menneskelige fødselen 3. februar 1984. Denne prosedyren ble utført ved Harbor UCLA Medical Center under ledelse av Dr. John Buster og University of California ved Los Angeles School of Medicine.
I prosedyren ble et embryo som nettopp begynte å utvikle overført fra en kvinne der det var unnfanget ved kunstig befruktning til en annen kvinne som fødte barnet 38 uker senere. Sædcellen som ble brukt i kunstig befruktning kom fra mannen til kvinnen som fødte babyen.
Dette vitenskapelige gjennombruddet etablerte standarder og ble en forandringsagent for kvinner som lider av infertilitetsplager og for kvinner som ikke ønsket å gi genetiske lidelser videre til barna sine. Donorembryooverføring har gitt kvinner en mekanisme for å bli gravid og føde et barn som vil inneholde ektemannens genetiske sammensetning. Selv om donorembryooverføring som praktisert i dag har utviklet seg fra den opprinnelige ikke-kirurgiske metoden, står den nå for omtrent 5% av in vitro-befruktning registrerte fødsler.
Før dette hadde tusenvis av kvinner som var ufruktbare , adopsjon som den eneste veien til foreldreskap. Dette satte scenen for å tillate åpen og ærlig diskusjon om embryodonasjon og overføring. Dette gjennombruddet har gitt plass for donasjon av menneskelige embryoer som en vanlig praksis som ligner på andre donasjoner som blod og større organdonasjoner. På tidspunktet for denne kunngjøringen ble hendelsen fanget opp av store nyhetsbærere og drev med sunn debatt og diskusjon om denne praksisen som påvirket fremtiden for reproduktiv medisin ved å skape en plattform for ytterligere fremskritt i kvinnens helse.
Dette arbeidet etablerte det tekniske grunnlaget og det juridisk-etiske rammeverket rundt klinisk bruk av donasjon av menneskelig oocytt og embryo , en vanlig klinisk praksis, som har utviklet seg de siste 25 årene.
Effektivitet
En systematisk gjennomgang av Cochrane som ble oppdatert i 2012 viste at overføring av blastocyststadium er mer effektiv enn spaltning (dag 2 eller 3) trinnoverføring i assistert reproduksjonsteknologi. Det viste en liten forbedring i levende fødselsrate per par for overføring av blastocyst. Dette ville bety at for en typisk rate på 31% på klinikker som bruker tidlige sykluser i spaltningsfasen, ville frekvensen øke til 32% til 42% levendefødte hvis klinikker brukte blastocystoverføring. Nylig systematisk gjennomgang viste at sammen med valg av embryo kan teknikkene som ble fulgt under overføringsprosedyren resultere i et vellykket graviditetsresultat. Følgende inngrep støttes av litteraturen for å forbedre graviditeten:
• Abdominal ultralydveiledning for embryooverføring
• Fjerning av slim i livmorhalsen
• Bruk av myke embryooverføringskatetre
• Plassering av embryooverføringsspiss i det øvre eller midtre (sentrale) området av livmorhulen, større enn 1 cm fra fundus, for embryoutvisning
• Umiddelbar ambulering når embryooverføringsprosedyren er fullført
Embryooverføring hos dyr
Embryooverføringsteknikker gjør at kvinnelige husdyr av høy kvalitet kan ha større innflytelse på den genetiske utviklingen av en flokk eller flokk på omtrent samme måte som kunstig befruktning har tillatt større bruk av overordnede fedre. ET tillater også fortsatt bruk av dyr som konkurransehopper å fortsette å trene og vise, mens de produserer føll . De generelle epidemiologiske aspektene ved embryooverføring indikerer at overføring av embryoer gir mulighet til å introdusere genetisk materiale i populasjoner av husdyr samtidig som risikoen for overføring av smittsomme sykdommer reduseres sterkt. Den siste utviklingen innen kjønn av embryoer før overføring og implantasjon har et stort potensial i meieri og andre husdyrindustrier.
Embryooverføring brukes også i laboratoriemus . For eksempel kan embryoer av genmodifiserte stammer som er vanskelige å avle eller dyre å vedlikeholde lagres frosset, og bare tines og implanteres i en pseudopregnant demning når det er nødvendig.
19. februar 2020 ble det første paret Cheetah -unger som ble unnfanget gjennom embryooverføring fra en surrogat gepard -mor født i Columbus Zoo i Ohio.
Frossen embryooverføring hos dyr
Utviklingen av forskjellige fremgangsmåter for kryokonservering av bovine embryoer forbedret embryo teknikk betraktelig effektiv teknologi, ikke lenger er avhengig av den umiddelbare beredskap av egnede mottakere. Graviditetsraten er bare litt lavere enn de som oppnås med ferske embryoer. Nylig har bruk av kryobeskyttende midler som etylenglykol tillatt direkte overføring av storfeembryoer. Verdens første levende kryssede storfe som ble produsert under tropiske forhold ved Direct Transfer (DT) av embryo frosset i etylenglykol -frysemedier ble født 23. juni 1996. Dr. Binoy Sebastian Vettical fra Kerala Livestock Development Board Ltd har produsert embryoet lagret frosset i Etylenglykol frysemedier med langsom programmerbar fryse (SPF) teknikk og overføres direkte til mottaker storfe umiddelbart etter tining av frosne halm i vann for fødselen av denne kalv. I en studie ble in vivo produserte kryssbredde storfeembryoer lagret frosset i etylenglykol -frysemedier overført direkte til mottakere under tropiske forhold og oppnådde en graviditetsrate på 50 prosent. I en undersøkelse av den nordamerikanske embryooverføringsindustrien var suksessratene for embryooverføring fra direkte overføring av embryoer like gode som de som ble oppnådd med glyserol . I 2011 ble mer enn 95% av frosne tine embryoer i 2011 overført ved direkte overføring.


