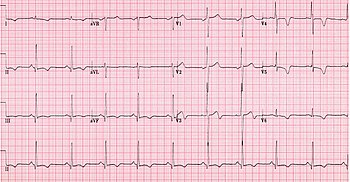
Hypertrofisk kardiomyopati - Hypertrophic cardiomyopathy
| Hypertrofisk kardiomyopati | |
|---|---|
| Andre navn | Asymmetrisk septal hypertrofi; idiopatisk hypertrofisk subaortisk stenose; hypertrofisk obstruktiv kardiomyopati (HOCM) |
 | |
| Spesialitet | Kardiologi |
| Symptomer | Trøtthet, hevelse i benet , kortpustethet , brystsmerter , besvimelse |
| Komplikasjoner | Hjertesvikt , uregelmessig hjerterytme , plutselig hjertedød |
| Årsaker | Genetikk , Fabrys sykdom , Friedreichs ataksi , visse medisiner |
| Diagnostisk metode | Elektrokardiogram , ekkokardiogram , stresstesting , gentesting |
| Differensialdiagnose | Hypertensiv hjertesykdom , aortastenose , idrettsutøverens hjerte |
| Behandling | Medisiner, implanterbar hjertestarter , kirurgi |
| Medisinering | Betablokkere , diuretika , disopyramid |
| Prognose | Mindre enn 1% per år dødsrisiko (med behandling) |
| Frekvens | 1 av 500 mennesker |
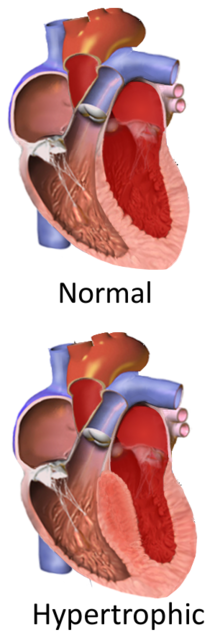
Hypertrofisk kardiomyopati ( HCM eller HOCM når den er obstruktiv ) er en tilstand der hjertet blir tykkere uten en åpenbar årsak. De delene av hjertet som er mest berørt er det interventrikulære septum og ventriklene. Dette resulterer i at hjertet er mindre i stand til å pumpe blod effektivt og kan også forårsake problemer med elektrisk ledning.
Personer som har HCM kan ha en rekke symptomer. Folk kan være symptomfrie, eller kan ha tretthet , hevelse i bein og kortpustethet . Det kan også resultere i brystsmerter eller besvimelse . Symptomer kan være verre når personen er dehydrert. Komplikasjoner kan omfatte hjertesvikt , uregelmessig hjerterytme og plutselig hjertedød .
HCM er oftest arvet fra en persons foreldre i et autosomalt dominerende mønster. Det skyldes ofte mutasjoner i visse gener som er involvert i å lage hjertemuskelproteiner . Andre arvelige årsaker til venstre ventrikkelhypertrofi kan omfatte Fabrys sykdom , Friedreichs ataksi og visse medisiner som takrolimus . Andre hensyn til årsakene til forstørret hjerte er idrettsutøverens hjerte og hypertensjon (høyt blodtrykk). Diagnostisering av HCM innebærer ofte en familiehistorie eller stamtavle , et elektrokardiogram , ekkokardiogram og stresstesting . Genetisk testing kan også utføres. HCM kan skilles fra andre arvelige årsaker til kardiomyopati ved sitt autosomalt dominerende mønster, mens Fabrys sykdom er X-bundet og Friedreichs ataksi arves i et autosomalt recessivt mønster.
Behandlingen kan avhenge av symptomer og andre risikofaktorer. Medisiner kan omfatte bruk av betablokkere eller disopyramid . En implanterbar hjertestarter kan anbefales hos de med visse typer uregelmessig hjerterytme. Kirurgi, i form av en septal myektomi eller hjertetransplantasjon , kan utføres hos de som ikke forbedrer seg med andre tiltak. Med behandling er risikoen for død av sykdommen mindre enn en prosent per år.
HCM rammer omtrent én av 500 mennesker. Prisene for menn og kvinner er omtrent like store. Folk i alle aldre kan bli påvirket. Den første moderne beskrivelsen av sykdommen var av Donald Teare i 1958.
Tegn og symptomer
Årsaken til HCM er variabel. Mange mennesker er asymptomatiske eller mildt symptomatiske, og mange av dem som bærer sykdomsgener for HCM, har ikke klinisk påviselig sykdom. De symptomer på HCM inkluderer kortpustethet på grunn av stivning og redusert blod fylling av ventriklene, brystsmerter ved anstrengelse (også kjent som angina ) på grunn av redusert blodstrøm til koronararteriene, ubehagelig bevissthet om hjerteslag ( hjertebank ), så vel som forstyrrelse av det elektriske systemet som går gjennom den unormale hjertemuskelen, ørhet , svakhet, besvimelse og plutselig hjertedød .
Kortpustethet skyldes i stor grad økt stivhet i venstre ventrikkel (LV), noe som svekker fyllingen av ventriklene, men også fører til forhøyet trykk i venstre ventrikkel og venstre atrium, noe som forårsaker mottrykk og interstitiell overbelastning i lungene. Symptomer er ikke nært knyttet til tilstedeværelsen eller alvorlighetsgraden av en utløpskanalsgradient. Ofte etterligner symptomene symptomer på kongestiv hjertesvikt (spesielt aktivitetsintoleranse og dyspné), men behandlingen er forskjellig. Betablokkere brukes i begge tilfeller, men behandling med diuretika, en bærebjelke i CHF -behandling, vil forverre symptomene ved hypertrofisk obstruktiv kardiomyopati ved å redusere ventrikkelforspenningsvolumet og derved øke utstrømningsmotstanden (mindre blod for å skyve til side det fortykkede hindrende vevet).
Store risikofaktorer for plutselig død hos personer med HCM inkluderer tidligere hjertestans eller ventrikelflimmer , spontan vedvarende ventrikulær takykardi , unormalt blodtrykk i øvelsen og ikke-vedvarende ventrikulær takykardi, uforklarlig synkope , familiehistorie med for tidlig plutselig død og større tykkelse på LVW enn 15 mm til 30 mm, på ekkokardiogram.
"Spike and dome" puls og "triple ripple apical impuls " er to andre tegn som kan oppdages ved fysisk undersøkelse.
Genetikk
| Gene | Lokus | Type |
|---|---|---|
| MYH7 | 14q12 | CMH1 ( 192600 ) |
| TNNT2 | 1q32 | CMH2 ( 115195 ) |
| TPM1 | 15q22.1 | CMH3 ( 115196 ) |
| MYBPC3 | 11p11.2 | CMH4 ( 115197 ) |
| ? | ? | CMH5 |
| PRKAG2 | 7q36 | CMH6 ( 600858 ) |
| TNNI3 | 19q13.4 | CMH7 ( 613690 ) |
| MYL3 | 3p | CMH8 ( 608751 ) |
| TTN | 2q24.3 | CMH9 ( 613765 ) |
| MYL2 | 12q23-q24 | CMH10 ( 608758 ) |
| ACTC1 | 15q14 | CMH11 ( 612098 ) |
| CSRP3 | 11p15.1 | CMH12 ( 612124 ) |
Familiær hypertrofisk kardiomyopati er arvet som et autosomalt dominant trekk og skyldes mutasjoner i ett av et antall gener som koder for de sarkomere proteiner .
For tiden vil omtrent 50–60% av mennesker med høy indeks for klinisk mistanke om HCM ha en mutasjon identifisert i minst ett av ni sarkomiske gener. Omtrent 40% av disse mutasjonene forekommer i β- myosin-tungkjedegenet på kromosom 14 q11.2-3, og omtrent 40% involverer det hjertemyosinbindende protein C- genet. Siden HCM vanligvis er et autosomalt dominerende trekk, har barn til en enkelt HCM-forelder 50% sjanse for å arve den sykdomsfremkallende mutasjonen. Når en slik mutasjon er identifisert, kan familiespesifikk genetisk testing brukes til å identifisere slektninger som er utsatt for sykdommen, selv om klinisk alvorlighetsgrad og alder for begynnelsen ikke kan forutsies.
Hos personer uten en familiehistorie av HCM, er den vanligste årsaken til sykdommen en de novo mutasjon av genet som produserer β-myosin tung kjede.
En innsetting/sletting polymorfisme i genet som koder for angiotensinkonverterende enzym (ACE) endrer den kliniske fenotypen av sykdommen. D/D (sletting/sletting) genotypen til ACE er assosiert med mer markert hypertrofi i venstre ventrikkel og kan være assosiert med høyere risiko for bivirkninger.
Noen mutasjoner kan ha mer skadelig potensial sammenlignet med andre (β-myosin tung kjede). For eksempel var troponin T -mutasjoner opprinnelig assosiert med en 50% dødelighet før fylte 40 år. Imidlertid fant en nyere og større studie en lignende risiko for andre sarkomeriske proteinmutasjoner. Alderen ved sykdomsutbrudd av HCM med MYH7 er tidligere og fører til mer alvorlige symptomer. Videre kan mutasjoner på troponin C endre Ca +2 -følsomhet for kraftutvikling i hjertemuskulaturen. Disse mutasjonene er oppkalt etter aminosyren som ble endret etter stedet der det skjedde, for eksempel A8V , A31S, C84Y og D145E .
Diagnose
En diagnose av hypertrofisk kardiomyopati er basert på en rekke funksjoner i sykdomsprosessen. Selv om det er bruk av ekkokardiografi , hjertekateterisering eller hjerte -MR ved diagnosen av sykdommen, inkluderer andre viktige hensyn EKG , genetisk testing (selv om det ikke først og fremst brukes til diagnose), og enhver familiehistorie av HCM eller uforklarlig plutselig død ved ellers sunne enkeltpersoner. I omtrent 60 til 70% av tilfellene viser hjerte -MR fortykning av mer enn 15 mm av den nedre delen av ventrikkelseptum. T1-vektet bildebehandling kan identifisere arrdannelse i hjertevev mens T2-vektet bildebehandling kan identifisere ødem og betennelse i hjertevev som er forbundet med akutte kliniske tegn på brystsmerter og besvimelse.
Pulsus bisferiens kan av og til bli funnet under undersøkelsen.
Varianter
Avhengig av om forvrengning av normal hjerteanatomi forårsaker en obstruksjon av blodstrømmen fra hjerteets venstre ventrikkel, kan HCM klassifiseres som obstruktiv eller ikke-obstruktiv. Den obstruktive varianten av HCM er hypertrofisk obstruktiv kardiomyopati ( HOCM ), også historisk kjent som idiopatisk hypertrofisk subaortisk stenose ( IHSS ) eller asymmetrisk septal hypertrofi ( ASH ).
En annen, ikke-obstruktiv variant av HCM er apikal hypertrofisk kardiomyopati ( AHC ), også kalt Yamaguchi syndrom . Det ble først beskrevet hos individer av japansk avstamning.
Hjertekateterisering

AO = synkende aorta; LV = Venstre ventrikkel; EKG = elektrokardiogram.
Etter det tredje QRS -komplekset har ventrikelen mer tid til å fylle. Siden det er mer tid til å fylle, vil venstre ventrikkel ha mer volum på slutten av diastolen (økt forspenning ). På grunn av Frank -Starling -loven i hjertet , vil sammentrekningen av venstre ventrikkel (og trykket generert av venstre ventrikkel) være større på den påfølgende takten (slag #4 i dette bildet). På grunn av den dynamiske naturen til utstrømningsobstruksjonen i HCM, øker obstruksjonen mer enn trykkene i venstre ventrikkel. Dette forårsaker et fall i aortatrykket når trykket i venstre ventrikkel stiger (sett på som det gule, skyggelagte området på bildet).
Ved hjertekateterisering kan katetre plasseres i venstre ventrikkel og den stigende aorta , for å måle trykkforskjellen mellom disse strukturene. Hos normale individer, i løpet av ventrikulær systole , trykket i den oppstigende aorta og venstre hjertekammer vil jevne seg ut og aorta ventilen er åpen. Hos personer med aortastenose eller med HCM med en utgangskanalgradient, vil det være en trykkgradient (forskjell) mellom venstre ventrikkel og aorta, med venstre ventrikkeltrykk høyere enn aortatrykket. Denne gradienten representerer graden av obstruksjon som må overvinnes for å kaste ut blod fra venstre ventrikkel.
Brockenbrough - Braunwald - Morrow -tegnet observeres hos personer med HCM med utløpskanalsgradient. Dette tegnet kan brukes til å skille HCM fra aortastenose. Hos personer med aortastenose, etter en for tidlig ventrikulær sammentrekning (PVC), vil følgende ventrikelsammentrekning være mer kraftig, og trykket som genereres i venstre ventrikkel vil være høyere. På grunn av den faste obstruksjonen som den stenotiske aortaklaffen representerer, vil aortetrykket etter PVC også stige. Hos personer med HCM vil imidlertid obstruksjonsgraden øke mer enn sammentrekningskraften i post-PVC-takten. Resultatet av dette er at venstre ventrikkeltrykk øker og det stigende aortatrykket synker , med en økning i LVOT -gradienten.
Mens Brockenbrough-Braunwald-Morrow-tegnet er mest dramatisk demonstrert ved bruk av samtidige intra-hjerte- og intra-aortakateter, kan det sees på rutinemessig fysisk undersøkelse som en reduksjon i pulstrykket i post-PVC-beat hos personer med HCM.
Screening
Selv om HCM kan være asymptomatisk, kan berørte individer vise symptomer fra mild til kritisk hjertesvikt og plutselig hjertedød når som helst fra tidlig barndom til ansiennitet. HCM er den viktigste årsaken til plutselig hjertedød hos unge idrettsutøvere i USA, og den vanligste genetiske kardiovaskulære lidelsen. En studie fant at forekomsten av plutselig hjertedød hos unge konkurransedyktige idrettsutøvere falt i Veneto -regionen i Italia med 89% siden introduksjonen av rutinemessig hjertescreening for idrettsutøvere i 1982, fra en uvanlig høy startrate. Fra og med 2010 har imidlertid studier vist at forekomsten av plutselig hjertedød, blant alle mennesker med HCM, har sunket til en prosent eller mindre. Screen-positive individer som er diagnostisert med hjertesykdom blir vanligvis fortalt å unngå konkurransedyktig friidrett.
HCM kan detekteres med et ekkokardiogram (ECHO) med 80%+ nøyaktighet, som kan foregå med screening med et elektrokardiogram (EKG) for å teste for hjerteavvik. Hjertemagnetisk resonansavbildning (CMR), betraktet som gullstandarden for å bestemme de fysiske egenskapene til venstre ventrikkelvegg, kan tjene som et alternativt screeningsverktøy når et ekkokardiogram gir avgjørende resultater. For eksempel kan identifiseringen av segmental lateral ventrikkelhypertrofi ikke oppnås med ekkokardiografi alene. Også venstre ventrikulær hypertrofi kan være fraværende hos barn under tretten år. Dette undergraver resultatene av ekkokardiogrammer før ungdom. Forskere har imidlertid studert asymptomatiske bærere av en HCM-forårsakende mutasjon ved bruk av CMR og har vært i stand til å identifisere krypter i det interventrikulære septalvevet hos disse menneskene. Det har blitt foreslått at dannelsen av disse kryptene er en indikasjon på myocyttforstyrrelse og endrede karvegger som senere kan resultere i det kliniske uttrykket for HCM. En mulig forklaring på dette er at den typiske samling av familiehistorie bare fokuserer på om plutselig død skjedde eller ikke. Den klarer ikke å anerkjenne alderen da pårørende fikk plutselig hjertedød, så vel som frekvensen av hjertehendelsene. Gitt de flere faktorene som er nødvendige for å bli vurdert som risiko for plutselig hjertedød, mens de fleste faktorene ikke har sterk prediktiv verdi individuelt, eksisterer det uklarhet når det skal implementeres spesialbehandling.
forente stater
Det er flere potensielle utfordringer knyttet til rutinemessig screening for HCM i USA. For det første er den amerikanske idrettsbefolkningen på 15 millioner nesten dobbelt så stor som Italias estimerte utøverpopulasjon. For det andre er disse hendelsene sjeldne, med færre enn 100 dødsfall i USA på grunn av HCM hos konkurrerende idrettsutøvere per år, eller omtrent 1 dødsfall per 220 000 idrettsutøvere. Til slutt vil genetisk testing gi en endelig diagnose; På grunn av de mange HCM-forårsakende mutasjonene er imidlertid denne metoden for screening kompleks og er ikke kostnadseffektiv. Derfor er genetisk testing i USA begrenset til personer som viser tydelige symptomer på HCM og deres familiemedlemmer. Dette sikrer at testen ikke er bortkastet på å oppdage andre årsaker til ventrikulær hypertrofi (på grunn av den lave følsomheten), og at familiemedlemmer til den enkelte blir utdannet om den potensielle risikoen for å være bærere av mutantgenene.
Canada
Kanadiske retningslinjer og anbefalinger for genetisk testing for personer diagnostisert med HCM er som følger:
- Hovedformålet med genetisk testing er for screening av familiemedlemmer.
- I følge resultatene kan pårørende i fare bli oppfordret til å gjennomgå omfattende tester.
- Genetisk testing er ikke ment for å bekrefte en diagnose.
- Hvis den diagnostiserte personen ikke har noen slektninger som er i fare, er det ikke nødvendig med genetisk testing.
- Genetisk testing er ikke ment for risikovurdering eller behandlingsbeslutninger.
- Bevis støtter bare klinisk testing for å forutsi progresjon og risiko for å utvikle komplikasjoner av HCM.
For personer mistenkt for å ha HCM:
- Genetisk testing anbefales ikke for å bestemme andre årsaker til venstre ventrikkelhypertrofi (for eksempel " idrettsutøverens hjerte ", hypertensjon og kardial amyloidose).
- HCM kan differensieres fra andre hypertrofiforårsakende tilstander ved bruk av klinisk historie og klinisk testing.
Storbritannia
Et obduksjon etter dødsfallet til TV-programlederen David Frost i 2013 fant at han hadde HCM, selv om det ikke bidro til hans død og familien hans ikke ble informert. Den plutselige hjertedøden til hans 31 år gamle sønn i 2015 førte til at familien samarbeidet med British Heart Foundation for å skaffe midler til bedre screening.
Behandling
Asymptomatiske mennesker
Et betydelig antall mennesker med hypertrofisk kardiomyopati har ingen symptomer og vil ha en normal levetid, selv om de bør unngå spesielt anstrengende aktiviteter eller konkurransedyktig friidrett. Asymptomatiske mennesker bør screenes for risikofaktorer for plutselig hjertedød. Hos personer med hvile eller induserbare utstrømningshindringer, bør situasjoner som kan forårsake dehydrering eller vasodilatasjon (for eksempel bruk av vasodilatoriske eller vanndrivende blodtrykksmedisiner) unngås. Septal reduksjonsterapi anbefales ikke hos asymptomatiske mennesker.
Medisiner
Hovedmålet med medisiner er å lindre symptomer som brystsmerter, kortpustethet og hjertebank. Betablokkere regnes som førstelinjemedisiner, ettersom de kan senke pulsen og redusere sannsynligheten for ektopiske slag. For personer som ikke tåler betablokkere, kan nondihydropyridin kalsiumkanalblokkere som verapamil brukes, men er potensielt skadelige hos mennesker som også har lavt blodtrykk eller alvorlig kortpustethet i hvile. Disse medisinene reduserer også hjertefrekvensen, selv om bruken av dem hos personer med alvorlig utstrømningsobstruksjon, forhøyet kiletrykk i lungearterien og lavt blodtrykk bør gjøres med forsiktighet. Dihydropyridin kalsiumkanalblokkere bør unngås hos personer med tegn på obstruksjon. For personer hvis symptomene ikke lindres ved behandlingene ovenfor, kan disopyramid vurderes for ytterligere symptomlindring. Diuretika kan vurderes for personer med tegn på væskeoverbelastning, men brukes forsiktig hos personer med tegn på obstruksjon. Folk som fortsetter å ha symptomer til tross for medikamentell behandling, kan vurdere mer invasive behandlinger. Intravenøs fenylefrin (eller et annet rent vasokonstriktivt middel) kan brukes ved akutt innstilling av lavt blodtrykk hos personer med obstruktiv hypertrofisk kardiomyopati som ikke reagerer på væsketilførsel.
Kirurgisk septal myektomi
Kirurgisk septal myektomi er en åpen hjerteoperasjon som utføres for å lindre symptomer hos mennesker som forblir alvorlig symptomatiske til tross for medisinsk behandling. Den har blitt fremført vellykket siden begynnelsen av 1960 -tallet. Kirurgisk septal myektomi reduserer hindring av venstre ventrikkels utstrømningskanal jevnt og forbedrer symptomene, og på erfarne sentre har en kirurgisk dødelighet mindre enn 1%, samt 85% suksessrate. Det innebærer en median sternotomi (generell anestesi, åpning av brystet og kardiopulmonal bypass ) og fjerning av en del av det interventrikulære septum. Kirurgisk myektomi -reseksjon som fokuserer bare på subaortisk septum, for å øke størrelsen på utstrømningskanalen for å redusere Venturikrefter, kan være utilstrekkelig for å avskaffe systolisk fremre bevegelse (SAM) av mitralventilens fremre hefte. Med denne begrensede reseksjonen omdirigerer den gjenværende midtseptale bulen fremdeles flyten etterpå; SAM vedvarer fordi strømmen fortsatt kommer bak mitralventilen. Det er først når den dypere delen av septalbulen resekteres at strømmen omdirigeres fremover fra mitralventilen, og avskaffer SAM. Med dette i bakhodet har en modifikasjon av Morrow myektomi kalt utvidet myektomi, mobilisering og delvis eksisjon av papillærmusklene blitt valg av eksisjon. Hos personer med spesielt store redundante mitralventiler, kan fremre brosjyreplikasjon legges til for å fullføre separasjonen av mitralventilen og utløpet. Komplikasjoner ved septal myektomi kirurgi inkluderer mulig død, arytmier, infeksjon, ustanselig blødning, septal perforering/defekt og hjerneslag.
Alkohol septalablation
Alkohol septal ablasjon , introdusert av Ulrich Sigwart i 1994, er en perkutan teknikk som innebærer injeksjon av alkohol i en eller flere septal grener av venstre fremre synkende arterie . Dette er et kateter teknikk med resultater som ligner på den kirurgiske septal myectomy prosedyre men er mindre invasiv, ettersom det ikke involverer generell anestesi og åpning av brystveggen og hjerteposen (som er gjort i et septal myectomy). I en utvalgt populasjon med symptomer sekundært til en høy grad av utstrømningskanal, kan ablasjon av alkoholseptal redusere symptomene på HCM. I tillegg vil eldre individer og de med andre medisinske problemer, som kirurgisk myektomi ville utgjøre økt prosessuell risiko, sannsynligvis ha nytte av den mindre invasive septalablationsprosedyren.
Når den utføres på riktig måte, induserer en alkohol septal ablasjon et kontrollert hjerteinfarkt , der den delen av det interventrikulære septum som involverer venstre ventrikkels utstrømningskanal er infarkt og vil trekke seg sammen til et arr. Det er debatt om hvilke mennesker som er best tjent med kirurgisk myektomi, alkohol septal ablasjon eller medisinsk terapi.
Mitral klipp
Siden 2013 har mitralklips blitt implantert via kateter som en ny strategi for å korrigere bevegelsen til mitralventilen hos mennesker med alvorlig obstruktiv HCM. Enheten fester sammen mitralventilbladene for å forbedre hjertets blodutstrømning. Mitralklippet har ennå ikke etablert den langsiktige påliteligheten til septal myektomi eller alkohol septal ablasjon, men HCM-spesialister tilbyr i økende grad klippet som et mindre invasivt behandlingsalternativ.
Implanterbar pacemaker eller defibrillator
Bruk av en pacemaker har blitt fremmet i en delmengde av individer for å forårsake asynkron sammentrekning av venstre ventrikkel. Siden pacemakeren aktiverer det interventrikulære septum før den venstre ventrikkelfrie veggen, kan gradienten over det venstre ventrikkelutløpskanalen avta. Denne behandlingsformen har vist seg å gi mindre symptomlindring og mindre reduksjon i utstrømningskanalen i venstre ventrikkel sammenlignet med kirurgisk myektomi. Teknologiske fremskritt har også ført til utviklingen av en pacemaker med to kammer, som bare slås på når det trengs (i motsetning til en vanlig pacemaker som gir en konstant stimulans). Selv om pacemakeren med to kammer har vist å redusere obstruksjon av ventrikulære utstrømningskanaler, har eksperimentelle studier funnet bare noen få individer med forbedrede symptomer. Forskere mistenker at disse rapportene om forbedrede symptomer skyldes placebo -effekt.
Prosedyren inkluderer et snitt på det anterolaterale området under kragebenet. To ledninger settes deretter inn; den ene inn i høyre atrium og den andre inn i høyre ventrikkels topp via de subklaviske venene. Når de er på plass, er de festet og festet til generatoren som vil forbli inne i fascia, fremre til brystmusklen. Komplikasjoner av denne prosedyren inkluderer infeksjon, elektrisk ledning og funksjonsfeil i generatoren som krever utskifting.
For personer med HCM som viser en eller flere av de viktigste risikofaktorene for plutselig hjertedød, kan en implanterbar kardioverter-defibrillator (ICD) eller en kombinert pacemaker/ICD alt-i-ett-enhet anbefales som en passende forholdsregel. I 2014 foreslo European Society of Cardiology en praktisk risikoscore for å beregne denne risikoen.
Hjertetransplantasjon
I tilfeller som ikke reagerer på alle andre behandlingsformer, er hjertetransplantasjon ett alternativ. Det er også den eneste behandlingen som er tilgjengelig for hjertesvikt i sluttstadiet. Imidlertid må transplantasjon skje før symptomene begynner som hypertensjon i lungekar, nyrefunksjon og tromboemboli for at det skal lykkes. Studier har indikert en syvårig overlevelsesrate på 94% hos personer med HCM etter transplantasjon.
Prognose
En systematisk gjennomgang fra 2002 konkluderte med at: "Totalt sett gir HCM en årlig dødelighet på omtrent 1%... HCM kan være forbundet med viktige symptomer og for tidlig død, men oftere uten eller relativt mild funksjonshemming og normal levetid."
Barn
Selv om hypertrofisk kardiomyopati (HCM) kan være tilstede tidlig i livet og sannsynligvis er medfødt, er det en av de mest uvanlige hjertemisdannelsene som oppstår i pediatrisk kardiologi, hovedsakelig fordi symptomene vanligvis er fraværende, ufullstendige eller forsinket til voksen alder . Mesteparten av den nåværende informasjonen om HCM stammer fra studier i voksne populasjoner, og implikasjonen av disse observasjonene for pediatrisk populasjon er ofte usikker. Likevel har nylige studier innen pediatrisk kardiologi avslørt at HCM står for 42% av barndommens kardiomyopatier, med en årlig forekomst på 0,47/100 000 hos barn. I asymptomatiske tilfeller regnes plutselig død som en av de mest fryktede komplikasjonene forbundet med sykdommen hos utvalgte barnepopulasjoner. Følgelig er anbefalt praksis å undersøke barn av berørte individer gjennom barndommen for å oppdage hjerteabnormaliteter på et tidlig stadium, i håp om å forhindre ytterligere komplikasjoner av sykdommen.
Vanligvis stilles diagnosen HCM i en pediatrisk populasjon under vurdering for murring, hjertesvikt, fysisk utmattelse og genetisk testing av barn av berørte individer. Spesielt har ekkokardiogram (ECHO) blitt brukt som et definitivt ikke -invasivt diagnostisk verktøy hos nesten alle barn. ECHO vurderer hjertekammerstørrelse, veggtykkelse, systolisk og diastolisk funksjon og utstrømningsobstruksjon. Dermed har ECHO blitt valgt som et ideelt middel for å oppdage overdreven veggtykkelse av hjertemuskelen i HCM.
For barn med HCM har behandlingsstrategier som mål å redusere sykdomssymptomer og redusere risikoen for plutselig død. På grunn av sykdommens heterogenitet, blir behandlingen vanligvis endret i henhold til individets behov. β-blokkere forbedrer fylling og avslapning i venstre ventrikkel og forbedrer derved symptomer. Hos noen barn ble β -blokkere (f.eks. Propranolol) vist effektive for å redusere risikoen for plutselig død. Videre kan kalsiumkanalblokkere (verapamil) og antiarytmiske legemidler brukes som tilleggsbehandling til β-blokkere hos symptomatiske barn. Likevel er det nødvendig med ytterligere testing for å fastslå deres endelige fordeler.
Andre dyr
Katter
Feline hypertrofisk kardiomyopati (HCM) er den vanligste hjertesykdommen hos huskatter ; sykdomsprosessen og genetikk antas å være lik sykdommen hos mennesker. Hos Maine Coon -katter har HCM blitt bekreftet som et autosomalt dominerende arvelig trekk. Mange katteraser har HCM som et problem i rasen. Den første genetiske mutasjonen (i hjerte -myosinbindende protein C) som er ansvarlig for katt -HCM ble oppdaget i 2005 hos Maine Coon -katter. En test for denne mutasjonen (A31P) er tilgjengelig. Omtrent en tredjedel av Maine Coon-kattene som er testet for mutasjonen er enten heterozygote eller homozygote for mutasjonen, selv om mange av kattene som er heterozygote ikke har åpenbare tegn på sykdommen på et ekkokardiogram (lav penetrasjon). Noen Maine Coon -katter med kliniske tegn på hypertrofisk kardiomyopati tester negative for denne mutasjonen, noe som sterkt tyder på at det finnes en annen årsak hos rasen. Kardial myosinbindende protein C -mutasjon identifisert i Maine Coon -katter har ikke blitt funnet hos noen annen kattras med HCM, men mer nylig har en annen myosinbindende protein C -mutasjon blitt identifisert hos Ragdoll -katter med HCM. Som hos mennesker er ikke katt -HCM tilstede ved fødselen, men utvikler seg over tid. Det er identifisert for første gang hos katter helt ned til 6 måneders alder og minst like gamle som 7 år.
Klinisk har katter med hypertrofisk kardiomyopati vanligvis en systolisk fremre bevegelse (SAM) av mitralventilen (se grafikk). Katter med alvorlig HCM utvikler ofte venstre hjertesvikt (lungeødem, pleural effusjon) på grunn av alvorlig diastolisk dysfunksjon i venstre ventrikkel. De kan også utvikle en venstratriumtrombus som oftest emboliserer til terminal aorta og skaper akutt smerte og lammelse i bakbenet (se nedenfor). Plutselig død kan også oppstå, men ser ut til å være uvanlig.
Hjertens ultralyd ( ekkokardiografi ) er nødvendig for å diagnostisere HCM hos katter. Måling av sirkulerende hjerte biomarkører , som N-terminalt proBNP-( NT-proBNP ) og troponin I (TNI) kan brukes i katter for å styrke den mistanke om hjertesykdommer. Det er en Point-of-care test for feline NT-proBNP tilgjengelig som kan brukes på veterinærklinikken når ekkokardiografi ikke er mulig å utføre.
Det finnes ingen kur mot katt -HCM. Mange, men ikke alle katter, har hjertemusling. Mange katter som har hjerteklump har ikke HCM. Ofte er de første tegnene på at en katt har HCM takypné/dyspné på grunn av hjertesvikt eller akutte smerter og lammelse på grunn av systemisk tromboemboli. Selv om medisiner vanligvis gis til katter med HCM som ikke har kliniske tegn, har ingen medisiner vist seg å være nyttige på dette stadiet, og det har blitt vist at en ACE -hemmer ikke er gunstig før hjertesvikt er tilstede (da er vanndrivende mest fordelaktig). Diltiazem gir vanligvis ingen påviselig fordel. Atenolol administreres vanligvis når en alvorlig systolisk fremre bevegelse av mitralventilen er tilstede.
Feline arteriell tromboembolisme (FATE) er en relativt vanlig og ødeleggende komplikasjon av katt -HCM og andre katte -kardiomyopatier. Tromben dannes vanligvis i venstre atrium, oftest venstre auricle. Formasjonen antas hovedsakelig å skyldes stasis i blodstrømmen. Klassisk sett ligger tromboembolismen ved iliacatrifurking av aorta, som lukker enten den ene eller begge de vanlige iliacarteriene. Fordi denne splittelsen kalles salen, og er det hyppigste stedet for tromben, er FATE ofte kjent som sadeltromb. Klinisk presenterer dette seg som en katt med fullstendig tap av funksjon i en eller begge bakbenene. Bakbenene er kalde og katten har store smerter. Emboli kan sjelden ligge på andre steder, oftest høyre fremre lem og nyrearteriene.
Clopidogrel brukes til å prøve å forhindre dannelse av venstre atrialtromb hos katter med HCM og et stort venstre atrium. FATCAT -studien ved Purdue University viste at det er bedre enn aspirin for å forhindre at det dannes en annen trombus hos katter som allerede har opplevd en blodpropp. Trombolytiske midler (f.eks. Vevsplasminogenaktivator) har blitt brukt med en viss suksess for å bryte ned en eksisterende aortatrombose, men kostnaden er høy og utfallet ser ikke ut til å være bedre enn å gi en katt tid (48–72 timer) til å bryte ned dens egen blodpropp. Smertebehandling er ekstremt viktig. Prognosen for katter med FATE er ofte dårlig, ettersom de sannsynligvis allerede har betydelig HCM, og en tilbakevendende kamp om FATE er sannsynlig. Av denne grunn er dødshjelp ofte et gyldig hensyn.
Gorillaer
I juli 2013 døde Rigo, en 42 år gammel vestlandsk gorilla , bosatt i Melbourne Zoo og far til Mzuri, den første gorillaen som ble født ved kunstig befruktning , uventet som følge av HCM. Tilstanden er ikke uvanlig hos mannlige gorillaer over 30 år, og i mange tilfeller er det ingen tegn til sykdommen før individets plutselige død.
Referanser
Eksterne linker
| Klassifisering | |
|---|---|
| Eksterne ressurser |