Bukspyttkjertel nevroendokrin svulst - Pancreatic neuroendocrine tumor
| Bukspyttkjertel nevroendokrin svulst | |
|---|---|
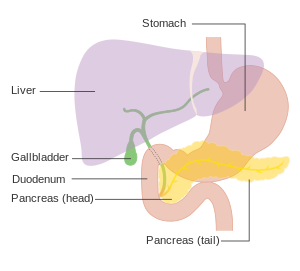 | |
| Spesialitet | Onkologi |
| Behandling | Stråling, cellegift |
| Prognose | Fem års overlevelse ~ 61% |
Pankreatiske nevroendokrine tumorer ( PanNETs , kjæledyr , eller PNETs ), ofte referert til som "øy-celle svulster", eller "pankreatiske endokrine svulster" er neuroendokrine neoplasmer som oppstår fra celler av endokrine ( hormonelle ) og nervesystemet innenfor bukspyttkjertelen .
PanNET er en type nevroendokrine svulster , som representerer omtrent en tredjedel av gastroenteropankreatiske nevroendokrine svulster (GEP-NET). Mange PanNET -er er godartede , mens noen er ondartede . Aggressive PanNET -svulster har tradisjonelt blitt betegnet som "holme cellekarsinom".
PanNET er ganske forskjellige fra den vanlige formen for kreft i bukspyttkjertelen , hvorav de fleste er adenokarsinomer , som oppstår i den eksokrine bukspyttkjertelen. Bare 1 eller 2% av klinisk signifikante neoplasmer i bukspyttkjertelen er PanNET.
Typer
Flertallet av PanNET er godartede , mens noen er ondartede . Verdens helseorganisasjons (WHO) klassifiseringsskjema plasserer nevroendokrine svulster i tre hovedkategorier, som understreker svulstkvaliteten i stedet for den anatomiske opprinnelsen . I praksis de svulster kalles godt eller mellom differensierte PanNETs i WHO ordningen kalles " holmen celle svulster". Den høykvalitets undertypen som kalles nevroendokrin kreft (NEC) i WHO-ordningen, er synonymt med "holme cellekarsinom".
| Type | Relativ forekomst | Typisk plassering av svulst | Biomarkører | Symptomer |
|---|---|---|---|---|
| Insulinom | 35–40% | Hodet, kroppen, halen i bukspyttkjertelen | insulin, proinsulin , C-peptid | Hypoglykemi |
| Gastrinom | 16–30% | Gastrinoma trekant | gastrin , PP |
|
| VIPoma | <10% | Distal bukspyttkjertel (kropp og hale) | VIP |
|
| Somatostatinoma | <5% | Pankreatoduodenal rille, ampullær, periampullær | somatostatin | |
| PPoma | Hode eller bukspyttkjertel | bukspyttkjertel polypeptid | ||
| Glucagonoma | 1% | Kropp og hale i bukspyttkjertelen | glukagon , glycentin |
Relativ forekomst er angitt som prosentandel av alle funksjonelle nevroendokrine svulster i bukspyttkjertelen.
Tegn og symptomer
Noen PanNET -er gir ingen symptomer, og i så fall kan de oppdages ved en CT -skanning utført for et annet formål. Symptomer som magesmerter eller ryggsmerter eller trykk, diaré, fordøyelsesbesvær eller gulfarging av huden og det hvite i øynene kan oppstå fra virkningene av en større PanNET -svulst, enten lokalt eller ved metastase . Omtrent 40% av PanNETS har symptomer relatert til overdreven sekresjon av hormoner eller aktive polypeptider og blir derfor merket som "funksjonelle"; symptomene gjenspeiler typen hormon som utskilles, som diskutert nedenfor. Opptil 60% av PanNET er ikke -sekretoriske eller ikke -funksjonelle, der det ikke er noen sekresjon, eller mengden eller typen produkter, for eksempel bukspyttkjertel -polypeptid (PPoma), chromogranin A og neurotensin , forårsaker ikke et klinisk syndrom, selv om blodnivået kan bli forhøyet. Totalt har 85% av PanNET -er en forhøyet blodmarkør.
Funksjonelle svulster klassifiseres ofte etter hormonet som er sterkest utskilt, for eksempel:
- gastrinom : overdreven gastrin forårsaker Zollinger - Ellison syndrom (ZES) med magesår og diaré
- insulinoma : hypoglykemi oppstår ved samtidig økning av insulin , proinsulin og C -peptid
- glucagonoma : symptomene skyldes ikke alle glukagonforhøyelser, og inkluderer utslett , vondt i munnen, endrede tarmvaner, venøs trombose og høyt blodsukkernivå
- VIPoma , produserer for vasoaktivt intestinalt peptid , noe som kan føre til dyp kronisk w atery d iarrhea og resulterende dehydrering , h ypokalemia , og en chlorhydria (WDHA eller bukspyttkjertel kolera syndrom)
- somatostatinoma : disse sjeldne tumorer har sammenheng med forhøyet blodglukosenivåer, aklorhydri , gallestein og diaré
- mindre vanlige typer inkluderer ACTHoma , CRHoma , calcitoninoma , GHRHoma , GRFoma , og paratyroid hormon-relatert peptid tumor
I disse forskjellige typer av funksjonelle tumorer, hyppigheten av malignitet og overlevelses prognose har blitt estimert ulikt, men en relevant tilgjengelig oppsummering er tilgjengelig.
Diagnose
Fordi symptomene er uspesifikke, blir diagnosen ofte forsinket.
Måling av hormoner inkludert bukspyttkjertelpolypeptid , gastrin , proinsulin , insulin , glukagon og vasoaktivt tarmpeptid kan avgjøre om en svulst forårsaker hypersekresjon.
Multifase CT og MR er de primære metodene for morfologisk avbildning av PNET -er. Mens MR er bedre enn CT for avbildning, både av primærtumoren og evaluering av metastaser, er CT lettere tilgjengelig. Spesielt, mens mange ondartede lesjoner er hypodens i kontrastforsterkede studier, er levermetastaser av PNET hypervaskulære og lett visualiserte i den sene arterielle fasen av CT-studien etter kontrast. Imidlertid er morfologisk avbildning alene ikke tilstrekkelig for en sikker diagnose
På biopsi er immunhistokjemi generelt positiv for kromogranin og synaptofysin . Genetisk testing av disse viser vanligvis endrede MEN1 og DAXX / ATRX .
Iscenesettelse
WHO-klassifiseringen i 2010 av svulster i fordøyelsessystemet klassifiserer alle nevroendokrine svulster i tre kategorier, basert på graden av celledifferensiering (fra godt differensiert "NET G1" til dårlig differensiert "NET G3"). NCCN anbefaler bruk av det samme AJCC-UICC-iscenesettingssystemet som bukspyttkjerteladenokarsinom. Ved å bruke denne ordningen, er trinn for trinn -utfallene for PanNET -er forskjellige med eksokrine kreft i bukspyttkjertelen. Et annet TNM -system for PanNET har blitt foreslått av The European Neuroendocrine Tumor Society.
- Bukspyttkjertel neuroendokrine tumorstaging ( AJCC )
Behandling
Generelt omfatter behandling for PanNET det samme utvalget av alternativer som andre nevroendokrine svulster , som diskutert i hovedartikkelen. Det er imidlertid noen spesifikke forskjeller, som diskuteres her.
I fungerende PanNET -er anbefales oktreotid vanligvis før biopsi eller kirurgi, men unngås vanligvis ved insulinomer for å unngå dyp hypoglykemi .
PanNETs i Multiple endocrine neoplasia type 1 er ofte flere, og krever derfor forskjellige behandlings- og overvåkingsstrategier.
Noen PanNET -er reagerer mer på cellegiftbehandling enn gastroenteriske karsinoide svulster. Flere agenter har vist aktivitet. I godt differensierte PanNETer er cellegift generelt reservert for når det ikke er andre behandlingsalternativer. Kombinasjoner av flere medisiner har blitt brukt, for eksempel doxorubicin med streptozocin og fluorouracil (5-FU) og capecitabin med temozolomid. Selv om det er marginalt effektivt i godt differensierte PET-er, har cisplatin med etoposid en viss aktivitet ved dårlig differensierte nevroendokrine kreftformer (PDNEC), spesielt hvis PDNEC har en ekstremt høy Ki-67- score på over 50%.
Flere målrettede terapimidler har blitt godkjent i PanNETs av FDA basert på forbedret progresjonsfri overlevelse (PFS):
- everolimus (Afinitor) er merket for behandling av progressive nevroendokrine svulster med bukspyttkjertelopprinnelse hos pasienter med ikke -resekterbar, lokalt avansert eller metastatisk sykdom. Sikkerheten og effektiviteten til everolimus i karsinoide svulster er ikke fastslått.
- sunitinib (Sutent) er merket for behandling av progressive, godt differensierte nevroendokrine svulster i bukspyttkjertelen hos pasienter med ikke-resekterbar lokalt avansert eller metastatisk sykdom. Sutent har også godkjenning fra EU-kommisjonen for behandling av 'ikke-resekterbare eller metastatiske, godt differensierte nevroendokrine svulster i bukspyttkjertelen med sykdomsprogresjon hos voksne'. En fase III-studie av sunitinib-behandling i godt differensiert pNET som hadde forverret seg de siste 12 månedene (enten avansert eller metastatisk sykdom) viste at sunitinib-behandling forbedret progresjonsfri overlevelse (11,4 måneder vs. 5,5 måneder), total overlevelse og målet svarprosent (9,3% mot 0,0%) sammenlignet med placebo.
Genetikk
Bukspyttkjertelneuroendokrine svulster kan oppstå i forbindelse med multiple endokrine neoplasier type 1 , Von Hippel – Lindau sykdom , neurofibromatosis type 1 (NF-1) eller tuberose sklerose (TSC)
Analyse av somatiske DNA- mutasjoner i godt differensierte nevroendokrine svulster i bukspyttkjertelen identifiserte fire viktige funn:
- Som forventet, genene mutert i garn, MEN1 , ATRX , DAXX , TSC2 , PTEN og PIK3CA , er forskjellig fra de muterte gener som tidligere er funnet i pankreas adenokarsinom .
- en av seks godt differensierte bukspyttkjertel NET har mutasjoner i mTOR pathway gener, for eksempel TSC2 , PTEN og PIK3CA . Oppdagelsen av sekvensering kan tillate valg av hvilke NET som vil ha fordeler av mTOR -inhibering, for eksempel med everolimus , men dette venter på validering i en klinisk studie .
- mutasjoner som påvirker en ny kreftvei som involverer ATRX og DAXX gener ble funnet i omtrent 40% av bukspyttkjertelenettene. Proteinene kodet av ATRX og DAXX deltar i kromatin -ombygging av telomerer ; disse mutasjonene er assosiert med en telomerase -uavhengig vedlikeholdsmekanisme kalt ALT (alternativ forlengelse av telomerer) som resulterer i unormalt lange telomere ender av kromosomer .
- ATRX / DAXX og MEN1 mutasjoner var assosiert med en bedre prognose .
Referanser
Eksterne linker
| Klassifisering |
|---|






